定時能量遞送的制作方法
本申請涉及一種用于采用非熱學且最優的方式來標測組織并產生用于治療心臟心律失常的損傷的方法和系統,使得選擇性頓抑或消融所述靶組織所需的能量的量最小化。僅在最佳設備位置和電極接近靶組織的時刻、并且僅在心動周期中被確定為針對可逆或不可逆效應是最優的一段時間期間遞送能量。可以消除與熱消融技術相關的并發癥。
背景技術:
組織消融是通常用于治療如心臟心律失常(其包括心房顫動)等病癥的醫療手術。為了治療心臟心律失常,可以進行消融以修改組織,如停止通過心臟組織的異常電傳播和/或破壞異常電傳導。雖然經常使用熱消融技術(諸如冷凍消融和射頻(rf)消融),但是也可以使用非熱學技術(諸如脈沖場消融(pfa))。
脈沖場消融涉及施加短脈沖電場(pef),所述短脈沖電場可以通過電滲透來可逆地或不可逆地使細胞膜不穩定,但通常不影響組織成分(包括無細胞心臟細胞外基質)的結構完整性。pfa的性質允許非常短暫的治療能量遞送時間段,持續時間大約數十毫秒。此外,pfa可能不會像熱消融技術那樣頻繁地或嚴重地引起對非靶組織的附帶損傷。此外,藥理學藥劑可以優先引入暴露于具有可逆的膜滲透性的pef的靶組織的細胞中。
然而,所有心內刺激、記錄和消融導管都受到心臟運動、呼吸運動、器械剛度/機動性和隨機患者運動的影響。這些運動源影響與例如心臟壁的電極接觸的質量。在能量遞送以消融靶組織的過程中,這種運動可以在電極移動遠離靶組織的時間段期間降低這種遞送的效果。
因此期望的是提供一種用于評價電極-組織接觸的質量的系統和方法。更具體地對于pfa來說,期望的是提供一種僅當電極與靶組織很接近并且心動周期內的定時最優時才將能量遞送到靶組織的系統和方法。這與當使用rf能量進行超熱消融時與組織的良好熱接觸的要求不同。使用pfa來有效消融組織僅需要電場必須包含目標消融區域以便引起消融。以類似的方式,當pef包含目標組織區域時,可以在靶組織中施加可逆的滲透作用。
技術實現要素:
本申請有利地提供了一種用于當在一個或多個能量遞送電極與靶組織之間存在良好接近度并且當患者的心動周期處于最優消融時間時選擇性地將脈沖場能遞送到靶組織位置的方法和系統。一種利用脈沖場能治療可具有心動周期的患者的心臟的靶組織的方法可以包括:確定所述心動周期的定時以及所述心動周期內用于能量遞送的最優時間;評估至少一個能量遞送電極與所述靶心臟組織之間的接近度;以及在用于能量遞送的所述最優時間期間當所述至少一個能量遞送電極接近所述靶心臟組織時將脈沖場能從所述至少一個能量遞送電極遞送到所述靶組織。可以使用體表心電圖或心內電描記圖來確定心動周期定時。心臟可以包括心室,并且確定心動周期內用于能量遞送的最優時間可以包括識別心動周期內的心室的去極化和心室的復極化。此外,在心室去極化之后且在心室復極化之前,可以將能量遞送到靶組織。確定心動周期定時可以進一步包括測量包括r波、s波和t波的qt間期,并且確定心動周期內用于脈沖場能遞送的最優時間可以包括識別qt間期內的st段。可以在st段期間遞送脈沖場能,所以所述遞送不會引發心律失常。此外,到靶組織的能量遞送可以在r波開始后大約60-120毫秒啟動,并且在t波開始之前終止。所遞送的脈沖場能可能在靶組織中引起可逆的或不可逆的效應。例如,當遞送到靶組織的脈沖場能最多為約200v并且以一個至二十個脈沖遞送時,可能在靶組織中引起可逆效應。相反,當遞送到靶組織的脈沖場能最少為約300v并且以一個至二十個脈沖遞送時,可能在靶組織中引起不可逆效應。所述至少一個能量遞送電極中的每一個都可以包括溫度傳感器,對所述至少一個能量遞送電極與所述靶組織之間的接觸的評估基于由緊隨著脈沖場能遞送之后的至少一個溫度傳感器記錄的溫度測量結果。另外地或替代性地,評估所述至少一個能量遞送電極與靶組織之間的接近度可以基于以下各項中的至少一項:在所述靶組織中測量的心內電描記圖振幅;在所述靶組織中測量的單極電描記圖;使用在所述靶組織中測量的單極電描記圖而測量的單相動作電勢的存在,單相動作電勢的存在表明所述至少一個能量遞送電極與所述靶組織之間的直接接觸;通過所述至少一個能量遞送電極遞送雙極或單極起搏脈沖以通過所述靶組織內的局部心肌刺激來實現心臟奪獲的能力,實現心臟奪獲指示所述至少一個能量遞送電極與所述靶組織之間的接觸;由所述至少一個能量遞送電極遞送以用于通過所述靶組織內的局部心肌刺激來實現心臟奪獲的雙極或單極起搏脈沖的振幅閾值;靠近所述靶組織的神經或肌肉組織對由所述至少一個能量遞送電極遞送的能量刺激的反應;電極-組織接觸力測量結果;對足以在所接觸的靶組織中產生可測量的加熱的低級別能量的溫度響應;低頻阻抗大小測量結果;高頻阻抗大小測量結果;高頻阻抗相位角測量結果;在脈沖場能遞送期間測量的電流;從能量遞送設備中的至少一個加速度計測量的所述至少一個能量遞送電極的瞬時穩定性;并且所述至少一個能量遞送電極中的每一個的實時位置,基于以下各項中的至少一項:用于確定所述至少一個能量遞送電極在所述心臟內的3d位置的電(場)勢測量結果;用于確定所述至少一個能量遞送電極在所述心臟內的3d位置的電磁導航測量結果;與解剖部位有關的電磁或電場導航,所述解剖部位通過體表標測而被識別為用于能量遞送以治療心律失常的靶部位;與解剖部位有關的電磁或電場導航,所述解剖部位通過非接觸式心內感測或多電極心內心內膜標測而被識別為用于能量遞送以治療心律失常的靶部位;與解剖部位有關的第一醫療設備的超聲發射和接收元件以及第二醫療設備的超聲發射、接收或回波元件,所述解剖部位通過非接觸式心內感測或多電極心內心內膜標測而被識別為用于能量遞送以治療心律失常的靶部位;以及與解剖部位有關的治療設備中所并入的超聲元件,所述解剖部位通過非接觸式心內感測或多電極心內心內膜標測而被識別為用于能量遞送以治療心律失常的靶部位。
一種將脈沖場能遞送到患者心臟的靶組織的的方法,所述心臟具有心動周期,所述方法可以包括:識別所述心動周期的qt間期,所述qt間期至少包括q波、r波、s波、t波以及在s波與t波開始之間的st段;確定心動周期內用于脈沖場能遞送的最優時間,所述最優時間在至少一部分st段期間;在所述用于脈沖場能遞送的最優時間期間將脈沖場能從能量遞送設備的電極陣列遞送到靶組織,以在靶組織中引起可逆效應;以及在所述用于脈沖場能遞送的最優時間期間將脈沖場能從電極陣列遞送到靶組織,以在靶組織中引起不可逆效應。例如,脈沖場能可以被從電極陣列遞送到靶組織,以便在r波開始之后大約60毫秒與r波開始后大約120毫秒之間的第一次遞送中在靶組織中引起不可逆效應。所述電極陣列可以具有至少基本上圓形的構造,并且可以包括九個能量遞送電極。可以采用雙極模式在奇數編號的能量遞送電極之間(即,在第一和第三電極之間、在第三和第五電極之間、在第五和第七電極之間以及在第七和第九電極之間)和在偶數編號的能量遞送電極之間(即在第二和第四電極之間、在第四和第六電極之間以及在第六和第八電極之間)遞送脈沖場能。替代性地,可以采用雙極模式在所述電極陣列的第一部分中的能量遞送電極與所述電極陣列的第二部分中的能量遞送電極之間遞送脈沖場能。另外地或替代性地,可以在任何能量遞送電極與接地片之間以單極模式遞送脈沖場能。所述方法可以進一步包括:評估至少一個能量遞送電極與靶組織之間的接近度,在所述用于脈沖場能遞送的最優時間期間并且當所述至少一個能量遞送電極與所述靶組織非常接近時從所述電極陣列遞送脈沖場能以在靶組織中引起不可逆效應。
一種用于利用脈沖場能治療患者心臟的靶組織的系統,所述心臟具有心動周期,所述系統可以包括:能量遞送設備,所述能量遞送設備包括具有多個能量遞送電極的至少基本上圓形的電極陣列;以及控制單元,所述控制單元包括脈沖場能遞送發生器,所述控制單元被編程用于:確定所述心動周期的定時;確定所述心動周期內用于脈沖場能遞送的最優時間;評估至少一個能量遞送電極與所述靶組織之間的接近度;并且,在所述用于脈沖場能遞送的最優時間期間當所述多個能量遞送電極中的至少一個與所述靶組織非常接近時,將脈沖場能從所述電極陣列遞送到所述靶組織。將脈沖場能從電極陣列遞送到靶組織可以包括:遞送脈沖場能,所述脈沖場能例如在所述用于脈沖場能遞送的最優時間期間當所述多個能量遞送電極中的至少一個與靶組織非常接近時將脈沖場能從電極陣列遞送到靶組織時在靶組織中引起可逆效應,或者可以被遞送以使得所述脈沖場能例如當遞送到靶組織的脈沖場能為大約為200v或更小、并且以一個至二十個脈沖進行遞送時在靶組織中引起不可逆效應,或者所述脈沖場能例如當遞送到靶組織的脈沖場能為大約300v或更大、并且以至少一個到二十個脈沖進行遞送時可以在所述靶組織中引起不可逆效應。確定所述心動周期的所述定時可以包括評估具有q波、r波、s波和t波的體表心電圖,所述控制單元被編程用于在所述r波開始后大約60毫秒與大約120毫秒之間將所述脈沖場能遞送至所述靶組織。另外地或替代性地,確定所述心動周期的所述定時可以包括評估具有q波、r波、s波和t波的體表電描記圖,所述控制單元被編程用于在所述s波與所述t波開始之間將所述脈沖場能遞送至所述靶組織。
附圖說明
通過結合附圖參考以下詳細說明,將更容易更全面理解本申請及其伴隨優點和特征,其中:
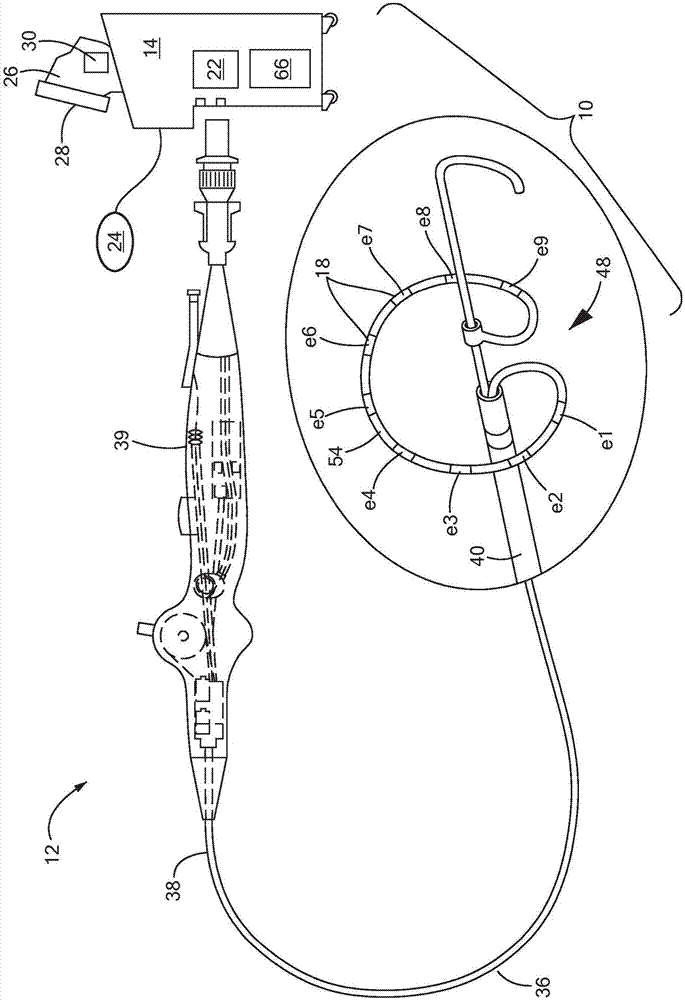
圖1示出了用于向靶組織施加能量的示例性醫療系統,所述系統具有能量遞送設備;
圖2示出了能量遞送設備,所述能量遞送設備具有基本上圓形的多電極陣列,用于將能量遞送到靶組織,如在血管口周圍;
圖3示出了用于向靶組織施加能量的示例性醫療系統,所述系統具有第一能量遞送設備和第二能量遞送設備;
圖4a和4b示出了組合使用以治療組織的第一能量遞送設備和第二能量遞送設備;
圖5示出了來自脈沖場能的順序遞送的數據,當將足夠高的電場強度遞送到心臟組織時,所述遞送首先引起可逆效應,然后產生對心臟組織的可逆效應;
圖6示出了將能量遞送到靶組織的方法的流程圖;以及
圖7示出了心動周期的示例性心電圖。
具體實施方式
現在參考圖1,示出了用于將能量遞送到靶組織的示例性醫療系統。系統10可以用于治療心內膜表面,但是應當理解的是,所述系統可以用于治療其他區域,包括心外膜組織、食管組織、真皮組織、支氣管組織、肺組織、軟組織、腫瘤以及利用應用能量進行治療并受到心臟運動、呼吸運動、隨機患者運動和/或可能影響電極-組織接觸的其他因素的影響的任何其他組織。系統10通常可以包括能量遞送設備12和控制單元14。然而,可以使用多于一個遞送設備(例如,如圖3-4b所示)能量遞送設備12可以包括用于遞送電流的一個或多個能量遞送電極18,并且可以進一步包括一個或多個電極,如標測電極、pfa電極和/或用于測量諸如阻抗等特性的電極(未示出)。
設備12和/或系統10還可以包括一個或多個傳感器20,如溫度傳感器、壓力傳感器、壓電元件、應變儀和/或光纖布拉格傳感器。例如,運動、力或加速度檢測器可以具有各種設計,如壓電設計、電容設計、慣性設計或光學設計。在一些實施例中,系統10可以包括一個或多個輔助設備,如留置導管或起搏器、輔助治療導管或其他設備。例如,所述輔助設備可以是留置導管。此外,如圖3中更詳細地示出和描述的,系統10可以包括第一能量遞送設備12a和第二能量遞送設備12b。
術語“控制單元”可以通常用來指的是任何不是所述遞送設備一部分的系統部件。控制單元14可以被描述為包括在物理上位于操作單元內或與操作單元集成的系統部件,或者與操作單元通信。控制單元14可以被配置為使用脈沖場消融(pfa)來遞送用于組織治療的脈沖場電能。pfa是非熱學式治療方法,所以可以消除與有效的常規熱消融(如射頻或冷凍消融)相關的挑戰。具體地,不需要組織加熱或冷卻,并且可以消除產生凝結物或燒焦的風險。另外,由于pfa能量遞送的總持續時間對于典型過程而言可能需要不到一分鐘、而對于熱消融而言可能需要20-40分鐘,所以可以顯著地縮短過程時間。具有定時消融能量遞送的pfa可以降低能量遞送設備定位的技術復雜性,因為組織接觸或與靶組織的接近度可以由設備12感測到,并且能量被選通以僅在最優接觸或靶組織接近度的時刻進行遞送。因為能量脈沖選擇性地并且具體地主要靶向心臟肌肉細胞,pfa可以消除熱并發癥(如燒焦或凝固)和不期望的創傷對心臟和鄰近結構(例如食道、肺靜脈壁、冠狀動脈或膈神經)的風險。可選地,控制單元14還可以被配置為提供rf能量、微波能量、激光能量、超聲能量和/或可以被配置為用于低溫處理過程。除了用于心臟組織消融的定時能量遞送之外,定時能量遞送可以用于使用本文所述的、但是與呼吸運動有關的方法來治療表現運動的其他組織,如氣道。
此外,控制單元14可以包括與一個或多個遞送電極18電通信的能量發生器22,并且能量發生器22也可以與一個或多個標測或其他電極(未示出)電通信。能量發生器22可以能夠遞送用于刺激自主神經系統或能量被遞送到的基質中的固有自動性的高頻非消融脈沖。發生器22還可以能夠在大約0.1毫秒到10毫秒的范圍內的持續時間和大約20hz到2000hz的頻率范圍內遞送刺激脈沖。此外,發生器22和/或控制單元14可以被配置為使得操作者能夠從0v與200v峰值電壓之間調制雙相方波刺激脈沖的振幅,并且使得操作者能夠從發生器連續地或間歇地遞送脈沖刺激,同時保留在任何所需時刻切換到消融能量的能力。這樣可以使操作者有能力在遞送消融能量之前執行部分或全部心臟腔室的標測,或者在這些位置被發現時并在移動到新的位置之前在例如異位或房室(a-v)結反應的每個或所選的部位處進行消融。此外,能量發生器22和/或控制單元14可以具有可由操作者選擇的自動化系統,由此被檢測到的異位可以激活消融系統以根據每次檢測(例如異位活動)來遞送消融能量而同時移動組織部位上的設備并遞送脈沖刺激以引起異位反應。類似地,發生器22和/或控制單元14可能能夠自動確定燒蝕能量遞送的最優定時。
對刺激的反應可能表現為a-v結傳導減慢或過早心房收縮(異位活動)的形式。這樣的反應可以由電生理學(ep)記錄系統監測,所述系統可以是控制單元14的部件。另外,這樣的反應可以由所述記錄系統以及從所述記錄系統傳送到發生器22和/或控制單元14的數據來進行量化,例如,具有將數據置于解剖顯示器中的心臟導航系統的接口(其也可以是控制單元14的部件)。描述在引發反應的特定位置處的心臟肌肉的性質的數據對于操作者確定用于消融的靶組織可能是有用的。高度異位活動或a-v結反應的區域可能是消融的期望目標,以便有效治療心房顫動和其他心律失常。
控制單元14還可以包括皮膚表面接地電極片24(也稱為接地電極或患者返回電極),所述皮膚表面接地電極片可以在能量遞送過程期間與患者的皮膚接觸,如當以單極模式遞送能量。此外,控制單元14可以包括用戶界面,操作者可以通過所述用戶界面來選擇能量遞送模式,監測能量遞送參數,調整或停止能量遞送,和/或選擇一個或多個電極來遞送能量。例如,所述用戶界面可以包括腳踏板、鼠標、操縱桿、一個或多個計算機26、一個或多個顯示器28、按鈕、旋鈕、觸摸板、觸摸屏或其他輸入裝置,可選地位于能量遞送設備12手柄上。雖然系統10和能量遞送可以是完全自動化的,但操作者可以通過用戶界面來控制能量波的形式,各個電極18的開/關狀態和/或遞送電壓。可以通過例如在心臟電描記圖記錄系統上施加用于一旦由使用者執行則指示在心動周期期間何時遞送脈沖串的標記來向使用者指示所提議的能量遞送的定時。可以使用一個或多個顯示器28將這樣的信息傳送給操作者。
控制單元14還可以包括一個或多個處理器30,所述處理器被編程用于接收、處理和/或傳送從一個或多個能量遞送設備12、一個或多個輔助設備和/或系統10的其他部件接收的數據。控制單元14還可被編程用于接收和處理數據(例如,電勢測量結果和/或電磁導航測量結果),并且確定設備12在心臟內的3d位置。
現在參考圖1和圖2,能量遞送設備12可以包括細長主體36,所述細長主體具有可以聯接至手柄39的近側部分38以及遠側部分40。一個或多個遞送電極18可以聯接至遞送設備12的遠側部分40,位于所述遠側部分上,與所述遠側部分集成在一起,或以其他方式位于所述遠側部分內。此外,遞送設備12的遠側部分40可以具有各種構造中的任何一種。例如,圖1示出了具有多個電極18的焦點設備,所述電極包括位于細長主體36的遠側尖端44處的電極18以及至少沿著一部分細長主體遠側部分40、靠近遠側尖端44的多個電極18。然而,可以理解,可以使用比圖中所示的更少或更多的電極。
圖2所示的設備12可以包括遠側部分40,所述遠側部分包括電極陣列48,其中一個或多個電極18耦合、附連、附接或以其他方式結合至所述電極陣列或在所述電極陣列中。此外,一個或多個傳感器,如以上討論的那些傳感器,可以耦合至或位于電極陣列48的結構中或在細長主體36上或其內,并且還可以包括在如圖1所示的局部型設備的細長主體36上或內部。遠側部分40可以包括在細長主體36內可滑動地且可旋轉地運動的軸50。電極陣列48還可以包括柔性承載臂54,所述承載臂的遠側部分聯接至軸50,并且所述承載臂的近側部分聯接至細長主體遠側部分40,使得細長主體36內的軸50的縱向運動和/或旋轉可以調節電極陣列48的配置。例如,軸50向遠端的前進可以使電極陣列48具有可以用于將所述設備遞送到靶點的線性的或至少基本上線性的構造(未示出),而軸50的縮回可以導致承載臂54從軸50徑向擴張并呈現至少基本上圓形的構造(如圖2所示)。此外,可以通過軸50在細長主體36內的旋轉來調節承載臂54的至少基本上圓形的構造的直徑。承載臂54可以沿其長度承載多個遞送電極18。所述構造可以用于將能量遞送到例如肺靜脈口。應當理解,可以使用比圖中所示更少的或更多的電極,并且可以使用替代的遠側部分和/或電極陣列構造。例如,電極陣列可以包括多于一個承載臂和/或可以包括一個或多個傳感器、標測電極、不透射線標記或其他部件。
能量遞送設備12可以可選地包括從細長主體近側部分38延伸到細長主體遠側部分40的流體遞送管腔62,并且可以包括遠側部分40中的一個或多個開口64,如位于或接近遠端尖端44,如圖1所示。在這種情況下,控制單元14可以包括與流體遞送管腔62流體連通的流體儲存器66。流體遞送管腔62可以用于遞送例如血管擴張藥物(如硝酸甘油),以解決可能根據能量發生的血管痙攣或收縮。另外地或替代性地,治療性藥理學藥劑可以通過流體遞送管腔62施用,以允許通過電滲透來增強治療藥理學藥劑的攝取。
現在參考圖3-4b,系統10可以包括第一能量遞送設備和第二能量遞送設備。圖3所示的第一能量遞送設備12a和第二能量遞送設備12b可以類似于圖1所示的設備12,但是將理解的是,系統10可以替代性地包括類似于圖2所示的設備12的第一和第二能量遞送設備,或者系統10可以包括兩個設備,所述兩個彼此相同、但具有與圖1和圖2所示的構造不同的構造或者具有彼此不同的構造、并且與圖1和圖2所示的構造相同或不同的構造。
如圖4a和4b所示,兩個遞送設備12a、12b可以用于將能量遞送到靶組織。來自單個遞送設備上的電極18的能量流可以被配置為在存在多個電極18的情況下在每隔一個電極之間(例如,在偶數編號的電極e2、e4之間或奇數編號的電極e1、e3之間,如圖1所示;或在偶數編號的電極e2、e4、e6、e8之間或在奇數編號的電極e1、e3、e5、e7之間,如圖2所示)流動,或者其可以被配置為在患者身上的一個或多個電極18與皮膚表面接地電極片24之間流動。在某些情況下,可能期望在例如每隔一個電極18之間產生雙極能量流,并且在電極18與皮膚表面接地電極片24之間產生某些部分的單極能量流。如果電極18太靠近在一起,則能量可以從一個電極到另一個電極發生電弧,但是如果電極18相距太遠,則消融圖案可能具有間隙,并且操作者可能必須重新定位所述設備以產生連續損傷,或者可能必須使用更高的電壓。所以,可以在第一次遞送中在奇數編號的電極之間遞送能量,并且可以在第二次遞送中在偶數編號的電極之間遞送能量,反之亦然。這樣可以導致連續的損傷而不需要移動導管,并且可以提供用于感測和脈沖場能遞送的最優電極起搏。
在使用多于一個遞送設備12a、12b的情況下(例如,如圖3-4b所示),可以引導能量在第一設備12a的電極18與第二設備12a的電極18之間流動,以可逆地或不可逆地影響它們之間的組織。如果電極面積的大小相似,則認為這是雙極能量遞送。作為非限制性示例,第一遞送設備12a可以位于心臟腔室內,并且第二遞送設備12b可以位于心臟的另一區域中、但鄰近第一遞送設備12a的位置,如心包腔或冠狀竇或冠狀靜脈。例如,圖4a和4b示出了第二遞送設備12b位于接近位于左心房內的第一遞送設備12a的位置的冠狀竇中。另外地或替代性地,可以在位于冠狀靜脈內的第一遞送設備12a和位于冠狀動脈內的第二遞送設備12b之間遞送能量,以首先頓抑、然后在需要時消融兩個設備12a、12b之間的心臟組織區域。如圖1所示的和描述的,第一和第二遞送設備12a、12b中的至少一個可以可選地包括用于遞送一種或多種治療化合物的流體遞送管腔62。
能量遞送可以被選擇為其對靶組織的影響中是可逆的或是不可逆的。例如,圖5示出了豬心內實驗的結果,其中將脈沖場能遞送到心臟中的固定部位,并且在多個能量遞送過程中測量所述能量遞送電極下的心臟肌肉活動的測量結果。在采集圖5中的數據的實驗中,通過導致可逆效應的遞送設備12來遞送第一級能量。接下來,由遞送設備12遞送的能量級增加,以對心臟組織造成不可逆效應。在所述實驗中,諸如圖2所示的多電極遞送設備12位于左心耳(laa)中。在向靶組織遞送能量之前,從所述電極對之一來測量以毫伏為單位的電描記圖(egm)振幅。然后,使用一個脈沖或一串20個脈沖,從設備12遞雙極能量。在已經遞送了能量之后,然后重新測量來自所述電極對的egm振幅(稱為遞送后測量),并且在已經遞送了能量之后大約兩分鐘后再次重新測量egm(稱為恢復后測量)。如果egm沒有減少,則在隨后的能量遞送中使用較高振幅或更多數量的脈沖。在圖5中示出了一系列九次能量遞送,每次遞送與先前的能量遞送相比具有增加的電壓和/或更多數量的脈沖。使用具有基本上圓形的電極陣列48(如圖2中所示的設備)的設備來遞送脈沖場能,所述電極陣列具有在陣列48上間隔大約3.75mm的9個圓柱形的3.0mm長的遞送電極18,其中以每隔一個電極18具有相反的極性(構成雙極配置的奇數編號對偶數編號的電極)的雙極方式實施脈沖場能遞送。另外,通過針對每次后續脈沖在每隔一個電極之間交替極性而以雙相方式遞送脈沖,從而產生交替的脈沖電流。在實際應用中,正脈沖和負脈沖之間的時間延遲可以為零或延長到幾百微秒。結果表明,高達200v的脈沖遞送對egm振幅具有可逆效應,而300v或更高的、1個脈沖至20個脈沖之間的電壓是對egm產生不可逆效應所需的最小設置。取決于周圍組織的類型,300v的施加電壓可以產生大約400v/cm的峰值電場強度。對于下面的組織的低能量頓抑的這種電勢可以允許操作者在遞送將導致永久性或不可逆損傷的更高的能量之前測試能量遞送對心律失常的影響。多個脈沖中的高振幅的遞送可以用于不可逆消融,而較低的振幅可以僅僅使組織頓抑。一旦識別了心律不齊的疑似焦點起源部位,則可能有利的是在永久性破壞所述部位之前測試此疑似部位的頓抑效果。如果所需的心律失常的解析是由頓抑引起的,則可以遞送更高振幅的脈沖串以不可逆地消融所述部位。當試圖定位和消融用于支持旋轉傳導波前的部位的心律失常的焦源時,如在心房顫動的傳導轉子中時,這可能是所期望的。
現在參考圖6,示出了用于將能量遞送到靶組織的方法的流程圖。通常,檢測電極-組織接觸的質量和/或消融電極朝向或遠離靶組織的運動的各種裝置。然后可以在最優組織接觸的時間期間遞送能量,并且除了心動周期內的定時之外,遞送可以基于電極-組織接觸。例如,當電極與靶組織處于可接受的接觸或者接近靶組織、并且心動周期是最優時,能量將被遞送(例如,圖7所示的遞送窗口)。通過僅在所述最優時間段內遞送,可以顯著改善消融功效。本方法可以包括用于評估與靶組織的接近度的兩個或更多個測量參數,所述測量參數當在一起分析時可以提供用于遞送治療性pfa脈沖串的最優定時點。這可以包括記錄阻抗測量結果,所述阻抗測量結果指示跟蹤導管運動的組織接觸狀態和/或導航方法。作為非限制性示例,系統10可以連續地跟蹤電極陣列48的每個能量遞送電極18的空間中的三維位置(例如,圖2所示的至少基本上圓形的陣列48),同時記錄一個或多個阻抗測量結果。
在所述方法的第一個步驟70中,可以確定患者的心動周期定時。例如,可以基于表面(例如,心外膜)心電圖(ecg)測量結果和/或基于心內電描記圖(egm)來確定心動周期定時。例如,可以測量qt間期(心臟電循環中的q波開始與t波結束之間的時間的測量,包含在qrst復合波中),并且可以確定治療能量遞送的定時,以確保在已經發生心室去極化(其可以由s波結束來表示)之后、但在開始心室復極化(其可以由t波開始或啟動來表示)之前發生。在典型的患者中,心室的去極化可能有100毫秒。
在所述方法的第二個步驟72中,可以確定心動周期內的最優消融時間。可逆的或不可逆的治療能量的遞送的最優時間可以例如基于來自一個或多個能量遞送設備12、輔助留置導管和/或體表電極的矩陣的心臟心律失常的標測來確定。從這樣的數據流可以確定最優治療能量遞送定時以中斷異常心臟傳導電路。這樣的遞送可以被定時以中斷心臟狀態,所述遞送可以圍繞核心區域旋轉或在心臟組織區域中曲流。此外,可以通過心內多電極陣列或基于體表電極的心臟傳導圖來檢測活動的焦點部位的原點。然后可以基于所述至少一個能量遞送電極18在心臟運動或電活動的循環的最優定時處位置來靶向這種心律不齊的原點。
此外,為了在某些情況下增強脈沖場消融能量的有效性,可能期望產生更廣泛的消融區域。在這種情況下,脈沖場遞送的最優定時可以在心動周期的多個時間點。通過在心臟運動循環中在多于一個或多個時間點遞送脈沖場,pfa的作用可以更廣泛地分布在組織表面上。這樣又可能導致更大的被消融的心肌的面積。多次遞送的這種定時可以被定時以與在心臟、呼吸或其他患者身體運動期間獲得的空間的物理點的范圍相一致。例如,遞送可以被定時以與x、y和z平面中的每一個平面中的心臟運動的末端一致。在心房或心室的心肌的復極化的脆弱時間段,也可能消隱或阻止這樣的遞送的發生。這樣的能量遞送可以被選擇為其對靶組織的影響中是可逆的或是不可逆的。多個脈沖中的高振幅遞送用于不可逆的消融,而較低的振幅將導致組織的可逆的頓抑。根據心律不齊的疑似焦點起源部位,則可能有利的是在永久性破壞所述部位之前測試此疑似部位的頓抑效果。如果所需的心律失常的解析是由頓抑引起的,則可以遞送更高振幅的脈沖串以不可逆地消融所述部位。當試圖定位和消融用于支持旋轉傳導波前的部位的心律失常的焦源時,如在心房顫動的傳導轉子中時,這項技術可能是所期望的。
例如,在qrs復合波完成或接近完成之后,意圖是消融心肌同時避免可能導致心律失常的肌肉刺激的治療能量的遞送的定時可以定時或發生。如圖7所示,體表心電圖(ecg)可以包括p波、q波、r波、s波、t波以及s波與t波開始之間的st段。當r波通過心室壁的主要部分時,r波可以代表電刺激。檢測到r波之后的示例性能量遞送定時可以在大約60-120毫秒,使得至少在一部分st段期間遞送能量。能量遞送可以在t波發生之前終止,而不管在st段的哪個點啟動能量遞送。此st段在圖7中被稱為“遞送窗口”。在這段時間內可以遞送能量一次或者可以多次遞送能量,如在檢測到r波之后大約80毫秒第一次遞送能量,并且在檢測到r波之后大約120毫秒第二次遞送能量。以這種方式,可以基于可選地僅在st段期間多次遞送能量,并且在初始接觸評估之后不需要評估接觸,因為在此期間能量遞送不可能引發心律失常。然而,在檢測到r波之后,遲早可以遞送能量。例如,脈沖場能可以通過增加每個脈沖之間的時間延遲而被擴展以包含更寬的時間間隔,使得整個脈沖串在心動周期期間填充所需的時間部分,其中認為遞送(如st段)或包含整個心動周期的間隔更寬的脈沖的持續時間更長是安全的,如當能量遞送電極18位于不太可能引發室性心律失常的部位時。在這種情況下,操作者可以選擇脈沖能量遞送以在更寬的時間跨度內散布以有效地將能量分配在較寬的組織表面上。糾正遞送的定時和/或確保所述電極遠離心室通常可以確保能量遞送不會引發心律失常。例如,在心房顫動的情況下,可以將能量遞送定時為在心房的p波之后立即發生。然而,在認為消融心臟內的特定細胞(確定所述細胞在其處于完全復極化狀態時暴露于高電場時更易于細胞死亡)是至關重要的情況下,盡管可能產生潛在的心律失常,但也可以定制所述遞送以做到這一點。另外,當在給予了可能具有瞬時心臟停止作用的腺苷之后檢測到心搏停止時,可以定時發生脈沖場能遞送。
在所述方法的第三個步驟74中,遞送設備12可以通過患者的脈管系統導航到心臟內的靶點。作為非限制性示例,所述遞送設備可以經由股骨通路插入患者的脈管系統中,并且可以被引導或以其他方式傳遞到心臟,并且然后進入心臟的左心房,接近一部分心房壁。盡管在圖6中示出此步驟是在確定心動周期定時的第一個步驟之后,但是應當理解,在確定患者的心動周期定時之前,可以首先將所述設備定位在靶點附近。
在所述方法的第四個步驟76中,可以確定遞送設備12的一個或多個遞送電極18與靶組織之間的接觸質量或接近度。可以在此步驟中測量和監測多個心臟特征中的任何一個或多個而用于幫助。例如,電極-組織接觸的質量可以基于:(a)心內電描記圖(egm)振幅;(b)使用單極egm測量的損傷電流;(c)egm形態,由此單相動作電勢(map)egm形態的存在表明如使用單極egm測量的直接組織接觸;(d)雙極或單極起搏脈沖通過局部心肌刺激實現心臟奪獲的能力;(e)通過局部心肌刺激實現心臟奪獲的雙極或單極起搏脈沖的振幅閾值;(f)可以通過能量遞送來刺激的神經或肌肉的接近度,可以通過監測對從所述遞送電極(可以用相同的電極實現起搏和感測)遞送的刺激來確定所述能量遞送;(g)電極-組織接觸力測量結果;(h)對足以在所接觸的組織中產生可測量的加熱的低級別能量的溫度響應;(i)低頻阻抗大小測量結果;(j)高頻阻抗大小測量結果;(k)高頻阻抗相位角測量結果;(l)在脈沖能量遞送期間測量的電流(例如,在pfa期間遞送的電流可以對應于電極-組織接觸,所以較高量的所遞送的電流可能與更好的接觸相關);(m)基于用于確定心臟中的3d位置的電勢測量結果,所述一個或多個遞送電極中的每一個的實時的勢置;(n)基于用于確定心臟中的3d位置的電磁導航測量結果,所述一個或多個遞送電極中的每一個的實時的位置;(o)基于與通過身體表面標測識別為要消融以治療心律失常的靶點的解剖部位相關的電磁或電場導航,所述一個或多個遞送電極中的每一個實時的位置;(p)基于與通過非接觸式心內感測或多電極心內心內膜標測而被識別為用于治療心律失常的能量遞送的靶點的解剖部位有關的電磁或電場導航,所述一個或多個遞送電極中的每一個實時的位置;(q)基于例如第一遞送設備12a中的超聲發射和接收元件以及第二遞送設備中的類似的超聲發射、接收或回波元件或與通過非接觸式心內感測或多電極心內心內膜標測被識別為用于消融以治療心律失常的靶點的解剖部位有關的輔助設備,所述一個或多個遞送電極中的每一個的實時的位置;(r)所述一個或多個遞送電極中的每一個的實時的位置,基于與解剖部位有關的結合到電極陣列48中的超聲元件,所述解剖部位通過非接觸式心內感測或多電極心內心內膜標測而被識別為用于能量遞送以治療心律失常的靶部位;(s)從一個或多個加速度計或安裝在所述遞送設備中的其他傳感器20測量的一個或多個遞送電極的瞬時穩定性;和/或(t)通過經胸和心內阻抗測量(例如,取自兩個、三個或四個電極)確定的心動周期中的時間和呼吸周期的定時。(a)-(t)中涉及的所有或任何測量都可以在pfa程序期間連續進行。
上述這樣的測量可以提供關于能量遞送導管與靶組織的接觸質量或接近度的信息。可以從放大器系統(也稱為ep記錄系統)采集表示組織接觸和/或接近度的測量結果,其中將來自一個或多個導管電極的電描記圖顯示給操作者,并且可以進行分析、保存和/或存檔。可以使用基于計算機的定位系統(也稱為電解剖標測或導航系統)進一步采集示出導管接觸和/或接近度的測量結果,這樣可以使用阻抗和/或電磁(接觸和/或非接觸)來對電極和/或導管進行定位。另外,可以從能量遞送導管內的超聲換能器以及從在所述過程中使用的其他心內或經胸超聲心動圖設備來采集測量結果,其可以在超聲心動圖系統上提供視覺導管接觸和/或接近度信息。放置在所述能量遞送導管和/或其他心內導管中的加速度計還可以經由與加速度計運動相關聯的電壓來提供導管接觸和/或接近度的測量結果。
在所述方法的第五個步驟78中,當電極-組織接觸的質量被確定為足夠時,或者電極18位于最優的接近靶組織的位置、并且所述接觸或接近發生在心動周期內的最優消融時間時,可以將脈沖相能量從遞送設備12遞送到靶組織。可以遞送能量,使得引起對組織可逆的或不可逆的效應。例如,如以上所討論的,可以頓抑所述組織(引起可逆效應),以便定位目標消融部位并且然后可以消融所述部位(引起不可逆效應)。可以通過在遞送脈沖場能之前主動地向心臟遞送起搏刺激來控制心動周期的定時。這種起搏可以從例如單獨的留置導管或能量遞送設備12的遞送電極18進行遞送。一旦在簡短的一系列起搏脈沖之后實現心臟奪獲,例如,奪獲心臟五個心跳,并且當滿足指示能量傳遞電極18到靶組織的接近度的選擇標準時,所遞送的能量可以被定時以跟隨所需時間窗口內的最后的起搏刺激。這種能量遞送可以設定為使組織頓抑并且不會引起實質上不可逆的損傷的水平,或者其可以處于不可逆的燒蝕電場強度。另外,可以進行這種能量遞送,緊接著是評估可逆的或不可逆的能量遞送的影響的立即的或延遲的起搏刺激。
除了或代替加速度計之外,與組織的運動或接觸可以由其他傳感器20來檢測,如位于一個或多個遞送設備12的電極陣列48的結構中的壓電元件(如壓電晶體)、應變儀或光纖布拉格傳感器。這類運動、力或加速度檢測器可以具有如壓電的、電容的、慣性的或光學的各種設計。雖然在圖1和圖2中示出了廣義的傳感器20,但是應當理解,可以使用一個或多個傳感器20并且在除了所示的傳感器之外的位置處。這些傳感器20可以確定電極陣列和所述陣列的能量遞送元件的相對運動,使得能量遞送可以被定時以與特定時間點一致,無論根據操作者的意愿是在特定組織部位上還是在更廣泛分布的組織部位上進行能量遞送。可選地,能量遞送可以分布在更大組織區域上,以完成更大的頓抑和/或消融區域。在這種情況下,可以使用遞送設備的電極部的三維加速度、運動或力/接觸檢測來確定三維空間內的運動的極限,以在心臟或其他組織的區域內的最寬的位置范圍內遞送能量。可以有利地使用力或壁的運動或擴張來降低實現肌細胞死亡的閾值。所述力或擴張可以解釋為組織中拉伸的措施,其具有將肌肉細胞物理伸長到較低的施加電壓將導致每個肌細胞的致死電壓的程度。在這種情況下,使用減小的施加電場強度可以更容易地消融心臟的拉伸或細長部分。特別是在廣泛分布的能量遞送的這種情況下,可能需要使用在極短時間幀內最優的脈沖能量參數。在這種情況下,可能需要在短達0.10微秒至高達20微秒的脈沖持續時間中遞送脈沖能量。可以設置脈沖間或相間的定時,以使整個遞送在幾十毫秒或更短的時間內完成,取決于到靶組織的能量遞送的所需精度。這樣的短脈沖持續時間也可以避免神經和骨骼肌的刺激,這種刺激可能是不期望的。在需要在較大區域上傳播能量遞送的情況下,可以使用延長數十毫秒以上的較長的脈沖串。
在一些實施例中,可以在第一遞送設備12a的一個或多個電極18與第二遞送設備12b之間遞送雙極能量。在這種情況下,最優消融定時可以是:(a)在第一遞送設備12a上的特定的或全部遞送電極18與第二遞送設備12b上的特定電極18或所有電極18之間的距離最小的時刻;(b)身體內針對靶組織的消融而言最優的組織接觸質量或位置;(c)如果第二遞送設備12b或輔助設備用作局部接地返回路徑、并且不旨在消融與第二遞送設備12b直接相鄰的組織,則缺少組織接近度或缺少第二傳送設備12b的電極-組織接觸;和/或(d)通過在所述第一和第二遞送裝置上的一個或多個電極之間的最小阻抗值、透視成像、電磁場導航、電場導航或其組合過程中進行發現和遞送、采用第一和第二遞送設備12a、12b上的電極之間的阻抗大小、使用第一和第二遞送設備12a、12b中的超聲發射和接收元件進行確定的如在(a)-(c)中的最優定時。在非限制性示例中,第一遞送設備12a可以是多電極心內導管,并且第二遞送設備12b可以是冠狀竇多電極導管,并且能量遞送可以被選擇為在第二遞送設備12b上的選定電極18與第一遞送設備12a上的電極18之間進行引導,基于使用例如以上討論的方法(a)-(t)來確定的位置被確定為最接近第二遞送裝置12b上的所選的一個或多個電極18。然后可以在第一和第二遞送設備12a、12b上的這些最優電極之間遞送能量遞送。
在pfa中,幾十毫秒是確保一個或多個電極18在最優位置保持足夠長的時間段以實現有效的能量遞送的足夠短的時間段。除了對能量遞送進行定時以與所述電極相對于目標消融部位的最優位置和穩定性相一致之外,能量遞送還可以被定時以與靶組織部位內的細胞的最脆弱狀態相一致。對于脈沖場能遞送,這可以包括心肌細胞或其他肌細胞的最大長度狀態。另外,在能量遞送電極附近可能存在不是預期的消融目標、并且應該被保護以免于消融的脆弱組織。在這種情況下,能量遞送可以被定時以與這些組織的最不易受損的狀態相一致。這可能涉及非靶組織內的細胞的物理狀態,或者其可能與最不有效的能量向量的時刻有關以確保非靶組織的保留。例如,這可以通過激活或停用多電極消融系統內的特定電極來實現。作為確保不發生意外的組織損傷的另外的措施,可以通過每個電極18中的溫度傳感器20a在pfa之后立即測量組織溫度,以確認沒有產生過多的熱效應。
此外,為了在某些情況下增強脈沖場消融能量的有效性,可能期望產生更廣泛的消融區域。在這種情況下,脈沖場遞送的最優定時可以在心動周期的多個時間點。通過在心臟運動循環中在多于一個或多個時間點遞送脈沖場,pfa的作用可以更廣泛地分布在組織表面上。這樣又可能導致更大的被消融的心肌的面積。多次遞送的這種定時可以被定時以與在心臟或呼吸或其他患者身體運動期間獲得的空間的物理點的范圍相一致。遞送可以被定時以與x、y和z平面中的每一個平面中的心臟運動的末端一致。在心房或心室的心肌的復極化的脆弱時間段,也可能消隱或阻止這樣的遞送的發生。
使用這種方法,可以在被確定為可能產生非預期消融或非靶組織消融的時間期間避免能量遞送。除了進行以上討論的一個或多個連續測量(a)-(t)之外,所述方法還可以包括隨時間監測活動以確定呼吸、心臟或其他特征循環長度的趨勢。這些趨勢可以在幾秒到幾十秒的時間內進行評估,以驗證位置或接觸的變化是否隨時間發生或者電極的接觸和位置是否穩定。另外,可以相對于通過體表或其他非侵入性標測技術將所述靶部位識別為足夠接近用于能量遞送以實現預期消融效果的靶部位來監測電極18的相對位置。
具有定時能量遞送的pfa可以治療大多數心律失常而需要在每個組織部位處不超過幾秒鐘,用于完成多個治療性脈沖能量串,而熱消融技術通常每個能量遞送部位需要30至240秒。在需要消融多個部位的過程中,pfa可以實質上減少整個手術時間。
另外,pfa技術可以降低手術復雜性,并且可以消除與熱消融技術相關的最可怕的風險和并發癥。此外,pfa不需要鹽水沖洗來冷卻電極,這樣消除了具有心力衰竭或腎并發癥的患者的流體超載問題。熱消融技術(如射頻消融)也可能破壞心臟內膜表面,激活外源性凝血級聯,并導致燒焦/凝塊和血栓的形成,這樣又可能導致全身血栓栓塞、腦損傷以及可能的中風或心肌缺血。pfa還可以為持續形式的心房顫動(af)的治療提供重要的優點。持續形式的af的當前治療包括肺靜脈隔離,所述肺靜脈隔離可以用常規技術相對安全地進行。然而,為了有效治療持續性房顫,經常在左后心房造成附加的消融,其中存在可能對位于后壁后面僅數毫米處的食道造成損傷的顯著風險。這種風險限制了醫生愿意進行消融的程度,從而限制了手術的療效。避免與產生組織加熱相關的風險的參數包括小于大約60微秒(例如小于20微秒)的方波脈沖持續時間。脈沖之間的定時可以在例如100微秒與800微秒之間的范圍內。可以使用例如10個至2000個脈沖串,取決于治療的具體情況和期望的效果。通過在每個電極定位中遞送多于一個脈沖串,也可以增強能量遞送的有效性。這種增強可以通過遞送數個脈沖串而在心臟組織中完成,每個心動周期遞送一個脈沖串。
本領域技術人員將理解的是,本申請不限制上文中已經具體示出和/或描述的內容。另外,除非上文相反地陳述,否則應當注意所有附圖是不按比例的。鑒于以上傳授內容,在不背離本發明的范圍和精神的情況下,多種修改和變化是可能的。
- 還沒有人留言評論。精彩留言會獲得點贊!