酰基輔酶A:膽固醇酰基轉移酶ACAT1抑制劑的新用途的制作方法
本發明屬于生物技術領域,特別是涉及酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑的新用途。
背景技術:
惡性腫瘤是目前致死率最大的疾病之一,常規治療手段如手術切除、放療和化療等手段較多應用于腫瘤治療中,但目前這些手段在治療腫瘤中有其局限性,且很難徹底治愈腫瘤,尤其是一些轉移型惡性腫瘤。
免疫治療一直以來是腫瘤治療的研究熱點。雖然靶標特異性弱且毒性較大,細胞因子白介素-2(interleukin-2,il2)和干擾素α(interferon-α,ifnα)被用于腎細胞癌和黑色素瘤治療已有二十多年。近年來,隨著抗pd-1和抗ctla-4等免疫檢測點阻斷抗體在腫瘤免疫治療中得到應用,腫瘤免疫治療已經取得突破性的進展。目前腫瘤免疫治療的手段主要有t細胞過繼療法(adoptivecelltherapy,act)、免疫檢測點阻斷療法(抗pd-1,抗pd-l1和抗ctla-4抗體治療)、腫瘤疫苗以及嵌合抗原受體t細胞治療(chimericantigenreceptort-cellimmunotherapy)等,這些方法雖然目前都已經在臨床研究上取得不錯的進展,但由于腫瘤細胞的異質性以及腫瘤微環境的復雜性,腫瘤免疫治療目前仍然面臨許多重要障礙。
cd8t細胞是腫瘤免疫治療的核心,是腫瘤的特異性殺傷細胞,其殺傷能力強弱以及在腫瘤組織中的浸潤情況直接與腫瘤的預后直接相關,而且直接關系腫瘤免疫治療的成敗。由于腫瘤微環境是一個免疫抑制的環境,cd8t細胞的功能受到腫瘤微環境的抑制,目前免疫檢測點阻斷抗體抗pd-1,抗pd-l1和抗ctla-4抗體在治療黑色素瘤的臨床試驗中雖然整體效果不錯,但單獨使用時各自的客觀反應率(objectiveresponserate)以及抗pd-1和抗ctla-4抗體聯合治療客觀反應率還是不盡如人意。這意味著急需發展新的靶點以進一步增強腫瘤中cd8t細胞的功能。
細胞內膽固醇代謝通路包括膽固醇合成、轉運以及儲存等途徑,其中膽固醇合成通路主要由scap/srebp復合物以及其下游膽固醇合成限速酶hmgcr調控;膽固醇的轉運途徑的調控主要受低密度脂蛋白受體(ldlreceptor)、內體(endosome)和溶酶體(lysosome)中npc1/2等蛋白及復合物的調控;而膽固醇存儲則受膽固醇的酯化修飾以及去酯化修飾的調控,關鍵調控蛋白包括酰基輔酶a:膽固醇酰基轉移酶acat1/2和膽固醇酯水解酶(ceh)。已 有研究表明,acat1是一個治療動脈粥樣硬化以及阿爾茨海默病的靶點,并已基于此開發了一些小分子抑制劑在進行臨床實驗,如avasimibe具有很好的臨床安全性。但是現有技術并沒有披露acat1與腫瘤的免疫治療之間的關聯。
技術實現要素:
鑒于以上所述現有技術的缺點,本發明的目的在于提供酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑的新用途。
本發明一方面提供了酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑在制備化學產品中的用途,所述化學產品至少具備以下功用之一:
1)增強cd8t細胞對腫瘤的殺傷活性;
2)增強cd8t細胞的效應功能;
3)促進cd8t細胞的增殖;
4)減少cd8t細胞的凋亡;
5)促進cd8t細胞細胞質膜上t細胞抗原受體(tcr)成簇;
6)促進cd8t細胞免疫突觸的形成;
7)促進cd8t細胞定向釋放細胞毒顆粒;
8)提高哺乳動物對于腫瘤的免疫能力。
所述酰基輔酶a:膽固醇酰基轉移酶acat1的抑制劑是指對于酰基輔酶a:膽固醇酰基轉移酶acat1具有抑制效果的化合物。
對于酰基輔酶a:膽固醇酰基轉移酶acat1具有抑制效果包括但不限于:抑制酰基輔酶a:膽固醇酰基轉移酶acat1活性,或者抑制酰基輔酶a:膽固醇酰基轉移酶acat1的基因轉錄或表達。
所述的酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑可為sirna、shrna、抗體、小分子化合物。
如本發明實施例列舉的,所述酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑選自:avasimibe、k604、cp113,818,所述酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑還可選自:purpactins、manassantina、diphenylpyridazinederivatives、glisoprenina、pactimibe、ci976、tmp-153、ym750、geri-bp002-a、sandoz58-035、vulm1457、cl-283,546、ci-999、e5324、ym17e,fr182980、pd132301-2、f-1394、hl-004、f-12511(eflucimibe)、cinnamicacidderivatives、dup128、rp-73163、pyripyropenec、fo-1289、as-183、spc-15549、beaui、beauiii、fo-6979、angelica、ginseng、decursin、terpendolec、beauvericin、spylidone、 pentacecilides、cl-283,546、cinnamicderivatives、betulinicacid、shikoninderivatives、esculeogenina和wu-v-23等。
所述化學產品必然包含酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑,并以酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑作為前述功用的有效成分。
所述化學產品中,發揮前述功用的有效成分可僅為酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑,亦可包含其他可起到類似功用的化學品。
所述化學產品可以為單成分物質,亦可為多成分物質。
所述化學產品的形式無特殊限制,可以為固體、液體、凝膠、半流質、氣霧等各種物質形式。
所述化學產品所使用的領域可以為藥品領域、保健品領域、食品領域等。
所述腫瘤免疫治療針對的腫瘤包括實體瘤和非實體瘤,包括但不限于:鼻腔及鼻竇惡性腫瘤、鼻咽癌、口腔癌、喉癌、涎腺腫瘤、顱內腫瘤、甲狀腺癌、舌癌、肺癌、食管癌、賁門癌、乳腺癌、縱膈腫瘤、胃癌、大腸癌、乙狀結腸和直腸癌、肝癌、胰腺癌與壺腹周圍癌、膽道癌、小腸腫瘤、腎癌、前列腺癌、膀胱癌、睪丸惡性腫瘤、陰莖癌、子宮頸癌、子宮內膜癌、卵巢癌、纖維組織細胞瘤、橫紋肌肉瘤、滑膜肉瘤、黑色素瘤、骨肉瘤、尤文氏肉瘤、淋巴瘤、多發性骨髓瘤、白血病等。
所述腫瘤免疫治療及提高對于腫瘤的免疫能力主要針對的對象為哺乳動物,如嚙齒類動物、靈長類動物等。
本發明第二方面提供了一種腫瘤免疫治療的方法,為向對象施用酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑。
所述的對象為哺乳動物或所述哺乳動物的cd8t細胞。所述哺乳動物優選為嚙齒目動物、偶蹄目動物、奇蹄目動物、兔形目動物、靈長目動物等。所述靈長目動物優選為猴、猿或智人。所述cd8t細胞可為離體cd8t細胞。
所述對象可以是罹患腫瘤的患者或期待提高抗腫瘤免疫力的個體,或者所述對象為腫瘤患者或期待提高腫瘤預防能力的個體的離體ctl細胞。
所述酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑可以在接受腫瘤免疫治療前、中、后向對象施用。
本發明第三方面提供了一種腫瘤免疫治療藥物,包括有效量的酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑及藥用載體。
本發明第四方面提供了一種腫瘤聯合治療藥物組合,包括有效量的酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑和至少一種其他腫瘤治療藥物。
所述其他腫瘤治療藥物是指除酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑以外的腫瘤治療藥物。
所述聯合治療藥物組合可以是以下形式中的任意一種:
一)將酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑和其他腫瘤治療藥物分別制成獨立的制劑,制劑的劑型可相同或不同,給藥途徑亦可相同或不同。
當其他腫瘤治療藥物為抗腫瘤抗體時,一般采用胃腸外給藥型。當其他腫瘤治療藥物為化療藥物時,給藥形式可以比較豐富,可以是胃腸道給藥亦可以是非胃腸道給藥。一般推薦針對各化療藥物的已知給藥途徑給藥。
二)將酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑和其他腫瘤治療藥物配置成復方制劑。在將酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑和其他腫瘤治療藥物采用相同給藥途徑給藥并同時施加時,可采用將兩者配置成復方制劑的形式。
本發明第四方面提供了一種腫瘤治療方法,為向對象施用有效量的酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑,以及向對象施用有效量的其他腫瘤治療藥物和/或向對象實施其他腫瘤治療手段。
可以同步的或順序地給予有效量的酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑和至少一種有效量的其他腫瘤治療藥物。
基于酰基輔酶a:膽固醇酰基轉移酶acat1為新發現的腫瘤免疫治療靶點,在與酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑以外的其他腫瘤治療藥物聯合用藥中,至少可以起到療效相加的效果,進一步增強對于腫瘤的抑制。
所述其他腫瘤治療藥物指不具備包括但不限于:抗腫瘤抗體、化療藥物或靶向型藥物等。
所述酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑可以是胃腸道給藥或者胃腸外給藥。所述其他腫瘤治療藥物可以是胃腸道給藥或者胃腸外給藥。對于抗腫瘤抗體或化療藥物,一般采用胃腸外給藥。
本發明的優點在于:
(1)通過一系列體外實驗,發現acat1在調控cd8t細胞免疫應答反應上起著關鍵作用,抑制acat1的活性可以增強cd8t細胞的抗原特異性免疫應答反應,增強其對靶細胞的殺傷能力,而不影響cd8t細胞對自身抗原的響應;
(2)通過膽固醇定量、顯微成像、流式以及westernblot等方法,發現抑制acat1活性重編程cd8t細胞膽固醇代謝,上調cd8t細胞脂膜上膽固醇水平。細胞質膜膽固醇水平的上升一方面進而促進tcr微簇形成,增強tcr信號通路的活化,最終增強cd8t細胞的免疫應答反應;另一方面細胞質膜膽固醇水平提高后,可以促進cd8t細胞免疫突觸的形成,增強cd8t細胞對靶細胞的直接殺傷能力;
(3)在動物水平上,t細胞特異性基因敲除acat1或者通過抑制劑抑制acat1活性可以增強cd8t細胞免疫應答能力,在小鼠黑色素瘤模型和小鼠肺癌模型中增強cd8t細胞的抗腫瘤活性;表明acat1作為關鍵免疫靶點,在腫瘤免疫治療上有著潛在的臨床應用價值。
(4)現有技術雖然論證了酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑的用藥安全性,但是酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑原適應癥的臨床效果并不理想。本發明在腫瘤免疫治療領域給酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑提供了新的臨床應用價值,為其進一步的市場應用開辟了廣闊的前景。
附圖說明
圖1.抑制膽固醇代謝相關通路影響cd8t細胞的效應功能。
a-d.分別抑制膽固醇合成(lovastatin:hmgcr抑制劑)、膽固醇運輸(u18666a)和膽固醇酯酰化修飾(cp113,818和k604)后,通過胞內染色和流式細胞術檢測cd8t細胞活化(α-cd3(5μg/ml)和α-cd28(5μg/ml)鋪板刺激)后顆粒酶b(gzmb),細胞因子ifnγ和tnfα的表達。
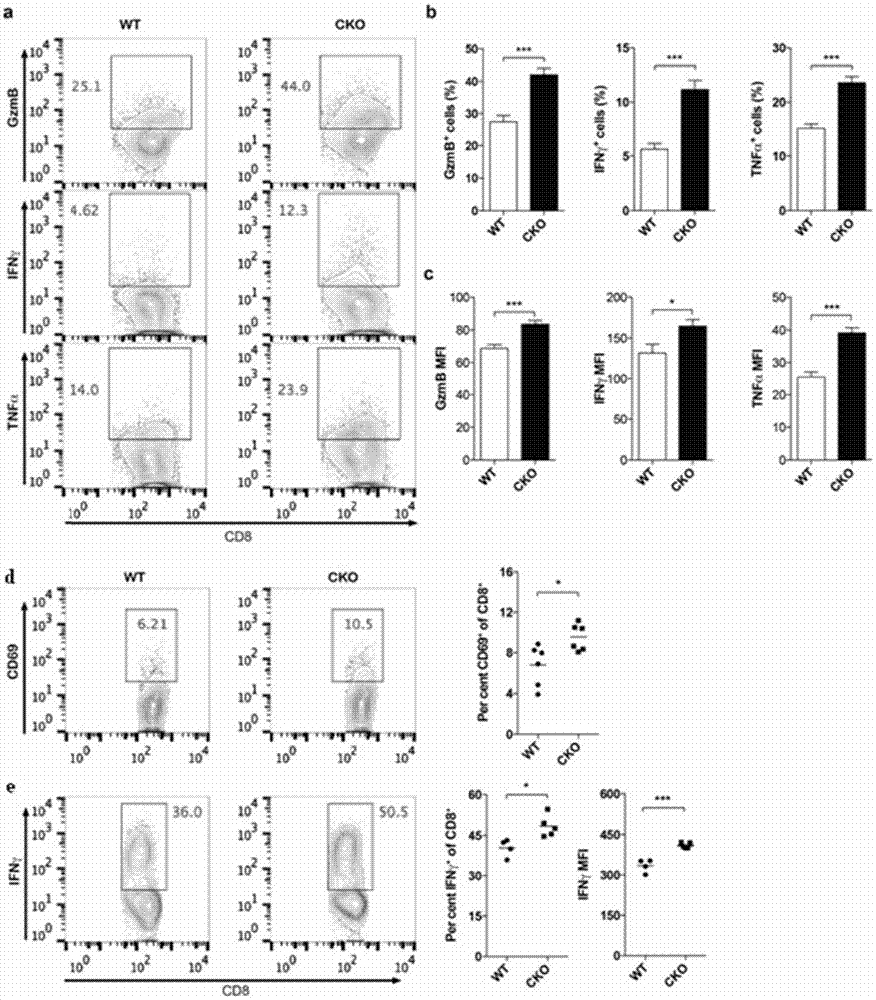
圖2.t細胞特異性敲除acat1增強cd8t細胞功能。
a‐c.通過胞內染色和流式細胞術檢測野生型(wt)和acat1基因敲除acat1cko(cko)cd8t細胞活化(α-cd3(5μg/ml)和α-cd28(5μg/ml)鋪板刺激)后顆粒酶b,細胞因子ifnγ和tnfα的表達;
d‐e.野生型小鼠(wt)和acat1cko小鼠(cko)感染李斯特菌(listeriamonocytogenes)7天后,流式檢測脾臟中cd8t細胞活化標志物cd69(n=6)和細胞因子ifnγ的表達(n=4-5)。
圖3.acat1敲除促進cd8t細胞增殖以及減少cd8t細胞凋亡。
a.活細胞熒光染料cfse標記野生型(wt)和acat1基因敲除(cko)cd8t細胞,然后鋪板抗體刺激細胞(1μg/mlα-cd3+1μg/mlα-cd28),通過流式檢測cfse熒光強度檢測細胞的分裂情況;
b.小鼠脾臟分離得到的cd8t細胞培養24小時后,annexinv和pi(propidiumidiode)染色,檢測細胞的凋亡情況;
c.鋪板抗體(5μg/mlα-cd3+5μg/mlα-cd28)刺激野生型和acat1ckocd8t細胞24小時,然后annexinv和pi(propidiumidiode)染色,檢測細胞的凋亡情況。
圖4.acat1敲除增強ot-icd8t細胞對特異性抗原的免疫應答,且并不引發對自身抗原的免疫應答。
a.c57bl/6小鼠來源的脾臟細胞呈遞外來抗原(n4,a2,t4和g4)或者自身抗原(r4和catnb)后作為抗原遞呈細胞(antigen-presentingcell,apc)刺激
b.c57bl/6小鼠來源的脾臟細胞呈遞ova抗原(ova257-264)后作為抗原遞呈細胞刺激
c.取3月齡小鼠血清,elisa方法檢測血清中細胞因子ifnγ和自身抗體抗雙鏈dnaigg水平。
圖5.acat1敲除增強cd8t細胞抗腫瘤活性。
a-b.野生型小鼠和acat1cko小鼠中黑色素瘤生長速度以及小鼠的生存曲線分析。腫瘤生長曲線用two-wayanova統計方法分析,小鼠的生存曲線用log-rank(mantel-cox)統計方法分析;
c-d.野生型和acat1cko小鼠在注射b16f10黑色素瘤細胞后,在第16天將腫瘤取出,通過流式分析cd8t細胞中cd44、顆粒酶b、ifnγ和tnfα的表達,同時對腫瘤浸潤的cd8t細胞進行計數,通過流式檢測cd8/cd4t細胞比比率以及cd8t細胞增殖標志物ki-67的表達;
e.流式檢測腫瘤浸潤cd8t細胞表面免疫檢測點受體pd-1和ctla-4的表達;
f.胞內染色和流式檢測腫瘤浸潤的treg細胞(cd4+foxp3+)的比例;
g-h.流式檢測引流淋巴結中cd8t細胞中cd44、ifnγ的表達,同時對cd8t細胞進行計數,通過流式檢測cd8/cd4t細胞比比率;
i-k.黑色素瘤肺轉移模型,在注射黑色素瘤細胞后第20天,檢測肺臟中腫瘤數量,同時繼續記錄剩余小鼠的生存率和生存時間,小鼠的生存曲線用log-rank(mantel-cox)統計方法分析;
l.黑色素瘤肺轉移模型中,蘇木精-伊紅染色觀察腫瘤細胞在肺臟中的浸潤情況;
m.黑色素瘤肺轉移模型中,流式檢測肺臟中cd8t細胞cd44、顆粒酶b、ifnγ和tnfα 的表達;
n-p.將體外誘導分化成熟的野生型和acat1ckoot-ictl尾靜脈注射到荷瘤b16f10-ova(b16f10黑色素瘤細胞中表達ovalbumin)的c57bl/6野生型小鼠中,檢測腫瘤的生長以及小鼠的生存率。
圖6.acat1敲除促進cd8t細胞tcr微簇形成并增強tcr信號通路活化。
a.野生型和acat1cko
b.流式檢測野生型和acat1ckocd8t細胞表面tcr(cd3)和cd8水平;
c.storm對野生型和acat1ckocd8t細胞活化前后膜表面tcr的分布進行成像;
d-e.對圖c獲得的成像結果進行ripley’skfunction分析,r代表tcr微簇的大小,l(r)-r代表tcr微簇形成的程度。
圖7.acat1敲除促進cd8t細胞免疫突觸的形成。
a-b.tirfm對cd8t細胞的tcr進行活細胞動態成像,檢測野生型和acat1ckocd8t細胞免疫突觸的形成;
c-e.對免疫突觸中tcr微簇的動態行為進行分析;追蹤了來自19個野生型cd8t細胞和20個acat1ckocd8t細胞中超過1400個tcr微簇的運動,分析其平均平方位移msd(meansquaredisplacement),擴散系數的累計概率分布cpd(cumulativeprobabilitydistribution)和擴散系數diffusioncoefficient。
圖8.acat1敲除不影響cd4t細胞的免疫應答反應。
a-b.α-cd3(5μg/ml)和α-cd28(5μg/ml)鋪板刺激活化
c.實時定量pcr檢測
d.α-cd3(5μg/ml)和α-cd28(5μg/ml)鋪板刺激活化野生型和acat1cko
e-f.通過胞內染色和流式細胞術檢測野生型(wt)和acat1敲除(cko)cd4t細胞活化(α-cd3(5μg/ml)和α-cd28(5μg/ml)鋪板刺激活化后細胞因子il-2和tnfα的表達;
g-h.野生型小鼠(wt)和acat1敲除小鼠(cko)感染李斯特菌(listeriamonocytogenes)7天后,流式檢測脾臟中cd4t細胞活化標志物cd69(n=6)和細胞因子ifnγ的表達(n =5–6)。
圖9.acat抑制劑avasimibe處理增強cd8t細胞抗腫瘤能力。
a.野生型cd8t細胞用avasimibe處理(37℃,6小時,即于rpmi1640完全培養基中加藥后,37℃co2培養箱中培養處理6小時,處理完之后用培養基或pbs離心清洗3次),隨后通過鋪板抗體α-cd3(5μg/ml)+α-cd28(5μg/ml)刺激24小時,然后胞內染色和流式檢測顆粒酶b,細胞因子ifnγ和tnfα的表達;
b.avasimibe處理ot-ictl(37℃,6小時)處理方式同a,通過檢測ldh的釋放分析ot-ictl對靶細胞el-4的殺傷效率;
c.mts方法檢測avasimibe處理對黑色素瘤細胞b16f10細胞活率的影響;
d-f.avasimibe處理b16f10黑色素瘤荷瘤c57bl/6野生型小鼠,檢測腫瘤生長曲線和小鼠生存率;
g-h.在注射腫瘤后第18天將腫瘤取出,通過流式分析腫瘤浸潤的cd8t細胞中cd44、顆粒酶b、ifnγ和tnfα的表達,同時對腫瘤浸潤的cd8t細胞進行計數,通過流式檢測cd8/cd4t細胞比比率以及cd8t細胞增殖標志物ki-67的表達;
i.流式檢測腫瘤浸潤cd8t細胞表面免疫檢測點受體pd-1和ctla-4的表達;
j.胞內染色和流式檢測腫瘤浸潤的treg細胞(cd4+foxp3+)的比例;
k.流式檢測腫瘤組織中mdsc細胞(gr1+cd11b+cd45+)的比例。
圖10.avasimibe處理上調cd8t細胞質膜上膽固醇水平,促進tcr微簇和免疫突觸形成,增強tcr信號通路的活化。
a-b.avasimibe處理cd8t細胞(37℃,6小時),filipiniii染色檢測cd8t細胞游離膽固醇的分布;細胞質膜膽固醇的相對定量結果通過leicalasaf軟件處理獲取;
c.avasimibe處理cd8t細胞后,通過storm對cd8t細胞質膜表面tcr的分布進行分析;
d-e.對圖c獲得的成像信息進行ripley’kfunction分析,r代表tcr微簇的大小,l(r)-r代表tcr微簇形成的程度;
f-g.avasimibe處理cd8t細胞后,通過tirfm檢測cd8t細胞免疫突觸的形成;
h.avasimibe處理ot-ictl細胞后,用2μg/mlα-cd3和2μg/mlα-cd28激活ctl,然后western-blotting檢測tcr近端信號通路和下游信號通路的活化情況;
i-k.storm對腫瘤浸潤的cd8t細胞進行成像以及ripley’kfunction分析。
圖11.acat2基因敲除不影響cd8t細胞的效應功能。
a-f.通過胞內染色和流式細胞術檢測野生型(acat2+/+)和acat2基因敲除(acat2-/-)cd8t細胞活化(α-cd3+α-cd28鋪板刺激)后顆粒酶b,細胞因子ifnγ和tnfα的表達。
圖12.acat1基因敲除促進ctl細胞定向釋放細胞毒顆粒
a.三維共聚焦熒光顯微檢測cd107a+細胞毒顆粒在ctl細胞中的分布,三維重構后用imaris軟件計算免疫突觸2μm范圍內cd107a+細胞毒顆粒體積;mann-whitneyu檢驗用于差異顯著性分析。
b.ot-ictl細胞與遞呈ova257-264抗原肽的el-4靶細胞共培養,通過流式檢測ctl細胞表面和內吞的cd107a來檢測細胞毒顆粒脫顆粒效應;雙尾t檢驗用于差異顯著性分析。
圖13.acat抑制劑增強人pbmc中cd8+t細胞的效應功能
*p<0.05;**p<0.01;***p<0.001。
圖14.acat1基因敲除和avasimibe抑制小鼠llc肺癌發展進程。
a-c.llc肺癌在野生型小鼠和acat1基因敲除小鼠中的進程,小鼠生存曲線用log-rank(mantel-cox)統計方法進行分析;
d-g.avasimibe處理llc(lewislungcarcinoma)肺癌荷瘤的小鼠,評估avasimibe在治療小鼠肺癌中的功效,給藥路徑、給藥天數及每日劑量見圖d,小鼠生存曲線用log-rank(mantel-cox)統計方法進行分析;
圖15.avasimibe與α-pd-1抗體聯合處理抑制小鼠黑色素瘤發展進程。
a-c.對b16f10黑色素瘤荷瘤的野生型c57bl/6小鼠進行avasimibe與α-pd-1抗體聯合治療,檢測腫瘤生長曲線和小鼠生存率,比較聯合治療與單一療法效果的差異,給藥路徑、給藥天數及每日劑量見圖a,小鼠生存曲線用log-rank(mantel-cox)統計方法進行分析(n=10)。
d.在注射腫瘤后第18天(avasimibe給藥4次)將腫瘤取出,通過流式分析腫瘤浸潤的pd-1高表達和低表達的dcd8t細胞中cd44、顆粒酶b、ifnγ和tnfα的表達;
e.在抗pd-1抗體給藥3次后(注射腫瘤后18天),通過磁珠分選得到腫瘤浸潤的cd8t細胞,抽提rna,檢測相關基因的表達水平。
i.g.-灌胃給藥,i.p.-腹腔注射給藥
圖16.avasimibe與化療藥dacarbazine聯合用藥抑制小鼠黑色素瘤發展進程。
a-c.對b16f10黑色素瘤荷瘤的野生型c57bl/6小鼠進行avasimibe與化療藥dacarbazine聯合用藥治療,檢測腫瘤生長曲線和小鼠生存率,比較聯合治療與單一療法效果的差異,給藥路徑、給藥天數及每日劑量見圖a,小鼠生存曲線用log-rank(mantel-cox)統計方 法進行分析。
i.g.-灌胃給藥,i.p.-腹腔注射給藥
具體實施方式
本發明在研究中發現,acat1在調控cd8t細胞免疫應答反應上起著關鍵作用,抑制acat1的活性可增強cd8t細胞的免疫應答能力;增強cd8t細胞對腫瘤的殺傷活性;增強cd8t細胞的效應功能;促進cd8t細胞的增殖;減少cd8t細胞的凋亡;促進cd8t細胞細胞質膜上tcr成簇;促進cd8t細胞免疫突觸的形成,且抑制acat1的活性不影響cd8t細胞對自身抗原的響應。由此認為酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑可用于腫瘤免疫治療或者提高對于腫瘤的免疫能力。
酰基輔酶a:膽固醇酰基轉移酶acat
酰基輔酶a:膽固醇酰基轉移酶acat是調控細胞內膽固醇代謝的平衡的一種酶,在生物體內催化膽固醇與長鏈脂肪酸形成膽固醇酯。在哺乳動物細胞中發現兩種同工異構酶acat1和acat2。acat1選擇性地在組織與細胞中表達,與細胞內膽固醇代謝平衡有關;而acat2則廣泛存在于肝臟、胃腸道等細胞中,主要參與飲食中膽固醇的吸收和載脂蛋白的裝配。
酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑
是指對于酰基輔酶a:膽固醇酰基轉移酶acat1具有抑制效果的化合物。對于酰基輔酶a:膽固醇酰基轉移酶acat1具有抑制效果包括但不限于:抑制酰基輔酶a:膽固醇酰基轉移酶acat1活性,或者抑制酰基輔酶a:膽固醇酰基轉移酶acat1的基因轉錄或表達。
所述的酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑包括但不限于為sirna、shrna、抗體、小分子化合物。
所述酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑可以是對acat1與acat2沒有選擇性的acat抑制劑,已知的例如purpactins,manassantina,diphenylpyridazinederivatives,glisoprenina,cp113,818、avasimibe、pactimibe等,也可以是對acat1具有選擇性抑制的抑制劑,已知的例如k604等。還可以選自ci976、tmp-153、ym750、geri-bp002-a、sandoz58-035、vulm1457、cl-283,546、ci-999、e5324、ym17e,fr182980、pd132301-2、f-1394、hl-004、f-12511(eflucimibe)、cinnamicacidderivatives、dup128、rp-73163、pyripyropenec、fo-1289、as-183、spc-15549、beaui、beauiii、fo-6979、angelica、ginseng、decursin、terpendolec、beauvericin、spylidone、pentacecilides、cl-283,546、cinnamicderivatives、betulinicacid、shikoninderivatives、esculeogenina和wu-v-23等。
抑制酰基輔酶a:膽固醇酰基轉移酶acat1活性是指使酰基輔酶a:膽固醇酰基轉移酶acat1酶活力下降。優選的,相比抑制前,酰基輔酶a:膽固醇酰基轉移酶acat1酶活力降低至少10%,較佳的降低至少30%,再佳的降低至少50%,更佳的降低至少70%,最佳的降低至少90%。
抑制酰基輔酶a:膽固醇酰基轉移酶acat1的基因轉錄或表達是指:使酰基輔酶a:膽固醇酰基轉移酶acat1的基因不轉錄,或降低酰基輔酶a:膽固醇酰基轉移酶acat1的基因的轉錄活性,或者使酰基輔酶a:膽固醇酰基轉移酶acat1的基因不表達,或降低酰基輔酶a:膽固醇酰基轉移酶acat1的基因的表達活性。
本領域技術人員可以使用常規方法對acat1基因轉錄或表達進行調節,如基因敲除、同源重組,干擾rna等。
酰基輔酶a:膽固醇酰基轉移酶acat1的基因轉錄或表達的抑制可以通過pcr及westernblot檢測表達量驗證。
優選地,與野生型相比,acat1基因轉錄或表達降低至少10%,較佳的降低至少30%,再佳的降低至少50%,更佳的降低至少70%,又佳的降低至少90%,最佳地acat1基因完全沒有表達。
小分子化合物
本發明中指由幾個或幾十個原子組成,分子質量在1000以下的化合物。
avasimibe(ci-1011)
化學名稱:2,6-diisopropylphenyl2-(2,4,6-triisopropylphenyl)acetylsulfamate
分子式:c29h43no4s
ic50:acat,3.3μm;cyp2c9,2.9μm;cyp1a2,13.9μm;cyp2c19,26.5μm
casno.166518-60-1
結構式如下
k604
化學名稱:
2-[4-[2-(benzimidazol-2-ylthio)ethyl]piperazin-1yl]-n-[2,4-bis(methyllthio)-6-methyl-3-pyridyl]acetamide
ic50:acat1,0.45μm;acat2,102.85μm
結構式:
在文獻ikenoya,m.etal.aselectiveacat-1inhibitor,k-604,suppressesfattystreaklesionsinfat-fedhamsterswithoutaffectingplasmacholesterollevels..atherosclerosis191,290-297,doi:10.1016/j.atherosclerosis.2006.05.048(2007)中公開。
cp113,818
化學名稱:(-)-n-(2,4-bis(methylthio)-6-methylpyridin-3-yl)-2-(hexylthio)decanoicamide
ic50:17-75nm
結構式:
在文獻hutter-paier,b.etal.theacatinhibitorcp-113,818markedllyreducesamyloidpathologyinamousemodelofalzheimer'sdisease.neuron44,227-238,doi:10.1016/j.neuron.2004.08.043(2004)中公開
u18666a
casno.3039-71-2
ci976
化學名稱:2,2-dimethyl-n-(2,4,6-trimethoxyphenyl)dodecanamide
分子式:c23h39no4
casno.114289-47-3;
ic50:soat1:ic50=73nm(human);acylcoenzymea:cholesterolacyltransferase1:ic50=73nm(rat);sterolo-acyltransferase,soat:ic50=110nm(rat);foamcellformation:ic50=3.8μm(ratperitonealmacrophages);golgi-associatedlpatactivity:ic50=15μm
結構式
tmp-153
分子式:c24h18cif2n3o
casno.128831-46-9
ic50:cholesterolacyltransferase(acat):ic50=5-10nm;acylcoenzymea:cholesterolacyltransferase1:ic50=5.8nm(rattusnorvegicus)
ym750
分子式:c31h36n2o
casno.138046-43-2
ic50:0.18μm
geri-bp002-a
化學名稱:2,2'-methylenebis(6-tert-butyl-4-methyl-phenol);
分子式c23h32o2
casno.119-47-1
sandoz58-035
化學名稱:
3-[decyldimethylsilyl]-n-[2-(4-methylphenyl)-1-phenethyl]propanamiidesa58-035
分子式:c30h47nosi
casno.78934-83-5
ic50:acat1,0.3μm(rat)
vulm1457
化學名稱:
n-[2,6-bis(1-methylethyl)phenyl]-n'-[4-[(4-nitrophenyl)thio]phenyl]urea;
分子式:c25h27n3o3s
casno.228544-65-8
lovastatin,
結構式如下:
u18666a
casno.3039-71-2
ctl細胞
ctl細胞即為細胞毒性t淋巴細胞(cytotoxiclymphocyte,ctl),是一種終末分化的cd8t細胞,可以通過其tcr識別相應抗原并對表達相應抗原的腫瘤細胞或者受感染的細胞進行殺傷。
cd8t細胞
cd8t細胞即為cd8陽性t細胞。cd8(群集分化8)是作為協同受體的t細胞受體(tcr)的跨膜糖蛋白。
酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑制備藥物
以酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑為主要活性成分或主要活性成分之一制備藥物。通常,藥物中除了有效成分外,根據不同劑型的需要,還會包括一種或多種藥學上可接受的載體或輔料。
“藥學上可接受的”是指當分子本體和組合物適當地給予動物或人時,它們不會產生不利的、過敏的或其它不良反應。
“藥學上可接受的載體或輔料”應當與酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑相容,即能與其共混而不會在通常情況下大幅度降低藥物組合物的效果。可作為藥學上可接受的載體或輔料的一些物質的具體例子是糖類,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和土豆淀粉;纖維素及其衍生物,如甲基纖維素鈉、乙基纖維素和甲基纖維素;西黃蓍膠粉末;麥芽;明膠;滑石;固體潤滑劑,如硬脂酸和硬脂酸鎂;硫酸鈣;植物油,如花生油、棉籽油、芝麻油、橄欖油、玉米油和可可油;多元醇,如丙二醉、甘油、山梨糖醇、甘露糖醇和聚乙二醇;海藻酸;乳化劑,如tween;潤濕劑,如月桂基硫酸鈉;著色劑;調味劑;壓片劑、穩定劑;抗氧化劑;防腐劑;無熱原水;等滲鹽溶液;和磷酸鹽緩沖液等。這些物質根據需要用于幫助配方的穩定性或有助于提高活性或它的生物有效性或在口服的情況下產生可接受的口感或氣味。
本發明中,除非特別說明,藥物劑型并無特別限定,可以被制成針劑、口服液、片劑、膠囊、滴丸、噴劑等劑型,可通過常規方法進行制備。藥物劑型的選擇應與給藥方式相匹配。
聯合治療藥物組合和施用方法
所述聯合治療藥物組合可以是以下形式中的任意一種:
一)將酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑和其他抗腫瘤藥物分別制成獨立的制劑,制劑的劑型可相同或不同,給藥途徑亦可相同或不同。使用時,可幾種藥同時使用,也可幾種藥先后使用。先后給藥時,應當在先用藥物仍對機體有效的期間內向機體施加其他藥物。
二)將酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑和其他抗腫瘤藥物配置成復方制劑。在將酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑和其他抗腫瘤藥物采用相同給藥途徑給藥并同時施加時,可采用將兩者配置成復方制劑的形式。
抗體常用的用藥方法為靜脈注射、靜脈滴注或動脈灌注。其用法用量可參考現有技術。
小分子化合物常用的用藥方法可以是胃腸道給藥或者是胃腸外給藥。sirna、shrna、抗體則一般采用胃腸外給藥。可以是局部給藥亦可以為全身給藥。avasimibe為已知用于治療動脈粥樣硬化以及阿爾茨海默病的藥物,其用法用量可參考現有技術,其他酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑的用法用量亦可參考avasimibe。
可以同步的或順序地給予有效量的酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑和有效量的其他抗腫瘤藥物。在部分實施例中,酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑采用胃腸道給藥劑型,其他抗腫瘤藥物采用胃腸外給藥劑型。或者,酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑及其他抗腫瘤藥物采用胃腸外給藥劑型。或者,酰基輔酶a:膽固醇酰基轉移酶acat1抑制劑對離體的ctl細胞進行處理,并在體外擴大培養ctl細胞后回輸機體,而其他抗腫瘤藥物直接對機體采用胃腸外給藥。使用時,可兩種藥同時使用,也可兩種藥先后使用。先后給藥時,應當在先用藥物仍對生物體有效的期間內向生物體施加其他藥物。
化療藥物包括烷化劑(如尼莫司汀、卡莫司汀、洛莫司汀、環磷酰胺、異環磷酰胺和甘磷酰芥等)、抗代謝藥(如去氧氟鳥苷、多西弗鳥啶、氟尿嘧啶、巰嘌呤、甲氨蝶呤等核苷酸類似物)、抗腫瘤抗生素(如放線菌素d、阿霉素和柔紅霉素等抗生素)、抗腫瘤動植物成分藥(如長春瑞濱、紫杉醇、三尖杉酯堿、伊立替康、泰索帝和長春堿等)、抗腫瘤激素藥(如阿他美坦、阿那曲唑、氨魯米特、來曲唑、福美坦和他莫昔芬等)以及如順鉑、達卡巴嗪、奧沙利鉑、樂沙定、可鉑奧沙、米托蒽醌和丙卡巴肼等常用化療藥。
靶向型藥物包括egfr阻斷劑如吉非替尼(gefitinib、iressa和易瑞沙)和埃羅替尼(erlotinib、tarceva)、特定細胞標志物的單克隆抗體如西妥昔單抗(cetuximab、erbitux)和抗her-2單抗(赫賽汀,trastuzumab、herceptin)、酪氨酸激酶受體抑制劑如克唑替尼(crizotinib、xalkori)、抗腫瘤血管生成藥物如bevacizumab、endostatin和bevacizumab等、bcr-abl酪氨酸激酶抑制劑如imatinib和dasatinib、抗cd20單抗如rituximab、igfr-1激酶抑制劑如nvp-aew541、mtor激酶抑制劑如cci-779、泛素-蛋白酶體抑制劑如bortezomib等。
其他腫瘤治療手段可選自手術切除、射頻消融、氬氦超導手術治療、激光消融治療、高強度聚焦超聲以及放射治療包括x-刀、r-刀、3d-crt和imrt中的一種或多種。
在進一步描述本發明具體實施方式之前,應理解,本發明的保護范圍不局限于下述特定的具體實施方案;還應當理解,本發明實施例中使用的術語是為了描述特定的具體實施方案,而不是為了限制本發明的保護范圍。
除非另外定義,本發明中使用的所有技術和科學術語與本技術領域技術人員通常理解的意義相同。除實施例中使用的具體方法、設備、材料外,根據本技術領域的技術人員對現有技術的掌握及本發明的記載,還可以使用與本發明實施例中所述的方法、設備、材料相似或等同的現有技術的任何方法、設備和材料來實現本發明。
除非另外說明,本發明中所公開的實驗方法、檢測方法、制備方法均采用本技術領域常規的分子生物學、生物化學、染色質結構和分析、分析化學、細胞培養、重組dna技術及相關領域的常規技術。這些技術在現有文獻中已有完善說明,具體可參見sambrook等molecularcloning:alaboratorymanual,secondedition,coldspringharborlaboratorypress,1989andthirdedition,2001;ausubel等,currentprotocolsinmolecularbiology,johnwiley&sons,newyork,1987andperiodicupdates;theseriesmethodsinenzymology,academicpress,sandiego;wolffe,chromatinstructureandfunction,thirdedition,academicpress,sandiego,1998;methodsinenzymology,vol.304,chromatin(p.m.wassarmananda.p.wolffe,eds.),academicpress,sandiego,1999;和methodsinmolecularbiology,vol.119,chromatinprotocols(p.b.becker,ed.)humanapress,totowa,1999等。
1.材料和試劑
細胞培養基(dmem)、胎牛血清(fbs)購自lifetechnologies;filipiniii,lovastatin,mβcd,mβcd-cholesterol購自sigma;α-cd3和α-cd28購自biolegend;流式分析抗體α-mcd4(rm4-5),α-mcd8(53-6.7),α-mcd3ε(145-2c11),α-ifn-γ(xmg1.2),α-tnf-α(mp6-xt22),α-granzymeb(ngzb),α-cd44(im7),α-cd69(h1.2f3),α-pd-1(j43),α-ctla-4(uc10-4b9),α-ki67(16a8),α-foxp3(fjk-16s),α-gr1(rb6-8c5),α-cd11b(m1/70)和α-cd45(30-f11)購自ebioscience;western-blotting抗體α-pcd3ζ購自abcam,α-cd3ζ購自santacruze,α-pzap70,α-zap70,α-plat,α-lat,α-perk1/2和α-erk1/2購自cellsignaling;mts檢測試劑盒購自promega;u18666a購自merck;avasimibe購自selleck;k604由中科院上海藥物研究所合成;cp113,818由pierrefabre提供;b16f10細胞系和llc(lewislungcarcinoma)細胞系最 初來源于atcc,由中國科學院細胞庫提供;李斯特菌由中國科學院巴斯德研究所冷啟彬研究組提供;
2.實驗動物
c57bl/6小鼠購自slac;ot-itcr轉基因小鼠和acat2基因敲除小鼠來自jaxmice;cd4cre轉基因小鼠由中國科學院生物化學與細胞生物研究所劉小龍研究組提供(最初來源于jaxmice);acat1flox/flox來自ingeneiouslabs,該試驗動物在acat1基因的14號外顯子毗鄰的兩個內含子上分別有一個loxp位點,該外顯子編碼有his460位點,該位點是acat1的酶活所必需的,acat1flox/flox可采用現有常規技術構建。實驗中所有的動物都飼養在spf設施中。
3.t細胞分離,培養和流式檢測
分離得到的細胞用含50μmβ-巰基乙醇的rpmi1640完全培養基在37℃co2培養箱培養。為進一步分析t細胞的功能表型,針對細胞表面標志物如cd8,cd44,cd69,細胞離心后直接用percp-α-cd8,fitc-α-cd44,pe-α-cd69進行染色,然后流式檢測;而針對胞內顆粒酶和細胞因子的檢測,分離到的細胞繼續用1μmionomycin和50ng/mlpma刺激培養4個小時,在培養過程中加入5μg/mlbfa,以阻斷顆粒酶和細胞因子向胞外分泌。刺激結束后,4%多聚甲醛(pfa)室溫固定10分鐘,然后胞內染色檢測胞內顆粒酶和細胞因子的水平。
4.膽固醇定量
a.filipin染色和激光共聚焦成像技術對細胞質膜膽固醇進行相對定量
filipiniii溶于甲醇中至5mg/ml。t細胞用4%pfa固定,然后用50μg/mlfilipiniii于4℃染色30分鐘,然后pbs洗5次以去除游離filipin。成像圖片由leicasp8激光共聚焦顯微成像系統獲取,相對定量結果由leicalasaf軟件分析得到。
b.基于膽固醇氧化的膽固醇定量方法
細胞經0.1%戊二醛固定15分鐘后,pbs洗3次,然后用2u/ml膽固醇氧化酶室溫處理15分鐘以氧化細胞質膜上游離膽固醇;氧化反應結束后pbs洗3次以去除殘留的膽固醇氧化酶,細胞內未被氧化的游離膽固醇用甲醇/氯仿(v:v=1:2)提取,然后用amplexred cholesterol檢測試劑盒(lifetechnology)對游離膽固醇進行定量。細胞質膜膽固醇的含量由未被氧化酶處理的樣品膽固醇含量減去氧化酶處理過的樣品膽固醇含量得到。
5.mβcd和mβcd-cholesterol處理改變細胞質膜膽固醇水平
為降低細胞質膜膽固醇水平,0.1–1mmmβcd37℃處理cd8t細胞5分鐘,然后pbs洗三次。為提高細胞質膜膽固醇水平,1-10μg/mlmbcd-cholesterol37℃處理cd8t細胞15分鐘,然后pbs洗三次。
6.ova抗原激活ot-icd8t細胞
將c57bl/6小鼠脾臟細胞中的t細胞用t細胞陽性磁珠分選試劑盒(miltenyibiotech)去除,然后分別遞呈ova抗原ova257-264(siinfekl,簡稱n4),及突變體sainfekl(簡稱a2),siitfekl(簡稱t4),siigfekl(簡稱g4)以及自身抗原rtytyekl(簡稱catnb)和陽性選擇抗原siirfekl(簡稱r4)作為抗原遞呈細胞(apc)。具體的,為分別將ova抗原ova257-264,a2,t4,g4,r4和自身抗原catnb與前述處理后的小鼠脾臟細胞一起在37℃孵育以得到抗原呈遞細胞,同時;將陰性磁珠分選得到的ot-icd8t細胞與抗原遞呈細胞共同培養(1:5)24小時,在培養的最后4小時加入5μg/mlbfa(是布雷菲德菌素a),以阻止細胞因子向胞外分泌,最后通過胞內染色和流式檢測細胞因子的表達。
7.檢測cd8t細胞(ctl)的細胞殺傷能力。
分離ot-i轉基因小鼠的脾臟,紅細胞裂解液去除紅細胞后用5nmova257-264(n4)刺激,并在培養基中加入10ng/mlil-2,3天后換液補加il-2并繼續培養2天得到分化成熟的殺傷性cd8t細胞(ctl)。將el-4小鼠淋巴瘤細胞分別與2nm抗原肽ova257-264及其突變體a2,t4,g4,r4和自身抗原catnb在37℃孵育30分鐘以遞呈相關抗原,pbs洗3次后將遞呈抗原的el-4細胞和ctl重懸在無酚紅rpmi1640培養基(含2%fbs)中,然后以1:1,1:2,1:5比例混合(el-4細胞數量為1×105)加入96孔板中,200g離心2分鐘。37℃co2培養箱培養4小時,200g離心5分鐘,取培養上清液,通過cytotox96non-radioactivecytotoxicity試劑盒(promega)檢測培養基中乳酸脫氫酶ldh的釋放以計算ctl對靶細胞的殺傷效率。
8.李斯特菌(listeriamonocytogenes)感染實驗
新鮮培養的李斯特菌離心后重懸在pbs中,通過od200計算細菌濃度,然后以2×104cfu的劑量尾靜脈注射到8-10周小鼠體內,7天后,將小鼠安樂死,取脾臟分離其t細胞,流式檢測t細胞表面標志物和胞內細胞因子的表達水平。
9.小鼠b16黑色素瘤模型
b16f10黑色素瘤細胞用胰酶消化后,pbs洗3次后過40μm濾網,計數用pbs稀釋至2×106/ml,然后皮下注射(s.c.)到8-10周雄鼠背部左側(100μl體積),從第10天開始,游標卡尺測量腫瘤大小,每兩天測一次,腫瘤大小=長度×寬度。當腫瘤其最長軸超過20mm時,將小鼠安樂死,并記錄死亡時間點。
10.小鼠黑色素瘤t細胞過繼治療
表達雞卵清蛋白ovalbumin的b16f10-ova黑色素瘤細胞(ref)(可參考文獻:yangjetal.,kuper-typeimmunologicalsynapsecharacteristicsdonotpredictanti-braintumorcytolytict-cellfunctioninvivo.procnatlacadsciusa.2010.197(10):4716-21;獲zhoupetal.,invivodiscoveryofimmunotherapytargetsinthetumourmicroenvironment.nature.2014,506(7486):52-7獲得)用胰酶消化后,pbs洗3次后過40μm濾網,計數用pbs稀釋至2×106/ml,然后皮下注射(s.c.)到8-10周雄鼠背部左側(100μl)。在注射腫瘤細胞后第10天,將成瘤且腫瘤大小一致的小鼠隨機分成3組,以尾靜脈注射(i.v.)的方式分別注射200μlpbs,野生型ot-ictl和acat1基因敲除的ot-ictl(1.5×106),3天后開始測量腫瘤大小,每兩天測一次。當腫瘤其最長軸超過20mm時,將小鼠安樂死,并記錄死亡時間點。
acat1基因敲除的ot-i小鼠的獲得:cd4cre小鼠與acat1flox/flox小鼠交配獲得cd4cre-acat1flox/flox,然后與otitcr轉基因小鼠交配,最終獲得ot-i-cd4cre-acat1flox/flox小鼠和相應的對照小鼠ot-i-e-acat1flox/flox小鼠。
ctl的誘導方法是:取野生型或acat1基因敲除的oti小鼠脾臟,分別用10nm的ova257-264(n4)肽段刺激,并提供10ng/mlil-2,刺激2天后,在第3天換無n4肽段的培養基(含10ng/mlil-2)繼續培養2天即可獲得成熟的ctl。
11.avasimibe,α-pd-1抗體治療小鼠黑色素瘤
b16f10黑色素瘤細胞用胰酶消化后,pbs洗3次后過40μm濾網,計數用pbs稀釋至2×106/ml,然后皮下注射(s.c.)到8-10周雄鼠背部左側(100μl),在注射腫瘤細胞后第10天,將成瘤且腫瘤大小一致的小鼠隨機分成4組,以腹腔注射(i.p.)或者灌胃(i.g.)對小鼠進行治療,avasimibe劑量為15mg/kg,每兩天一次;α-pd-1抗體(j43,bioxcell)劑量為200μg/次,每三天一次;在注射腫瘤第12天開始測量腫瘤大小,每兩天測一次。當腫瘤其最長軸超過20mm時,將小鼠安樂死,并記錄死亡時間點。
12.小鼠llc肺癌模型
llc(lewislungcarcinoma)肺癌細胞用胰酶消化后,pbs洗3次后過40μm濾網,計數用pbs稀釋至107/ml,然后尾靜脈注射(i.v.)到8-10周雄鼠體內(200μl體積)。在注射腫瘤細胞 后第11天,將荷瘤小鼠隨機分成2組,以腹腔注射(i.p.)的方式給小鼠注射avasimibe,劑量為15mg/kg,3天注射一次,連續給藥9次。在注射腫瘤細胞后7周,取部分小鼠的肺臟,對腫瘤斑點進行計數,以評估腫瘤治療效果,同時記錄剩余小鼠的死亡時間點。
13.超高分辨率隨機光學重構顯微鏡storm(super-resolutionstochasticalopticalreconstructionmicroscopy)檢測細胞質膜上tcr(抗原受體)的分布。
超高分辨率隨機光學重構顯微鏡storm成像在nikonn-storm成像系統上進行,該系統配有eclipseti-e電動相差顯微鏡,apochromat100倍tirf油鏡和emccd。熒光染料選用alexa647,通過647nm連續可見光激光器(200mw)和450nm二極管激光器激發熒光染料。成像時tirf角度參數在3900-4000,以保證樣品成像深度在1μm左右。
為了分析tcr在質膜上的成簇情況,對圖片中tcr微簇的位置信息用ripley’skfunction和matlab分析,l(r)-r值代表在一定半徑(r)內分子聚集的概率,而l(r)-r最大值對應的r即分析選定區域內tcr微簇的半徑。
14.全內反射熒光顯微成像tirfm(totalinternalreflectionfluorescencemicroscopy,)方法動態檢測t細胞免疫突觸形成過程。
dopc(1,2-dioleoyl-sn-glycero-3-phosphocholine)與生物素標記的dope(1,2-dioleoyl-sn-glycero-3-phosphoethanolamine-cap-biotin)以25:1的摩爾比混合,超聲形成脂質體。使用no.1.5h厚度玻璃底的細胞培養皿,食人魚酸液處理玻璃底表面并用雙蒸水清洗干凈。用濃度0.1mm的生物素標記的脂質體孵育玻片20分鐘。pbs充分清洗后,用鏈霉親和素(streptavidin)孵育30分鐘。pbs充分清洗后,用生物素標記的小鼠cd3ε抗體(bionylatedα-mcd3ε,145-2c11)孵育30分鐘。pbs充分清洗后,用1%酪蛋白封閉20分鐘。pbs充分清洗,平面脂雙分子層準備完畢。
α-mtcrβ抗體(biolegend)進行熒光染料標記(alexafluor568nhsester,lifetechnologies),經脫鹽柱脫鹽后使用papain蛋白酶酶切(piercefabmicropreparationkit,thermoscientific),最后經proteina柱分離(proteinaplusspincolumn,thermoscientific)得到alexa568-α-mtcrβ-fab。
新鮮分離的小鼠脾臟淋巴細胞用alexa568-α-mtcrβ-fab和fitc-α-mcd8a(ebioscience)冰上染色,pbs清洗2次。重懸的細胞加入如上所述的鋪有平面脂雙分子層的培養皿,置于37℃加熱臺,以3秒每幀的速度拍攝,進行活細胞全內反射熒光顯微鏡成像。或者重懸的細胞加入上文所述鋪有平面脂雙分子層的培養皿,置于37℃培養箱,刺激一定時間后用4%pfa固定,全內反射熒光顯微鏡成像。fitc陽性的cd8t細胞用imageproplussoftware(mediacybernetics)、imagej(nih)和matlab(mathworks)軟件經行數據分析。
15.mts方法檢測腫瘤細胞活率。
b16f10細胞(5×103)重懸于100μl含有1μmavasimibe或dmso對照的培養基中。37℃培養24、48、或72小時。加入20μlmts試劑(promega),孵育1-3小時后,測量490nm吸光度。490nm處的吸光值與培養中的活細胞數成正比。avasimibe對細胞活性的影響通過以dmso處理的細胞為對照組進行歸一化處理得到,設定dmso處理組的細胞活性為1。
16.數據統計分析
除在圖釋中特別注明外,本文所有數據統計都是用graphpadprism(graphpadsoftware,inc.)進行統計分析,分析方法采用two-tailedunpairedstudent’st-test;*p<0.05,**p<0.01,***p<0.001,ns:無顯著差異(nosignificantdifference)。
17.t細胞特異性敲除acat1小鼠的構建及acat1ckocd8t、acat1ckocd4t細胞的獲得
將acat1flox/flox小鼠與cd4cre小鼠交配,獲得的小鼠經pcr及westernblot檢測表達量驗證為t細胞特異性敲除acat1小鼠(cd4cre-acat1flox/flox,簡稱acat1cko)。
acat1ckocd8t細胞的獲得:采用cd8磁珠分選得到(分選試劑盒來自stemcell)
acat1ckocd4t細胞的獲得:采用cd4磁珠分選得到(分選試劑盒來自stemcell)
18.acat2基因敲除小鼠的來源及acat2-/-cd8t細胞的獲得
acat2基因敲除小鼠(acat2-/-)來自于中科院生物化學與細胞生物學研究所李伯良研究組,最初由robertv.farese,jr構建(參考文獻:buhmankketal.,resistencetodiet-inducedhypercholesterolemiaandgallstoneformationinacat2-deficientmice.natmed.2000,6(12):1341-7).
acat2-/-
19.cd8t細胞活化方法
通過磁珠分選得到的新鮮t細胞,重懸于rpmi1640完全培養基中,α-cd3(5μg/ml)和α-cd28
實施例1抑制膽固醇酯化可以增強cd8t細胞的效應功能
試驗方法:磁珠分選得到的細胞重懸于rpmi1640完全培養基中,加入相應濃度的抑制劑,37度co2培養箱中培養處理6小時,然后rpmi1640完全培養基清洗3次,最后重懸于rpmi1640完全培養基中并轉移到鋪有激活抗體a-cd3和a-cd28的孔板中,37度co2培養箱中培養刺激20小時,然后加入brefeldina(5ug/ml)繼續培養4小時,抑制細胞因子的分泌。培養結束后收集細胞,進行cd8抗體表面標記,然后用4%多聚甲醛室溫固定10分鐘,0.1%triton-x100對細胞膜打孔后加抗granzymeb,ifnγ,tnfα抗體標記細胞內相應蛋白,最后通過流式檢測檢測cd8陽性細胞中相應蛋白如granzymeb,ifnγ和tnfα的表達水平。
本實施例的目的是研究膽固醇代謝與cd8t細胞功能的相關性。實驗通過一系列抑制劑抑制膽固醇代謝相關通路,然后檢測cd8t細胞的功能是否發生相應的改變。實驗結果表明,細胞膽固醇合成抑制劑lovastatin和細胞膽固醇的轉運抑制劑u18666a都顯著抑制cd8t細胞顆粒酶b(granzymeb,gzmb)的釋放以及細胞因子如ifnγ和tnfα的表達,且抑制效果呈劑量效應(圖1.a,b)。通過cp113,818抑制酰基輔酶a:膽固醇酰基轉移酶acat1和acat2的活性,則明顯促進cd8t細胞的效應功能(圖1.c)。如前所述,在cd8t細胞中acat1的轉錄水平約是acat2的20倍,選取acat1的特異性抑制劑k604處理cd8t細胞,實驗結果表明,k604處理同樣增強cd8t相比的效應功能(圖1.d)。表明通過抑制acat1的功能則增強cd8t細胞的效應功能,因此acat1可能是一個增強cd8t細胞功能的靶點,以應用于臨床治療如腫瘤免疫治療中。
實施例2t細胞特異性敲除acat1增強cd8t細胞免疫應答反應。
本實施例的目的是為了驗證acat1在cd8t細胞中的功能。通過將acat1flox/flox小鼠與cd4cre小鼠交配,獲得t細胞特異性敲除acat1小鼠(cd4cre-acat1flox/flox,簡稱acat1cko)和相應的野生型對照小鼠(acat1flox/flox)。
間接體內試驗方法:磁珠分選得到的cd8t細胞重懸于rpmi1640完全培養基中,加入相應濃度的抑制劑,37度co2培養箱中培養處理6小時,然后rpmi1640完全培養基清洗3次,最后重懸于rpmi1640完全培養基中并轉移到鋪有激活抗體α-cd3和α-cd28的孔板中,37度co2培養箱中培養刺激20小時,然后加入brefeldina(5μg/ml)繼續培養4小時,抑制細胞因子的分泌。培養結束后收集細胞,進行cd8抗體表面標記,然后用4%多聚甲醛室溫 固定10分鐘,0.1%triton-x100對細胞膜打孔后加抗granzymeb,ifnγ,tnfα抗體標記細胞內相應蛋白,最后通過流式檢測檢測cd8陽性細胞中相應蛋白如granzymeb,ifnγ和tnfα的表達水平。
間接體內實驗(exvivo)結果發現,cd8t細胞受到刺激活化后,acat1ckocd8t細胞的免疫應答能力增強,表現為更多的顆粒酶b(gzmb)的釋放以及更多細胞因子ifnγ和tnfα的表達(圖2.a,b,c)。
為了在體內研究中驗證acat1在cd8t細胞中的功能,采用了李斯特菌(listeriamonocytogenes)感染模型進行驗證。李斯特菌是一種細胞內繁殖的致病菌,cd8t細胞在響應李斯特菌感染后會高表達細胞因子ifnγ,并誘發后續的免疫應答反應以達到最終清除病原菌的作用。尾靜脈注射李斯特菌誘發感染7天后,通過檢測小鼠脾臟中cd8t細胞的響應情況,發現acat1ckocd8t細胞表達更多的ifnγ,同時cd8t細胞早期活化標志蛋白cd69的表達也呈顯著升高(圖2.d,e)。
實施例3acat1基因敲除促進cd8t細胞的增殖并減少凋亡
本實施例的目的是為了檢測acat1對cd8t細胞增殖的影響。通過cfse標記實驗,用α-cd3+α-cd28抗體刺激cd8細胞,進一步檢測acat1對cd8t細胞增殖的影響,發現與野生型cd8t細胞相比,acat1ckocd8t細胞的增殖能力增強(圖3.a)。同時通過annexinv和pi染色檢測cd8t細胞激活后的凋亡,結果顯示acat1ckocd8t細胞annexinv-pi-的活細胞所占比例相比較與野生型細胞的明顯增多,而處于凋亡狀態的細胞(annexinv+pi-和annexinv+pi+)所占比例則顯著減少(圖3.b,c)。
實施例4acat1基因敲除不會引發cd8t細胞對自身抗原產生反應和自身免疫
本實施例的目的是為了研究去除acat1功能后cd8t細胞獲得增強的效應功能是否會使得cd8t細胞對自身抗原產生反應從而誘發自身免疫病。為了研究這一點,將acat1cko小鼠進一步與ot-itcr轉基因小鼠(jaxmice)進行交配,獲得ot-i背景的acat1特異性基因敲除小鼠(ot-iacat1cko)和相應的對照小鼠(ot-i)。ot-i轉基因小鼠的絕大部分t細胞為ot-icd8t細胞,其tcr特異性識別h2kb遞呈的ovabumin(ova257-264)抗原(簡稱n4),并產生相應的cd8t細胞免疫應答反應;同時ot-itcr除了識別其野生型抗原(n4)外,也可識別一系列的ova突變體(a2,t4,g4,r4),并產生相應的強弱免疫應答反應。試驗發現,acat1缺陷除了能促進ot-icd8t細胞對強弱抗原的免疫應答反應,具體表現為 細胞因子ifnγ的分泌量增加以及對靶細胞的殺傷效應(圖4.a-b)。但是acat1缺陷不會引起ot-icd8t細胞對自身抗原catnb(β-catenin片段,可以被h2kb呈遞)以及類自身抗原r4產生免疫應答。這個結果表明acat1基因敲除不影響t細胞對抗原親和力(affinity)識別能力。為進一步驗證acat1基因敲除后小鼠自身免疫情況,試驗檢測了小鼠血清中細胞因子ifnγ和自身抗體抗雙鏈dna抗體。結果顯示,與對照小鼠相比,這兩項指標沒有任何改變(圖4.c),表明acat1基因敲除并不引起自身免疫反應,進一步表明acat1作為腫瘤免疫治療靶點的安全性。
實施例5利用三種黑色素瘤模型研究acat1基因敲除促進cd8t細胞的抗腫瘤活性
免疫治療是當前治療腫瘤的熱點,而cd8t細胞對腫瘤細胞的殺傷能力直接關系到腫瘤免疫治療的效果。為了驗證acat1敲除對cd8t細胞的抗腫瘤能力的影響,本實施例首先建立了皮下黑色素瘤模型,在acat1cko小鼠和野生型小鼠中皮下注射b16f10黑色素瘤細胞誘導黑色素瘤,實驗發現acat1cko小鼠黑色素瘤的進程被顯著延緩,表現為腫瘤生長更慢,小鼠的生存率和生存期更長(圖5.a,b)。對荷瘤小鼠的t細胞的表型進行分析,發現在acat1cko小鼠中,腫瘤浸潤的cd8t細胞活性更強,表現為acat1cko小鼠腫瘤浸潤cd8t細胞中,cd44高表達的效應細胞更多,表達顆粒酶b和細胞因子ifnγ和tnfα的比例也更高;而且acat1cko小鼠腫瘤浸潤cd8t細胞的數量、cd8/cd4細胞的比例也要高于野生型、細胞增殖的標志物ki-67的表達水平也更高(圖5.c,d)。免疫檢測點受體如pd-1和ctla-4目前是腫瘤免疫治療的熱門靶點,實驗也檢測了腫瘤浸潤的cd8t細胞表面pd-1和ctla-4的表達水平,發現其在acat1cko和野生型小鼠中沒有明顯差異(圖5.e);同時實驗也檢測了腫瘤中cd4t細胞中treg細胞(cd4+foxp3+)的比例,發現acat1敲除并不改變treg細胞在cd4t細胞中的比例(圖5.f)。以上結果表明acat1敲除使cd8t細胞的抗腫瘤效應功能增強。
為了進一步驗證cd8t細胞在該腫瘤模型中的應答反應受acat1的調控,實驗在皮下注射b16f10黑色素瘤細胞后第7天,將acat1cko和野生型小鼠的引流淋巴結(draininglymphnode)取出,分析其中t細胞的表型。實驗發現acat1cko小鼠引流淋巴結中的cd8t細胞cd44水平和細胞因子ifnγ的表達上升(圖5.g),而且cd8t細胞的數量以及cd8/cd4的比率也顯著升高(圖5.h),表明acat1缺陷促進cd8t細胞的初始免疫應答反應。
相比較與皮下實體瘤,轉移型腫瘤的進程更為復雜,其治療更為艱難。為進一步檢測acat1缺陷是否影響cd8t細胞對轉移瘤的免疫應答反應,實驗建立了黑色素瘤肺轉移小鼠 模型,向acat1cko和野生型小鼠尾靜脈注射b16f10黑色素瘤細胞,然后檢測肺臟中黑色素瘤的發展進程。實驗發現在acat1cko小鼠中,與野生型對照小鼠相比,其肺臟腫瘤數量明顯減少,而且小鼠的生存率和生存期更長(圖5.i-k)。通過蘇木精-伊紅(h&e)對肺臟組織進行染色,發現acat1基因敲除后,黑色素瘤在肺臟中的浸潤明顯減弱(圖5.l)。對肺臟t細胞的表型進行分析,也發現acat1cko小鼠cd8t細胞中cd44高表達的效應細胞更多,表達顆粒酶b和細胞因子ifnγ和tnfα的比例也更高(圖5.m)。這些結果表明acat1缺陷增強cd8t細胞在非轉移和轉移型腫瘤中的抗腫瘤免疫應答效應。
由于acat1cko中所有的t細胞都缺失acat1,為了驗證acat1基因敲除是對腫瘤浸潤的cd8t細胞而非cd4t細胞的功能的影響而獲得更強抗腫瘤作用,在野生型c57小鼠皮下注射b16f10-ova黑色素瘤細胞,該細胞表達ovalbumin,可以被黑色素瘤細胞的h2kb遞呈在細胞表面,從而被ot-icd8t細胞識別。在野生型小鼠成功誘導黑色素瘤后,在注射腫瘤后第10天以尾靜脈注射的方式,將來自acat1cko小鼠和野生型小鼠的ot-ictl注射到荷瘤野生型小鼠體內,然后監測腫瘤生長并記錄小鼠的生存情況(圖5.n),結果表明,注射了acat1ckoot-ictl的實驗組腫瘤生長比注射了野生型ot-ictl的對照組更慢,而且小鼠的生存時間更長(圖5.o,p),進一步表明acat1特異性敲除的cd8t細胞有更好的抗腫瘤作用。
實施例6acat1基因敲除促進cd8t細胞細胞質膜上t細胞抗原受體tcr的微簇形成并增強tcr信號通路的活化。
本實施例研究了acat1敲除對tcr的信號轉導的影響。實驗通過α-cd3加α-cd28抗體激活acat1ckocd8t細胞,檢測tcr和其下游信號分子的活化情況。實驗發現,acat1敲除明顯促進tcr磷酸化和tcr近端活化信號的增強,表現為cd3ζ、zap70和lat的磷酸化明顯增強,同時tcr的下游通路信號分子如erk1/2的磷酸化也顯著升高(圖6.a)。實驗采用了超高分辨率隨機光學重構顯微成像技術(super-resolutionstochasticalopticalreconstructionmicroscopy,storm)對cd8t細胞質膜表面的tcr微簇進行分析。結果顯示,acat1基因敲除不改變cd8t細胞質膜上tcr的表達水平(圖6.b),但是能明顯促進tcr微簇的形成:acat1ckocd8t細胞的tcr微簇比野生型cd8t細胞的更大。由于tcr微簇的形成受tcr活化信號的影響,t細胞活化后其tcr微簇會明顯增大,因此實驗進一步分析了活化后tcr微簇的形成情況。結果表明,cd8t細胞活化后其tcr微簇增大,而且活化的acat1ckocd8t細胞的tcr微簇比活化的野生型cd8t細胞的更大(圖6.c-e)。這 些結果表明acat1基因敲除后cd8t細胞tcr微簇的增大,從而使得tcr及其下游信號通路活化增強。
實施例7acat1基因敲除促進cd8t細胞免疫突觸(immunologicalsynapse,is)的形成
t細胞在識別抗原后,與靶細胞在細胞-細胞接觸面形成免疫突觸結構(immunologicalsynapse),免疫突觸的形成有助于維持信號體(signalsome)的穩定,以保證t細胞的充分活化并產生相應的免疫應答反應。對于起細胞殺傷作用的cd8t細胞,免疫突觸的形成不僅有助于穩定signalsome,還能通過這個突觸結構向靶細胞釋放顆粒酶等,增強其對靶細胞的殺傷能力。本實驗研究了acat1敲除的cd8t細胞對免疫突觸形成的影響。實驗進一步通過活細胞全內反射熒光顯微鏡技術(totalinternalreflectionfluorescencemicroscopy,tirfm),實時跟蹤檢測免疫突觸的形成過程,實驗發現acat1ckocd8t細胞能更有效地形成免疫突觸結構,表現為tcr所在的csmac結構形成更快,而且收斂更好(圖7.a-b)。對免疫突觸形成過程中tcr微簇的分子動態行為進行分析,結果表明acat1ckocd8t細胞的免疫突觸中可運動的tcr微簇占全部的tcr微簇的比例更高,且向心移動速度更快,有助于免疫突觸的進一步穩定(圖7.c-e)。
實施例8acat1基因敲除不影響cd4t細胞的免疫應答反應
cd4輔助t細胞在機體應對外來病原的免疫應答中也起著關鍵作用,為了進一步研究acat1基因敲除是否影響cd4t細胞的功能,本實施例首先檢測了cd4t細胞在活化前后細胞質膜膽固醇水平的變化。通過filipiniii標記以及成像實驗,結果發現acat1cko
實施例9acat抑制劑avasimibe增強cd8t細胞的抗腫瘤功能
本實施例目的是進一步驗證acat1抑制劑在腫瘤免疫治療中的應用。acat1作為用作治療動脈粥樣硬化的靶點,目前已有一系列小分子藥物在進行動物和臨床實驗。avasimibe是其中一種,目前多次臨床實驗已經驗證了avasimibe在的安全性。因此選用avasimibe,驗證acat1作為腫瘤免疫治療靶點的可能性。體外實驗表明,avasimibe與其他acat抑制劑如cp113,818和k604一樣,可以促進cd8t細胞顆粒酶b的釋放和細胞因子ifnγ和tnfα的表達(圖9.a)。體外殺傷實驗也表明avasimibe增強ctl的靶細胞殺傷能力,且呈劑量效應(圖9.b)。實驗進一步在小鼠黑色素瘤模型中驗證avasimibe的作用,通過對黑色素瘤荷瘤野生型小鼠進行腹腔注射給藥(15mg/kg)處理,與對照小鼠相比,avasimibe給藥的小鼠腫瘤生長減慢,小鼠的生存時間也顯著延長(圖9.d-f)。為了驗證avasimibe不是通過直接抑制腫瘤細胞的生長,在體外實驗中用avasimibe處理b16f10黑色素瘤細胞,發現avasimibe處理不影響b16f10細胞的活性(圖9.c)。對小鼠腫瘤浸潤的免疫細胞進行分析發現,avasimibe給藥的小鼠中:其腫瘤浸潤的cd8t細胞活性更高,表現為cd8t細胞表面活化標記cd44的表達比例更高,而且表達顆粒酶b,細胞因子ifnγ和tnfα的細胞比例也更高。對小鼠腫瘤浸潤的t細胞進行計數,發現avasimibe給藥組的腫瘤浸潤cd8t細胞數量更多,且cd8/cd4比率更高。另外avasimibe給藥組腫瘤浸潤cd8t細胞中的細胞增殖標記物ki-67的表達水平也更高(圖9.g-h)。考慮到腫瘤微環境的免疫抑制效應,實驗也檢測了cd8t細胞上的免疫抑制受體pd-1和ctla-4的表達水平,發現avasimibe給藥并未改變這些免疫檢測點受體的表達(圖9.i)。
腫瘤微環境中還存在有一些抑制型的免疫細胞如treg(regulatorytcell)和mdsc(myeloid-derivedsuppressorcell),這些細胞通過抑制cd8t細胞等腫瘤殺傷細胞的活性,在腫瘤的發展進程中起著關鍵的作用。因此實驗進一步檢測了腫瘤組織中treg和mdsc的比例,avasimibe給藥后,treg(cd4+foxp3+)細胞在cd4t細胞中的比例沒有明顯改變,而mdsc(gr1+cd11b+cd45+)在cd45+免疫細胞中的比例有較輕微的降低(圖9.j,k),考慮到avasimibe給藥組的腫瘤組織中cd8t細胞的數量明顯上升,mdsc在cd45+細胞中 的比例降低可能是由于cd8t細胞在cd45+細胞中的比例上升所致(圖9.h)。這些證據表明,acat抑制劑avasimibe可以通過上調cd8t細胞殺傷性效應而在腫瘤治療中起作用。
實施例10avasimibe通過抑制acat1促進cd8t細胞的抗腫瘤活性
本實施例的目的是驗證avasimibe是否是通過抑制acat1發揮其腫瘤免疫能力。為了驗證這一點,在體外用avasimibe對cd8t細胞進行處理,檢測其細胞質膜膽固醇水平的變化。通過filipiniii對細胞進行染色,發現avasimibe處理后,cd8t細胞質膜游離膽固醇水平明顯上升(圖10.a,b)。通過storm對cd8t細胞表面tcr的定位進行分析發現,avasimibe處理促進tcr微簇的形成(圖10.c-e);通過tirfm對t細胞活化過程中免疫突觸的形成進行分析,也表明avasimibe處理促進cd8t細胞免疫突觸的形成(圖10.f,g)。進一步通過western-blotting方法檢測avasimibe處理后tcr信號通路的活化情況,結果也表明avasimibe處理增強tcr信號通路的活化(圖10.h)。這些結果與acat1敲除的cd8t細胞的表現一致。同時,為進一步在動物體內驗證該機制,實驗從avasimibe給藥的荷瘤小鼠的腫瘤中分離腫瘤浸潤的cd8t細胞,通過storm對腫瘤浸潤的cd8t細胞上tcr的分布進行成像分析,發現avasimibe處理(于rpmi1640完全培養基中加藥后,37℃co2培養箱中培養處理6小時,處理完之后用培養基或pbs離心清洗3次)后,腫瘤浸潤的cd8t細胞表面tcr微簇更大(圖10.i-k)。這些證據表明avasimibe確實是通過抑制acat1促進cd8t細胞的活化,從而增強其抗腫瘤活性。
實施例11acat2基因敲除不影響cd8t細胞的免疫應答反應
由于avasimibe能抑制acat1和acat2,雖然acat2在cd8t細胞中的表達水平很低,為進一步排除avasimibe通過抑制acat2增強cd8t細胞的功能,從acat2基因敲除小鼠中分離cd8t細胞,用cd3和cd28抗體刺激激活,檢測細胞因子ifnγ,tnfα和顆粒酶b,結果顯示acat2基因敲除后cd8t細胞的免疫反應沒有明顯改變,表明acat2并不影響cd8的效應功能如細胞因子的分泌(圖11)。
實施例12acat1基因敲除促進ctl細胞定向釋放細胞毒顆粒
ctl對靶細胞進行直接殺傷時,首先需要與靶細胞接觸并形成免疫突觸結構。在這個過程中,ctl細胞會發生極化,包含顆粒酶在內的細胞毒顆粒(granule)會移動到免疫突觸處并向靶細胞定向釋放顆粒酶,進而誘導靶細胞的程序性死亡。通過三維共聚焦熒光顯微鏡技 術(3-dconfocalfluorescencemicroscopy)對ctl細胞中細胞毒顆粒的分布進行成像和三維重構,然后計算ctl中距離免疫突觸2μm范圍內的細胞毒顆粒體積。
試驗方法:
1.成顆粒過程檢測
ctl細胞用alexa568-α-mtcrβ-fab和apc-α-mcd8a(ebioscience)冰上染色,pbs清洗2次。重懸的細胞加入如上所述的鋪有平面脂雙分子層的培養皿,置于37℃培養箱,刺激一定時間后用4%pfa固定,0.1%tritonx-100穿孔。4℃胞內染色過夜,標記細胞毒顆粒表面蛋白cd107a(又名lamp-1,抗體克隆號1d4b)。α-mcd107a提前用alexafluor488nhsester(lifetechnologies)進行熒光染料標記。pbs充分清洗后三維共聚焦熒光顯微鏡成像。免疫突觸附近2μm距離內的細胞毒顆粒體積用imaris軟件經行數據分析。
2.脫顆粒檢測
el-4細胞與ova257-264肽段37度孵育30分鐘,作為遞呈抗原的靶細胞。ot-ictl與遞呈抗原的el-4細胞以1:1比例混合,同時加入1μg/mlalexa488-α-cd107a抗體和2μmmonensin。在37度co2培養箱分別培養1、2或4小時后,取出細胞,用pbs洗兩次然后在冰上流式染色,以pe-cy7-α-cd8a標記cd8t細胞,最后通過流式細胞術檢測ctl(cd8+)細胞表面和內吞的cd107a水平。
結果顯示,acat1基因敲除后,ctl細胞免疫突觸近端的細胞毒顆粒明顯增多(圖12.a)。由于顆粒酶釋放過程中,形成毒顆粒囊泡表面的cd107a分子并未與顆粒酶一同進入靶細胞中,而是留在ctl細胞質膜表面,然后通過內吞的形式回到胞內重新參與細胞毒顆粒囊泡的組裝,這個過程為脫顆粒過程。因此也可以通過檢測脫顆粒水平來評估ctl對靶細胞釋放毒顆粒的能力。通過流式細胞術檢測細胞質膜上和內吞的cd107a的水平,發現acat1基因敲除會增加ctl的脫顆粒能力。這些證據表明acat1基因敲除促進ctl細胞向靶細胞定向釋放細胞毒顆粒的能力。
實施例13acat抑制劑增強人pbmc中cd8+t細胞的效應功能
本試驗的目的是驗證acat1作為藥物靶點在臨床上使用的潛在價值,在人cd8t細胞中分別用acat抑制劑avasimibe和cp113,818抑制acat的活性,然后通過抗體交聯的方式激活cd8t細胞,通過流式細胞術檢測cd8t細胞細胞因子ifnγ和tnfα的表達。
試驗方法:通過ficoll從健康志愿者體內獲得的外周血中分離pbmc,然后用5μg/mlpha刺激獲得cd8+殺傷性t細胞。3天后換成不含pha的培養液繼續培養24小時,以降低本 底信號。再使用相應濃度的avasimibe或cp113,818孵育處理12小時,細胞換液并通過鋪板刺激的方式用5μg/mlα-cd3+5μg/mlα-cd28抗體刺激24小時,在最后4小時加入5μg/mlbrefeldina以阻斷細胞因子的分泌,最后通過胞內染色和流式細胞術檢測cd8+t細胞中細胞因子ifnγ和tnfα的表達。雙尾非配對t-test用于差異顯著性分析。
試驗結果:acat抑制劑cp113,818和avasimibe均能促進cd8t細胞細胞因子的表達,且具劑量效應,表明acat1作為增強cd8t細胞效應功能的靶點同樣適用于人的cd8t細胞(圖13)。
實施例14avasimibe在小鼠肺癌模型中的功效
本實施例的目的為進一步驗證acat1作為腫瘤免疫治療靶點的有效性。實驗建立了小鼠llc(lewislungcarcinoma)肺癌模型,檢測llc在野生型小鼠和acat1基因敲除小鼠中肺癌發展進程,結果發現t細胞中acat1基因敲除顯著抑制腫瘤的生長,荷瘤小鼠的生存期也明顯長于對照的野生型小鼠(圖14.a-c)。為了驗證acat1抑制劑avasimibe對llc肺癌的治療效果,進一步對造模成功的小鼠進行avasimibe給藥,結果發現avasimibe在治療小鼠肺癌上也有一定的療效,表現為腫瘤細胞數量較對照組少,小鼠的生存時間延長(圖14d-g)。
實施例15avasimibe與α-pd-1聯合治療小鼠黑色素瘤的功效
目前腫瘤免疫治療方法中,α-pd-1和α-ctla-4抗體治療取得較好的療效,但由于腫瘤微環境的復雜性以及腫瘤細胞的異質性,因此針對多個靶點的聯合治療方法正成為目前腫瘤免疫治療的熱點。本實施例的目的是驗證acat1作為腫瘤免疫治療靶點在聯合治療中的功效。實驗在小鼠黑色素瘤模型中,結合α-pd-1抗體治療和avasimibe治療,檢測腫瘤的發展進程。試驗動物共40只,分成4組,每組10只。結果表明avasimibe在與α-pd-1的聯合治療中取得更好的療效,小鼠腫瘤的生長顯著減慢,同時小鼠的生存時間明顯延長(圖15.a-c)。通過對腫瘤浸潤t細胞進行分析發現,avasimibe治療后,無論是pd-1高表達還是低表達的cd8t細胞,其效應均明顯增強,表明avasimibe對cd8t細胞效應的增強與pd-1的表達無關。為進一步檢測抗pd-1抗體治療是否影響到acat1通路,通過實時定量pcr方法檢測了腫瘤浸潤cd8t細胞acat1相關基因的表達,比較了抗pd-1抗體治療與對照組基因表達水平的差異發現,抗pd-1抗體治療并不改變acat1相關基因如acat1,acat2和酯化膽固醇水解酶nceh的表達,而t細胞細胞因子ifnγ的表達水平明顯上升。
實施例16avasimibe與dacarbazine(達卡巴嗪)聯合治療小鼠黑色素瘤的功效
本實施例的目的是為了驗證acat1作為免疫治療靶點在與化療藥聯合用藥中的效果。化療是目前治療腫瘤的有效手段之一,dacarbazine是目前fda批準用于治療轉移型黑色素瘤的化療藥。本實施例在小鼠黑色素瘤模型中,給小鼠dacarbazine和avasimibe聯合用藥,結果表明顯著抑制小鼠黑色素瘤的生長,而聯合用藥明顯增強avasimibe的抗腫瘤效果(圖16)。
試驗動物分成4組,每組9-13只,具體見圖16b,c,n值即小鼠數量,經統計分析,組之間的差異顯著性即p值見圖16b,c。
以上的實施例是為了說明本發明公開的實施方案,并不能理解為對本發明的限制。此外,本文所列出的各種修改以及發明中方法、組合物的變化,在不脫離本發明的范圍和精神的前提下對本領域內的技術人員來說是顯而易見的。雖然已結合本發明的多種具體優選實施例對本發明進行了具體的描述,但應當理解,本發明不應僅限于這些具體實施例。事實上,各種如上所述的對本領域內的技術人員來說顯而易見的修改來獲取發明都應包括在本發明的范圍內。
- 還沒有人留言評論。精彩留言會獲得點贊!