包含至少一種透明質(zhì)酸和抗壞血酸磷酸酯鎂的經(jīng)滅菌組合物的制作方法
技術(shù)領(lǐng)域:
本發(fā)明涉及包含至少一種透明質(zhì)酸和抗壞血酸磷酸酯鎂的經(jīng)滅菌組合物。
背景技術(shù):
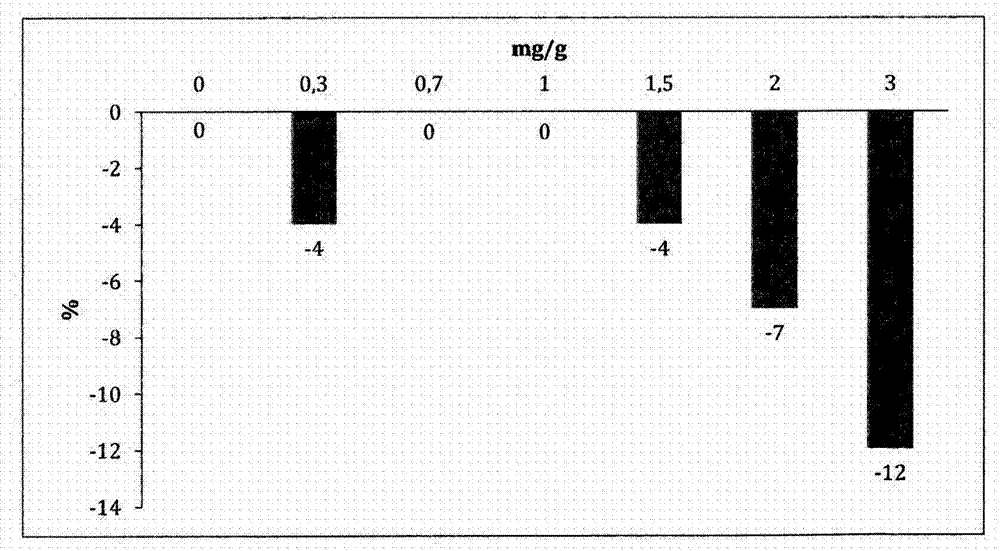
:透明質(zhì)酸已在美容領(lǐng)域中使用了超過十五年,在該領(lǐng)域,其被證明是無害且有效的。目前,在美容填充凝膠或填料市場(chǎng)中使用最廣泛的產(chǎn)品為基于來自生物發(fā)酵的交聯(lián)透明質(zhì)酸的凝膠。來自生物發(fā)酵的透明質(zhì)酸在例如填充皺紋、黏彈性補(bǔ)充(viscosupplémentation,viscosupplementation)、眼科治療或尿失禁治療領(lǐng)域中的用途被更加認(rèn)可和理解,這是因?yàn)槠涮烊淮嬖谟谌梭w中,且更特別地存在于真皮、滑液和角膜中,使得副作用導(dǎo)致的風(fēng)險(xiǎn)最小化。為了改善這些透明質(zhì)酸制劑和/或賦予其特別的特性,可向這些制劑添加多種添加劑。無論是在添加階段或滅菌階段直接地添加還是隨時(shí)間例如在儲(chǔ)存期間添加,向制劑添加添加劑的一個(gè)主要缺點(diǎn)是其流變性和/或黏彈性或其穩(wěn)定性的潛在劣化。抗壞血酸(也稱為維生素C)是參與多種生物學(xué)過程(例如膠原蛋白的合成和某些氨基酸的代謝)的強(qiáng)抗氧化劑。遺憾的是,維生素C在水溶液中不穩(wěn)定,因而不能用于在水中配制的透明質(zhì)酸制劑中。其一些衍生物,抗壞血酸磷酸酯鹽(常規(guī)地稱為磷酸抗壞血酸酯鹽)在水性制劑中是穩(wěn)定的。因此,理論上可將這些衍生物并入到透明質(zhì)酸制劑中。二甲基砜是強(qiáng)抗炎劑,其抑制由外源物導(dǎo)致的變態(tài)反應(yīng),能夠保護(hù)角質(zhì)形成細(xì)胞和成纖維細(xì)胞免受紫外輻照的不良作用,并且抑制細(xì)胞因子的作用。因此,考慮這些制劑用于填充皺紋或黏彈性補(bǔ)充,并入二甲基砜也是有利的。包含透明質(zhì)酸和抗壞血酸磷酸酯鹽的很多組合物已有描述,尤其是化妝品組合物,例如LVMH的專利申請(qǐng)WO1996/19099或CHISSOCorporation的專利申請(qǐng)GB2228197中描述的組合物,但是對(duì)大部分來說,這些組合物為其中透明質(zhì)酸不是主要成分、透明質(zhì)酸量與抗壞血酸磷酸酯鹽量的比值一般小于1的組合物。此外,這些組合物用于表面使用,而不用于黏彈性補(bǔ)充或填充,并因此不進(jìn)行滅菌操作。AMWAYCorporation的WO2000/71094中也描述了另一些組合物,這些組合物與上述專利申請(qǐng)中描述的制劑表現(xiàn)出相同的特征,并且盡管確定了抗壞血酸磷酸酯鹽的目的,但是未教導(dǎo)可用抗壞血酸磷酸酯鹽配制用于填充或用于黏彈性補(bǔ)充的、其中主要成分為透明質(zhì)酸的產(chǎn)品。但是,ALLERGAN的專利申請(qǐng)WO2011/086458中描述了用于填充皺紋或黏彈性補(bǔ)充且經(jīng)過滅菌的組合物,這些組合物包含透明質(zhì)酸以及相對(duì)于組合物重量的按重量計(jì)0.6%至2%的量的維生素C衍生物,例如抗壞血酸2-葡糖苷、抗壞血酸磷酸酯鈉或抗壞血酸磷酸酯鎂。根據(jù)專利權(quán)人,包含抗壞血酸2-葡糖苷的組合物可提供穩(wěn)定的制劑,并且當(dāng)抗壞血酸2-葡糖苷濃度升高時(shí),其穩(wěn)定性提高(參見實(shí)施例6)。認(rèn)為包含2%抗壞血酸磷酸酯鈉的制劑是穩(wěn)定的(實(shí)施例5)。但是,專利權(quán)人描述了包含相對(duì)于組合物總重量的按重量計(jì)2%量的抗壞血酸磷酸酯鎂的組合物在經(jīng)歷高壓蒸氣滅菌后變得不穩(wěn)定(參見實(shí)施例4);然而,卻未公開所述組合物中透明質(zhì)酸的含量,因此無法計(jì)算[HA]/[MAP]比值且不能利用和重復(fù)結(jié)果。Q-MED的專利申請(qǐng)WO2012/104419描述了旨在用于填充皺紋或用于黏彈性補(bǔ)充且經(jīng)受滅菌的可注射組合物。這些組合物包含透明質(zhì)酸、局部麻醉劑和0.01至1mg/mL量的抗壞血酸衍生物,例如特別是抗壞血酸磷酸酯鈉、抗壞血酸磷酸酯鎂或抗壞血酸2-葡糖苷。在這些組合物中,抗壞血酸衍生物的存在防止或減輕了局部麻醉劑在滅菌期間對(duì)組合物黏度和/或彈性的不良作用。實(shí)際上,該專利申請(qǐng)描述了,添加局部麻醉劑后,組合物的黏度和彈性分量(composantesélastiques,elasticcomponent)G’均顯著提高。該專利申請(qǐng)明確說明,相對(duì)于不含抗壞血酸的相同組合物,含有抗壞血酸衍生物的組合物的穩(wěn)定性未得到提高,并且添加抗壞血酸衍生物可導(dǎo)致組合物的穩(wěn)定性發(fā)生稍微降低。實(shí)例表明添加抗壞血酸磷酸酯鎂能夠抵消利多卡因?qū)宦?lián)透明質(zhì)酸組合物的彈性的影響。在此情況下,組合物的彈性在加入抗壞血酸磷酸酯鎂后有所降低。另一些實(shí)例表明,添加抗壞血酸磷酸酯鎂能夠抵消利多卡因?qū)Ψ墙宦?lián)透明質(zhì)酸組合物的黏度的影響。在此情況下,組合物的黏度在添加抗壞血酸磷酸酯鎂后有所降低。CARBYLANBIOSURGERY的專利申請(qǐng)WO2009/005790描述了用在用于例如黏彈性補(bǔ)充之可注射或可植入制劑或用于生物醫(yī)學(xué)應(yīng)用之黏性組合物中的組合物。這些組合物經(jīng)受滅菌,并且包含經(jīng)包含巰基官能團(tuán)之取代基化學(xué)修飾的透明質(zhì)酸和抗壞血酸或其衍生物,例如抗壞血酸鈉或棕櫚酰抗壞血酸酯/鹽。包含經(jīng)修飾之透明質(zhì)酸的這些組合物表現(xiàn)出提高的穩(wěn)定性。鑒于上述現(xiàn)有技術(shù)中的教導(dǎo),完全令人吃驚和意外的是,已證明相對(duì)于單獨(dú)包含交聯(lián)透明質(zhì)酸的組合物,包含交聯(lián)透明質(zhì)酸之組合物中小于或等于1%量的抗壞血酸磷酸酯鎂在滅菌后提高或保持了彈性分量G’的流變特性。如實(shí)例中所證明,這種作用在包含抗壞血酸磷酸酯鈉的組合物中未觀察到。此外,申請(qǐng)人已表明,包含非交聯(lián)透明質(zhì)酸之組合物中小于或等于1%的量的抗壞血酸磷酸酯鎂在滅菌后能夠保持組合物的黏度,并且相對(duì)于單獨(dú)包含非交聯(lián)透明質(zhì)酸的組合物,在滅菌后提高或保持了彈性分量G’流變特性。技術(shù)實(shí)現(xiàn)要素:因此,本發(fā)明提供了滅菌后流變性提高或保持的包含透明質(zhì)酸和抗壞血酸磷酸酯鎂的組合物。在一個(gè)實(shí)施方案中,當(dāng)透明質(zhì)酸是交聯(lián)的時(shí),相對(duì)于不包含抗壞血酸磷酸酯鎂的組合物,根據(jù)本發(fā)明的組合物在滅菌后顯示出提高的流變性值。本發(fā)明提供了包含單獨(dú)的或混合物中的交聯(lián)或非交聯(lián)的至少一種透明質(zhì)酸或其鹽以及抗壞血酸磷酸酯鹽的組合物、用于制備所述組合物的方法及其配制用于填充皺紋之組合物或黏彈性補(bǔ)充組合物的用途。本發(fā)明提供了一種無菌的組合物,其包含單獨(dú)的或混合物中的至少一種透明質(zhì)酸或其生物學(xué)上可接受的鹽以及抗壞血酸磷酸酯鎂,透明質(zhì)酸或其鹽的量[HA]與抗壞血酸磷酸酯鎂的量[MAP]的質(zhì)量比[HA]/[MAP]大于或等于1,抗壞血酸磷酸酯鎂的量為相對(duì)于所述組合物總重量的按重量計(jì)0.001%至1%,其中彈性分量G’在滅菌后保持或提高,并且為5至400Pa。在一個(gè)實(shí)施方案中,彈性分量G’在滅菌后保持或提高,并且為5至350Pa。在一個(gè)實(shí)施方案中,彈性分量G’在滅菌后保持或提高,并且為50至300Pa。在一個(gè)實(shí)施方案中,通過高壓蒸汽對(duì)所述組合物進(jìn)行滅菌。在一個(gè)實(shí)施方案中,通過環(huán)氧乙烷對(duì)所述組合物進(jìn)行滅菌。在一個(gè)實(shí)施方案中,通過用γ射線輻照對(duì)組合物進(jìn)行滅菌。單獨(dú)的或混合物中的透明質(zhì)酸或其生物學(xué)上可接受的鹽意指單獨(dú)的或混合物中的交聯(lián)或非交聯(lián)透明質(zhì)酸,任選地單獨(dú)地或在混合物中通過取代進(jìn)行化學(xué)修飾。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物包含單獨(dú)的或混合物中的至少一種非交聯(lián)透明質(zhì)酸或其鹽。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物包含單獨(dú)的或混合物中的至少一種交聯(lián)透明質(zhì)酸或其鹽。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物包含單獨(dú)的或混合物中的至少一種共交聯(lián)透明質(zhì)酸或其鹽。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物包含單獨(dú)的或混合物中的至少一種通過取代進(jìn)行化學(xué)修飾的透明質(zhì)酸或其鹽。在一個(gè)實(shí)施方案中,透明質(zhì)酸是鈉鹽或鉀鹽的形式。在一個(gè)實(shí)施方案,根據(jù)本發(fā)明的組合物的透明質(zhì)酸或其鹽的量[HA]與抗壞血酸磷酸酯鎂的量[MAP]的質(zhì)量比[HA]/[MAP]為10至30。在一個(gè)實(shí)施方案,根據(jù)本發(fā)明的組合物的透明質(zhì)酸或其鹽的量[HA]與抗壞血酸磷酸酯鎂的量[MAP]的質(zhì)量比[HA]/[MAP]為15至25。在一個(gè)實(shí)施方案,根據(jù)本發(fā)明的組合物的透明質(zhì)酸或其鹽的量[HA]與抗壞血酸磷酸酯鎂的量[MAP]的質(zhì)量比[HA]/[MAP]為約20。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為相對(duì)于所述組合物總重量的按重量計(jì)0.01%至0.5%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為相對(duì)于所述組合物總重量的按重量計(jì)0.03%至1%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為相對(duì)于所述組合物總重量的按重量計(jì)0.05%至0.15%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為相對(duì)于所述組合物總重量的按重量計(jì)0.03%至0.1%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為相對(duì)于所述組合物總重量的按重量計(jì)0.07%至0.1%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為0.01至10mg/g組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為0.3至10mg/g組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為0.1至5mg/g組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為0.5至1.5mg/g組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為0.3至1mg/g組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的抗壞血酸磷酸酯鎂含量為0.7至1mg/g組合物。Mw或“分子量”指以道爾頓測(cè)量的聚合物的質(zhì)量平均分子量。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的特征在于透明質(zhì)酸或其鹽的分子量Mw為0.01MDa至5MDa。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的特征在于透明質(zhì)酸或其鹽的分子量Mw為0.1MDa至3.5MDa。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的透明質(zhì)酸或其鹽的總含量為相對(duì)于所述組合物總重量的按重量計(jì)0.2%至5%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的透明質(zhì)酸或其鹽的總含量大于或等于相對(duì)于所述組合物總重量的按重量計(jì)1%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的透明質(zhì)酸或其鹽的總含量為2mg/g至50mg/g組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的透明質(zhì)酸或其鹽的總含量為4mg/g至40mg/g組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的透明質(zhì)酸或其鹽的總含量為5mg/g至30mg/g所述組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的透明質(zhì)酸或其鹽的總含量為10mg/g至30mg/g所述組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物包含至少一種非交聯(lián)的透明質(zhì)酸或其鹽。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物包含至少一種交聯(lián)的透明質(zhì)酸或其鹽。在本發(fā)明中,將交聯(lián)度X定義為等于如下比例:在一個(gè)實(shí)施方案中,交聯(lián)透明質(zhì)酸的交聯(lián)度X為0.001至0.5。在一個(gè)實(shí)施方案中,交聯(lián)透明質(zhì)酸的交聯(lián)度X為0.01至0.25。在一個(gè)實(shí)施方案中,交聯(lián)透明質(zhì)酸的交聯(lián)度X為0.1至0.2。在一個(gè)實(shí)施方案中,如專利申請(qǐng)WO2000/046253中所述,透明質(zhì)酸是共交聯(lián)的。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物包含交聯(lián)透明質(zhì)酸或其鹽和非交聯(lián)透明質(zhì)酸或其鹽的混合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物包含交聯(lián)透明質(zhì)酸或其鹽的混合物。在一個(gè)實(shí)施方案中,交聯(lián)透明質(zhì)酸或其鹽的混合物是專利申請(qǐng)WO2009/071697中所述的單相混合物類型。在一個(gè)實(shí)施方案中,如專利申請(qǐng)WO2004/092222中所述,交聯(lián)透明質(zhì)酸或其鹽的混合物為通過在交聯(lián)前混合不同分子量的多種透明質(zhì)酸或其鹽獲得的混合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物包含至少一種經(jīng)賦予親脂性或水合性之基團(tuán)取代的透明質(zhì)酸或其鹽,例如,以本申請(qǐng)人名義的專利申請(qǐng)F(tuán)R1161125中所述的經(jīng)取代透明質(zhì)酸。在一個(gè)實(shí)施方案中,所述組合物還包含另一種多糖。在一個(gè)實(shí)施方案中,該另一種多糖選自纖維素、褐藻酸或其鹽。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物還包含二甲基砜。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的二甲基砜含量為相對(duì)于所述組合物總重量的按重量計(jì)0.001%至5%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的二甲基砜含量為相對(duì)于所述組合物總重量的按重量計(jì)0.1%至1%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的二甲基砜含量為0.1至20mg/g組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的二甲基砜含量為1至10mg/g組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物還包含至少一種額外試劑。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物具有選自單獨(dú)的或混合物中的抗氧化劑和局部麻醉劑的額外試劑。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物具有選自利多卡因、普魯卡因、甲哌卡因、羅哌卡因、布比卡因或其可藥用鹽的局部麻醉劑。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物具有的局部麻醉劑為鹽酸利多卡因。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物具有選自多元醇的抗氧化劑。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物具有選自單獨(dú)的或混合物中的甘露糖醇和山梨糖醇的抗氧化劑。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物具有的抗氧化劑為甘露糖醇。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物具有的抗氧化劑為山梨糖醇。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物具有的抗氧化劑為甘露糖醇和山梨糖醇的混合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的額外試劑含量為相對(duì)于所述組合物總重量的按重量計(jì)0.01%至10%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的額外試劑含量為相對(duì)于所述組合物總重量的按重量計(jì)0.1%至5%。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的額外試劑含量為0.1至100mg/g組合物。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的組合物的額外試劑含量為1至50mg/g組合物。在一個(gè)實(shí)施方案中,本發(fā)明為包含至少一種根據(jù)本發(fā)明的組合物的黏彈性補(bǔ)充組合物。在一個(gè)實(shí)施方案中,本發(fā)明為用于治療干眼病或眼部干燥的組合物,其包含至少一種根據(jù)本發(fā)明的組合物。根據(jù)一些實(shí)施方案,所述組合物用作人工淚液、淚凝膠或潤(rùn)滑劑。在一個(gè)實(shí)施方案中,本發(fā)明組合物的彈性分量G’在滅菌后保持或提高,并且為5至400Pa。在一個(gè)實(shí)施方案中,彈性分量G’在滅菌后保持或提高,并且為5至350Pa。在一個(gè)實(shí)施方案中,彈性分量G’在滅菌后保持或提高,并且為50至300Pa。在一個(gè)實(shí)施方案中,本發(fā)明提供了0.3至10mg/g濃度的抗壞血酸磷酸酯鎂用于在組合物滅菌后保持或改善彈性的用途,所述組合物包含單獨(dú)的或混合物中的至少一種透明質(zhì)酸或其生物學(xué)上可接受的鹽。在該用途的一個(gè)實(shí)施方案中,所述組合物中單獨(dú)的或混合物中的透明質(zhì)酸或其鹽的量為相對(duì)于所述組合物總重量的按重量計(jì)0.2%至5%。在該用途的一個(gè)實(shí)施方案中,所述組合物中單獨(dú)的或混合物中的透明質(zhì)酸或其鹽的量大于或等于相對(duì)于所述組合物總重量的按重量計(jì)1%。在該用途的一個(gè)實(shí)施方案中,透明質(zhì)酸或其鹽是交聯(lián)的。在該用途的一個(gè)實(shí)施方案中,透明質(zhì)酸或其鹽的交聯(lián)度為0.001至0.5。在該用途的一個(gè)實(shí)施方案中,所述組合物中抗壞血酸磷酸酯鎂的濃度為0.3至10mg/g,以便在滅菌后改善所述組合物的彈性。在該用途的一個(gè)實(shí)施方案中,透明質(zhì)酸或其鹽是非交聯(lián)的。在該用途的一個(gè)實(shí)施方案中,所述組合物中抗壞血酸磷酸酯鎂的濃度為0.7至3mg/g。在該用途的一個(gè)實(shí)施方案中,所述組合物中抗壞血酸磷酸酯鎂的濃度為0.7至1mg/g,以便在滅菌后改善所述組合物的彈性。此外,本發(fā)明還提供了抗壞血酸磷酸酯鎂作為試劑用于在組合物滅菌后保持或改善彈性的用途,所述組合物包含單獨(dú)的或混合物中的至少一種透明質(zhì)酸或其生物學(xué)上可接受的鹽,抗壞血酸磷酸酯鎂的濃度為0.3至10mg/g,并且透明質(zhì)酸或其鹽的量[HA]與抗壞血酸磷酸酯鎂的量[MAP]的質(zhì)量比[HA]/[MAP]大于或等于1。此外,本發(fā)明提供了用于在組合物滅菌后保持或改善彈性的方法,所述組合物包含單獨(dú)的或混合物中的至少一種透明質(zhì)酸或其生物學(xué)上可接受的鹽,所述方法包括向所述組合物添加0.3至10mg/g濃度的抗壞血酸磷酸酯鎂,透明質(zhì)酸或其鹽的量[HA]與抗壞血酸磷酸酯鎂的量[MAP]的質(zhì)量比[HA]/[MAP]大于或等于1。在該方法和/或該用途的一個(gè)實(shí)施方案中,所述組合物中透明質(zhì)酸或其鹽的分子量Mw為0.01MDa至5MDa。在該方法和/或該用途的一個(gè)實(shí)施方案中,所述組合物中單獨(dú)的或混合物中的透明質(zhì)酸或其鹽的量為相對(duì)于所述組合物總重量的按重量計(jì)0.2%至5%。在該方法和/或該用途的一個(gè)實(shí)施方案中,所述組合物中單獨(dú)的或混合物中的透明質(zhì)酸或其鹽的量大于或等于相對(duì)于所述組合物總重量的按重量計(jì)1%。在該方法和/或該用途的一個(gè)實(shí)施方案中,所述組合物包含交聯(lián)的透明質(zhì)酸或其鹽。在該方法和/或該用途的一個(gè)實(shí)施方案中,所述組合物中透明質(zhì)酸或其鹽的交聯(lián)度為0.001至0.5。在該方法和/或該用途的一個(gè)實(shí)施方案中,所述組合物中抗壞血酸磷酸酯鎂的濃度為0.3至10mg/g以在滅菌后改善所述組合物的彈性。在該方法和/或該用途的一個(gè)實(shí)施方案中,所述組合物包含非交聯(lián)的透明質(zhì)酸或其鹽。在該方法和/或該用途的一個(gè)實(shí)施方案中,所述組合物中的抗壞血酸磷酸酯鎂濃度為0.7至3mg/g。在該方法和/或該用途的一個(gè)實(shí)施方案中,所述組合物中抗壞血酸磷酸酯鎂的濃度為0.7至1mg/g,以便在滅菌后改善所述組合物的彈性。此外,本發(fā)明提供了用于制備根據(jù)本發(fā)明的組合物的方法。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法至少包括:-使單獨(dú)的或混合物中的至少一種透明質(zhì)酸或其鹽的纖維水合以提供水凝膠的步驟,-將抗壞血酸磷酸酯鎂的溶液與上述步驟中獲得的水凝膠混合的步驟,-均質(zhì)化步驟;和-滅菌步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法在室溫下進(jìn)行其水合步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法在室溫下進(jìn)行其均質(zhì)化步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法具有在適合所述制備方法的溫度下進(jìn)行將抗壞血酸磷酸酯鎂溶液與水合步驟中獲得的水凝膠混合的步驟。在一個(gè)實(shí)施方案中,其在室溫下進(jìn)行。在一個(gè)實(shí)施方案中,通過高壓蒸汽進(jìn)行滅菌步驟。在一個(gè)實(shí)施方案中,通過環(huán)氧乙烷進(jìn)行滅菌步驟。在一個(gè)實(shí)施方案中,通過用γ射線輻照進(jìn)行滅菌步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法在121℃至134℃的溫度下進(jìn)行高壓蒸氣滅菌,持續(xù)適應(yīng)于所述溫度的時(shí)間。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法還包括至少一個(gè)將經(jīng)均質(zhì)化的混合物包裝在注射器中的步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法還包括至少一個(gè)將經(jīng)均質(zhì)化的混合物包裝在單劑量小瓶中的步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法還包括至少一個(gè)交聯(lián)步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法的交聯(lián)步驟位于水合步驟和混合步驟之間。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法通過至少一種交聯(lián)劑進(jìn)行交聯(lián)步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法具有雙功能交聯(lián)劑或多功能交聯(lián)劑。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法具有選自以下的雙功能交聯(lián)劑或多功能交聯(lián)劑:乙二醇二縮水甘油醚;丁二醇二縮水甘油醚(BDDE);聚甘油聚縮水甘油醚;聚乙二醇二縮水甘油醚;聚丙二醇二縮水甘油醚;雙環(huán)氧化合物或聚環(huán)氧化合物,例如1,2,3,4-二環(huán)氧丁烷或1,2,7,8-二環(huán)氧辛烷;二烷基砜;二乙烯基砜;甲醛;表氯醇或戊二醛或碳二亞胺,例如1-乙基-3-[3-二甲基氨基丙基]碳二亞胺鹽酸鹽(EDC)。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法的雙功能交聯(lián)劑為丁二醇二縮水甘油醚(BDDE)或1,2,7,8-二環(huán)氧辛烷。在一個(gè)實(shí)施方案中,本發(fā)明的制備方法根據(jù)本領(lǐng)域技術(shù)人員熟知的技術(shù)進(jìn)行交聯(lián)步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法包括在交聯(lián)步驟之后的至少一個(gè)純化和洗滌步驟,其根據(jù)本領(lǐng)域技術(shù)人員所熟知的技術(shù)進(jìn)行。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法還包括至少一個(gè)將二甲基砜的溶液與水合步驟中獲得的水凝膠混合的步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法使將二甲基砜溶液與水合步驟中獲得之水凝膠混合的步驟置于均質(zhì)化步驟之前。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法在適合所述制備方法的溫度下進(jìn)行將二甲基砜溶液與水合步驟中獲得之水凝膠混合的步驟。在一個(gè)實(shí)施方案中,其在室溫下進(jìn)行。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法還包括至少一個(gè)將至少一種額外試劑的溶液與水合步驟中獲得之水凝膠混合的步驟。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法使將至少一種額外試劑的溶液與水合步驟中獲得之水凝膠混合的步驟置于均質(zhì)化步驟之前。在一個(gè)實(shí)施方案中,根據(jù)本發(fā)明的方法在適合所述制備方法的溫度下進(jìn)行將至少一種額外試劑的溶液與水合步驟中獲得之水凝膠混合的步驟。在一個(gè)實(shí)施方案中,其在室溫下進(jìn)行。本發(fā)明提供了根據(jù)本發(fā)明的組合物用于配制用于填充皺紋的組合物的用途。本發(fā)明提供了根據(jù)本發(fā)明的組合物用于配制黏彈性補(bǔ)充組合物的用途。更具體地,預(yù)期應(yīng)用為在可注射黏彈性產(chǎn)品和多糖背景下通常觀察到的那些應(yīng)用,所述產(chǎn)品和多糖用于或潛在地可用于下列病理狀況或治療中:-美容面部注射:用于填充皺紋、皮膚缺陷或體積缺陷(顴骨、頦、唇);-體內(nèi)的豐盈注射物:乳房和臀部增大、G點(diǎn)增大、陰道成形、陰唇重建、陰莖擴(kuò)大;-治療骨關(guān)節(jié)炎:注射到關(guān)節(jié)內(nèi)以替代或補(bǔ)充缺乏的滑液;-尿道周注射以用于治療由于括約肌功能不全而導(dǎo)致的尿失禁;-手術(shù)后注射以特別地預(yù)防腹膜黏連;-在遠(yuǎn)視手術(shù)后通過鞏膜激光切口注射;-注射到玻璃體腔內(nèi);-在白內(nèi)障手術(shù)期間注射;-注射到生殖器部位內(nèi)。更具體地,在美容手術(shù)中,根據(jù)其黏彈性和持久性,通過本發(fā)明方法獲得的組合物可:-用于填充細(xì)紋、中度皺紋或深皺紋,并且可使用窄徑針(例如,27號(hào)針)進(jìn)行注射;-用作通過直徑較大的針(例如,22號(hào)至26號(hào))和較長(zhǎng)的針(例如,30mm至40mm)進(jìn)行注射的豐盈產(chǎn)品;在該情況下,其黏著性將確保其被保持在注射部位。根據(jù)本發(fā)明的組合物還主要應(yīng)用于關(guān)節(jié)手術(shù)和牙科手術(shù)中以例如用于填充牙周袋。這些用途實(shí)例絕不是限制性的,并且更廣泛地,考慮將根據(jù)本發(fā)明的組合物用于:-填充體積;-在某些組織中產(chǎn)生空間,從而促進(jìn)其發(fā)揮最佳功能;-替代缺乏的生理流體。本發(fā)明還提供了一種藥盒,其包含包裝在注射器中并在包裝后經(jīng)過滅菌的根據(jù)本發(fā)明的組合物。本發(fā)明還提供了一種藥盒,其包含包裝在單劑量小瓶中并在包裝后經(jīng)過滅菌的根據(jù)本發(fā)明的組合物。根據(jù)本發(fā)明的組合物還應(yīng)用在化妝品領(lǐng)域或制藥領(lǐng)域中。更具體地,在化妝品領(lǐng)域中,根據(jù)本發(fā)明的組合物將用作化妝品組合物中的活性保濕成分。在制藥領(lǐng)域中,根據(jù)本發(fā)明的組合物將用作用于水化因眼部干燥而受到影響之眼睛的組合物,即人工淚液。在這些化妝品應(yīng)用和/或制藥應(yīng)用中,所述組合物還可包含任何化妝品上或藥學(xué)上可接受的成分。附圖說明圖1是舉例說明在通過高壓蒸汽滅菌組合物后,作為圖中橫坐標(biāo)上抗壞血酸磷酸酯鎂量(mg/g組合物)函數(shù)的圖中縱坐標(biāo)上彈性分量G’百分比提高的圖,所述組合物包含交聯(lián)透明質(zhì)酸和抗壞血酸磷酸酯鎂。圖2是舉例說明在通過高壓蒸汽滅菌組合物后,作為圖中橫坐標(biāo)上抗壞血酸磷酸酯鎂量(mg/g組合物)函數(shù)的圖中縱坐標(biāo)上黏度η百分比提高的圖,所述組合物包含非交聯(lián)透明質(zhì)酸和抗壞血酸磷酸酯鎂。具體實(shí)施方式在下文的實(shí)施例中對(duì)根據(jù)本發(fā)明的組合物的特征及其制備方法和特性進(jìn)行舉例說明。實(shí)施例1該實(shí)施例舉例說明了根據(jù)本發(fā)明的一種組合物,其包含非交聯(lián)的透明質(zhì)酸和抗壞血酸磷酸酯鎂。稱取可注射級(jí)的透明質(zhì)酸鈉(NaHA)的纖維(1g;分子量:約2.7MDa)到容器中。添加磷酸鹽緩沖液(32.3g)的水溶液,并使用刮勺于室溫和900mmHg大氣壓下均質(zhì)化全部溶液約1小時(shí)。由此獲得的非交聯(lián)NaHA水凝膠的NaHA含量為約30mg/g。將抗壞血酸磷酸酯鎂(MAP)(60mg或2.4×10-4mol)溶解于磷酸鹽緩沖液(19.94g)中以得到含量為3mg/g的抗壞血酸磷酸酯鎂水溶液。通過添加預(yù)先制備的抗壞血酸磷酸酯鎂水溶液來稀釋上述步驟中獲得的NaHA水凝膠。然后,均質(zhì)化所得組合物。這樣得到了包含20mg/g量的非交聯(lián)NaHA和1mg/g量的MAP的組合物;質(zhì)量比[HA]/[MAP]為20。將由此獲得的組合物包裝在經(jīng)高壓蒸汽滅菌(T=121℃,10分鐘)的注射器中。實(shí)施例2該實(shí)施例舉例說明了根據(jù)本發(fā)明的一個(gè)組合物實(shí)例,其包含交聯(lián)的透明質(zhì)酸和抗壞血酸磷酸酯鎂。以透明質(zhì)酸鈉(NaHA)的纖維(1g;分子量:約2.7MDa)和丁二醇二縮水甘油醚(BDDE,54mg)起始通過VIVACY的WO2009/071697中描述的交聯(lián)方法(實(shí)施例1,第一部分)獲得包含交聯(lián)透明質(zhì)酸的組合物。所得組合物包含約30mg/g交聯(lián)度X為約0.12的交聯(lián)NaHA。按照實(shí)施例1制備含量為3mg/g的抗壞血酸磷酸酯鎂水溶液。通過添加預(yù)先制備的抗壞血酸磷酸酯鎂的水溶液來稀釋上述步驟中獲得的交聯(lián)NaHA水凝膠。然后,均質(zhì)化所得組合物。這樣得到了包含20mg/g量的交聯(lián)NaHA和1mg/g量的抗壞血酸磷酸酯鎂的組合物;質(zhì)量比[HA]/[MAP]為20。將由此獲得的組合物包裝在經(jīng)高壓蒸氣滅菌(T=121℃,10分鐘)的注射器中。實(shí)施例3該實(shí)施例舉例說明了根據(jù)本發(fā)明的一個(gè)組合物實(shí)例,其包含交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和利多卡因。以含量為30mg/g的NaHA水凝膠和含量為10mg/g的抗壞血酸磷酸酯鎂起始,通過實(shí)施例2中所述的方法制備包含交聯(lián)NaHA的組合物。通過ANTEIS之WO2009/024670中描述的方法或通過VIVACY之專利申請(qǐng)US61/791,977或FR13/52971中描述的方法向如上獲得的組合物中加含量為13mg/g的利多卡因溶液。所得組合物包含20mg/g量的交聯(lián)透明質(zhì)酸、3mg/g量的利多卡因和1mg/g量的抗壞血酸磷酸酯鎂;質(zhì)量比[HA]/[MAP]為20。將由此獲得的組合物包裝在經(jīng)高壓蒸汽滅菌(T=121℃,10分鐘)的注射器中。實(shí)施例4該實(shí)施例舉例說明了根據(jù)本發(fā)明的一個(gè)組合物實(shí)例,其包含非交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和二甲基砜。以含量為30mg/g的透明質(zhì)酸水凝膠和含量為10mg/g的抗壞血酸磷酸酯鎂溶液起始,通過實(shí)施例1的方法制備包含非交聯(lián)透明質(zhì)酸和抗壞血酸磷酸酯鎂的組合物。另外,向如上獲得的組合物添加含量為4.3mg/g的二甲基砜溶液。然后,將所得組合物均質(zhì)化。這樣得到了包含20mg/g量的非交聯(lián)透明質(zhì)酸、1mg/g量的二甲基砜和1mg/g量的抗壞血酸磷酸酯鎂的組合物;質(zhì)量比[HA]/[MAP]為20。將所得組合物包裝在經(jīng)高壓蒸汽滅菌(T=121℃,10分鐘)的注射器中。實(shí)施例5該實(shí)施例舉例說明了根據(jù)本發(fā)明的一個(gè)組合物實(shí)例,其包含交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和二甲基砜。以含量為30mg/g的NaHA水凝膠和含量為10mg/g的抗壞血酸磷酸酯鎂起始,通過實(shí)施例2中所述的方法制備包含交聯(lián)NaHA的組合物。另外,向如上獲得的組合物添加含量為4.3mg/g的二甲基砜溶液。然后,將所得組合物均質(zhì)化。這樣得到了包含20mg/g量的交聯(lián)透明質(zhì)酸、1mg/g量的二甲基砜和1mg/g量的抗壞血酸磷酸酯鎂的組合物;質(zhì)量比[HA]/[MAP]為20。將所得組合物包裝在經(jīng)高壓蒸汽滅菌(T=121℃,10分鐘)的注射器中。實(shí)施例6該實(shí)施例舉例說明了包含非交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和甘露糖醇的一個(gè)組合物實(shí)例。以含量為30mg/g的NaHA水凝膠和含量為10mg/g的抗壞血酸磷酸酯鎂起始,通過實(shí)施例1中所述的方法制備包含非交聯(lián)NaHA的組合物。另外,向如上獲得的組合物添加含量為4.3mg/g的甘露糖醇溶液。然后,將所得組合物均質(zhì)化。這樣得到了包含20mg/g量非交聯(lián)透明質(zhì)酸、1mg/g量抗壞血酸磷酸酯鎂和1mg/g量甘露糖醇的組合物;質(zhì)量比[HA]/[MAP]為20。將所得組合物包裝在經(jīng)高壓蒸汽滅菌(T=121℃,10分鐘)的注射器中。實(shí)施例7該實(shí)施例舉例說明了包含交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和甘露糖醇的一個(gè)組合物實(shí)例。以含量為30mg/g的NaHA水凝膠和含量為10mg/g的抗壞血酸磷酸酯鎂起始,通過實(shí)施例2中所述的方法制備包含交聯(lián)NaHA的組合物。另外,向如上獲得的組合物添加含量為4.3mg/g的甘露糖醇溶液。然后,將所得組合物均質(zhì)化。這樣得到了包含20mg/g量交聯(lián)透明質(zhì)酸、1mg/g量抗壞血酸磷酸酯鎂和1mg/g量甘露糖醇的組合物;質(zhì)量比[HA]/[MAP]為20。將所得組合物包裝在經(jīng)高壓蒸汽滅菌(T=121℃,10分鐘)的注射器中。實(shí)施例8該實(shí)施例舉例說明了包含交聯(lián)透明質(zhì)酸和抗壞血酸磷酸酯鈉(SAP)的一個(gè)組合物實(shí)例。以含量為30mg/g的透明質(zhì)酸凝膠和含量為3mg/g的抗壞血酸磷酸酯鈉起始,通過實(shí)施例2中所述的方法制備包含交聯(lián)透明質(zhì)酸和抗壞血酸磷酸酯鈉的組合物。所得組合物包含20mg/g量的交聯(lián)透明質(zhì)酸和1mg/g量的抗壞血酸磷酸酯鈉;質(zhì)量比[HA]/[MAP]為20。將所得組合物包裝在經(jīng)高壓蒸汽滅菌(T=121℃,10分鐘)的注射器中。實(shí)施例9該對(duì)比例舉例說明了包含非交聯(lián)透明質(zhì)酸和甘露糖醇的一個(gè)組合物實(shí)例。以含量為30mg/g的透明質(zhì)酸水凝膠和含量為3mg/g的甘露糖醇溶液起始,通過實(shí)施例1的方法制備包含非交聯(lián)透明質(zhì)酸和甘露糖醇(MAN)的組合物。所得組合物包含20mg/g量的非交聯(lián)透明質(zhì)酸和1mg/g量的甘露糖醇;質(zhì)量比[HA]/[MAN]為20。將所得組合物包裝在經(jīng)高壓蒸汽滅菌(T=121℃,10分鐘)的注射器中。實(shí)施例10該對(duì)比例舉例說明了包含交聯(lián)透明質(zhì)酸和甘露糖醇的一個(gè)組合物實(shí)例。以含量為30mg/g的NaHA水凝膠和含量為3mg/g的甘露糖醇起始,通過實(shí)施例2中所述的方法制備包含交聯(lián)NaHA的組合物。所得組合物包含20mg/g量的交聯(lián)透明質(zhì)酸和1mg/g量的甘露糖醇;質(zhì)量比[HA]/[MAN]為20。將所得組合物包裝在經(jīng)高壓蒸汽滅菌(T=121℃,10分鐘)的注射器中。實(shí)施例11表征如上列舉之包含交聯(lián)透明質(zhì)酸的組合物在經(jīng)高壓蒸汽滅菌前后的流變性。用TAInstrumentAR2000Ex流變儀于25℃振蕩下測(cè)量包含交聯(lián)透明質(zhì)酸的組合物在經(jīng)高壓蒸汽滅菌前后的彈性分量G’,其中彈性分量G’的值是相對(duì)于1Hz的頻率而言。對(duì)于所有的測(cè)量,通過用等量的磷酸鹽緩沖水溶液代替抗壞血酸磷酸酯鎂水溶液來配制參考組合物。彈性分量G’的百分比提高定義如下:其中Y=在參考組合物滅菌后,彈性分量G’損失的百分比并且Y’=在所測(cè)試組合物滅菌后,彈性分量G’損失的百分比。通過實(shí)施例2中所述的方法制備在組合物中包含交聯(lián)透明質(zhì)酸和0.3至20mg/g量的抗壞血酸磷酸酯鎂的八種組合物。通過實(shí)施例10中所述的方法制備組合物中包含交聯(lián)透明質(zhì)酸和1至10mg/g量的甘露糖醇的三種組合物。根據(jù)實(shí)施例8制備組合物中包含交聯(lián)透明質(zhì)酸和1至5mg/g量的抗壞血酸磷酸酯鈉的兩種組合物。通過實(shí)施例2中所述的方法制備包含交聯(lián)透明質(zhì)酸的參考組合物。用等量的磷酸鹽緩沖水溶液代替抗壞血酸磷酸酯鎂的水溶液。在滅菌前后測(cè)量所測(cè)試組合物的彈性分量,并計(jì)算彈性分量G’的百分比提高,其中所得結(jié)果示于下表1中:表1n/a:不適用如上獲得的包含MAP的組合物的結(jié)果還在圖1中舉例說明,圖1是表示通過對(duì)包含交聯(lián)透明質(zhì)酸和抗壞血酸磷酸酯鎂的組合物進(jìn)行高壓蒸汽滅菌后,作為抗壞血酸磷酸酯鎂含量之函數(shù)的彈性分量G’百分比提高的圖。對(duì)于包含交聯(lián)透明質(zhì)酸和0.3至20mg/g量抗壞血酸磷酸酯鎂的組合物,觀察到相對(duì)于參考組合物,當(dāng)抗壞血酸磷酸酯鎂的量為0.3至10mg/g時(shí),彈性分量G’有所提高;當(dāng)該量大于10mg/g時(shí),G’急劇下降。這些結(jié)果與包含交聯(lián)透明質(zhì)酸和甘露糖醇的組合物所獲得的結(jié)果相矛盾,后者表明,組合物中甘露糖醇含量提高得越多,相對(duì)于參考組合物,彈性分量G’提高得越多。這些結(jié)果還與包含交聯(lián)透明質(zhì)酸和SAP的組合物所獲得的結(jié)果相矛盾,對(duì)于后者這些組合物,彈性分量G’在兩個(gè)測(cè)試濃度下均有所降低。實(shí)施例12表征包含非交聯(lián)透明質(zhì)酸的組合物在經(jīng)高壓蒸汽滅菌前后的流變性。以其黏度η來表征包含非交聯(lián)透明質(zhì)酸的組合物。用TAInstrumentAR2000Ex流變儀于25℃施加應(yīng)力下測(cè)量組合物的黏度η。黏度值是相對(duì)于0.02s-1的應(yīng)力而言。通過實(shí)施例1中所述的方法制備在組合物中包含非交聯(lián)透明質(zhì)酸和0.3至3mg/g量抗壞血酸磷酸酯鎂的六種組合物。通過實(shí)施例1中所述的方法制備包含非交聯(lián)透明質(zhì)酸的參考組合物。用等量的磷酸鹽緩沖水溶液代替實(shí)施例1方法中所述的抗壞血酸磷酸酯鎂水溶液。將黏度η的百分比提高如下定義:其中Z=在參考組合物滅菌后,黏度η損失的百分比并且Z’=在所測(cè)試組合物滅菌后,黏度η損失的百分比。在滅菌前后測(cè)量所測(cè)試組合物的黏度,并計(jì)算黏度的百分比提高,其中所得結(jié)果示于下表2中:表2圖2中還舉例說明了上文所獲得的結(jié)果,圖2是表示在通過高壓蒸汽滅菌組合物后,作為抗壞血酸磷酸酯鎂含量之函數(shù)的黏度η百分比提高的圖,所述組合物包含非交聯(lián)透明質(zhì)酸和抗壞血酸磷酸酯鎂。相對(duì)于參考組合物,在抗壞血酸磷酸酯鎂含量為0.7至1mg/g的根據(jù)本發(fā)明的組合物中觀察到黏度保持。實(shí)施例12bisa)進(jìn)行類似的測(cè)試并在流變學(xué)上監(jiān)測(cè)彈性分量G’。通過實(shí)施例1中所述的方法制備在組合物中包含非交聯(lián)透明質(zhì)酸和0.3至1.25mg/g量的抗壞血酸磷酸酯鎂的七種組合物(透明質(zhì)酸鈉的分子量為約2.7MDa)。通過實(shí)施例1中所述的方法制備包含非交聯(lián)透明質(zhì)酸的參考組合物。用等量的磷酸鹽緩沖水溶液代替實(shí)施例1方法中所述的抗壞血酸磷酸酯鎂水溶液。在滅菌前后測(cè)量所測(cè)試組合物的彈性分量G’,并計(jì)算彈性分量G’的百分比提高,其中所得結(jié)果示于下表3中:表3相對(duì)于參考組合物,在抗壞血酸磷酸酯鎂含量為0.3至1mg/g的根據(jù)本發(fā)明的組合物中觀察到彈性有所提高;而且,在1.25mg/g的抗壞血酸磷酸酯鎂含量中觀察到彈性保持。實(shí)施例12bisb)用包含分子量約為1.4MDa的非交聯(lián)透明質(zhì)酸鈉的組合物進(jìn)行與如上所述測(cè)試12bisa)相同的測(cè)試,并在流變學(xué)上監(jiān)測(cè)彈性分量G’。通過實(shí)施例1中所述的方法制備組合物,同時(shí)用1.4MDa分子量透明質(zhì)酸鈉代替2.7MDa分子量透明質(zhì)酸鈉。在滅菌前后測(cè)量所測(cè)試組合物的彈性分量G’,并計(jì)算彈性分量G’的百分比提高,其中所得結(jié)果示于下表4中:表4相對(duì)于參考組合物,在抗壞血酸磷酸酯鎂含量為0.7至1mg/g的根據(jù)本發(fā)明的組合物中觀察到彈性有所提高;而且,在3mg/g的抗壞血酸磷酸酯鎂含量中觀察到彈性保持。實(shí)施例13表征包含交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和額外試劑的組合物在經(jīng)高壓蒸汽滅菌前后的流變性。根據(jù)實(shí)施例11中所述的方案測(cè)量包含交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和額外試劑的組合物在經(jīng)高壓蒸汽滅菌前后的流變性,計(jì)算彈性分量G’的百分比提高。通過實(shí)施例7中所述的方法制備組合物中包含交聯(lián)透明質(zhì)酸、1mg/g量抗壞血酸磷酸酯鎂和1mg/g量額外試劑的四種組合物。所述額外試劑為甘露糖醇(MAN)、山梨糖醇(SOR)、蔗糖八硫酸酯鉀(KSOS)水溶性鹽和鹽酸利多卡因(LIDO)。通過實(shí)施例2中所述的方法制備包含交聯(lián)透明質(zhì)酸和1mg/g量抗壞血酸磷酸酯鎂的組合物。通過實(shí)施例2中所述的方法制備包含交聯(lián)透明質(zhì)酸的參考組合物。用等量的磷酸鹽緩沖水溶液代替抗壞血酸磷酸酯鎂水溶液。在滅菌前后測(cè)量所測(cè)試組合物的彈性分量,并計(jì)算彈性分量G’的百分比提高,其中所得結(jié)果示于下表5中:表5發(fā)現(xiàn)在所有額外試劑的存在下,保持了在實(shí)施例11中觀察到的包含透明質(zhì)酸和抗壞血酸磷酸酯鎂之組合物的提高的流變性。僅添加鹽酸利多卡因?qū)е略撎岣甙l(fā)生顯著降低。實(shí)施例13bis表征包含交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和3mg/g利多卡因的組合物在經(jīng)高壓蒸汽滅菌前后的流變性。在滅菌前后測(cè)量所測(cè)試組合物的彈性分量并計(jì)算彈性分量G’的百分比提高,其中獲得的結(jié)果示于下表6中:表6發(fā)現(xiàn),添加利多卡因?qū)е陆M合物的彈性分量G’在滅菌后發(fā)生降低。添加1mg/gMAP不能抵消利多卡因?qū)M合物彈性的影響。然而,在存在利多卡因的情況下,添加3mg/g和10mg/gMAP確實(shí)提高了組合物的彈性。這些結(jié)果是未預(yù)期到的,并且與現(xiàn)有技術(shù),尤其是上述Q-MED的WO2012/104419中所述的教導(dǎo)和效果相反。實(shí)施例14表征包含非交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和額外試劑的組合物在經(jīng)高壓蒸汽滅菌前后的流變性。根據(jù)實(shí)施例12中所述的方案,測(cè)量包含非交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和額外試劑的組合物在經(jīng)高壓蒸汽滅菌前后的流變性,并計(jì)算黏度的百分比提高。通過實(shí)施例6中所述的方法制備組合物中包含非交聯(lián)透明質(zhì)酸、1mg/g量抗壞血酸磷酸酯鎂和1mg/g量額外試劑的三種組合物。所述額外試劑為甘露糖醇(MAN)、山梨糖醇(SOR)、以及蔗糖八硫酸酯鉀(KSOS)的水溶性鹽。通過實(shí)施例1中所述的方法制備包含非交聯(lián)透明質(zhì)酸和1mg/g量抗壞血酸磷酸酯鎂的組合物。通過實(shí)施例1中所述的方法制備包含非交聯(lián)透明質(zhì)酸的參考組合物。用等量的磷酸鹽緩沖水溶液代替實(shí)施例1方法中所述的抗壞血酸磷酸酯鎂水溶液。在滅菌前后測(cè)量所測(cè)試組合物的黏度,并計(jì)算黏度的百分比提高,其中所得結(jié)果示于下表7中:表7對(duì)于所有組合物,均觀察到黏度保持。實(shí)施例15表征包含交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和二甲基砜(DMS)的組合物在經(jīng)高壓蒸汽滅菌前后的流變性。根據(jù)實(shí)施例11中所述的方案,測(cè)量包含交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和二甲基砜(DMS)的組合物在經(jīng)高壓蒸汽滅菌前后的流變性,并計(jì)算彈性分量G’的百分比提高。通過實(shí)施例5中所述的方法制備包含交聯(lián)透明質(zhì)酸、組合物中的1mg/g量抗壞血酸磷酸酯鎂和組合物中的1至10mg/g量二甲基砜的兩種組合物。通過實(shí)施例2中所述的方法制備包含交聯(lián)透明質(zhì)酸和1mg/g量抗壞血酸磷酸酯鎂的一種組合物。通過實(shí)施例2中所述的方法制備包含交聯(lián)透明質(zhì)酸的參考組合物。用等量的磷酸鹽緩沖水溶液代替實(shí)抗壞血酸磷酸酯鎂水溶液。在滅菌前后測(cè)量所測(cè)試組合物的彈性分量,并計(jì)算彈性分量G’的百分比提高,其中所得結(jié)果示于下表8中:表8發(fā)現(xiàn)在1至10mg/g量DMS的存在下,保持了在實(shí)施例11中觀察到的包含透明質(zhì)酸和抗壞血酸磷酸酯鎂之組合物的流變性提高。實(shí)施例16表征包含非交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和二甲基砜(DMS)的組合物在經(jīng)高壓蒸汽滅菌前后的流變性。根據(jù)實(shí)施例12中所述的方案,測(cè)量包含非交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和二甲基砜(DMS)的組合物在經(jīng)高壓蒸汽滅菌前后的流變性,并計(jì)算黏度的百分比提高。通過實(shí)施例4中所述的方法制備包含非交聯(lián)透明質(zhì)酸、組合物中的1mg/g量抗壞血酸磷酸酯鎂和組合物中的1mg/g量二甲基砜的組合物并對(duì)其進(jìn)行滅菌,并根據(jù)實(shí)施例12通過流變學(xué)進(jìn)行表征。通過實(shí)施例1中所述的方法制備包含非交聯(lián)透明質(zhì)酸和1mg/g量抗壞血酸磷酸酯鎂的一種組合物。通過實(shí)施例1中所述的方法制備包含非交聯(lián)透明質(zhì)酸的參考組合物。用等量的磷酸鹽緩沖水溶液代替實(shí)施例1方法中所述的抗壞血酸磷酸酯鎂水溶液。在滅菌前后測(cè)量所測(cè)試組合物的黏度,并計(jì)算黏度的百分比提高,其中所得結(jié)果示于下表9中:表9發(fā)現(xiàn),包含非交聯(lián)透明質(zhì)酸、1mg/g量抗壞血酸磷酸酯鎂和1mg/g量二甲基砜的組合物的黏度得以保持。實(shí)施例17與現(xiàn)有技術(shù)中描述的組合物進(jìn)行比較。在ALLERGAN的國(guó)際專利申請(qǐng)WO2011/086458中,實(shí)施例4描述了包含交聯(lián)透明質(zhì)酸和相對(duì)于組合物總重量的按重量計(jì)0.6%至2%的抗壞血酸磷酸酯鎂的組合物。根據(jù)該專利權(quán)人,由于所述組合物的ΔTanδ1Hz值大于0.1,所以認(rèn)為這些組合物是不穩(wěn)定的。未限定包含交聯(lián)透明質(zhì)酸和分別為0.6%和1%量的抗壞血酸磷酸酯鎂的組合物的ΔTanδ1Hz值。僅限定了包含交聯(lián)透明質(zhì)酸和2%量抗壞血酸磷酸酯鎂的組合物的ΔTanδ1Hz值,其為0.344,是大于0.1的值。WO2011/086458還教導(dǎo),組合物中抗壞血酸磷酸酯鎂的量越大,所述組合物的ΔTanδ1Hz值容易降低的越多,并且趨向接近0.1的值。如上文引用的專利申請(qǐng),早期研究的組合物以其ΔTanδ1Hz表征,ΔTanδ1Hz是所測(cè)試組合物的Tanδ1Hz與參考組合物的Tanδ1Hz之間的差值,其中Tanδ1Hz為黏性分量G”與彈性分量G’的比值。所測(cè)試組合物相對(duì)于參考組合物的ΔTanδ1Hz值示于下表7中:表10測(cè)試[MAP](mg/g)[MAN](mg/g)[SAP](mg/g)ΔTanδ1Hz1000020.300-0.013530.700-0.01454100-0.014051.500-0.01286200-0.01367300-0.008481000-0.0008920000.024010010-0.013111050-0.0196120100-0.0210130010.0203140050.0771發(fā)現(xiàn),包含交聯(lián)透明質(zhì)酸和0.3至20mg/g量抗壞血酸磷酸酯鎂的組合物的ΔTanδ1Hz值小于0.1。同時(shí)還可看出,包含交聯(lián)透明質(zhì)酸和1至10mg/g量甘露糖醇的組合物的ΔTanδ1Hz值小于0.1,并且包含交聯(lián)透明質(zhì)酸和1至5mg/g量SAP的組合物的ΔTanδ1Hz值也小于0.1。總而言之,在包含交聯(lián)透明質(zhì)酸和0.3至20mg/g抗壞血酸磷酸酯鎂的組合物中獲得的結(jié)果相對(duì)于WO2011/086458的教導(dǎo)是矛盾的,原因是,根據(jù)本發(fā)明的組合物中的抗壞血酸磷酸酯鎂量等于或小于WO2011/086458中的抗壞血酸磷酸酯鎂的量,因此,ΔTanδ1Hz值小于0.1。對(duì)包含交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和額外試劑的組合物進(jìn)行相同的ΔTanδ1Hz測(cè)定,獲得的值示于下表8中:表11發(fā)現(xiàn),如前所述,經(jīng)高壓蒸汽滅菌后,ΔTanδ1Hz值小于0.1。對(duì)包含交聯(lián)透明質(zhì)酸、抗壞血酸磷酸酯鎂和二甲基砜(DMS)的組合物進(jìn)行相同的ΔTanδ1Hz測(cè)定,獲得的值示于下表9中:表12測(cè)試[MAP](mg/g)[DMS](mg/g)ΔTanδ1Hz330003410-0.00503511-0.006136110-0.0064再次發(fā)現(xiàn),ΔTanδ1Hz值小于0.1。以下內(nèi)容對(duì)應(yīng)于母案申請(qǐng)中的原始權(quán)利要求書,現(xiàn)作為說明書的一部分并入此處:1.經(jīng)滅菌組合物,其包含單獨(dú)的或混合物中的至少一種透明質(zhì)酸或其生物學(xué)上可接受的鹽,以及抗壞血酸磷酸酯鎂,透明質(zhì)酸或其鹽的量[HA]與抗壞血酸磷酸酯鎂的量[MAP]的質(zhì)量比[HA]/[MAP]大于或等于1,抗壞血酸磷酸酯鎂的量為相對(duì)于所述組合物總重量的按重量計(jì)0.001%至1%,其中彈性分量G’在滅菌后保持或提高,并且為5至400Pa。2.如項(xiàng)1所述的組合物,其中抗壞血酸磷酸酯鎂的量為相對(duì)于所述組合物總重量的按重量計(jì)0.03%至1%。3.如前述項(xiàng)中任一項(xiàng)所述的組合物,其中抗壞血酸磷酸酯鎂的量為相對(duì)于所述組合物總重量的按重量計(jì)0.05%至0.15%。4.如前述項(xiàng)中任一項(xiàng)所述的組合物,其中抗壞血酸磷酸酯鎂的量為相對(duì)于所述組合物總重量的按重量計(jì)0.03%至0.1%。5.如前述項(xiàng)中任一項(xiàng)所述的組合物,其中抗壞血酸磷酸酯鎂的量為相對(duì)于所述組合物總重量的按重量計(jì)0.07%至0.1%。6.如項(xiàng)1所述的組合物,其還包含二甲基砜。7.如項(xiàng)2至4中任一項(xiàng)所述的組合物,其中二甲基砜的量為相對(duì)于所述組合物總重量的按重量計(jì)0.001%至5%。8.如項(xiàng)2至4中任一項(xiàng)所述的組合物,其中二甲基砜的量為相對(duì)于所述組合物總重量的按重量計(jì)0.1%至1%。9.如前述項(xiàng)中任一項(xiàng)所述的組合物,其中透明質(zhì)酸或其鹽的分子量Mw為0.01至5MDa。10.如前述項(xiàng)中任一項(xiàng)所述的組合物,其中單獨(dú)的或混合物中的透明質(zhì)酸或其鹽的量為相對(duì)于所述組合物總重量的按重量計(jì)0.2%至5%。11.如前述項(xiàng)中任一項(xiàng)所述的組合物,其中單獨(dú)的或混合物中的透明質(zhì)酸或其鹽的量大于或等于相對(duì)于所述組合物總重量的按重量計(jì)1%。12.如前述項(xiàng)中任一項(xiàng)所述的組合物,其包含至少一種非交聯(lián)的透明質(zhì)酸或其鹽。13.如項(xiàng)1至9中任一項(xiàng)所述的組合物,其包含至少一種交聯(lián)的透明質(zhì)酸或其鹽。14.如項(xiàng)11所述的組合物,其中所述交聯(lián)透明質(zhì)酸或其鹽的交聯(lián)度為0.001至0.5。15.如前述項(xiàng)中任一項(xiàng)所述的組合物,所述組合物還包含至少一種額外的試劑。16.如項(xiàng)13所述的組合物,其中所述額外的試劑選自單獨(dú)的或混合物中的抗氧化劑和局部麻醉劑。17.如項(xiàng)14所述的組合物,其中所述局部麻醉劑選自利多卡因、普魯卡因、甲哌卡因、羅哌卡因、布比卡因或其可藥用鹽。18.如項(xiàng)14所述的組合物,其中所述抗氧化劑選自多元醇。19.用于制備如項(xiàng)1至16中任一項(xiàng)所述組合物的方法,其中所述制備方法至少包括:-使單獨(dú)的或混合物中的至少一種透明質(zhì)酸或其鹽的纖維水合以得到水凝膠的步驟,-將抗壞血酸磷酸酯鎂的溶液與前述步驟中獲得的水凝膠混合的步驟,-均質(zhì)化步驟;和-滅菌步驟。20.用于制備如項(xiàng)17所述組合物的方法,其中所述方法還包括至少一個(gè)交聯(lián)步驟。21.如項(xiàng)17和18中任一項(xiàng)所述的制備方法,其中所述方法還包括將二甲基砜的溶液與所述使單獨(dú)的或混合物中的至少一種透明質(zhì)酸或其鹽的纖維水合的步驟中獲得的水凝膠混合的至少一個(gè)步驟。22.如項(xiàng)1至16所述的組合物用于配制用于填充皺紋的組合物的用途。23.如項(xiàng)1至16所述的組合物用于配制用于黏彈性補(bǔ)充的組合物的用途。24.藥盒,其包含包裝在無菌注射器中的如項(xiàng)1至16所述的組合物。當(dāng)前第1頁(yè)1 2 3
相關(guān)技術(shù)
網(wǎng)友詢問留言
已有0條留言
- 還沒有人留言評(píng)論。精彩留言會(huì)獲得點(diǎn)贊!
1