檢測腎臟濾過功能的CT測量方法與流程
本發明涉及檢測腎臟濾過功能的CT測量方法。
背景技術:
血液經腎小球濾過生成原尿,再經腎小管和集合管吸收其中的部分水份和電解質濃縮成尿液排出,腎臟濾過功能對清除體內的代謝廢物、維持水和電解質的平衡至關重要。
通常所說的腎臟濾過功能即單位時間內腎臟濾過血漿的能力,因為濾過過程發生在腎小球,所以稱作腎小球濾過率(GFR),正常成人的GFR為120ml/min,也就是說每分鐘會有120ml的血漿經腎小球濾過形成原尿(每側腎臟約為60ml),并經過腎小管、集合管系統重新吸收原尿中的絕大多數水分(約98%,即濃縮)最終形成尿液,血漿內的代謝廢物隨同尿液排出體外,如腎功能受損、GFR下降,代謝廢物不能有效清除,就會在體內蓄積形成尿毒癥。
GFR是量化評估腎功能的指針。假如某一藥物能從腎小球自由濾過,并且在腎小管內不會被重新吸收,也不會有分泌,這個藥物的腎臟清除率在數值上等于GFR,這時GFR=濾過量/(血漿濃度*時間)。在生理學試驗中菊粉具有這樣的特點因而被用來測量GFR,但是在臨床實踐中因為注藥、抽血、留尿等諸多不便,沒有實際應用價值,放射性藥物99mTc-DTPA也具有類似特性,同時它在腎臟內的濾過、積聚能夠被SPECT等測量裝置在體外探測到,因此被用來測量GFR(Gates法)。
大多數CT對比劑如碘普羅胺,碘海醇,等等都俱有類似菊粉的特性,即自由濾過、不會被重吸收和分泌,最終隨尿液排出,因此也是良好的GFR測量標記物。并且CT掃描所測得的CT值和組織內的藥物(碘)濃度呈線性關系,因此注射對比劑的CT掃描(俗稱增強CT)在觀察病變形態的同時也可以用來測量GFR,即用來評價腎臟的濾過功能。
然而,已有文獻報導的Patlak模式CT測量腎小球濾過率(腎功能)因為種種局限并不能應用于臨床。
技術實現要素:
有鑒于此,本發明的目的在于提供一種方便、快捷地檢測腎臟濾過功能的CT測量方法。
為達到上述目的,本發明采用下述技術方案:
經注入對比劑后的某個時間t1進行CT掃描并測量腎臟內對比劑的聚積量,以此聚積量除以總的對比劑的注入量得到腎臟的聚積分數(fractional renal accumulation,FRA),該FRA可以做為評估腎功能GFR高低的指標;更進一步可以建立簡便的數學公式利用FRA來計算GFR。
上述檢測腎臟濾過功能的CT測量方法具體包括如下步驟:
將開始注射對比劑作為計時零點,經過規定時間的時刻t1,對腎臟進行CT掃描得到t1時刻腎臟的增強CT數據,該數據包括構成腎臟三維圖像的所有體素,從中可以得到每個體素的CT值,即代表對比劑濃度,以及所有體素體積之和,即代表腎臟的體積(V);
根據所述腎臟的增強CT數據和腎臟的體積(V)獲得t1時刻腎臟的對比劑聚積量(Q);
將所述t1時刻腎臟內對比劑的聚積量(Q)除以總的對比劑注入量,得到腎臟的聚積分數(FRA);
所述腎臟的聚積分數(FRA)可以直接作為評估腎臟濾過功能高低的指針。
進一步地,所述方法還包括基于腎臟的聚積分數(FRA)建立線性回歸模型來計算腎小球濾過率(GFR)。
優選地,根據申請人的大量前期研究,基于腎臟的聚積分數建立線性回歸模型來計算腎小球濾過率GFR的模型如式1所示:
GFR=1416.42×FRA+2.58……(式1)。
優選地,所述時刻t1的取值范圍為注射對比劑后2-3分鐘。
更優選地,所述時刻t1的取值范圍為注射對比劑后2.5分鐘。
時刻t1的取值范圍選取原則是CT掃描采集數據時對比劑在腎內的聚積數量較大且流出輸尿管和膀胱的量較小,此時進行CT掃描采集數據最準確。
優選地,在注射對比劑之前,還包括對腎臟進行CT平掃的步驟,以獲得腎臟的平掃CT數據,該數據包括構成腎臟三維圖像的所有體素,從中可以得到每個體素的CT值,即對比劑濃度為零時的CT值的本底。
所述t1時刻腎臟的對比劑聚積量(Q)是通過所述t1時刻腎臟的增強CT數據中所有體素的平均CT值(HU1)減去所述平掃CT數據中所有體素的平均CT值(HU0),再乘以腎臟的體積(V)得到的,
或者是通過所述t1時刻腎臟的增強CT數據中每個體素的CT值(HUi)和其體積(Vvoxel)的乘積之和,減去所述平掃CT數據中每個體素的CT值(HUk)和其體積(Vvoxel)的乘積之和得到。
需要說明的是,CT測量數據中有關體素的CT值和體積的統計或計算都是第三方軟件完成的,或CT機上的后處理軟件完成的,可以由商業軟件或CT機生產商配套軟件完成。
優選地,當所述CT掃描為雙能CT掃描或能譜CT掃描時,所述t1時刻腎臟的對比劑聚積量(Q)有另外一種計算方法,是通過雙能減影或能譜減影得到的,具體為:
雙能CT掃描或能譜CT掃描時,不需要在注入對比劑前對腎臟進行平掃,直接由t1時刻的雙能減影或能譜減影得到腎臟內每個體素CT值的增加量(HUy),乘以各體素的體積(Vvoxel)并求和得到腎臟的對比劑聚積量(Q),
或者由每個體素CT值的增加量(HUy)得到腎臟內所有體素CT值的平均增加量(HUm),再乘以腎臟的體積(V)得到腎臟的對比劑聚積量(Q)。
優選地,所述總的對比劑注入量是通過對比劑的體積乘以對比劑濃度再乘以對比劑和CT值的轉換系數(k)得到的。
優選地,測量方法所使用的對比劑為碘對比劑。
碘濃度和CT值的轉換系數k(單位:HU*ml/mgI),(mgI為毫克碘),和CT掃描的球管電壓值kV有關,球管電壓值越高,該轉換系數的值越小,當球管電壓為某一固定值時,該轉換系數相對恒定,可以通過CT體模掃描來測定。
對于確定的管電壓和CT掃描儀,該轉換系數較穩定,即:
當CT掃描的球管電壓為120KV時,碘對比劑和CT值的轉換系數為25,單位為HU*ml/mgI,即1mgI相當于25HU*ml;可以理解為1豪克碘可以使1豪升組織的CT值提升25HU。
當CT掃描的球管電壓為100KV時,碘對比劑和CT值的轉換系數為30,單位為HU*ml/mgI,即1mgI相當于30HU*ml;可以理解為1豪克碘可以使1豪升組織的CT值提升30HU。
另一方面,所述總的對比劑注入量也可以由對比劑的體積和對比劑濃度的乘積來表示,計算聚積分數(FRA)時為了統一量綱,所述腎臟的對比劑聚積量(Q)應當除以轉換系數(k)。
此時所述總的碘對比劑注入量的量綱為mgI(豪克碘),上述對比劑聚積量(Q)的量綱(HU*ml)應當通過除以轉換系數k(k的量綱為HU*ml/mgI)換算為mgI(豪克碘)
優選地,對比劑注射所用時間應當控制在一個合理的范圍,對比劑注射應當在20秒內完成,更優選地,在15秒內完成對比劑注射。
進一步地,為了避免不同個體間從開始注射對比劑到對比劑出現在主動脈內的時間差別對測量結果的影響,對所述時間t1的計時零點做如下進一步的規定:
在注射對比劑后,將主動脈內開始出現對比劑作為計時零點,經過時間t1對腎臟進行CT掃描,得到t1時刻腎臟的增強CT數據,其余的計算腎臟的聚積分數(FRA)的測量方法及步驟與將開始注射對比劑作為計時零點的測量方法及步驟相同。
這樣做不僅可以避免不同個體間從開始注射對比劑到對比劑出現在主動脈內的時間差別對測量結果的影響,并且會增強結果的穩定性和可靠性。但是在注入對比劑后需要進行CT單層動態掃描以追蹤主動脈內CT值的變化,確定對比劑出現的時刻,在一定程度上增加了本技術的復雜性。
由于本發明采用影像學的CT掃描測量方法,能夠得到每側腎的CT掃描數據,因此可以用來計算出單側腎的FRA,進而用來評估單側的腎功能GFR高低。
根據本發明,提出一種新的檢測腎臟濾過功能的CT測量方法,利用常規CT增強掃描的數據資料評估腎臟功能。該方法簡單直觀,在行常規CT診斷的同時能夠量化評估腎臟功能,并且不會額外增加患者的x線輻射量,具有較高的臨床應用價值。
附圖說明
圖1是基于本發明的檢測腎臟濾過功能的CT測量方法的腎臟CT平掃期的圖像。
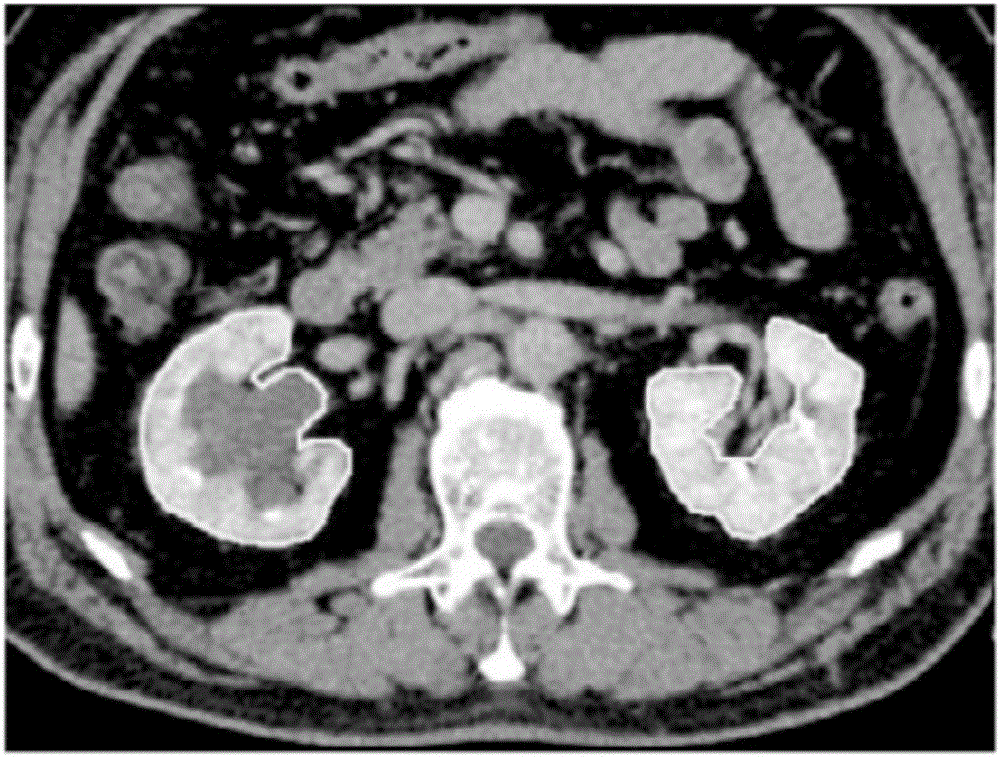
圖2是基于本發明的檢測腎臟濾過功能的CT測量方法t1時刻腎臟增強CT掃描的圖像。
圖3是基于本發明的檢測腎臟濾過功能的CT測量方法t1時刻增強CT掃描雙腎三維重建圖像,顯示雙腎體積和各自平均CT值。
圖4是基于體模研究實驗得出的碘對比劑濃度與CT值間的線性關系圖,CT掃描管電壓為100kV,兩者的線性關系為y=30.01x+45.14,據此可以得到對比劑碘濃度與CT值之間的轉換系數k=30(HU*ml/mgI)。
圖5是基于FRA和單腎Gates-GFR間的線性相關/回歸曲線分析圖。
圖6是基于單腎CT-GFR與單腎Gates-GFR間的相關性分析。
圖7是本發明方法所測得的腎功能(CT-GFR)和同位素腎圖測得的腎功能(Gates-GFR)之間結果一致性分析圖(Bland-Altman圖),從圖中可以得出,兩者一致性很高,測量誤差小。
具體實施方式
【實施方式】
在本發明的檢測腎臟濾過功能的CT測量方法的實施方式中,在注射對比劑之前,對受驗者腎臟做CT平掃,然后在注射對比劑之后的排泄期(2.5分鐘),再次進行CT掃描,本申請中稱為t1時刻腎臟增強CT掃描。通過比較t1時刻腎臟CT值增加量和碘對比劑總的注入量來計算腎小球濾過率GFR。
本實施方式的CT掃描為常規CT掃描,包含平掃和增強。
下面參照圖1、2、3,對本發明的第一實施方式進行詳細說明。
對受檢者實施的具體實施步驟按如下順序進行。
(平掃)
在對受檢者實施靜脈注射對比劑之前,先利用CT掃描儀對腎臟(組織)進行平掃,并獲得平掃期CT數據。
圖1示出了腎臟CT平掃的圖像,圖中的輪廓線為腎臟的邊緣。
(注射對比劑)
在獲得腎臟平掃期CT值后,對受檢者靜脈注射對比劑,這里使用的對比劑為碘對比劑。
(增強掃描)
靜脈內注入碘對比劑,動脈期過后隨著碘劑濾過并在腎小管、集合管內積聚,腎髓質呈漸進性增強,至排泄期早期(注藥后2-3分鐘)表現為腎髓質CT值明顯高于皮質,部分腎盞和腎盂內也充盈著高濃度的碘劑,這時腎臟的CT增強主要由腎小球的濾過導致。
注藥后約2-3分鐘,經腎小球濾出的碘劑在腎髓質和腎盂內積聚,尚未明顯排入輸尿管,這就提供了一個合適的CT掃描時間窗用來測量碘劑的濾過數量,該數量可以由此時的CT強化值(相對于平掃的CT值的增加量)和腎體積(含腎盂)的乘積來描述。
為此,在從開始注射對比劑經過規定時間的t1時刻,本實施選擇注射對比劑后2.5分鐘,對腎臟進行增強CT掃描,獲得增強CT數據和腎臟的體積V。這里CT掃描模式可以為容積或螺旋式掃描方式,范圍致少覆蓋雙腎。
參照圖2,在進行t1時刻增強CT掃描時,經腎小球濾過的對比劑絕大部分局限于腎臟及腎盂內。
在第一實施方式中,增強CT掃描和平掃CT所采用管電壓需相同,范圍均需覆蓋兩側腎臟,可以設置固定管電流掃描,也可以采用管電流調制(tube current modulation)。
(計算腎臟內對比劑的聚積量)
根據所述單側腎臟的CT數據和單側腎臟的體積V獲得t1時刻單側腎臟的對比劑聚積量Q。
在本實施例中,所述t1時刻單側腎臟的對比劑聚積量Q是通過所述t1時刻單側腎臟的CT數據中所有體素的平均CT值HU1減去所述平掃CT數據中單側腎臟所有體素的平均CT值HU0,再乘以單側腎臟的體積V得到的。
或者還可以選擇通過所述t1時刻腎臟的增強CT數據中每個體素的CT值(HUi)和其體積(Vvoxel)的乘積之和,減去所述平掃CT數據中每個體素的CT值(HUk)和其體積(Vvoxel)的乘積之和得到。
(計算腎臟內對比劑的聚積分數)
將所述腎臟內對比劑的聚積量Q除以總的對比劑注入量(I),得到腎臟的聚積分數FRA。
所述總的對比劑注入量是通過對比劑的體積乘以對比劑碘濃度再乘以對比劑和CT數據的轉換系數k得到的。
本實施例中,如圖4所示,為體模研究實驗得到的碘對比劑濃度與CT掃描值間的線性關系圖。從圖中可以看出:當確定CT掃描的球管電壓為100KV時,碘對比劑和CT值的轉換系數k為30HU*ml/mgI。
(計算每側腎臟的腎小球濾過率GFR)
如圖5所示,基于腎臟的聚積分數建立線性回歸模型來計算腎小球濾過率(GFR)的模型如式1所示:
GFR=1416.42×FRA+2.58……(式1)。
本實施中所采集的CT數據來自一位患有右腎腎盂積水的病人,圖3是基于本發明的檢測腎臟濾過功能的CT測量方法t1時刻增強CT掃描該病人的雙腎三維重建圖像,具體的數據和計算過程如下:
碘對比劑注入體積=64mL
碘對比劑濃度=370mgI/mL
球管電壓=100kV
碘對比劑和CT值的轉換系數=30.00(HU*ml/mgI)
左腎
體積=179.7ml
HU0=40.3Hu
HU1=189.8Hu
右腎
體積=144.3ml
HU0=32.5Hu
HU1=111.8Hu
FRA的計算過程如下:
FRA(左)=(體積×HU1–體積×HU0)/(碘對比注入體積×碘對比劑濃度×碘對比劑和CT值的轉換系數)
=(179.7×189.8–179.7×40.3)/(64×370×30.00)
=0.0378
FRA(右)=(體積×HU1–體積×HU0)/(碘對比注入體積×碘對比劑濃度×碘對比劑和CT值的轉換系數)
=(144.3×111.8–144.3×32.5)/(64×370×30.00)
=0.0161
GFR的計算公式為:CT-GFR=1416.42×FRA+2.58
左腎GFR的計算過程如下:
CT-GFR(左)=1416.42×FRA(左)+2.58
=1416.42×0.0378+2.58
=56.12(ml/min)
右腎GFR的計算過程如下:CT-GFR(右)=1416.42×FRA(右)+2.58
=1416.42×0.0161+2.58
=25.38(ml/min)
【對比實施方式】
以放射性同位素藥物99mTc-DTPA作為對比劑,以SPECT進行腎臟動態掃描,用Gates法來計算腎功能(Gates-GFR)。具體的操作過程參見文章Determination of Glomerular Filtration Rate with CT Measurement of Renal Clearance of Iodinated Contrast Material versus 99mTc-DTPA Dynamic Imaging"Gates"Method:A Validation Study in Asymmetrical Renal Disease.Radiology 2016Aug 24:160425.Yuan X,Zhang J,Tang K等著。
【第一實施方式與對比實施方式的實驗結果分析】
下面參照圖6-7比較本發明的檢測腎臟(濾過)功能的CT測量方法(CT-GFR)與臨床常規使用的同位素腎圖Gates法(Gates-GFR)以驗證CT-GFR的準確性。
圖6是基于單腎CT-GFR與單腎Gates-GFR間的相關性分析。該散點圖證實兩者之間具有高度的相關性(r=0.924,p<0.001)。
從圖6的分析結果中可以得出:CT-GFR的結果和Gates-GFR高度相關。
圖7是CT-GFR和Gates-GFR結果一致性分析圖(Bland-Altman圖)。橫坐標表示兩種測量結果的均數,縱坐標表示兩種測量結果的差值,該圖顯示兩種測量結果的差值被控制在合理的范圍內(分布在兩條橫向虛線之間)。
從圖7的分析結果中可以得出:CT-GFR和Gates-GFR測理偏差小,一致性高。
本發明通過提出一種新的檢測腎臟濾過功能的CT測量方法,利用常規CT增強掃描的數據資料評估腎臟功能。該方法可以得到碘對比劑在腎臟的聚積分數FRA,該FRA可以直接作為評估腎臟濾過功能GFR高低的指針,或者在FRA的基礎上建立線性回歸模型來計算腎小球濾過率GFR。該方法簡單直觀,在行常規CT診斷的同時能夠量化評估腎臟功能,并且不會額外增加患者的x線輻射量,在臨床上有非常重要的價值。
- 還沒有人留言評論。精彩留言會獲得點贊!