一種具有雙靶區(qū)同時遞藥效果的復合磷脂熱敏脂質體及其制備方法和應用與流程
本發(fā)明屬于藥學領域,涉及靶向制劑及其制備方法和應用,具體為一種具有雙靶區(qū)同時遞藥效果的復合磷脂熱敏脂質體及其制備方法和應用。
背景技術:
中藥成分一般具有多效性,在于“多靶點協(xié)同起效”,這些靶點往往位于不同靶區(qū),并且不同靶區(qū)之間對藥量的要求往往不同,因此需要多靶區(qū)同時遞藥,并且在不同靶區(qū)之間能夠實現(xiàn)遞藥比例的調節(jié)。
脂質體和包合物都屬于制劑新技術的范疇,能夠提高遞藥的效果。近年來,環(huán)糊精主動靶向修飾技術發(fā)展很快,通過在環(huán)糊精表面連接如葉酸等配體,可以實現(xiàn)將載藥環(huán)糊精包合物主動靶向遞藥入胞(主要是腫瘤細胞)。但是,由于僅通過物理作用包合,載藥環(huán)糊精包合物給藥后在血液循環(huán)中很容易泄漏藥物,并且環(huán)糊精還有一定的腎靶向性,因此嚴重限制了靶向效果。
包合物脂質體,即先將藥物載入環(huán)糊精中制成包合物,再載入脂質體中制成包合物脂質體。與包合物相比,包合物脂質體的靶向性和穩(wěn)定性更好;與脂質體相比,包合物脂質體中的載藥包合物位于內水相,藥物更加穩(wěn)定,并且環(huán)糊精本身也是良好的凍干保護劑。因此,包合物脂質體是一種更加高效的載體,并且能夠應用脂質雙分子層和內水相“雙重載藥”,但是并不能實現(xiàn)多靶區(qū)同時遞藥。
因此,亟需開發(fā)新的靶向制劑,以改善多靶區(qū)同時遞藥的效果,同時改善載體的載藥效果和穩(wěn)定性。
技術實現(xiàn)要素:
針對現(xiàn)有技術中存在的技術問題,本發(fā)明提供一種復合磷脂熱敏脂質體,所述復合磷脂熱敏脂質體包括內水相和脂質雙分子層,以及脂質體內水相中的主動靶向的載藥葉酸修飾環(huán)糊精包合物,和脂質雙分子層中的游離藥物。
根據(jù)本發(fā)明,所述磷脂熱敏脂質體可以為磷脂類如二棕櫚酰磷脂酰膽堿(dppc)、氫化大豆磷脂、隱形材料dspe-peg2000(二硬脂酰基磷脂酰乙醇胺-聚乙二醇)、單鏈磷脂mspc或膽固醇中的一種或多種。
根據(jù)本發(fā)明,所述載藥葉酸修飾環(huán)糊精包合物可以為將親脂性藥物或其混合物載入葉酸修飾環(huán)糊精構成載藥葉酸修飾環(huán)糊精包合物。
優(yōu)選地,所述親脂性藥物優(yōu)選為油水分配系數(shù)大于10的親脂性藥物,例如為莪術油、莪術醇、吉馬酮、β-欖香烯、莪術二酮、姜黃素、去甲氧基姜黃素中的一種或多種。
根據(jù)本發(fā)明,所述游離藥物可以為未經環(huán)糊精包合的藥物,例如上述親脂性藥物。
作為本發(fā)明的一個實例,將莪術油、莪術醇、吉馬酮、β-欖香烯或莪術二酮載入葉酸修飾環(huán)糊精包合物后將包封莪術油、莪術醇、吉馬酮、β-欖香烯或莪術二酮的葉酸修飾環(huán)糊精包合物和游離藥物分別載入磷脂熱敏脂質體的內水相和脂質雙分子層。
根據(jù)本發(fā)明,所述復合磷脂熱敏脂質體可以根據(jù)給藥需求調節(jié)載藥葉酸修飾環(huán)糊精包合物和游離藥物的比例,優(yōu)選地,所述游離藥物與載藥葉酸修飾環(huán)糊精包合物的摩爾比為0.1~5:1。
本發(fā)明還提供如上所述復合磷脂熱敏脂質體的制備方法,包括如下步驟:
1)將葉酸溶于二甲基亞砜中,加入催化劑反應,再加入濃度為0.1~0.5g/ml的氨基-β-環(huán)糊精吡啶溶液,繼續(xù)攪拌,反應得固體。將上述固體溶解于水中,靜置、過濾、濃縮、沉淀,沉淀經洗滌后干燥,即得葉酸修飾環(huán)糊精;
2)取親脂性藥物與步驟1)所得葉酸修飾環(huán)糊精制備載藥葉酸修飾環(huán)糊精包合物;
3)采用膜材將步驟2)所得載藥葉酸修飾環(huán)糊精包合物及游離藥物載入脂質體。
優(yōu)選地,步驟1)中,所述氨基-β-環(huán)糊精與葉酸的摩爾比可以為(1-5):1。所述催化劑可以為n-羥基琥珀酰亞胺和n,n-二環(huán)已基碳二亞胺中的一種或多種,其與氨基-β-環(huán)糊精的摩爾比為2.4:(1-5),例如使用摩爾比為1.2:1.2:(1-5)的n-羥基琥珀酰亞胺、n,n-二環(huán)已基碳二亞胺與氨基-β-環(huán)糊精。
根據(jù)本發(fā)明,所述氨基-β-環(huán)糊精、葉酸與催化劑的反應優(yōu)選在惰性氣體中不高于50℃的溫度下反應1-48小時,例如將葉酸與催化劑在氮氣下室溫反應3小時,加入氨基-β-環(huán)糊精后攪拌48小時,控溫至45℃繼續(xù)反應2小時。
所述沉淀可以為將濃縮后的濃縮液加入葉酸修飾環(huán)糊精的不良溶劑如丙酮中,例如逐滴加入丙酮中。
根據(jù)本發(fā)明,步驟2)中,
所述親脂性藥物與葉酸修飾環(huán)糊精的摩爾比為0.2~5:1。
優(yōu)選通過飽和水溶液法或研磨法制備載藥葉酸修飾環(huán)糊精包合物。
根據(jù)本發(fā)明,步驟3)中,
所述磷脂熱敏脂質體具有如上所述的定義,例如使用重量比為8:1~3:0.5~2:0.2~1的二棕櫚酰磷脂酰膽堿:氫化大豆磷脂:隱形材料dspe-peg2000(二硬脂酰基磷脂酰乙醇胺-聚乙二醇):單鏈磷脂mspc作為膜材,如使用摩爾比為67.6:18.4:4:10的二棕櫚酰磷脂酰膽堿(dppc)、氫化大豆磷脂(hspc)、隱形材料dspe-peg2000和單鏈磷脂mspc。
所述載藥葉酸修飾環(huán)糊精包合物與游離藥物的摩爾比可以為1:0.1~5。
本發(fā)明還提供如上所述復合磷脂熱敏脂質體的用途,其用于制備抗腫瘤藥物,例如用于制備具有雙靶區(qū)同時遞藥效果的抗腫瘤藥物。
有益效果
與現(xiàn)有技術相比,本發(fā)明所制備的同時包封有游離藥物與葉酸修飾載藥環(huán)糊精包合物的復合磷脂熱敏脂質體可以實現(xiàn)同時作用于腫瘤細胞與腫瘤間質,抗腫瘤效果得到增強。同時,現(xiàn)有技術中脂溶性藥物只能包封于脂質體的脂質雙分子層中,而本發(fā)明提供的復合磷脂熱敏脂質體中可以同時以游離藥物形式包封于脂質雙分子層和以環(huán)糊精包合物形式包封于內水相,因此載體的載藥效果和穩(wěn)定性也有顯著提升。本發(fā)明所述復合磷脂熱敏脂質體給藥后,在靶部位釋放出游離藥物和主動靶向環(huán)糊精包合物。游離藥物主要作用于腫瘤間質,主動靶向環(huán)糊精包合物通過葉酸受體介導進入腫瘤細胞,實現(xiàn)腫瘤間質和腫瘤細胞雙靶區(qū)同時遞藥。并且可以靈活調節(jié)兩者的比例以獲得最佳治療效果。
附圖說明
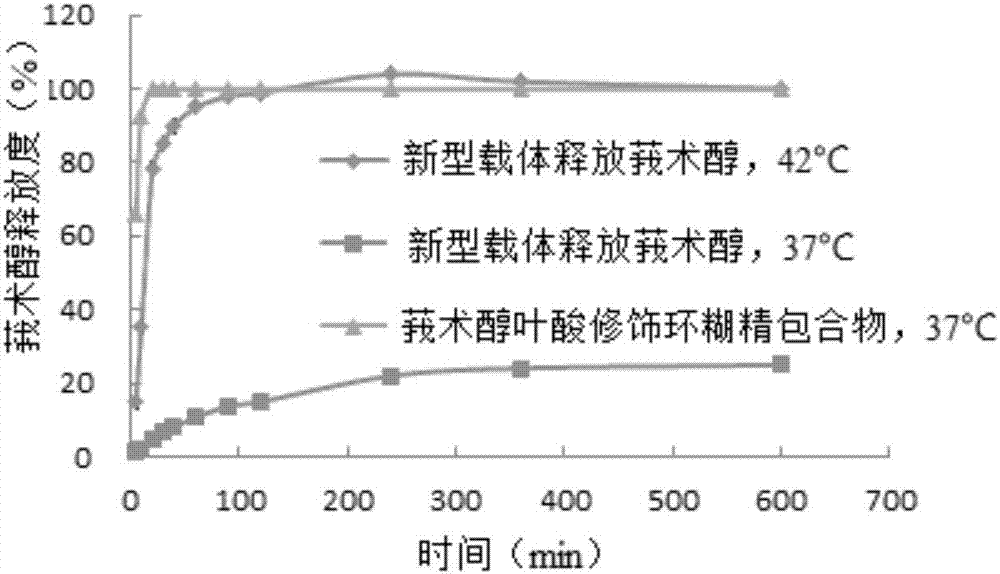
圖1為實施例6包封莪術醇復合磷脂熱敏脂質體在不同溫度下的釋放度比較(n=3)。
圖2為實施例7包封莪術油復合磷脂熱敏脂質體的體外抗腫瘤效果(n=5)。
具體實施方式
下文將結合具體實施例對本發(fā)明的化合物及其制備方法和應用做更進一步的詳細說明。下列實施例僅為示例性地說明和解釋本發(fā)明,而不應被解釋為對本發(fā)明保護范圍的限制。凡基于本發(fā)明上述內容所實現(xiàn)的技術均涵蓋在本發(fā)明旨在保護的范圍內。
除非另有說明,實施例中使用的原料和試劑均為市售商品,或者可以通過已知方法制備。
實施例1具有雙靶區(qū)同時遞藥效果的復合磷脂熱敏脂質體的制備
1)取葉酸1份,溶于二甲基亞砜中,加入n-羥基琥珀酰亞胺(nhs)1.2份和n,n-二環(huán)已基碳二亞胺(dcc)1.2份,在氮氣保護下避光磁力攪拌反應3h,加入溶解在8ml吡啶中的氨基-β-環(huán)糊精1份,繼續(xù)攪拌48h,45℃繼續(xù)攪拌2h。減壓蒸去大部分溶劑,得到的固體溶解于300ml蒸餾水中,4℃靜置12小時,過濾,濾液減壓蒸至15ml后,逐滴加到300ml丙酮中,攪拌2h后取沉淀,丙酮洗滌后真空干燥過夜,即得葉酸修飾環(huán)糊精。
2)取莪術醇按1:1摩爾比與葉酸修飾環(huán)糊精采用飽和水溶液法制備載藥主動靶向包合物。將葉酸修飾環(huán)糊精溶解于水中制成飽和溶液,將莪術醇溶解在無水乙醇中,逐滴加入葉酸修飾環(huán)糊精飽和水溶液中,50℃攪拌揮去乙醇,靜置至室溫,過0.45μm濾膜,濾液冷凍干燥,即得載有莪術醇的葉酸修飾環(huán)糊精包合物。
3)取二棕櫚酰磷脂酰膽堿(dppc):氫化大豆磷脂(hspc):隱形材料dspe-peg2000:單鏈磷脂mspc(摩爾比為67.6:18.4:4:10)作為膜材,將莪術醇和上述脂質一起溶解在無水乙醇中,將載有莪術醇的葉酸修飾環(huán)糊精包合物溶解在水相中,在磁力攪拌情況下將乙醇相注入水相,60℃攪拌1h揮去乙醇,超聲減小粒徑,即得同時包封莪術醇葉酸修飾環(huán)糊精包合物和游離莪術醇的復合磷脂熱敏脂質體。其中游離莪術醇與葉酸修飾環(huán)糊精包合物中的莪術醇比例為1:1。
實施例2具有雙靶區(qū)同時遞藥效果的復合磷脂熱敏脂質體的制備
參考實施例1的制備步驟,與實施例1不同的是,葉酸與氨基β-環(huán)糊精合成時的比例是1:2;載入的藥物為莪術油;莪術油與葉酸修飾環(huán)糊精制備包合物時的比例為5:1;脂質體中游離莪術油與葉酸修飾環(huán)糊精包合物中的莪術油的比例為1:2。
實施例3具有雙靶區(qū)同時遞藥效果的復合磷脂熱敏脂質體的制備
參考實施例1的制備步驟,與實施例1不同的是,葉酸與氨基β-環(huán)糊精合成時的比例是0.2:1;載入的藥物為β-欖香烯;β-欖香烯與葉酸修飾環(huán)糊精制備包合物時的比例為2:1;脂質體中游離β-欖香烯與葉酸修飾環(huán)糊精包合物中的β-欖香烯的比例為1:5。
實施例4具有雙靶區(qū)同時遞藥效果的復合磷脂熱敏脂質體的制備
參考實施例1的制備步驟,與實施例1不同的是,葉酸與氨基β-環(huán)糊精合成時的比例是1:5;載入的藥物為吉馬酮;吉馬酮與葉酸修飾環(huán)糊精制備包合物時的比例為1:5;脂質體中游離吉馬酮與葉酸修飾環(huán)糊精包合物中的吉馬酮的比例為2:1。
實施例5具有雙靶區(qū)同時遞藥效果的復合磷脂熱敏脂質體的制備
參考實施例1的制備步驟,與實施例1不同的是,葉酸與氨基β-環(huán)糊精合成時的比例是1:1;載入的藥物為莪術二酮;莪術二酮與葉酸修飾環(huán)糊精制備包合物時的比例為0.5:1;脂質體中游離莪術二酮與葉酸修飾環(huán)糊精包合物中的莪術二酮的比例為1:3。
實施例6包封莪術醇復合磷脂熱敏脂質體的溫敏釋放度研究
將實施例1制備得到的包封莪術醇葉酸修飾環(huán)糊精包合物和游離莪術醇的復合磷脂熱敏脂質體進行溫敏釋放度研究。釋放介質為ph7.4等滲磷酸鹽緩沖液(處方中含137mmol/lnacl、3mmol/lkcl、8mmol/lnahpo4、1mmol/lkh2po4)。將包封莪術醇復合磷脂熱敏脂質體加入100ml釋放介質中,于不同溫度恒溫磁力攪拌,于不同時間點取樣用截留分子量為100k的超濾管超濾,取超濾液采用hplc測定其中莪術醇濃度,計算釋放度,如圖1所示,可見莪術醇葉酸修飾環(huán)糊精包合物能夠迅速通過超濾膜,而復合磷脂熱敏脂質體在42℃條件下快速完全釋放,在體溫37℃下釋放比較緩慢,說明復合磷脂熱敏脂質體具有較好的溫敏釋放性能。
實施例7包封莪術油復合磷脂熱敏脂質體的細胞毒性研究
將實施例2制備得到的包封莪術油復合磷脂熱敏脂質體進行細胞毒性研究。采用葉酸受體高表達的人宮頸癌細胞hela細胞作為試驗對象,加入不同濃度的莪術油和包封莪術油復合磷脂熱敏脂質體,42℃加熱1h,然后孵育24h,采用mtt法測定腫瘤細胞活力,計算抑制率,結果如圖2所示,可見包封莪術油復合磷脂熱敏脂質體的體外抗腫瘤細胞遠高于游離莪術油。
實施例8包封β-欖香烯復合磷脂熱敏脂質體的抗腫瘤作用研究
將本發(fā)明實施例2制備得到的包封β-欖香烯復合磷脂熱敏脂質體與β-欖香烯進行抗腫瘤作用研究。采用葉酸受體高表達的人宮頸癌細胞hela細胞,裸鼠腋下接種,待腫瘤大小超過150mm3后開始給藥,每天靜脈給藥一次,劑量為100mg/kg,連續(xù)給藥5d,給藥后腫瘤部位42℃加熱1h,給藥后第7d處死動物,取腫瘤部位稱重,并計算抑制率,結果β-欖香烯和包封β-欖香烯復合磷脂熱敏脂質體的抑制率分別為34.66%和67.96%,可見采用包封β-欖香烯復合磷脂熱敏脂質體的抗腫瘤效果提升了近一倍。
以上,對本發(fā)明的實施方式進行了說明。但是,本發(fā)明不限定于上述實施方式。凡在本發(fā)明的精神和原則之內,所做的任何修改、等同替換、改進等,均應包含在本發(fā)明的保護范圍之內。
- 還沒有人留言評論。精彩留言會獲得點贊!