一種黑磷?金屬納米復合材料及其合成方法和應用與流程
本發明屬于黑磷技術領域,具體涉及一種黑磷-金屬納米復合材料及其合成方法和應用。
背景技術:
黑磷(BP,Black Phosphorus)二維納米材料是近一兩年發現的新型片狀材料。作為二維材料家族的新成員,BP具有直接、可調的帶隙,有望成為可取代石墨烯的下一代二維納米材料,運用在光電子學、納米電子學、光催化、生物傳感器、可循環電池及生物成像等眾多領域中。比如:Woomer等測量出了雙層BP片的帶隙可達1.88±0.24eV,遠高于其他二維材料,可作為一種理想的光電子材料(ACS Nano,2015,9,8869);在生物醫學領域,BP被發現具有很好的光致發光性質、近紅外光熱吸收特性和光動力治療潛質,有望成為良好的納米試劑用于腫瘤的治療(Small 2016,12,214;J.Am.Chem.Soc.2015,137,11376;Angew.Chem.Int.Ed.2015,54,11526)。
BP納米片的制備也很方便,與石墨烯一樣,是目前僅有的兩種可通過機械剝離而穩定存在的二維材料之一。目前常用的方法是采用超聲輔助液相剝離法從黑磷晶體中分離出單層和少數幾層的BP納米片(ACS Nano 2014,8,4033)。BP也適合與金屬(金屬氧化物)復合,構建出BP-金屬納米復合物。Lee等合成了穩定的BP和二氧化鈦(BP-TiO2)納米復合材料,表現出了很好的在UV-Vis區域的光催化活性和廣譜抗菌活性,成功實現了對染料的高效光催化降解和對革蘭氏陽性和陰性細菌的殺傷;并且與其單一組分(BP或TiO2)相比,BP-TiO2的這種光催化能力和抗菌活性要高出很多(Sci Rep2015,5,8691)。這一結果表明,在復合結構中金屬組分能夠顯著地增強BP納米片的物理化學特性,表現出更強的應用潛能。
現有的關于黑磷的專利主要是針對單層或少數幾層黑磷納米片或黑磷量子點的制備方法,如CN201510553085.0、CN201510968976.2、CN201510379948.7、CN201610063652.9、等等,所涉及的技術均是在液相機械剝離的方法上進行的改良。
技術實現要素:
本發明的第一個目的在于提供一種黑磷-金屬納米復合材料的合成方法,該合成方法首次發現黑磷(BP)納米片具有很好的化學還原性,在此基礎上,利用BP本身的還原性將吸附在BP表面的金屬離子還原成元素金屬,生成黑磷-金屬(BP-Metal)納米復合物,該方法簡潔,無需額外的還原劑可獲得黑磷-金屬納米復合材料即BP-Metal納米復合材料。
本發明的第二個目的在于提供利用上述黑磷-金屬納米復合材料的合成方法獲得的黑磷-金屬納米復合材料。
本發明的第三個目的在于提供上述黑磷-金屬納米復合材料作為活性基底在表面增強拉曼散射SERS中的應用。
本發明的第一個目的是通過如下技術方案來實現的:一種黑磷-金屬納米復合材料的合成方法,包括以下步驟:
(1)取黑磷BP晶體分散于N-甲基吡咯烷酮NMP中,將分散有黑磷BP晶體的N-甲基吡咯烷酮NMP溶液進行破碎處理,得破碎液;
(2)將破碎液進行超聲處理,離心,取沉淀,將沉淀重懸于N-甲基吡咯烷酮NMP中,再次離心,收集上清,得黑磷BP納米片懸液;
(3)將黑磷BP納米片懸液加入煮沸的水中,接著加入氯金酸HAuCl4或硝酸銀AgNO3溶液繼續沸騰反應,反應結束后冷卻,離心,收集沉淀,得黑磷-金屬納米復合材料。
在上述黑磷-金屬納米復合材料的合成方法中:
步驟(1)中將分散有黑磷BP晶體的N-甲基吡咯烷酮NMP溶液優選置于超聲波細胞破碎儀中進行破碎處理,所述超聲波細胞破碎儀的功率優選調整為500~600W,破碎處理時間優選為5~6h。
步驟(2)中將破碎液優選移入超聲波清洗機中繼續超聲,所述超聲波清洗機的功率優選調整為150~200W,超聲時間為10~12h。
步驟(1)中破碎處理和步驟(2)中超聲處理時溫度優選保持在20℃以下。
步驟(2)中離心時離心機轉速優選為7000~8000rpm,離心時間優選為15~20min,再次離心時轉速優選為1500~2000rpm,再次離心時間優選為10~15min。
步驟(3)中所述黑磷BP納米片懸液的濃度優選為4~5mg/mL,所述水優選為超純水,所述黑磷BP納米片懸液與所述超純水的體積比優選為0.05~0.1:20。
步驟(3)中所述黑磷BP納米片懸液的濃度優選為4~5mg/mL,所述氯金酸HAuCl4溶液或硝酸銀AgNO3溶液的濃度優選為5~10mmol·L,所述黑磷BP納米片懸液與所述氯金酸HAuCl4溶液或硝酸銀AgNO3溶液的體積比優選為1~2:1~4。
步驟(3)中加入氯金酸HAuCl4溶液或硝酸銀AgNO3溶液繼續沸騰反應優選1~10min,離心時離心機轉速優選為5000~6000rpm,離心時間優選為10~15min。
本發明的第二個技術目的是通過以下技術方案來實現的:采用上述的黑磷-金屬納米復合材料的合成方法獲得的黑磷-金屬納米復合材料。
本發明的第三個技術目的是通過以下技術方案來實現的:上述的黑磷-金屬納米復合材料在光熱效應方面的應用以及作為活性基底在表面增強拉曼散射SERS中的應用。
與現有技術相比,本發明具有如下優點:
(1)采用本發明方法第一次制備成功BP-Metal納米復合物;
(2)本發明方法無需額外的還原劑,利用BP本身的還原性即可實現BP-Metal復合材料的裝配,簡便、易操作;
(3)除了BP-Au的還原合成,其他可通過還原法制備的金屬納米粒子亦適用于該法制備得到BP-Metal復合材料(如:BP-Ag納米復合物);
(4)本發明方法制成的黑磷-金屬納米復合材料可以在光熱效應方面的應用以及作為活性基底在表面增強拉曼散射SERS中的應用。
附圖說明
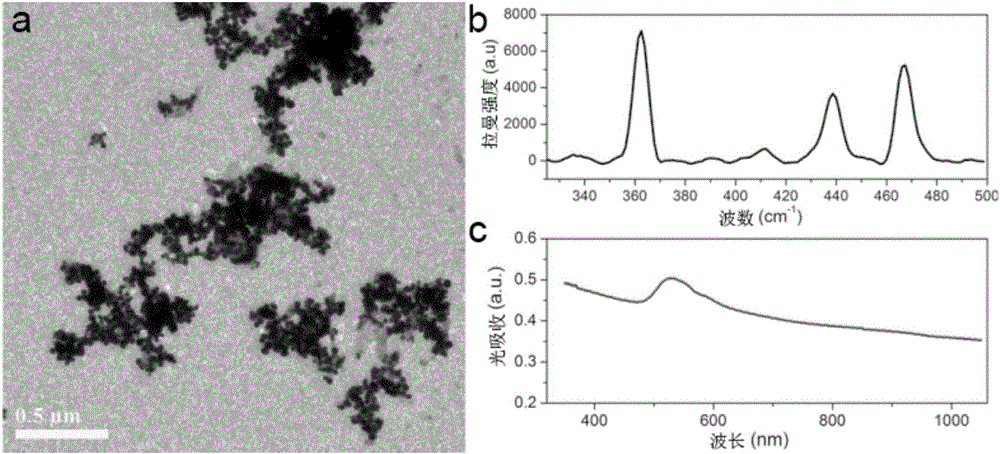
圖1是實施例1中BP-Au納米復合物的投射電鏡(TEM)圖(a)、拉曼譜(b)和紫外-可見(UV-Vis)吸收光譜(c);
圖2是實施例2中BP-Au納米復合物的SERS效應,其中1為染料IR-780的正常拉曼譜線,2為相同濃度IR-780的SERS譜線;
圖3是實施例2中BP-Au納米復合物對四種抗生素的SERS檢測;
圖4是實施例3中BP-Au納米復合物的光熱效應,其中1為純水的光熱效果,2為BP-Au納米復合物的光熱效應曲線;
圖5是實施例7中BP-Au納米復合物對癌細胞的SERS效應。
具體實施方式
實施例1
將30mg的BP晶體分散在30mL的N-甲基吡咯烷酮NMP中,置于細胞超聲波破碎儀(600W)中破碎6h,然后將破碎液移入超聲清洗機(200W)中繼續超聲10h。在整個超聲過程中需將溫度保持在20℃以下,超聲結束后將分散液以7000rpm的轉數離心20min,取沉淀重懸至N-甲基吡咯烷酮NMP中,繼續以1500rpm的轉數離心10min,收集上清,即為BP納米片懸液;調整BP納米片懸液的濃度至5mg/mL,隨后進行BP-Metal納米復合物的制備,先將50μL BP懸液加入至20mL煮沸的超純水中,接著迅速加入150μL HAuCl4(10mmol·L)繼續沸騰1min,反應結束后,待液體冷卻后以5000rpm的轉數離心10min,收集沉淀,即為BP-Au納米復合物。
本實施例制備獲得的納米材料的表征情況可見圖1。
透射電鏡(TEM)圖中可以很明顯地看到呈片狀的BP-Au二維納米復合物,在BP片層上遍布了大小不一的Au顆粒,二維雜合體系的大小約為幾百納米。
拉曼光譜表征可以檢測出BP的三個特征峰(360cm-1,437cm-1和466cm-1),同時在UV-Vis譜中Au的吸收峰也很明顯,證明了復合物中BP和Au兩種成分的存在。
實施例2
將實施例1制備得到的BP-Au納米復合物用于染料分子的SERS檢測。具體步驟為:將0.2mM BP-Au納米復合物與染料分子1:1混合后,吸取少量樣品至于拉曼光譜儀下檢測。儀器選用雷尼紹invia型顯微拉曼光譜系統,選擇785nm激光激發,功率0.1mW,中心波長1200cm-1,曝光時間5s。
圖2是BP-Au納米復合物對IR-780染料(5×10-8M)的SERS效應圖,可見在濃度為5×10-8M下,IR-780的正常拉曼光譜沒有任何光譜信息出現;用BP-Au作為SERS基底后,IR-780(5×10-8M)的拉曼信號得到顯著地增強,其中1207cm-1峰的SERS信號極為明顯。
另外,利用BP-Au的高SERS活性,將之用于抗生素的檢測。將BP-Au與四種低濃度的抗生素混合后,置于拉曼光譜儀下掃描,從圖3中可以觀察到四條譜峰清晰、信號非常明顯的SERS譜線,分別歸屬于環丙沙星、恩諾沙星、氯霉素和呋喃它酮等四種抗生素的。結果表明,BP-Au有望作為一種新型的拉曼活性底物用于各種抗生素及農藥殘留物或者一些食品非法添加劑的極限SERS檢測。
實施例3
將實施例1制備得到的BP-Au納米復合物用于光熱效應檢測。具體步驟為:將BP-Au納米復合物稀釋成濃度為0.1mM的懸濁液,移至1.5mL的EP管中;然后用波長為785nm的激光(功率為2W)對該懸濁液進行照射,每隔30s用紅外熱像儀對懸濁液進行溫度探測,記錄液體的溫度。
圖4顯示了BP-Au納米復合物的光熱效應,可以看出在持續10min的激光照射下,BP-Au懸濁液的溫度持續上升,并在10min后上升至53℃;而空白對照組溶液的溫度則升高不多。
實施例4
將一定量的BP晶體分散在NMP中(濃度約為1mg/mL),置于細胞超聲波破碎儀(500W)中破碎5h,然后將破碎液移入超聲清洗機(150W)中繼續超聲12h,在整個超聲過程中需將溫度保持在20℃以下,超聲結束后將分散液以8000rpm的轉數離心15min,取沉淀重懸至NMP中,繼續以2000rpm的轉數離心15min,收集上清,即為BP納米片懸液;調整BP納米片懸液的濃度至4mg/mL,隨后進行BP-Metal納米復合物的制備,先將100μL BP懸液加入至20mL煮沸的超純水中,接著迅速加入400μL HAuCl4(5mM)繼續沸騰10min,反應結束后,待液體冷卻后以6000rpm的轉數離心15min,收集沉淀,即為BP-Au納米復合物。
實施例5
將一定量的BP晶體分散在NMP中(濃度約為1mg/mL),置于細胞超聲波破碎儀(600W)中破碎6h,然后將破碎液移入超聲清洗機(150W)中繼續超聲10h,在整個超聲過程中需將溫度保持在20℃以下,超聲結束后將分散液以7000rpm的轉數離心20min,取沉淀重懸至NMP中,繼續以1500rpm的轉數離心10min,收集上清,即為BP納米片;調整BP納米片的濃度至5mg/mL,隨后進行BP-Metal納米復合物的制備,先將80μL BP懸液加入至20mL煮沸的超純水中,接著迅速加入200μL HAuCl4(10mM)繼續沸騰5min,反應結束后,待液體冷卻后以5000rpm的轉數離心10min,收集沉淀,即為BP-Au納米復合物。
實施例6
將一定量的BP晶體分散在NMP中(濃度約為1mg/mL),置于細胞超聲波破碎儀(600W)中破碎6h,然后將破碎液移入超聲清洗機(150W)中繼續超聲10h,在整個超聲過程中需將溫度保持在20℃以下,超聲結束后將分散液以7000rpm的轉數離心20min,取沉淀重懸至NMP中,繼續以1500rpm的轉數離心15min,收集上清,即為BP納米片;調整BP納米片的濃度至5mg/mL,隨后進行BP-Metal納米復合物的制備,先將100μL BP懸液加入至20mL煮沸的超純水中,接著迅速加入200μL AgNO3(10mM)繼續沸騰5min,反應結束后,待液體冷卻后以5000rpm的轉數離心10min,收集沉淀,即為BP-Ag納米復合物。
實施例7
將實施例1制備得到的BP-Au納米復合物用于細胞的SERS檢測。具體步驟為:首先,將細胞接種至拉曼襯底上,培養至70%融合后,加入BP-Au(100μM)與細胞共孵育4h后,取出拉曼襯底,PBS清洗5遍后,將細胞置于顯微拉曼光譜儀下掃描(785nm激發光)。
圖5是BP-Au納米復合物對人肝癌(Hep G2)細胞的SERS效應圖,可見在與BP-Au共孵育的情況下,癌細胞的拉曼信息得到了顯著的增強。表明,BP-Au有望作為一種新型的拉曼活性底物用于生物樣品的SERS檢測。
上述實施例為本發明較佳的實施方式,但本發明的實施方式并不受上述實施例的限制,其他的任何未背離本發明的精神實質與原理下所作的改變、修飾、替代、組合、簡化,均應為等效的置換方式,都包含在本發明的保護范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!