重組ΔfHbp?NadA融合蛋白載體及其制備方法和應(yīng)用與流程
本發(fā)明屬于生物技術(shù)領(lǐng)域,特別是涉及一種用于多價(jià)腦膜炎球菌和肺炎球菌綴合疫苗的重組δfhbp-nada蛋白載體及其制備方法和應(yīng)用。
背景技術(shù):
一、病原微生物與疫苗
能引起人體或動(dòng)物體發(fā)生傳染病的微生物,稱為病原微生物或致病微生物。傳染是指病原微生物侵入機(jī)體后,在一定的部位生長(zhǎng)、繁殖,并引起一系列病理生理的過(guò)程。當(dāng)病原微生物侵入機(jī)體后,病原微生物與機(jī)體互相作用,互相改變對(duì)方的活性與功能,因此能否引起傳染病,一方面取決于病原微生物的致病能力即致病性或毒力,另方面還取決于機(jī)體的抵抗力即免疫力。病原性細(xì)菌引起傳染的能力大小,就是細(xì)菌的毒力或致病性。細(xì)菌毒力的有無(wú)和毒力的強(qiáng)弱主要取決于它的侵襲力、產(chǎn)毒素性和引起超敏反應(yīng)的能力。
細(xì)菌產(chǎn)生的毒素可分為外毒素和內(nèi)毒素兩大類。外毒素是病原菌在生長(zhǎng)繁殖期間分泌到周圍環(huán)境種的一種代謝產(chǎn)物,主要由革蘭氏陽(yáng)性菌產(chǎn)生,少數(shù)革蘭氏陰性菌也能產(chǎn)生。其化學(xué)組成是蛋白質(zhì),抗原性強(qiáng),毒性也強(qiáng),但極不穩(wěn)定,對(duì)熱和某些化學(xué)物質(zhì)敏感,容易受到破壞。常見的如:白喉棒桿菌產(chǎn)生的白喉外毒素、破傷風(fēng)梭菌產(chǎn)生的破傷風(fēng)毒素、霍亂弧菌產(chǎn)生的腸毒素、肉毒梭菌產(chǎn)生的肉毒毒素等。大多數(shù)革蘭氏陰性細(xì)菌能產(chǎn)生內(nèi)毒素,實(shí)際上它存在于細(xì)菌細(xì)胞壁的外層,屬于細(xì)胞壁的組成部分,一般情況下并不分泌到環(huán)境中,只有當(dāng)細(xì)菌溶解后才釋放出來(lái),因而稱為內(nèi)毒素,其毒性比外毒素要低,抗原性也弱。
同種生物的不同個(gè)體,當(dāng)它們與病原菌接觸后,有的患病,有的則安然無(wú)恙,原因在于不同個(gè)體的免疫力不同。免疫就是指機(jī)體識(shí)別和排除抗原異物(如病原微生物等)的一種保護(hù)性反應(yīng)。一般來(lái)講,它對(duì)機(jī)體是有利的,在異常條件下,也可能損害機(jī)體。人體的免疫分為非特異性免疫和特異性免疫。其中特異性免疫是指機(jī)體針對(duì)某一種或某一類微生物或產(chǎn)物所產(chǎn)生的特異抵抗力。而疫苗即是科學(xué)家研制出來(lái)使機(jī)體產(chǎn)生特異性免疫抵抗病原微生物對(duì)人體侵害的生物制品,通常由病原微生物本身加以制備而成的。細(xì)菌、病毒和立克次氏體等病原微生物制成疫苗,注射機(jī)體后,使機(jī)體產(chǎn)生特異性或致敏性淋巴細(xì)胞,分泌抗體,達(dá)到特異性免疫效果。
而疫苗又分為治療性和預(yù)防性兩種,通過(guò)治療性疫苗治療疾病,并通過(guò)預(yù)防性疫苗保護(hù)人體不受致病性微生物的侵害。經(jīng)過(guò)多年的努力,醫(yī)學(xué)界已經(jīng)開發(fā)出各種不同的疫苗用以預(yù)防,諸如細(xì)菌、病毒和真菌等,感染造成的各種疾病,極大地提高了人類的健康水平。生物技術(shù)的不斷發(fā)展,促進(jìn)了疫苗品種的多樣化。用以預(yù)防病毒導(dǎo)致的傳染病有滅活病毒技術(shù)開發(fā)出來(lái)的疫苗,如乙腦疫苗、脊髓灰質(zhì)炎疫苗、流感疫苗等;減毒病毒技術(shù)開發(fā)出來(lái)的減毒活疫苗,如輪狀病毒疫苗、口服脊髓灰質(zhì)炎病毒疫苗、麻疹病毒疫苗、腮腺炎病毒疫苗、風(fēng)疹病毒疫苗和水痘疫苗等。用以預(yù)防細(xì)菌性傳染病的有用蛋白和多糖等生物大分子純化技術(shù)開發(fā)出來(lái)的細(xì)菌類疫苗,如破傷風(fēng)類毒素、白喉類毒素、百日咳類毒素及其亞細(xì)胞組分、流行性腦膜炎球菌多糖和23價(jià)肺炎球菌多糖等。更先進(jìn)的有用半化學(xué)結(jié)合技術(shù)開發(fā)出來(lái)的預(yù)防腦膜炎和肺炎的細(xì)菌疫苗,如流行性嗜血桿菌b型多糖-蛋白綴合疫苗、7價(jià)或10價(jià)肺炎球菌多糖-蛋白綴合疫苗以及4價(jià)腦膜炎球菌多糖-蛋白綴合疫苗。通過(guò)對(duì)生物技術(shù)的不斷改進(jìn),能夠開發(fā)出更多的新型疫苗產(chǎn)品來(lái)應(yīng)付不同的病原微生物對(duì)人類健康的挑戰(zhàn)。
二、多糖-蛋白綴合疫苗及其蛋白載體
多糖是病原菌中的一種重要免疫有效成分,有菌體多糖(ops)和莢膜多糖(cps)之分。當(dāng)病原體侵入機(jī)體后,它們作為免疫原,能刺激機(jī)體產(chǎn)生保護(hù)性免疫應(yīng)答。而目前許多能引起危害嚴(yán)重的疾病的病原體如流感嗜血桿菌b型(haemophilusinfluenzaetypeb,hib),肺炎鏈球菌(streptococcuspneumoniae,spn)和腦膜炎奈瑟菌(neisseriameningitidis,nm)其表面都具有多糖,這些多糖能夠賦予病原體對(duì)補(bǔ)體介導(dǎo)的殺傷和吞噬作用產(chǎn)生抗性,從而促進(jìn)它們發(fā)病期間在血液中的存活。第一代針對(duì)hib,spn和nm的疫苗即以多糖為抗原。但不幸的是,這些多糖疫苗在幼兒中不是免疫原性的,并且不能產(chǎn)生免疫記憶。這是因?yàn)槎嗵欠肿訉儆趖細(xì)胞不依賴性抗原(ti-ag),免疫原性較弱,接種嬰幼兒后免疫效果尤其不理想。為了提高多糖疫苗的免疫原性,在20世紀(jì)20年代和30年代由landsteiner,avery和goebel通過(guò)與蛋白質(zhì)偶聯(lián)來(lái)增強(qiáng)。1980年,johnrobbins和rachelschneerson描述了hib多糖與白喉和破傷風(fēng)類毒素蛋白的綴合物,極大的增強(qiáng)了動(dòng)物模型中的抗體反應(yīng)。最終hib多糖-蛋白質(zhì)綴合物,在人類嬰兒中引發(fā)記憶型抗體應(yīng)答。新一代的多糖-蛋白質(zhì)綴合疫苗,在疫苗學(xué)中創(chuàng)造了復(fù)興。這類綴合物將過(guò)去的t細(xì)胞非依賴性多糖疫苗轉(zhuǎn)化為在兒童中具有更強(qiáng)免疫原性的t細(xì)胞依賴性疫苗,顯示具有產(chǎn)生具有高親合力的抗體的能力,建立免疫記憶,并產(chǎn)生群免疫效應(yīng)。此外,它們改善了年輕嬰兒的未成熟免疫系統(tǒng)和老年人的衰老免疫系統(tǒng)的保護(hù)性應(yīng)答,從而達(dá)到最佳的免疫效果。
迄今為止,5種載體蛋白已用于許可上市的綴合疫苗中:白喉毒素?zé)o毒變異體(crm197),破傷風(fēng)類毒素(tt),腦膜炎球菌外膜蛋白復(fù)合物(omp),白喉類毒素(dt)和流感嗜血桿菌蛋白d(hid)。臨床試驗(yàn)已經(jīng)證明這些綴合疫苗在預(yù)防感染性疾病和改變hib,spn和nm的藥物中的功效。所有5種載體蛋白質(zhì)在增加疫苗免疫原性方面都是有效的,但是它們引起的抗體的量和親合力不同,在同一產(chǎn)品中攜帶多種多糖的能力以及與其它疫苗同時(shí)作用的能力也不同。
crm197是從白喉棒桿菌c7(β197)培養(yǎng)物中分離的白喉毒素的無(wú)毒變體。crm197與野生型白喉毒素的不同之處在于,在氨基酸位置52處的點(diǎn)突變用谷氨酸代替甘氨酸,這消除了其酶活性和毒性。crm197與白喉毒素在抗原上是不可區(qū)分的,但是具有作為綴合蛋白的優(yōu)點(diǎn):無(wú)毒的,并且具有更多的賴氨酰側(cè)鏈可用于綴合。用作綴合物的crm的另一種形式是純化的天然白喉毒素,其隨后用甲醛解毒,稱為白喉類毒素(dt),不應(yīng)與crm197混淆。tt是破傷風(fēng)梭菌培養(yǎng)物產(chǎn)生的破傷風(fēng)毒素用甲醛解毒來(lái)制備得來(lái)。omp為nm菌血清型b群外膜蛋白復(fù)合物。dt是白喉?xiàng)U菌培養(yǎng)物產(chǎn)生的白喉毒素,通過(guò)甲醛解毒制備得來(lái)。hid是最初用超聲處理流感嗜血桿菌中,通過(guò)sds-page步驟純化分離流感嗜血桿菌表面蛋白,但是目前的疫苗都是通過(guò)基因工程獲得重組蛋白。
tt、dt等類毒素早已工業(yè)化生產(chǎn),較易獲得,而且與多糖偶聯(lián)后確實(shí)可大大增強(qiáng)多糖的免疫原性。但為獲得類毒素,需對(duì)細(xì)菌毒素進(jìn)行化學(xué)脫毒。而在這一過(guò)程中會(huì)產(chǎn)生點(diǎn)對(duì)點(diǎn)突變或不必要的修飾,致毒素的理化性質(zhì)改變,破壞了重要的t細(xì)胞抗原表位,影響其免疫原性。如采用無(wú)毒的變異毒素crm197就可避免上述問(wèn)題。然而體內(nèi)存在的類毒素抗體(tt和dt已大量使用)可能會(huì)導(dǎo)致超敏反應(yīng)或引起抑制抗糖反應(yīng)(免疫抑制)等問(wèn)題。采用相同種屬細(xì)菌的多糖與載體蛋白就可避免這些潛在問(wèn)題。例如開發(fā)nm疫苗,以b群的蛋白或omp蛋白為載體制備a、c、y、w135群多糖-蛋白綴合疫苗不失為一個(gè)良好策略,理論上其可預(yù)防幾乎所有致病性nm,但前提是該b群蛋白載體是“廣譜”的或是具有很大交叉反應(yīng)性的。因此,開發(fā)新型的,能夠賦予疫苗以真正的保護(hù)性免疫原性的蛋白載體迫在眉睫。
三、腦膜炎奈瑟氏菌(nm)及其流行病學(xué)
流行性腦脊髓膜炎(epidemiccerebrospinalmeningitis)是由腦膜炎奈瑟氏菌,通過(guò)呼吸道傳播引起的急性化膿性腦膜炎,在世界各地均有不同程度的流行。腦膜炎奈瑟菌也稱為腦膜炎球菌,是一類革蘭染色陰性雙球菌,通常定植在人的鼻咽部。人類是其唯一宿主,因而nm表現(xiàn)出對(duì)人類鼻咽部高度的適應(yīng)性,10%-40%的健康人群都是nm的無(wú)臨床癥狀攜帶者,在腦膜炎爆發(fā)性流行時(shí)期,無(wú)癥狀攜帶者比例更可高達(dá)70%。少數(shù)情況下,nm可經(jīng)血侵入腦脊髓膜,引起化膿性炎癥,出現(xiàn)腦膜刺激癥和化膿性腦膜炎的腦脊液變化。疫苗預(yù)防是防治腦膜炎球菌病的重要手段,因?yàn)榧词共捎每股馗缮妫@種疾病仍有高發(fā)病率和死亡率。
具有致病性的nm菌株一般都具有莢膜結(jié)構(gòu),健康人群正常攜帶的菌株往往會(huì)缺失莢膜,成為不能分群的菌株。根據(jù)nm莢膜多糖的化學(xué)組成可將其分成a、b、c、d、h、i、k、l、x、y、z、29e和w13513個(gè)血清群(serogroup),而根據(jù)其外膜蛋白(omp)、porb(2或3類omp)和pora(1類omp)的抗原性差異,又可分成不同的血清型和血清亞型。全球每年約發(fā)生120萬(wàn)的nm感染病例,多數(shù)病例是由a、b、c、w135、y群菌株引起。而在發(fā)達(dá)國(guó)家中由b群nm引起的流行性腦脊髓膜炎病例更是高達(dá)總病例的80%。在我國(guó)的流行主要以a群為主,近年來(lái)由于疫苗的廣泛接種,a群引起的感染得到有效控制,而由b群引起的病例也相對(duì)增多。單一血清群、血清型和血清亞型的流腦菌苗在整體上很難預(yù)防流行性腦脊髓膜炎的發(fā)生。隨著對(duì)nm表面抗原結(jié)構(gòu)更加深入的研究,流腦菌苗正朝著多元化方向發(fā)展。
流腦多糖-蛋白綴合菌苗已有研制,chiron和wyem使用脫毒白喉類毒素(crm197)作為蛋白載體,baxter用破傷風(fēng)類毒素作為載體,開發(fā)了a/c群腦膜炎球菌綴合疫苗,于1999年11月引入了英國(guó)。此后sanofi-pasteur開發(fā)了a/c/y/w135群多糖共價(jià)結(jié)合白喉類毒素(mcv4)的四價(jià)綴合疫苗,我國(guó)已有幾種a、c群腦膜炎球菌莢膜多糖與載體蛋白tt的綴合疫苗批準(zhǔn)上市。由于腦膜炎球菌多糖及綴合疫苗應(yīng)用,有效的預(yù)防了a、c、y和w135群腦膜炎球菌的感染。與a、c、w135、y群菌株莢膜多糖不同,b群nm菌株的莢膜多糖免疫原性較低,并且menb莢膜多糖的結(jié)構(gòu)與正在發(fā)育的神經(jīng)組織及少數(shù)成熟組織中的神經(jīng)細(xì)胞黏附分子同源,免疫接種易產(chǎn)生自身免疫。因此,b群nm的莢膜多糖不能用作疫苗的抗原成份。b群疫苗的研究目前主要集中在非莢膜抗原,如蛋白、脂多糖(1ipopolysaccharide,los)等。篩選非莢膜表面抗原的主要挑戰(zhàn)是其安全性、抗原保守性及能引發(fā)廣泛有效的殺菌力反應(yīng)。能作為候選疫苗的具有免疫原性的蛋白質(zhì)需具備以下特點(diǎn):在大多數(shù)菌株中都表達(dá)且結(jié)構(gòu)保守;可誘生殺菌抗體或保護(hù)性抗體。目前在蛋白質(zhì)疫苗的研究方面取得了一定進(jìn)展,諾華公司應(yīng)用反向疫苗學(xué)研制的4cmenb疫苗已通過(guò)ⅲ期臨床實(shí)驗(yàn)。在研熱點(diǎn)候選抗原有pora,nhha、gna2132、nada和fhbp等,其中fhbp是最有前途的候選蛋白質(zhì)之一。
fhbp為因子h結(jié)合蛋白(factorh-bindingprotein,fhbp),又稱為脂蛋白2086,幾乎表達(dá)于所有腦膜炎奈瑟菌表面,由255個(gè)氨基酸殘基組成,分子量29000。因子h是補(bǔ)體替代途徑的關(guān)鍵調(diào)節(jié)子,它在因子i介導(dǎo)的c3b裂解為滅活片段ic3b過(guò)程中發(fā)揮輔助因子作用。也促進(jìn)替代途徑c3轉(zhuǎn)化酶c3bbb的衰變。fhbp和因子h結(jié)合可下調(diào)替代途徑,從而有利于腦膜炎奈瑟菌生存。fhbp對(duì)于腦膜炎球菌在人類的血液、血清和抗菌性多肽存在的情況下的生存是極為重要的。其氨基酸序列較保守,變種內(nèi)91.6%-100%氨基酸相同。重組fhbp抗體可引起針對(duì)同一類變種的補(bǔ)體介導(dǎo)的殺菌作用和誘導(dǎo)感染乳鼠模型的被動(dòng)保護(hù)。由完整fhbp獲得的抗體不僅滴度高,且對(duì)順序變異不敏感,即使有少量氨基酸改變,只要決定空間構(gòu)象的關(guān)鍵氨基酸不變,抗體殺菌活性變化不大。所有這些特點(diǎn)使fhbp成為腦膜炎奈瑟菌最有效的抗原之一和最有希望的候選通用疫苗。根據(jù)整個(gè)蛋白的抗原交叉反應(yīng)性和序列相似性,腦膜炎球菌fhbp可以被分為3個(gè)抗原變體組。通常,針對(duì)變體v1的fhbp(也被稱為亞家族b)制備的抗體對(duì)來(lái)自變體v1表達(dá)fhbp的菌株具有殺菌活性,但不針對(duì)變體v2和v3(也稱為亞族a)中表達(dá)fhbp的菌株,反之亦然。在每個(gè)變體組中也存在fhbp的亞變體。最近,fhbp的分子結(jié)構(gòu)已顯示為“模塊化”,fhbp變體含有五個(gè)可變結(jié)構(gòu)域的不同組合(va~ve),每個(gè)可變區(qū)段衍生自亞族a和亞族b。因此,通過(guò)基因工程手段自由組合五個(gè)結(jié)構(gòu)域可以得到覆蓋a、b兩個(gè)亞族三種變體的抗原的重組δfhbp蛋白,成為廣譜的疫苗抗原及蛋白載體。
但是,單獨(dú)使用fhbp蛋白也有一定的缺陷,因?yàn)樵谟行﹎enb菌株中fhbp蛋白表達(dá)水平較低,只有fhbp的抗原的疫苗不可能足以用于廣泛的免疫腦膜炎球菌的感染,融合表達(dá)多種抗原不失為一個(gè)良好的選擇。在研的一種純蛋白疫苗(lp2086)中含有三種組分,其中兩個(gè)組分是融合蛋白(gna2091與fhbp融合,gna2132與gna1030融合),第三個(gè)組分是重組nada。5種抗原負(fù)染應(yīng)用可以引起小鼠中的大多數(shù)血清殺菌應(yīng)答,起到良好的保護(hù)。其中,gna2091、gna2132和gna1030均為未知功能蛋白組分,而nada為奈瑟氏菌粘附素a,在體外結(jié)合上皮細(xì)胞的粘附素/侵襲素。該抗原在menb菌株中是非常保守的(>96%氨基酸同一性),但是不存在于某些遺傳譜系的菌株中,僅有50%的menb致病菌株表達(dá)nada蛋白,但這50%都是高致病菌。融合表達(dá)δfhbp蛋白和nada蛋白,無(wú)疑能提高其抗原性,并以此抗原為蛋白載體,結(jié)合a、c、y和w135群腦膜炎球菌的莢膜多糖,理論上該多價(jià)綴合疫苗可預(yù)防a、b、c、y和w135五個(gè)亞群致病菌的感染,從而預(yù)防絕大部分nm感染導(dǎo)致的流行性腦脊髓膜炎。
四、肺炎球菌的危害及其流行病學(xué)研究
由肺炎球菌所引起的感染是全世界肺炎發(fā)病率和死亡率的主要起因,已成為全球一個(gè)重要的公共衛(wèi)生問(wèn)題。肺炎球菌已成為全球兒童的頭號(hào)殺手。我國(guó)肺炎的病死率為16.4%,其中50歲以上中老年人及1歲以下嬰幼兒分別高達(dá)28.6%和22.0%。根據(jù)莢膜多糖免疫原性的不同,spn可分為93種血清型,但多數(shù)血清型很少引起疾病,世界范圍內(nèi)至少70%-75%的侵襲性肺炎是由13種常見的血清型引起的,而我國(guó)的統(tǒng)計(jì)資料顯示肺炎球菌感染菌株前幾個(gè)血清型依次為:5、6、19、23、14、2、4型,spn疫苗是預(yù)防其感染的重要手段。中國(guó)生物技術(shù)集團(tuán)成都生物制品研究所生產(chǎn)的23價(jià)肺炎球菌疫苗是選取了23種最常見的致病菌(1,2,3,4,5,6b,7f,8,9n,9v,10a,11a,12f,14,15b,17f,18c,19a,19f,20,22f,23f,33f),分別發(fā)酵培養(yǎng)并分離提純肺炎球菌莢膜上的各型多糖,按等比例混合制成疫苗。臨床使用證明,莢膜多糖制作的疫苗明確有效,并在多個(gè)國(guó)家廣泛使用。但是這類多糖疫苗存在產(chǎn)生的抗體親和力低、對(duì)侵入型肺炎球菌保護(hù)率只有50%-70%、只產(chǎn)生短暫免疫,不具備免疫記憶、對(duì)2歲以下嬰幼兒無(wú)保護(hù)作用等諸多問(wèn)題。最主要的原因是單純的多糖抗原不能激活t細(xì)胞,無(wú)法誘導(dǎo)免疫記憶效應(yīng),刺激機(jī)體產(chǎn)生的抗體主要是igm和igg2,不能夠有效地激活補(bǔ)體系統(tǒng)。
因此,肺炎球菌的多糖-蛋白質(zhì)綴合疫苗應(yīng)運(yùn)而生。通過(guò)多年的技術(shù)發(fā)展,2000年,美國(guó)惠氏(wyeth)公司成功開發(fā)并上市了7價(jià)肺炎球菌多糖-crm197綴合疫苗,是由7個(gè)不同的肺炎球菌血清型多糖分別共價(jià)鍵連接到crm197蛋白載體上,混合配制而成的一種多價(jià)疫苗,用以預(yù)防小兒肺炎,所述7個(gè)血清型肺炎球菌涵蓋了北美和歐洲90%以上流行的肺炎球菌不同血清型菌株。同年,美國(guó)輝瑞公司第一個(gè)7(4、6b、9v、14、18c、19f和23f)價(jià)肺炎球菌蛋白綴合疫苗上市,目前,輝瑞公司正在中國(guó)注冊(cè)13價(jià)綴合疫苗,增加了6個(gè)血清型(1,3,5,7f,6a,19a)。但是我國(guó)的流行病學(xué)顯示肺炎球菌感染菌株血清型依次為:5、6、1、19、23、14、2、4型,輝瑞7價(jià)肺炎球菌綴合疫苗對(duì)我國(guó)常見致病菌型覆蓋率只有50%左右,而13價(jià)綴合疫苗的覆蓋率也僅有70%。國(guó)外研發(fā)的綴合疫苗不太適合我國(guó)大范圍的兒童肺炎預(yù)防。
還有一個(gè)不容忽視的問(wèn)題是,隨著不同血清型的增加和同種載體蛋白的重復(fù)使用,使得載體蛋白用量增多,其免疫原性反而降低。臨床試驗(yàn)表明,當(dāng)多價(jià)肺炎綴合疫苗與其他含有與蛋白載體相同組分的單價(jià)疫苗或多聯(lián)疫苗同時(shí)接種時(shí),比如hib-tt、百白破-hib多糖綴合疫苗-ipv(滅活脊髓灰質(zhì)炎疫苗)-乙肝疫苗(簡(jiǎn)稱6聯(lián)疫苗),多價(jià)肺炎球菌綴合疫苗中的大部分血清型多糖的免疫原性會(huì)受到抑制,特別是對(duì)用破傷風(fēng)類毒素作為載體的血清型多糖免疫原性影響尤其明顯。原因是多價(jià)肺炎球菌綴合疫苗中作為載體的破傷風(fēng)類毒素和白喉類毒素總濃度過(guò)高,在同時(shí)接種含有百白破組分的聯(lián)合疫苗時(shí),會(huì)造成載體受體競(jìng)爭(zhēng)性抑制效應(yīng),降低了綴合疫苗多糖部分的免疫原性。在現(xiàn)有上市的五種載體蛋白(crm197、tt、omp、dt和hid)大量使用的情況下,開發(fā)新的載體蛋白迫在眉睫。在此基礎(chǔ)上開發(fā)適合中國(guó)流行病學(xué)的23價(jià)多糖-蛋白綴合疫苗,具有重大的意義和社會(huì)價(jià)值,保護(hù)我國(guó)嬰幼兒免受spn侵染引起的肺炎。
技術(shù)實(shí)現(xiàn)要素:
有鑒于此,本發(fā)明提供了一種重組δfhbp-nada融合蛋白,該融合蛋白具有更強(qiáng)的menb菌群免疫原性,能誘導(dǎo)體內(nèi)產(chǎn)生強(qiáng)大的血清殺菌應(yīng)答。同時(shí),以δfhbp-nada為蛋白載體,提供了一種能覆蓋a、b、c、y和w135五種菌群的強(qiáng)免疫原性綴合疫苗。
本發(fā)明第一方面提供了一種重組δfhbp-nada融合蛋白載體,包括重組δfhbp、柔性連接肽段和nada,所述重組δfhbp包含fhbp可變體v1的va、vb結(jié)構(gòu)域以及fhbp可變體v3的vc、vd、ve結(jié)構(gòu)域。
所述重組δfhbp的氨基酸序列如序列表seqidno:1所示,其核苷酸編碼序列如序列表seqidno:2所示。
所述柔性連接肽段的核苷酸編碼序列如序列表seqidno:3所示。
所述重組δfhbp-nada融合蛋白載體的氨基酸序列如序列表seqidno:4所示,其核苷酸編碼序列如序列表seqidno:5所示。
本發(fā)明第二方面提供了上述重組δfhbp-nada融合蛋白載體的制備方法,步驟包括:
s1、設(shè)計(jì)引物分別擴(kuò)增得到fhbpv1基因片段、fhbpv3基因片段,再以這兩段基因片段為模板進(jìn)行搭橋pcr擴(kuò)增得到重組的δfhbp全長(zhǎng)片段,回收δfhbp基因片段和pet載體,制備重組質(zhì)粒pet-δfhbp;
s2、設(shè)計(jì)引物擴(kuò)增得到nada蛋白的全長(zhǎng)cds序列,回收nada基因片段和重組質(zhì)粒pet-δfhbp,制備重組質(zhì)粒pet-δfhbp-nada;
s3、將重組質(zhì)粒pet-δfhbp-nada轉(zhuǎn)化表達(dá)菌株,得到重組δfhbp-nada融合蛋白載體。
本發(fā)明第三方面提供了上述重組δfhbp-nada融合蛋白載體在制備多糖-蛋白綴合疫苗中的應(yīng)用。
本發(fā)明第四方面提供了一種多價(jià)腦膜炎球菌綴合疫苗,該綴合疫苗中,a群、c群、y群和w135群腦膜炎球菌莢膜多糖與重組δfhbp-nada融合蛋白載體綴合。
本發(fā)明第五方面提供了一種多價(jià)肺炎球菌綴合疫苗,該綴合疫苗中,肺炎球菌莢膜多糖與重組δfhbp-nada融合蛋白載體綴合。
本發(fā)明的有益效果是:1、針對(duì)b群腦膜炎球菌莢膜多糖成份不適合用作疫苗,利用反向遺傳學(xué)的技術(shù),表達(dá)b群腦膜炎球菌人h因子結(jié)合蛋白重組蛋白與奈瑟氏菌粘附素a蛋白的融合產(chǎn)物δfhbp-nada。該融合蛋白的δfhbp含有fhbpa亞族和fhbpb亞族(v1~v3三種變體)的保守結(jié)構(gòu)域,能夠覆蓋所有表達(dá)fhbp蛋白的nmb群菌株,并且,δfhbp包含fhbp完整的va~ve五個(gè)結(jié)構(gòu)域,其結(jié)構(gòu)、功能和抗原位點(diǎn)保持了完整性;同時(shí),該融合蛋白的nada在50%的nmb群菌株中表達(dá),且這些菌株基本為高致病菌。因此即使不表達(dá)fhbp但表達(dá)nada的菌株也能被δfhbp-nada蛋白覆蓋,以此重組蛋白為抗原制成的蛋白疫苗能廣譜保護(hù)幾乎所有nmb群致病菌的感染。
2、重組δfhbp-nada是一種全新的可用于綴合疫苗的載體蛋白,不同于現(xiàn)有綴合疫苗工藝中常用蛋白載體(crm197、tt、omp、dt、hid),因而不會(huì)因同種蛋白載體接種過(guò)多導(dǎo)致綴合疫苗的免疫原性下降。
3、δfhbp-nada中的δfhbp和nada組分雖然是nm生存和致病的重要因子,但其本身無(wú)毒性,從而在工業(yè)生產(chǎn)中不需要對(duì)該活性蛋白進(jìn)行脫毒處理,不會(huì)改變其結(jié)構(gòu)和抗原活性位點(diǎn),從而獲得更佳的免疫效果。
4、δfhbp-nada通過(guò)設(shè)計(jì)軟性連接肽鏈將兩個(gè)活性蛋白融合表達(dá),再保持各自的活性的同時(shí)讓兩者成為單一的蛋白質(zhì),因而在工業(yè)生產(chǎn)及免疫接種是更具有可控性,風(fēng)險(xiǎn)大大降低,又能提供更多的多糖-蛋白結(jié)合位點(diǎn)。
5、本發(fā)明提供的以重組δfhbp-nada為蛋白載體的新型多價(jià)腦膜炎球菌綴合疫苗具有廣譜的免疫效果,其免疫小鼠血清能與a、b、c、y和w135五個(gè)群的模式菌株產(chǎn)生交聯(lián)反應(yīng),同時(shí)能夠覆蓋b群中表達(dá)fhbp(3中變體)以及不表達(dá)fhbp但表達(dá)nada的高致病菌,并在殺菌檢測(cè)中表現(xiàn)出廣譜且極強(qiáng)的殺菌效果。
6、本發(fā)明提供的以重組δfhbp-nada為蛋白載體的新型23價(jià)肺炎球菌綴合疫苗具有廣譜的免疫效果,其免疫小鼠血清能與1、2、3、4、5、6b、7f、8、9n、9v、10a、11a、12f、14、15b、17f、18c、19a、19f、20、22f、23f、33f血清型spn菌株多糖抗原產(chǎn)生交聯(lián)反應(yīng),同時(shí)能夠覆蓋中國(guó)流行的血清型1、3、4、5、6b、7f、9v、14、18c、19a、19f、23f、33f菌株,并在殺菌檢測(cè)中表現(xiàn)出廣譜且極強(qiáng)的殺菌效果,此類多糖-蛋白綴合疫苗更適合我國(guó)人群使用。
7、本發(fā)明提供的以重組δfhbp-nada為蛋白載體的新型綴合疫苗具有多糖-蛋白綴合疫苗的通用優(yōu)勢(shì):免疫后能激活t細(xì)胞效應(yīng),產(chǎn)生免疫記憶,從而真正保護(hù)2歲以下的嬰兒。
8、本發(fā)明應(yīng)用cdap活化多糖后衍化結(jié)合的工藝制備多價(jià)莢膜多糖-δfhbp-nada蛋白綴合疫苗。不僅消除了常規(guī)方法中溴化氰的毒性,且活化效能明顯提高。
附圖說(shuō)明
圖1為fhbpv1~v3可變體結(jié)構(gòu)域及重組δfhbp結(jié)構(gòu)域。
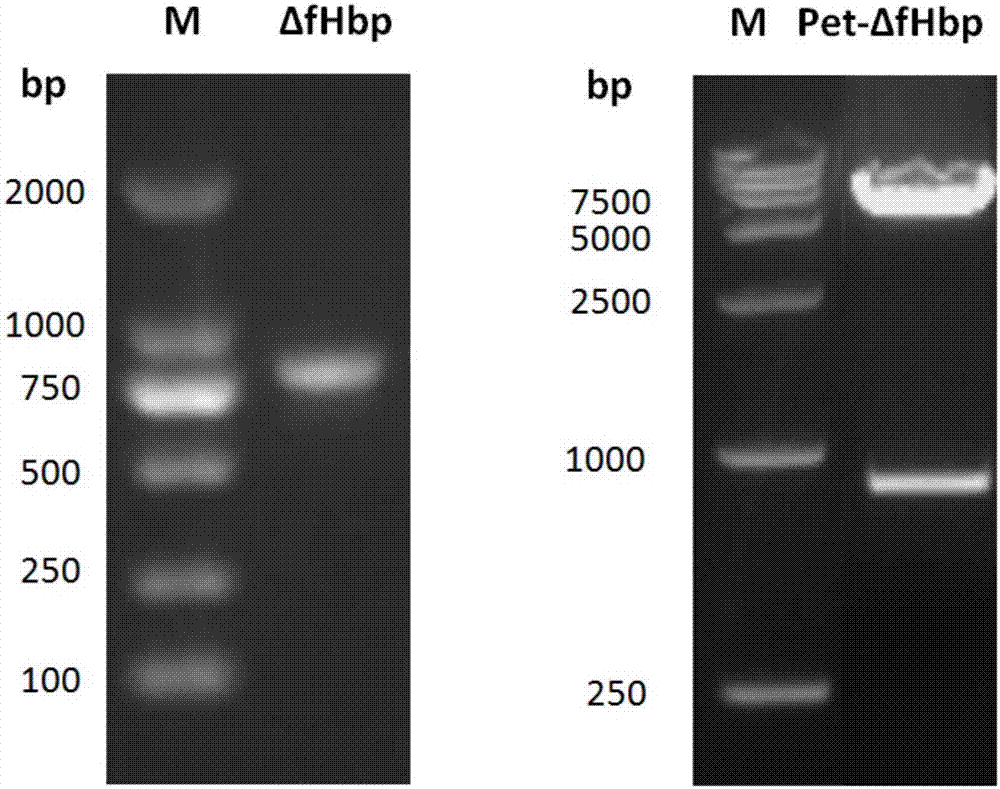
圖2為δfhbp擴(kuò)增電泳圖譜與pet-δfhbp鑒定電泳圖譜。
圖3為nada擴(kuò)增電泳圖譜與pet-δfhbp-nada鑒定電泳圖譜。
圖4為iptg誘導(dǎo)重組菌表達(dá)δfhbp和δfhbp-nada蛋白。
圖5為western-blot鑒定δfhbp和δfhbp-nada重組蛋白。
圖6為sds-page鑒定純化后的δfhbp和δfhbp-nada重組蛋白。
圖7為sds-page鑒定大規(guī)模純化后的δfhbp-nada重組蛋白。
具體實(shí)施方式
下面將結(jié)合具體實(shí)施例對(duì)本發(fā)明提供的一種δfhbp-nada蛋白載體及基于δfhbp-nada蛋白載體的多價(jià)腦膜炎球菌和肺炎球菌綴合疫苗予以進(jìn)一步說(shuō)明。下面描述的實(shí)施例是示例性的,僅用于解釋本發(fā)明,而不能理解為對(duì)本發(fā)明的限制。
下述實(shí)施例中的實(shí)驗(yàn)方法,如無(wú)特殊說(shuō)明,均為常規(guī)方法。下述實(shí)施例中所用的實(shí)驗(yàn)材料如無(wú)特殊說(shuō)明,均為市場(chǎng)購(gòu)買得到。
一、δfhbp和δfhbp-nada重組蛋白的克隆和原核表達(dá)
1、pet-δfhbp和pet-δfhbp-nada重組質(zhì)粒的構(gòu)建
fhbp是一種膜表面脂蛋白,許多腦膜炎球菌的菌株都帶有其基因,也發(fā)現(xiàn)不攜帶該基因的菌株。根據(jù)整個(gè)蛋白的抗原交叉反應(yīng)性和序列相似性,腦膜炎球菌fhbp可以被分為3個(gè)抗原變體組v1~v3。通常,針對(duì)變體v1的fhbp(也被稱為亞家族b)制備的抗體對(duì)來(lái)自變體v1表達(dá)fhbp的菌株具有殺菌活性,但不針對(duì)變體v2和v3(也稱為亞族a)中表達(dá)fhbp的菌株,反之亦然。fhbp的蛋白分子含有五個(gè)可變結(jié)構(gòu)域的不同組合(va~ve),每個(gè)可變區(qū)段衍生自亞族a和亞族b。我們根據(jù)其結(jié)構(gòu)域特點(diǎn),設(shè)計(jì)了δfhbp的結(jié)構(gòu)(如圖1所示),其包含v1的a、b結(jié)構(gòu)域(b結(jié)構(gòu)域上含有v1的抗原表位),以及v3的c、d、e結(jié)構(gòu)域(c、d、e結(jié)構(gòu)域含有v2和v3的抗原表位,且其174-216位氨基酸高度保守,只有個(gè)別氨基酸的差異),理論上,重組的δfhbp能覆蓋所有野生型fhbp3個(gè)變體的抗原位點(diǎn),具有廣譜抗菌的潛力。
根據(jù)genebank登錄的fhbpv1和fhbpv3全長(zhǎng)cds序列,我們?cè)O(shè)計(jì)如下2對(duì)引物:引物在p1和p4位置分別引入bamhⅰ和hindⅲ酶切位點(diǎn)。
p1:ggattcatgaaccgaactgccttctgctgcc
p2:gccgggcagttggttgaaggcggta
p3:acggcattcggttcagacgatgcca
p4:aagcttttactgcttggcggcaagaccgata
分別以表達(dá)fhbpv1和v3的兩株menb群菌為模板(購(gòu)自美國(guó)atcc),進(jìn)行pcr擴(kuò)增。其中p1,p2可擴(kuò)增fhbpv1的a、b結(jié)構(gòu)域基因片段,p3和p4可擴(kuò)增v3的c、d、e結(jié)構(gòu)域基因片段。再以這兩段基因片段為模板,p1,p4為引物,進(jìn)行搭橋pcr,可擴(kuò)增得到重組的δfhbp全長(zhǎng)片段。用bamhi和hindⅲ雙酶切目的基因(pcr產(chǎn)物)和原核表達(dá)載體pet32a(+),凝膠回收盒回收δfhbp基因片段和線性pet32a載體。膠回收后,用dna連接酶,16℃連接過(guò)夜,轉(zhuǎn)化大腸桿菌dh5a菌株,單克隆擴(kuò)增,小提質(zhì)粒后,bamhi和hindⅲ雙酶切鑒定的約800bp條帶,在卡那霉素抗性下篩選陽(yáng)性克隆,獲得重組質(zhì)粒pet-δfhbp,pcr擴(kuò)增電泳圖譜與鑒定正確電泳圖譜如圖2所示。將鑒定正確的重組質(zhì)粒以15%甘油菌形式-70℃保存,并測(cè)序鑒定正確,其δfhbp的氨基酸序列如序列表seqidno:1所示,其核苷酸編碼序列如序列表seqidno:2(826bp)所示。
seqidno:2(826bp):
atgaaccgaactgccttctgctgccttttcctgaccaccgccctgattctgaccgcctgcagcagcggaggcggcggaagcggaagcggcggtgtcgccgccgacatcggcacggggcttgccgatgcactaactacgccgctcgaccataaagacaaaggtttgaaatctctgacattggaagactccattccccaaaacggaacactaaccctgtcggcacaaggtgcggaaaaaactttcaaagccggcgacaaagacaacagcctcaacacgggcaaactgaagaacgacaaaatcagccgcttcgacttcgtgcaaaaaatcgaagtggacggacaaaccatcacgctggcaagcggcgaatttcaaatatacaaacaggaccactccgccgtcgttgccctacagattgaaaaaatcaacaaccccgacaaaatcgacagcctgataaaccaacgctccttccttgtcagcggtttgggcggagaacataccgccttcaaccaactgcccggcacggcattcggttcagacgatgccagtggaaaactgacctacaccatagatttcgccgccaagcagggacacggcaaaatcgaacatttgaaatcgccagaactcaatgttgacctggccgcctccgatatcaagccggataaaaaacgccatgccgtcatcagcggttccgtcctttacaaccaagccgagaaaggcagttactctctaggcatctttggcgggcaagcccaggaagttgccggcagcgcagaagtggaaaccgcaaacggcatacgccatatcggtcttgccgccaagcagtaa
其氨基酸序列為seqidno:1:
mnrtafcclflttaliltacssggggsgsggvaadigtgladalttpldhkdkglksltledsipqngtltlsaqgaektfkagdkdnslntgklkndkisrfdfvqkievdgqtitlasgefqiykqdhsavvalqiekinnpdkidslinqrsflvsglggehtafnqlpgtafgsddasgkltytidfaakqghgkiehlkspelnvdlaasdikpdkkrhavisgsvlynqaekgsyslgifggqaqevagsaevetangirhiglaakq
但單獨(dú)使用δfhbp蛋白也有一定的缺陷,因?yàn)樵谟行﹎enb菌株中fhbp蛋白表達(dá)水平較低,只有δfhbp抗原的疫苗不可能足以用于廣泛的免疫腦膜炎球菌的感染。奈瑟氏菌粘附素a(nada),在體外結(jié)合上皮細(xì)胞的粘附素/侵襲素。該抗原在menb菌株中是非常保守的(>96%氨基酸同一性),不存在于某些遺傳譜系的菌株中,僅有50%的menb致病菌株表達(dá)nada蛋白,但這50%都是高致病菌。融合表達(dá)δfhbp蛋白和nada蛋白,無(wú)疑能提高其抗原性,但兩個(gè)蛋白之間要加上柔性的鏈接肽段,最為經(jīng)典的即為huston設(shè)計(jì)合成的(ggggs)3序列,有利于兩個(gè)蛋白能夠正確折疊,從而不影響其各自的免疫原型。根據(jù)genebank登錄的nada全長(zhǎng)cds序列,設(shè)計(jì)引物:引物p5和p6分別引入hindⅲ和xhoⅰ酶切位點(diǎn),同時(shí)p5的酶切位點(diǎn)后設(shè)計(jì)表達(dá)(ggggs)3連接蛋白的序列。
p5:aagcttggcggcggcggcagtggcggcggcggcagtggcggcggcggcagtatgaaacactttccatccaaagtac(seqidno:3)
p6:ctcgagttaccactcgtaattgacgccgaca
以表達(dá)nada的menb群菌為模板(購(gòu)自美國(guó)atcc),p5,p6為引物,擴(kuò)增得到nada蛋白的全長(zhǎng)cds序列,用hindⅲ和xhoⅰ雙酶切目的基因(nada產(chǎn)物)和重組質(zhì)粒pet-δfhbp,凝膠回收盒回收nada基因片段和線性pet-δfhbp載體。膠回收后,用dna連接酶,16℃連接過(guò)夜,轉(zhuǎn)化大腸桿菌dh5a菌株,單克隆擴(kuò)增,小提質(zhì)粒后,bamhi和xhoⅰ雙酶切鑒定的約1900bp條帶,在卡那霉素抗性下篩選陽(yáng)性克隆,獲得重組質(zhì)粒pet-δfhbp-nada,pcr擴(kuò)增電泳圖譜與鑒定正確電泳圖譜如圖3所示。將鑒定正確的重組質(zhì)粒以15%甘油菌形式-70℃保存,并測(cè)序鑒定正確,重組δfhbp-nada融合蛋白載體的氨基酸序列如序列表seqidno:4所示,其核苷酸編碼序列如序列表seqidno:5(1089bp)所示。
seqidno:5(1089bp):
atgaaccgaactgccttctgctgccttttcctgaccaccgccctgattctgaccgcctgcagcagcggaggcggcggaagcggaagcggcggtgtcgccgccgacatcggcacggggcttgccgatgcactaactacgccgctcgaccataaagacaaaggtttgaaatctctgacattggaagactccattccccaaaacggaacactaaccctgtcggcacaaggtgcggaaaaaactttcaaagccggcgacaaagacaacagcctcaacacgggcaaactgaagaacgacaaaatcagccgcttcgacttcgtgcaaaaaatcgaagtggacggacaaaccatcacgctggcaagcggcgaatttcaaatatacaaacaggaccactccgccgtcgttgccctacagattgaaaaaatcaacaaccccgacaaaatcgacagcctgataaaccaacgctccttccttgtcagcggtttgggcggagaacataccgccttcaaccaactgcccggcacggcattcggttcagacgatgccagtggaaaactgacctacaccatagatttcgccgccaagcagggacacggcaaaatcgaacatttgaaatcgccagaactcaatgttgacctggccgcctccgatatcaagccggataaaaaacgccatgccgtcatcagcggttccgtcctttacaaccaagccgagaaaggcagttactctctaggcatctttggcgggcaagcccaggaagttgccggcagcgcagaagtggaaaccgcaaacggcatacgccatatcggtcttgccgccaagcagtaaggcggcggcggcagtggcggcggcggcagtggcggcggcggcagtatgaaacactttccatccaaagtactgaccacagccatccttgccactttctgtagcggcgcactggcagccacaagcgacgacgatgttaaaaaagctgccactgtggccattgttgctgcctacaacaatggccaagaaatcaacggtttcaaagctggagagaccatctacgacattggtgaagacggcacaattacccaaaaagacgcaactgcagccgatgttgaagccgacgactttaaaggtctgggtctgaaaaaagtcgtgactaacctgaccaaaaccgtcaatgaaaacaaacaaaacgtcgatgccaaagtaaaagctgcagaatctgaaatagaaaagttaacaaccaagttagcagacactgatgccgctttagcagatactgatgccgctctggatgaaaccaccaacgccttgaataaattgggagaaaatataacgacatttgctgaagagactaagacaaatatcgtaaaaattgatgaaaaattagaagccgtggctgataccgtcgacaagcatgccgaagcattcaacgatatcgccgattcattggatgaaaccaacactaaggcagacgaagccgtcaaaaccgccaatgaagccaaacagacggccgaagaaaccaaacaaaacgtcgatgccaaagtaaaagctgcagaaactgcagcaggcaaagccgaagctgccgctggcacagctaatactgcagccgacaaggccgaagctgtcgctgcaaaagttaccgacatcaaagctgatatcgctacgaacaaagctgatattgctaaaaactcagcacgcatcgacagcttggacaaaaacgtagctaatctgcgcaaagaaacccgccaaggccttgcagaacaagccgcgctctccggcctgttccaaccttacaacgtgggtcggttcaatgtaacggctgcagtcggcggctacaaatccgaatcggcagtcgccatcggtaccggcttccgctttaccgaaaactttgccgccaaagcaggcgtggcagtcggcacttcgtccggttcttccgcagcctaccatgtcggcgtcaattacgagtggtaa
其氨基酸序列為seqidno:4:
mnrtafcclflttaliltacssggggsgsggvaadigtgladalttpldhkdkglksltledsipqngtltlsaqgaektfkagdkdnslntgklkndkisrfdfvqkievdgqtitlasgefqiykqdhsavvalqiekinnpdkidslinqrsflvsglggehtafnqlpgtafgsddasgkltytidfaakqghgkiehlkspelnvdlaasdikpdkkrhavisgsvlynqaekgsyslgifggqaqevagsaevetangirhiglaakqggggsggggsggggsmkhfpskvlttailatfcsgalaatsdddvkkaatvaivaaynngqeingfkagetiydigedgtitqkdataadveaddfkglglkkvvtnltktvnenkqnvdakvkaaeseieklttkladtdaaladtdaaldettnalnklgenittfaeetktnivkidekleavadtvdkhaeafndiadsldetntkadeavktaneakqtaeetkqnvdakvkaaetaagkaeaaagtantaadkaeavaakvtdikadiatnkadiaknsaridsldknvanlrketrqglaeqaalsglfqpynvgrfnvtaavggyksesavaigtgfrftenfaakagvavgtssgssaayhvgvnyew
2、δfhbp和δfhbp-nada重組蛋白的原核表達(dá)及鑒定
將重組質(zhì)粒pet-δfhbp和pet-δfhbp-nada轉(zhuǎn)化e.colibl21(de3),37℃過(guò)夜培養(yǎng)(含50μg/ml卡納青霉素),得到δfhbp/bl21(de3)和δfhbp-nada/bl21(de3)表達(dá)菌,挑取單克隆,37℃振蕩培養(yǎng)至菌密度達(dá)od600約0.5~1.0,加入終濃度0.5mm的異丙基-β-d-硫代半乳糖苷(iptg),37℃振蕩誘導(dǎo)培養(yǎng)2-6小時(shí),經(jīng)sds-page鑒定,結(jié)果如圖4顯示,δfhbp/bl21(de3)和δfhbp-nada/bl21(de3)誘導(dǎo)后有明顯的表達(dá)條帶,分子量分別為30kd和72kd。經(jīng)western-blot鑒定為δfhbp和δfhbp-nada重組蛋白,如圖5所示:1,3泳道為δfhbp/bl21(de3)誘導(dǎo)表達(dá)物,2,4泳道為δfhbp-nada/bl21(de3)誘導(dǎo)表達(dá)物,1,2用fhbp單抗檢測(cè),分別有30kd和72kd的預(yù)期條帶,3,4用nada單抗檢測(cè),只有4泳道有72kd條帶,結(jié)果符合預(yù)期。最后兩個(gè)重組蛋白經(jīng)質(zhì)譜鑒定,確定為δfhbp和δfhbp-nada重組蛋白。
二、δfhbp和δfhbp-nada重組蛋白的小規(guī)模純化及其免疫效果評(píng)價(jià)
將δfhbp/bl21(de3)和δfhbp-nada/bl21(de3)接種lb(含50μg/ml卡納霉素)液體培養(yǎng)基,37℃、200rpm培養(yǎng)12小時(shí),以1%接種比例擴(kuò)大培養(yǎng),37℃、200rpm培養(yǎng)3-6小時(shí)后,od600至16~20,iptg(0.5mm)誘導(dǎo)4小時(shí)。離心機(jī)離心收集菌體。超聲破菌,之前的sds-page顯示,重組蛋白表達(dá)以包涵體的形式(圖3)。先后用te+300mmnacl,te+1%triton-100洗滌包涵體后,8000rpm離心20min獲得包涵體,洗滌后,溶解于3mol/lurea,20mmol/ltris-cl,1mmol/ledta,ph4.0溶液中,經(jīng)cm柱離子交換層析純化,可得到與目標(biāo)蛋白大小相符的兩個(gè)目的蛋白。最后待重組蛋白稀釋復(fù)性至24h后,超濾器低溫快速濃縮至原體積的1.2倍,過(guò)陰離子交換柱qsepharosef.f,收集目的蛋白峰,檢測(cè)方法同圖4與圖5,凝膠檢測(cè)蛋白含量達(dá)到95.3%以上,純化效果如圖6所示,wb檢測(cè)確為目的蛋白。用pbs(ph7.4)透析除鹽后,bca法測(cè)蛋白濃度含量約0.5mg/ml。
小鼠免疫:分別用純化后的δfhbp和δfhbp-nada重組蛋白皮下免疫6周齡spf級(jí)nih小鼠10只,免疫劑量為每次純化后的δfhbp或δfhbp-nada重組蛋白50ug/只(溶解于0.2ml生理鹽水中),免疫程序?yàn)?,2,4周,免疫結(jié)束后2周采血,離心收集血清;另設(shè)10只小鼠對(duì)照,相同方法注射生理鹽水。收集好的血清e(cuò)lisa法測(cè)血清抗體的滴度,具體方法如下:采用純化后的δfhbp或δfhbp-nada重組蛋白,分別以適宜劑量包被酶標(biāo)板,37℃孵育過(guò)夜,洗板后加入系列稀釋的待測(cè)小鼠血清,37℃孵育后洗板,加入辣根過(guò)氧化物酶標(biāo)記羊抗鼠igg二抗顯色,酶標(biāo)儀測(cè)定,讀取492nm(630nm為參比波長(zhǎng))吸光度值(a值)。陰性對(duì)照組血清a均值+3倍的標(biāo)準(zhǔn)偏差為cutoff值,待測(cè)血清a值大于cutoff值判為陽(yáng)性,以a值大于cutoff值的最大稀釋度計(jì)算各型別小鼠的幾何平均滴度,即為小鼠血清igg抗體效價(jià)(表1)。兩種重組蛋白免疫小鼠后均產(chǎn)生了高低度的血清抗體。
表1.各組抗原三次免疫小鼠后血清抗體的滴度測(cè)定(幾何平均值)
兩種重組蛋白免疫效果的評(píng)價(jià),采取兩種方法,一為全菌體包被測(cè)定全細(xì)胞elisa,另一為流行株的殺菌力實(shí)驗(yàn)。全菌體包被選擇menb群菌株mc58(高表達(dá)fhbpv1可變體)、8047(高表達(dá)fhbpv2可變體)、m1239高表達(dá)fhbpv3可變體),961-5945(中量表達(dá)fhbp蛋白)和67/00(低量表達(dá)fhbp蛋白),將這些菌株擴(kuò)大培養(yǎng)增殖后,刮取細(xì)菌菌苔,以生理鹽水溶解,甲醛殺菌后,稀釋為2×108個(gè)/ml,以此濃度包被96孔酶標(biāo)板,100ul/孔,4℃包被過(guò)夜,洗板后,進(jìn)行檢測(cè),結(jié)果見表2。同樣,培養(yǎng)menb群菌株mc58(高表達(dá)fhbpv1可變體)、8047(高表達(dá)fhbpv2可變體)、m1239高表達(dá)fhbpv3可變體),961-5945(中量表達(dá)fhbp蛋白)和67/00(低量表達(dá)fhbp蛋白)后用相應(yīng)血清抗體進(jìn)行殺菌檢測(cè),測(cè)定并計(jì)算殺菌抗體滴度(與補(bǔ)體陰性對(duì)照孔相比,50%以上殺菌率的血清最高稀釋度為血清抗體殺菌滴度),結(jié)果見表3。
表2.各menb菌株全細(xì)胞elisa
表3.各menb菌株殺菌力實(shí)驗(yàn):bc50titer(1:)
備注:殺菌力實(shí)驗(yàn)以大于1:8為具有保護(hù)性。
由表2和表3的結(jié)果綜合分析可得,δfhbp蛋白疫苗能夠有效免疫所有表達(dá)fhbp(v1、v3和v2變體)的menb菌株的侵染,但對(duì)低表達(dá)甚至不表達(dá)fhbp的menb菌株失去保護(hù)能力;而δfhbp-nada蛋白疫苗在免疫所有表達(dá)fhbp(v1、v3和v2變體)的menb菌株的侵染的基礎(chǔ)上,同時(shí)能對(duì)低表達(dá)甚至不表達(dá)fhbp的menb菌株依然具有保護(hù)作用。同時(shí),δfhbp-nada蛋白疫苗能夠產(chǎn)生更高的抗體效價(jià)并具有更強(qiáng)的殺菌能力,說(shuō)明兩種特異性蛋白的融合表達(dá)能夠起到協(xié)同促進(jìn)免疫反應(yīng)的作用,并能提供更為廣譜的疫苗保護(hù)功能。因此,我們的后續(xù)工藝選擇δfhbp-nada重組蛋白作為新型多價(jià)腦膜炎球菌及肺炎球菌綴合疫苗的蛋白載體。
三、工程菌的發(fā)酵培養(yǎng)、誘導(dǎo)表達(dá)及大規(guī)模抗原蛋白濃縮純化
將上述鑒定正確的δfhbp-nada/bl21(de3)重組菌株按照藥典的要求制成原始種子庫(kù)和工作種子庫(kù)。工藝流程如下:
1.取工程菌株工作種子庫(kù)菌種,劃種lb瓊脂培養(yǎng)基(含卡納霉素),37℃培養(yǎng)過(guò)夜,挑取單個(gè)菌落接種至lb液體培養(yǎng)基(含50μg/ml卡納霉素)中,并以1-2%的接種比例逐步擴(kuò)大至發(fā)酵罐發(fā)酵培養(yǎng),待od600達(dá)到16-20時(shí),采用異丙基-β-d-硫代半乳糖苷(iptg)誘導(dǎo)培養(yǎng)4-8小時(shí),停止培養(yǎng),大容量離心機(jī)離心收集菌體。
2.取菌體加入破菌緩沖液(50mmpb,2mmedta,ph7.5),高壓(800-1000bar)均質(zhì)破菌二遍后,離心(10000rpm,60min,8℃)取上清。采用30-60%硫酸銨分級(jí)沉淀,50mmpbph7.5溶解,50kd超濾5次,并濃縮至原體積的1/5-1/3。
3.采用sepharoseqff層析,平衡液:50mmpbph7.2,洗脫液:50mmpb+1mnaclph7.2。洗脫方法:0-100%梯度洗脫,收集10%的洗脫液。
4.取10%梯度洗脫液經(jīng)50kd超濾膜包超濾濃縮,采用sepharose4ff凝膠過(guò)濾層析,收集v0處蛋白峰,以0.15mol/l氯化鈉、10kd超濾5次以上,并濃縮至蛋白含量為1-2mg/ml,0.22μm除菌過(guò)濾。經(jīng)無(wú)菌檢查、蛋白含量檢查、分子量和純度檢查、蛋白特異性檢查、細(xì)菌內(nèi)毒素檢查即為δfhbp-nada蛋白原液。
技術(shù)要求為得到純度大于95%的重組δfhbp-nada蛋白原液。細(xì)菌內(nèi)毒素不高于20eu/ml,本發(fā)明應(yīng)不高于10eu/ml,最佳不高于5eu/ml。分子量和純度檢查見圖7,純度為96.3%。蛋白特異性檢測(cè)如圖5所示,wb檢測(cè)為目標(biāo)蛋白。
四、多價(jià)nm多糖-δfhbp-nada蛋白綴合疫苗的制備和免疫效果評(píng)價(jià)
1.a群、c群、y群和w135群nm菌莢膜多糖的制備
a群腦膜炎球菌采用29201菌株,c群腦膜炎球菌采用29205菌株,y群腦膜炎球菌采用29028菌株,w135群腦膜炎球菌采用29037菌株,腦膜炎球菌經(jīng)發(fā)酵培養(yǎng)后,采用沙培離心機(jī)、碟片式離心機(jī)或其他大容量離心機(jī)分離培養(yǎng)液,收集離心上清;將離心上清以100kd膜包超濾濃縮,采用25-80%的乙醇進(jìn)行分級(jí)沉淀,收集沉淀并用無(wú)水乙醇及丙酮分別洗滌,得到粗制多糖;滅菌注射用水溶解多糖并經(jīng)脫氧膽酸鈉處理后,采用ge填料captoadhere和captodeae或其他廠家相同功能性質(zhì)的離子交換填料,以串聯(lián)層析或分步層析的方法進(jìn)行粗糖精制,收集流穿峰,采用gesephadexg25coarse對(duì)流穿峰進(jìn)行脫鹽,乙醇沉淀或凍干回收多糖,置于-20℃保存?zhèn)溆谩?/p>
2.a/c/y/w135群多糖-δfhbp-nada蛋白綴合疫苗的制備
本行業(yè)常用的方法有兩種,即胺還原法或溴化氰活化法制備多糖蛋白結(jié)合物。胺還原法為將a/c/y/w135群多糖經(jīng)高碘酸鈉避光氧化,再加己二酰肼(adh)和硼氰化鈉制備多糖衍生物,采用超濾方法將adh和硼氰化鈉等去除,然后加入制備好的δfhbp-nada載體蛋白,在碳二亞胺(edac)作用下,形成多糖蛋白結(jié)合物。溴化氰活化法為將a/c/y/w135群腦膜炎球菌多糖經(jīng)溴化氰(cnbr)活化,在活化的糖鏈上連接上己二酰肼,采用超濾的方法將溴化氰、游離的己二酰肼去除,然后加入制備好的δfhbp-nada載體蛋白,在碳二亞胺的連接作用下,多糖蛋白結(jié)合形成多糖蛋白復(fù)合物。
其中,溴化氰具有較強(qiáng)的活化多糖羥基的作用,目前國(guó)內(nèi)上市的a群和a、c群腦膜炎球菌多糖綴合疫苗均采用溴化氰活化多糖的方法制備。但由于使用劇毒化學(xué)試劑溴化氰,制備過(guò)程對(duì)人員和環(huán)境均具有較大的潛在風(fēng)險(xiǎn),結(jié)合物產(chǎn)率不高。隨著化學(xué)合成技術(shù)的發(fā)展,已成功研制了一種新型水溶性氰化物,即1-氰基-4-二甲基氨基吡啶-四氟化硼(1-cyano-4-dimethylamin-opyridiniumtetrafluoroborate,cdap)。應(yīng)用該試劑不僅消除了溴化氰的毒性,且活化效能明顯提高。有研究者將溴化氰與cdap兩種方法進(jìn)行比較,cdap法的多糖收率可達(dá)35%-40%,而溴化氰僅有5%-20%,且結(jié)合物仍具有良好的免疫原性。
因此,本發(fā)明應(yīng)用cdap活化多糖后衍化結(jié)合的工藝制備多價(jià)莢膜多糖-δfhbp-nada蛋白綴合疫苗。具體方法為:將a/c/y/w135群腦膜炎球菌多糖溶解至5-15mg/ml,調(diào)節(jié)ph值至10.8左右,在多糖溶液中加入1/10(g/g)的cdap,室溫、維持ph值10.8的堿性環(huán)境下活化多糖8min。按1:1(與活化多糖的體積比)的比例加入0.5mol/l的已二酰肼,室溫反應(yīng)50-70min。50kd膜包超濾去除溴化氰及已二酰肼,得到多糖衍生物。將多糖衍生物與載體蛋白δfhbp-nada以1:1(g/g)的比例混合并攪拌,按碳二亞胺:多糖=1:10的比例加入碳二亞胺,室溫、酸性環(huán)境(ph5.6)下反應(yīng)60min。經(jīng)100kd超濾膜包超濾去除雜質(zhì),并濃縮。最后采用gesepharose4ff進(jìn)行凝膠層析純化,收集v0附近的洗脫液。用0.22μm濾膜除菌過(guò)濾,得到a/c/y/w135群腦膜炎球菌多糖-δfhbp-nada蛋白綴合疫苗原液。
將此原液采用磷酸鋁佐劑攪拌吸附,以0.15mol/l氯化鈉稀釋配制,至多價(jià)多糖蛋白結(jié)合物以多糖含量計(jì)終濃度分別為20μg/ml,鋁含量終濃度為0.45-0.6mg/ml,攪拌均勻,以預(yù)填充注射器分裝,0.5ml/支,制成a/c/y/w135群腦膜炎球菌多糖-δfhbp-nada蛋白綴合疫苗制劑,2-8℃保存。也可在疫苗原液中加入80mg/ml蔗糖作為賦形劑,每支多糖含量20μg/ml凍干后制成蛋白疫苗制劑,2-8℃保存。
3.a/c/y/w135群多糖-δfhbp-nada蛋白綴合疫苗效果評(píng)價(jià)
小鼠免疫:分別用a/c/y/w135群多糖-δfhbp-nada蛋白綴合疫苗蛋白原液、凍干制劑和佐劑吸附制劑皮下免疫6周齡spf級(jí)nih小鼠10只,免疫劑量為每次0.2ml/只,免疫程序?yàn)?,2,4周,免疫結(jié)束后2周采血,離心收集血清;另設(shè)10只小鼠對(duì)照,相同方法注射生理鹽水。收集好的血清e(cuò)lisa法測(cè)血清抗體的滴度,具體方法如下:采用純化后的δfhbp-nada重組蛋白,分別以適宜劑量包被酶標(biāo)板,37℃孵育過(guò)夜,洗板后加入系列稀釋的待測(cè)小鼠血清,37℃孵育后洗板,加入辣根過(guò)氧化物酶標(biāo)記羊抗鼠igg二抗顯色,酶標(biāo)儀測(cè)定,讀取492nm(630nm為參比波長(zhǎng))吸光度值(a值)。陰性對(duì)照組血清a均值+3倍的標(biāo)準(zhǔn)偏差為cutoff值,待測(cè)血清a值大于cutoff值判為陽(yáng)性,以a值大于cutoff值的最大稀釋度計(jì)算各型別小鼠的幾何平均滴度,即為小鼠血清igg抗體效價(jià)(表4)。綴合疫苗原液和兩種劑型免疫小鼠后均產(chǎn)生了高低度的血清抗體。
表4.各組抗原三次免疫小鼠后血清抗體的滴度測(cè)定(幾何平均值)
綴合疫苗各劑型免疫效果的評(píng)價(jià),同樣采取兩種方法,全菌體包被測(cè)定全細(xì)胞elisa和流行株的殺菌力實(shí)驗(yàn)。全菌體包被選擇a群腦膜炎球菌29201菌株,b群腦膜炎球菌mc58和67/00菌株,c群腦膜炎球菌29205菌株,y群腦膜炎球菌29028菌株,w135群腦膜炎球菌29037菌株,將這些菌株擴(kuò)大培養(yǎng)增殖后,刮取細(xì)菌菌苔,以生理鹽水溶解,甲醛殺菌后,稀釋為2×108個(gè)/ml,以此濃度包被96孔酶標(biāo)板,100ul/孔,4℃包被過(guò)夜,洗板后,用相應(yīng)疫苗血清抗體進(jìn)行elisa檢測(cè),結(jié)果見表5。
表5.各群腦膜炎球菌菌株全細(xì)胞elisa
同樣,a群腦膜炎球菌29201菌株,b群腦膜炎球菌mc58和67/00菌株,c群腦膜炎球菌29205菌株,y群腦膜炎球菌29028菌株,w135群腦膜炎球菌29037菌株后用相應(yīng)疫苗血清抗體進(jìn)行殺菌檢測(cè),測(cè)定并計(jì)算殺菌抗體滴度(與補(bǔ)體陰性對(duì)照孔相比,50%以上殺菌率的血清最高稀釋度為血清抗體殺菌滴度),結(jié)果見表6。
表6.各群腦膜炎球菌菌株殺菌力實(shí)驗(yàn):bc50titer(1:)
備注:殺菌力實(shí)驗(yàn)以大于1:8為具有保護(hù)性。
由以上結(jié)果綜合分析可得,以重組δfhbp-nada為蛋白載體的新型多價(jià)腦膜炎球菌綴合疫苗具有廣譜的免疫效果,其免疫小鼠血清能與a、b、c、y和w135五個(gè)群的模式菌株產(chǎn)生交聯(lián)反應(yīng),同時(shí)能夠覆蓋b群中表達(dá)fhbp(3種變體)以及不表達(dá)fhbp但表達(dá)nada的高致病菌,并在殺菌檢測(cè)中表現(xiàn)出廣譜且極強(qiáng)的殺菌效果,從而保護(hù)人們(尤其是嬰幼兒及年老體弱者)免受絕大部分nm致病菌侵害導(dǎo)致的脊髓腦膜炎危害。
五、多價(jià)肺炎球菌-δfhbp-nada綴合疫苗的制備和免疫效果評(píng)價(jià)
重組δfhbp-nada是由生物工程技術(shù)制備得來(lái),是一種全新的可用于綴合疫苗的載體蛋白,不同于現(xiàn)有綴合疫苗工藝中常用蛋白載體(crm197、tt、omp、dt、hid),因而不會(huì)因同種蛋白載體接種過(guò)多導(dǎo)致綴合疫苗的免疫原性下降。同時(shí),δfhbp和nada雖然是nm生存和致病的重要因子,但其本身無(wú)毒性,從而在工業(yè)生產(chǎn)中不需要對(duì)該活性蛋白進(jìn)行脫毒處理,不會(huì)改變其結(jié)構(gòu)和抗原活性位點(diǎn),從而獲得更佳的免疫效果。再次,δfhbp-nada通過(guò)柔性連接肽鏈將兩個(gè)活性蛋白融合表達(dá),再保持各自的活性的同時(shí)讓兩者成為單一的蛋白質(zhì),因而在工業(yè)生產(chǎn)及免疫接種時(shí)更具有可控性,風(fēng)險(xiǎn)大大降低,又能提供更多的多糖-蛋白結(jié)合位點(diǎn)。因而,δfhbp-nada可作為新型優(yōu)質(zhì)的載體蛋白用于其他致病菌(如hib和spn)綴合疫苗的開發(fā),就像nm的膜蛋白o(hù)mp,hib的菌表面蛋白hid,完全可作為常規(guī)載體蛋白應(yīng)用。本發(fā)明以δfhbp-nada重組蛋白為載體,提供一種能覆蓋23種血清型的強(qiáng)免疫原性肺炎球菌綴合疫苗。δfhbp-nada重組蛋白原液制備如前所述,后續(xù)具體制備方案如下:
1.23種血清型spn菌莢膜多糖的制備
選取23種血清型(1、2、3、4、5、6b、7f、8、9n、9v、10a、11a、12f、14、15b、17f、18c、19a、19f、20、22f、23f、33f)的肺炎球菌發(fā)酵培養(yǎng)后,采用沙培離心機(jī)、碟片式離心機(jī)或其他大容量離心機(jī)分離培養(yǎng)液,收集離心上清;將離心上清以100kd膜包超濾濃縮,采用25-80%的乙醇進(jìn)行分級(jí)沉淀,收集沉淀并用無(wú)水乙醇及丙酮分別洗滌,得到粗制多糖;滅菌注射用水溶解多糖并經(jīng)脫氧膽酸鈉處理后,采用ge填料captoadhere和captodeae或其他廠家相同功能性質(zhì)的離子交換填料,以串聯(lián)層析或分步層析的方法進(jìn)行粗糖精制,收集流穿峰,采gesephadexg25coarse對(duì)流穿峰進(jìn)行脫鹽,乙醇沉淀或凍干回收多糖,置于-20℃保存?zhèn)溆谩?/p>
2.23價(jià)spn菌多糖-δfhbp-nada蛋白綴合疫苗的制備
同樣應(yīng)用cdap活化多糖后衍化結(jié)合的工藝制備多價(jià)莢膜多糖-δfhbp-nada蛋白綴合疫苗。具體方法為:將23種血清型spn菌多糖溶解至5-15mg/ml,調(diào)節(jié)ph值至10.8左右,在多糖溶液中加入1/10(g/g)的cdap,室溫、維持ph值10.8的堿性環(huán)境下活化多糖8min。按1:1(與活化多糖的體積比)的比例加入0.5mol/l的已二酰肼,室溫反應(yīng)50-70min。50kd膜包超濾去除溴化氰及已二酰肼,得到多糖衍生物。將多糖衍生物與載體蛋白δfhbp-nada以1:1(g/g)的比例混合并攪拌,按碳二亞胺:多糖=1:10的比例加入碳二亞胺,室溫、酸性環(huán)境(ph5.6)下反應(yīng)60min。經(jīng)100kd超濾膜包超濾去除雜質(zhì),并濃縮。最后采用gesepharose4ff進(jìn)行凝膠層析純化,收集v0附近的洗脫液。用0.22μm濾膜除菌過(guò)濾,得到23價(jià)spn菌多糖-δfhbp-nada蛋白綴合疫苗原液。
可將此原液采用磷酸鋁佐劑攪拌吸附,以0.15mol/l氯化鈉稀釋配制,至多價(jià)多糖蛋白結(jié)合物以多糖含量計(jì)終濃度分別為20μg/ml,鋁含量終濃度為0.45-0.6mg/ml,攪拌均勻,以預(yù)填充注射器分裝,0.5ml/支,制成23價(jià)spn菌多糖-δfhbp-nada蛋白綴合疫苗制劑,2-8℃保存。也可在疫苗原液中加入80mg/ml蔗糖作為賦形劑,每支多糖含量20μg/ml凍干后制成蛋白疫苗制劑,2-8℃保存。
3.23價(jià)spn菌多糖-δfhbp-nada蛋白綴合疫苗效果評(píng)價(jià)
小鼠免疫:23價(jià)spn菌多糖-δfhbp-nada蛋白綴合疫苗蛋白原液、市售23價(jià)陽(yáng)性對(duì)照疫苗制劑皮下免疫6周齡spf級(jí)nih小鼠10只,免疫劑量為每次0.2ml/只,免疫程序?yàn)?,2,4周,免疫結(jié)束后2周采血,離心收集血清;另設(shè)10只小鼠對(duì)照,相同方法注射生理鹽水。收集好的血清e(cuò)lisa法測(cè)血清抗體的滴度,具體方法如下:采用純化后23種各血清型多糖,分別以適宜劑量包被酶標(biāo)板,37℃孵育過(guò)夜,洗板后加入系列稀釋的待測(cè)小鼠血清,37℃孵育后洗板,加入辣根過(guò)氧化物酶標(biāo)記羊抗鼠igg二抗顯色,酶標(biāo)儀測(cè)定,讀取492nm(630nm為參比波長(zhǎng))吸光度值(a值)。陰性對(duì)照組血清a均值+3倍的標(biāo)準(zhǔn)偏差為cutoff值,待測(cè)血清a值大于cutoff值判為陽(yáng)性,以a值大于cutoff值的最大稀釋度計(jì)算各型別小鼠的幾何平均滴度,即為小鼠血清igg抗體效價(jià)(表7)。綴合疫苗蛋白原液和市售23價(jià)陽(yáng)性對(duì)照多糖疫苗免疫小鼠后均產(chǎn)生了高低度的血清抗體,且綴合疫苗蛋白原液產(chǎn)生的滴度更高,說(shuō)明蛋白抗原具有協(xié)同促進(jìn)免疫的功能。
表7.疫苗三次免疫小鼠后各種血清型抗體的滴度測(cè)定(幾何平均值)
綴合疫苗與市售多糖疫苗免疫效果的評(píng)價(jià),同樣采取兩種方法,全菌體包被測(cè)定全細(xì)胞elisa和流行株的殺菌力實(shí)驗(yàn)。全菌體包被選擇中國(guó)流行的高致病spn菌株血清型1、3、4、5、6b、7f、9v、14、18c、19a、19f、23f、33f,將這些菌株擴(kuò)大培養(yǎng)增殖后,刮取細(xì)菌菌苔,以生理鹽水溶解,甲醛殺菌后,稀釋為2×108個(gè)/ml,以此濃度包被96孔酶標(biāo)板,100ul/孔,4℃包被過(guò)夜,洗板后,用相應(yīng)疫苗血清抗體進(jìn)行elisa檢測(cè),結(jié)果見表8。
表8.各血清型肺炎球菌菌株全細(xì)胞elisa
同樣,高致病spn菌株血清型1、3、4、5、6b、7f、9v、14、18c、19a、19f、23f、33f培養(yǎng)后用相應(yīng)疫苗血清抗體進(jìn)行殺菌檢測(cè),測(cè)定并計(jì)算殺菌抗體滴度(與補(bǔ)體陰性對(duì)照孔相比,50%以上殺菌率的血清最高稀釋度為血清抗體殺菌滴度),結(jié)果見表9。
表9.各血清型肺炎球菌菌株殺菌力實(shí)驗(yàn):bc50titer(1:)
備注:殺菌力實(shí)驗(yàn)以大于1:8為具有保護(hù)性。
由以上結(jié)果綜合分析可得,以重組δfhbp-nada為蛋白載體的新型23價(jià)肺炎球菌綴合疫苗具有廣譜的免疫效果,其免疫小鼠血清能與1、2、3、4、5、6b、7f、8、9n、9v、10a、11a、12f、14、15b、17f、18c、19a、19f、20、22f、23f、33f血清型spn菌株多糖抗原產(chǎn)生交聯(lián)反應(yīng),同時(shí)能夠覆蓋中國(guó)流行的血清型1、3、4、5、6b、7f、9v、14、18c、19a、19f、23f、33f菌株,并在殺菌檢測(cè)中表現(xiàn)出廣譜且極強(qiáng)的殺菌效果,從而保護(hù)人們(尤其是嬰幼兒及年老體弱者)免受絕大部分肺炎球菌致病菌侵害導(dǎo)致肺炎,此類多糖-蛋白綴合疫苗更適合我國(guó)人群使用。
以上所述僅為本發(fā)明的較佳實(shí)施例,并不用以限制本發(fā)明,凡在本發(fā)明的精神和原則之內(nèi),所作的任何修改、等同替換、改進(jìn)等,均應(yīng)包含在本發(fā)明的保護(hù)范圍之內(nèi)。
序列表
<110>武漢博沃生物科技有限公司
<120>重組δfhbp-nada融合蛋白載體及其制備方法和應(yīng)用
<130>2017
<160>5
<170>patentinversion3.3
<210>1
<211>274
<212>prt
<213>人工合成
<400>1
metasnargthralaphecyscysleupheleuthrthralaleuile
151015
leuthralacysserserglyglyglyglyserglyserglyglyval
202530
alaalaaspileglythrglyleualaaspalaleuthrthrproleu
354045
asphislysasplysglyleulysserleuthrleugluaspserile
505560
proglnasnglythrleuthrleuseralaglnglyalaglulysthr
65707580
phelysalaglyasplysaspasnserleuasnthrglylysleulys
859095
asnasplysileserargpheaspphevalglnlysilegluvalasp
100105110
glyglnthrilethrleualaserglyglupheglniletyrlysgln
115120125
asphisseralavalvalalaleuglnileglulysileasnasnpro
130135140
asplysileaspserleuileasnglnargserpheleuvalsergly
145150155160
leuglyglygluhisthralapheasnglnleuproglythralaphe
165170175
glyseraspaspalaserglylysleuthrtyrthrileasppheala
180185190
alalysglnglyhisglylysilegluhisleulysserprogluleu
195200205
asnvalaspleualaalaseraspilelysproasplyslysarghis
210215220
alavalileserglyservalleutyrasnglnalaglulysglyser
225230235240
tyrserleuglyilepheglyglyglnalaglngluvalalaglyser
245250255
alagluvalgluthralaasnglyilearghisileglyleualaala
260265270
lysgln
<210>2
<211>825
<212>dna
<213>人工合成
<400>2
atgaaccgaactgccttctgctgccttttcctgaccaccgccctgattctgaccgcctgc60
agcagcggaggcggcggaagcggaagcggcggtgtcgccgccgacatcggcacggggctt120
gccgatgcactaactacgccgctcgaccataaagacaaaggtttgaaatctctgacattg180
gaagactccattccccaaaacggaacactaaccctgtcggcacaaggtgcggaaaaaact240
ttcaaagccggcgacaaagacaacagcctcaacacgggcaaactgaagaacgacaaaatc300
agccgcttcgacttcgtgcaaaaaatcgaagtggacggacaaaccatcacgctggcaagc360
ggcgaatttcaaatatacaaacaggaccactccgccgtcgttgccctacagattgaaaaa420
atcaacaaccccgacaaaatcgacagcctgataaaccaacgctccttccttgtcagcggt480
ttgggcggagaacataccgccttcaaccaactgcccggcacggcattcggttcagacgat540
gccagtggaaaactgacctacaccatagatttcgccgccaagcagggacacggcaaaatc600
gaacatttgaaatcgccagaactcaatgttgacctggccgcctccgatatcaagccggat660
aaaaaacgccatgccgtcatcagcggttccgtcctttacaaccaagccgagaaaggcagt720
tactctctaggcatctttggcgggcaagcccaggaagttgccggcagcgcagaagtggaa780
accgcaaacggcatacgccatatcggtcttgccgccaagcagtaa825
<210>3
<211>76
<212>dna
<213>人工合成
<400>3
aagcttggcggcggcggcagtggcggcggcggcagtggcggcggcggcagtatgaaacac60
tttccatccaaagtac76
<210>4
<211>651
<212>prt
<213>人工合成
<400>4
metasnargthralaphecyscysleupheleuthrthralaleuile
151015
leuthralacysserserglyglyglyglyserglyserglyglyval
202530
alaalaaspileglythrglyleualaaspalaleuthrthrproleu
354045
asphislysasplysglyleulysserleuthrleugluaspserile
505560
proglnasnglythrleuthrleuseralaglnglyalaglulysthr
65707580
phelysalaglyasplysaspasnserleuasnthrglylysleulys
859095
asnasplysileserargpheaspphevalglnlysilegluvalasp
100105110
glyglnthrilethrleualaserglyglupheglniletyrlysgln
115120125
asphisseralavalvalalaleuglnileglulysileasnasnpro
130135140
asplysileaspserleuileasnglnargserpheleuvalsergly
145150155160
leuglyglygluhisthralapheasnglnleuproglythralaphe
165170175
glyseraspaspalaserglylysleuthrtyrthrileasppheala
180185190
alalysglnglyhisglylysilegluhisleulysserprogluleu
195200205
asnvalaspleualaalaseraspilelysproasplyslysarghis
210215220
alavalileserglyservalleutyrasnglnalaglulysglyser
225230235240
tyrserleuglyilepheglyglyglnalaglngluvalalaglyser
245250255
alagluvalgluthralaasnglyilearghisileglyleualaala
260265270
lysglnglyglyglyglyserglyglyglyglyserglyglyglygly
275280285
sermetlyshispheproserlysvalleuthrthralaileleuala
290295300
thrphecysserglyalaleualaalathrseraspaspaspvallys
305310315320
lysalaalathrvalalailevalalaalatyrasnasnglyglnglu
325330335
ileasnglyphelysalaglygluthriletyraspileglygluasp
340345350
glythrilethrglnlysaspalathralaalaaspvalglualaasp
355360365
aspphelysglyleuglyleulyslysvalvalthrasnleuthrlys
370375380
thrvalasngluasnlysglnasnvalaspalalysvallysalaala
385390395400
glusergluileglulysleuthrthrlysleualaaspthraspala
405410415
alaleualaaspthraspalaalaleuaspgluthrthrasnalaleu
420425430
asnlysleuglygluasnilethrthrphealaglugluthrlysthr
435440445
asnilevallysileaspglulysleuglualavalalaaspthrval
450455460
asplyshisalaglualapheasnaspilealaaspserleuaspglu
465470475480
thrasnthrlysalaaspglualavallysthralaasnglualalys
485490495
glnthralaglugluthrlysglnasnvalaspalalysvallysala
500505510
alagluthralaalaglylysalaglualaalaalaglythralaasn
515520525
thralaalaasplysalaglualavalalaalalysvalthraspile
530535540
lysalaaspilealathrasnlysalaaspilealalysasnserala
545550555560
argileaspserleuasplysasnvalalaasnleuarglysgluthr
565570575
argglnglyleualagluglnalaalaleuserglyleupheglnpro
580585590
tyrasnvalglyargpheasnvalthralaalavalglyglytyrlys
595600605
sergluseralavalalaileglythrglypheargphethrgluasn
610615620
phealaalalysalaglyvalalavalglythrserserglyserser
625630635640
alaalatyrhisvalglyvalasntyrglutrp
645650
<210>5
<211>1959
<212>dna
<213>人工合成
<400>5
atgaaccgaactgccttctgctgccttttcctgaccaccgccctgattctgaccgcctgc60
agcagcggaggcggcggaagcggaagcggcggtgtcgccgccgacatcggcacggggctt120
gccgatgcactaactacgccgctcgaccataaagacaaaggtttgaaatctctgacattg180
gaagactccattccccaaaacggaacactaaccctgtcggcacaaggtgcggaaaaaact240
ttcaaagccggcgacaaagacaacagcctcaacacgggcaaactgaagaacgacaaaatc300
agccgcttcgacttcgtgcaaaaaatcgaagtggacggacaaaccatcacgctggcaagc360
ggcgaatttcaaatatacaaacaggaccactccgccgtcgttgccctacagattgaaaaa420
atcaacaaccccgacaaaatcgacagcctgataaaccaacgctccttccttgtcagcggt480
ttgggcggagaacataccgccttcaaccaactgcccggcacggcattcggttcagacgat540
gccagtggaaaactgacctacaccatagatttcgccgccaagcagggacacggcaaaatc600
gaacatttgaaatcgccagaactcaatgttgacctggccgcctccgatatcaagccggat660
aaaaaacgccatgccgtcatcagcggttccgtcctttacaaccaagccgagaaaggcagt720
tactctctaggcatctttggcgggcaagcccaggaagttgccggcagcgcagaagtggaa780
accgcaaacggcatacgccatatcggtcttgccgccaagcagtaaggcggcggcggcagt840
ggcggcggcggcagtggcggcggcggcagtatgaaacactttccatccaaagtactgacc900
acagccatccttgccactttctgtagcggcgcactggcagccacaagcgacgacgatgtt960
aaaaaagctgccactgtggccattgttgctgcctacaacaatggccaagaaatcaacggt1020
ttcaaagctggagagaccatctacgacattggtgaagacggcacaattacccaaaaagac1080
gcaactgcagccgatgttgaagccgacgactttaaaggtctgggtctgaaaaaagtcgtg1140
actaacctgaccaaaaccgtcaatgaaaacaaacaaaacgtcgatgccaaagtaaaagct1200
gcagaatctgaaatagaaaagttaacaaccaagttagcagacactgatgccgctttagca1260
gatactgatgccgctctggatgaaaccaccaacgccttgaataaattgggagaaaatata1320
acgacatttgctgaagagactaagacaaatatcgtaaaaattgatgaaaaattagaagcc1380
gtggctgataccgtcgacaagcatgccgaagcattcaacgatatcgccgattcattggat1440
gaaaccaacactaaggcagacgaagccgtcaaaaccgccaatgaagccaaacagacggcc1500
gaagaaaccaaacaaaacgtcgatgccaaagtaaaagctgcagaaactgcagcaggcaaa1560
gccgaagctgccgctggcacagctaatactgcagccgacaaggccgaagctgtcgctgca1620
aaagttaccgacatcaaagctgatatcgctacgaacaaagctgatattgctaaaaactca1680
gcacgcatcgacagcttggacaaaaacgtagctaatctgcgcaaagaaacccgccaaggc1740
cttgcagaacaagccgcgctctccggcctgttccaaccttacaacgtgggtcggttcaat1800
gtaacggctgcagtcggcggctacaaatccgaatcggcagtcgccatcggtaccggcttc1860
cgctttaccgaaaactttgccgccaaagcaggcgtggcagtcggcacttcgtccggttct1920
tccgcagcctaccatgtcggcgtcaattacgagtggtaa1959
- 還沒(méi)有人留言評(píng)論。精彩留言會(huì)獲得點(diǎn)贊!
- Pcna融合蛋白及表達(dá)方法和生物素化方法
- 一種人類金屬硫蛋白-2a融合蛋白表達(dá)載體的制作方法
- 一種人類金屬硫蛋白-4融合蛋白表達(dá)載體的制作方法
- 一種人類金屬硫蛋白-1融合蛋白表達(dá)載體的制作方法
- 一種伴侶樣蛋白的融合蛋白表達(dá)載體的制作方法
- 一種融合蛋白cmfo及其應(yīng)用
- 抗蟲蛋白、抗蟲融合蛋白、編碼基因、載體及應(yīng)用
- 一種酶融合表達(dá)蛋白及其在蝦青素生產(chǎn)方面的應(yīng)用
- 一種醋酸纖維膜載體上蛋白抗體孵育結(jié)合實(shí)驗(yàn)裝置的制造方法
- 一株高表達(dá)Neuritin截短體蛋白的畢赤酵母重組菌株及其應(yīng)用