化合物及其用途的制作方法與工藝
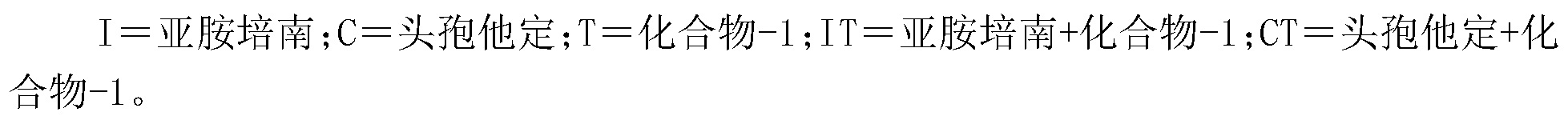
本發明所述的是β-內酰胺化合物作為β-內酰胺酶抑制劑的用途,其類似物、衍生物、互變異構形式、立體異構體、多晶型物、溶劑合物、藥學上可接受的鹽、酯、前藥及其代謝物用于與合適的抗生素組合治療細菌感染的用途。本發明描述了用于治療細菌感染的這些化合物的藥物組合物。本文所描述的化合物用作檢測β-內酰胺酶的診斷試劑。
背景技術:
β-內酰胺類抗生素,即青霉素類,頭孢菌素類,碳青霉烯類,單環β-內酰胺類是經常使用的抗生素。已知由微生物產生的β-內酰胺酶水解β-內酰胺環,從而使抗菌活性失活。為了抑制β-內酰胺酶,將β-內酰胺酶抑制劑與抗生素聯合給藥。這些抑制劑與β-內酰胺酶結合后比單獨β-內酰胺抗生素能發揮更大的作用。這種組合幫助抗生素發揮其抗菌效果,而其抗菌效果不會因β-內酰胺酶而下降。幾種抗生素/β-內酰胺酶抑制劑的組合在市場上已存在,例如,氨芐西林/舒巴坦,阿莫西林/克拉維酸,替卡西林/克拉維酸,哌拉西林/他佐巴坦等。這些β-內酰胺/β-內酰胺酶抑制劑組合抗生素用于在社區和在醫院環境中治療產β-內酰胺酶的細菌引起的感染-但除了碳青霉烯酶和抑制劑抗性的β-內酰胺酶。抗菌藥物,尤其是β-內酰胺抗生素的廣泛使用帶來的日益增長的問題是在抗生素耐藥性方面的發展。抗生素耐藥性的一個重要誘因在于β-內酰胺酶(例如,碳青霉烯酶,頭孢菌素酶,青霉素酶,ESBL,抑制劑抗性的β-內酰胺酶,等)。在許多已知的β-內酰胺酶中,碳青霉烯酶(例如,KPC,Sme,NMC-A,IMI等)是最近發現的,它們可水解所有類別的β-內酰胺抗生素(Drawz,S.M.和Bonomo,R.A.Clin.Microbiol.Rev.2010,23(1),160-201)。已知這些酶有多藥耐受性(MDR)的作用。考慮到開發有效抵抗不斷變化的β-內酰胺酶的β-內酰胺酶抑制劑(BLI)方面的迫切需要,我們的研究工作致力于鑒定潛在的由式(I)的化合物得到的BLI。為解決對于特定檢測β-內酰胺酶的合適診斷方法的需要,使用式(I)化合物確定診斷方法。已知許多β-內酰胺酶抑制劑在文獻中公開,而式(A)的化合物公開于US4,562,073中,其中R1為氫或三烷基甲硅烷基;R2為氫、三烷基甲硅烷基或COOR2',其中R2'為氫,C1-18烷基,C2-7烷氧基甲基,C3-8烷基羰基氧甲基,C4-9烷基羰基氧乙基、(C5-7環烷基)羰基氧甲基,C9-14苯甲基羰基氧甲基,C3-8烷氧基羰基甲基,C4-9烷氧基羰基乙基,酞基,2(5H)-呋喃酮-4-基,γ-丁內酯-4-基,被1至3個鹵素原子取代的鹵代C1-6烷基,C1-6烷氧基或硝基取代的或未取代的苯甲基,二苯甲基,四氫吡喃基,二甲基氨基乙基,二甲基氯硅烷基,三氯甲硅基,(5-取代的C1-6烷基或苯基或未取代的-2-氧代-1,3-二氧環戊烷(dioxoden)-4-基)甲基,C8-13苯甲酰基氧烷基或用于形成藥學上可接受的鹽的集團;且R3與以上R2'有相同的含義。我們的專利,US7,687,488B2(印度同族IN1217CHE2006)公開了式(B)化合物。這些化合物被證明能夠增強抗生素的活性。式中,A=C或N;Het為三至七元雜環;R1代表羧酸根陰離子或-COOR4,其中R4代表氫,羧酸保護基團或藥學上可接受的鹽;R2和R3可以為相同或不同的,并各自獨立地表示氫,鹵素,氨基,保護的氨基或任選被取代的烷基,烯基,炔基等,R表示取代或未取代的烷基,烯基,芳基,芳烷基,環烷基,氧代基,雜環基,雜環烷基。人們對于β-內酰胺酶抑制劑有廣泛的需求,因為它們能抑制β-內酰胺酶等酶,特別是產碳青霉烯酶多藥抗性細菌。此外,對于抗生素,特別是β-內酰胺類抗生素和克服了細菌耐藥性的和β-內酰胺酶抑制劑的組合的需求仍未被滿足。發明目的本發明的一個目的是使用式(Ⅰ)的β-內酰胺化合物作為β-內酰胺酶抑制劑與合適的抗生素組合用于治療產β-內酰胺酶的細菌引起的感染,該β-內酰胺酶如碳青霉烯酶,頭孢菌素酶,青霉素酶,ESBL,抑制劑抗性β-內酰胺酶,ESBL等。本發明的另一個目的是提供一種藥物組合物,其將式(I)化合物與合適的抗生素組合。本發明的還另一個目的是提供一種治療或預防宿主的細菌感染的方法,該宿主通常是動物且最典型的是人,該方法包括向宿主將治療量的式(I)化合物或藥學上可接受的鹽和/或其前藥以及β-內酰胺抗生素一起施用。本發明的另一目的是提供一種用于檢測β-內酰胺酶的診斷試劑。所述β-內酰胺酶屬于KPC家族(例如,KPC-2,KPC-3)及ESBL(例如,SHV18)生產腸桿菌。本發明的另一目的是恢復/增強抗生素,尤其是β-內酰胺抗生素,如青霉素類,頭孢菌素類,碳頭孢烯、氧頭孢烯,碳青霉烯類,青霉烷類,頭霉素類,青霉烯類和單環β-內酰胺,通過與式(I)的化合物組合對于碳青霉烯酶和ESBL的活性。因此,本發明的一個目的是提供一種用于抑制β-內酰胺酶的化合物;和/或包含所述化合物的藥物組合物;和/或用于抑制細胞中的β-內酰胺酶的改進的方法;和/或用于治療和/或預防β-內酰胺酶介導的疾病的改進的方法,和/或與β-內酰胺抗生素一起用于治療和/或預防細菌感染的改進方法;和/或恢復/增強抗生素的活性的方法;或者至少向公眾提供一種有用的選擇。
技術實現要素:
這里所描述的是式(I)化合物,其衍生物,類似物,互變異構形式,立體異構體,多晶型物,溶劑合物,藥學上可接受的組合物,代謝物,前藥,藥學上可接受的鹽和酯的方法或用途;特別地,本文所提供的是式(Ⅰ)化合物,它們的衍生物,類似物,互變異構形式,立體異構體,多晶型物,溶劑合物,代謝物,前藥,水合物,藥學上可接受的鹽和酯,用于抑制β-內酰胺酶的用途,該β-內酰胺酶包括碳青霉烯酶,頭孢菌素酶,青霉素酶,ESBL,細菌所產生的抗抑制劑的β-內酰胺酶;增強/恢復抗生素的活性的用途,包括向有需要的受試者施用治療有效量的式(I)化合物;其中A=C或N;Het代表取代的或未取代的三至七元雜環;R1代表羧酸根陰離子或-COOR4,其中R4代表氫,C1-C6烷基,C6-C10芳基,C6-C10芳基C1-C6烷基甲氧基苯甲基,硝基苯甲基,甲硅烷基,二苯基甲基、普塞基、醋氧乙基、環庚塞基、匹伏基、海替基(hexetil)、達羅塞特或其藥學上可接受的鹽;R2和R3可以相同或不同,且獨立地代表氫,鹵素,氨基,選自三苯甲基氨基,酰氨基(如苯基乙酰基氨基),苯氧基乙酰氨基和苯甲酰基氨基的保護的氨基或任選取代的C1-C6烷基,C2-C6烯基和C2-C6炔基;R表示取代或未取代的C1-C6烷基,C2-C6烯基,C6-C10芳基、C6-C10芳基C1-C6烷基、C3-C12環烷基,氧代基,雜環基和雜環烷基,在基團R,R2和R3被取代時,該取代基可為選自以下的一種或多種:低級烷基(C1-C4烷基,如甲基,乙基,丙基和異丙基);低級烷氧基(C1-C4烷氧基,如甲氧基,乙氧基和丙氧基);低級烷硫基(C1-C4烷硫基,如甲硫基和乙硫基);低級烷氨基(C1-C4烷氨基,如甲氨基,乙氨基和丙氨基);環(低級)烷基(C5-C6環烷基,如環戊基和環己基);環(低級)烯基(C5-C6環烯基如環己烯基和環己二烯基);羥基;鹵素(氯,溴,氟和碘);氨基;保護的氨基;氰基;硝基;氨基甲酰基;-CONHC1-C4烷基-COO-C1-C4烷基;羧基;保護的羧基;-COO-C1-C4烷基;-CO-雜環基;磺酰基;氨磺酰基;亞氨基;氧代基;氨基(低級)烷基,如氨基甲基,氨基乙基和氨基丙基;鹵代(低級)烷基如三氟甲基(-CF3),氟甲基,氟乙基,溴甲基和二氟甲基;羧酸和羧酸衍生物,如異羥肟酸,酯和酰胺。優選的取代基為C1-C4烷基,C1-C4烷氧基,C1-C4烷硫基,C1-C4烷氨基,羥基,鹵素及三鹵甲基。該取代物任選進一步被C1-C4烷氧基羰基C1-C4烷基,羥基C1-C4烷基;C1-C4烷基,C6-C10芳基,雜環基和酯。一方面,本文提供的是式(Ⅱ)化合物,其衍生物,類似物,互變異構形式,立體異構體,多晶型物,溶劑合物,代謝物,前藥,水合物,藥學上可接受的鹽和酯,用于抑制細菌所產生的碳青霉烯酶;增強/恢復抗生素活性,包括向有需要的受試者施用治療有效量的式(II)化合物;其中L=C或N;R,R1,R2和R3如上所述。R5代表氫,C1-C6烷基,C1-C6烷氧基,C1-C6烷硫基,C1-C6烷氨基,羥基,鹵素及三鹵甲基;且m為0,1或2。另一方面,本文提供的是化合物,其用于治療和/或預防由產碳青霉烯酶細菌引起的感染,包括向有需要的受試者給予治療有效量的式(I)化合物。在還另一方面,本文提供的是化合物,其用于治療和/或預防產碳青霉烯酶細菌引起的感染,包括向有需要的受試者施用治療有效量的式(I)化合物,并與合適的抗生素組合使用。在還另一方面,本文提供的是化合物,其用于治療由革蘭氏陰性菌表達的β-內酰胺酶引起的感染。在還另一方面,本文提供的是用于使用的化合物,其中細菌選自肺炎克雷伯桿菌(Klebsiellapneumoniae)和大腸桿菌(E.coli)。在還另一方面,本文提供的是用于使用的化合物,其中所述碳青霉烯酶選自KPC-2和KPC-3。在還另一方面,本文提供的是用于治療或預防產碳青霉烯酶細菌引起的感染的方法,該方法包括施用治療有效量的式(I)化合物。本文的另一方面包括腸桿菌和非腸桿菌表達的β-內酰胺酶的檢測。本文的還另一個方面包括式(I)化合物作為檢測β-內酰胺酶的診斷試劑的用途。所述β-內酰胺酶屬于KPC-2,KPC-3的家庭,以及ESBL例如產SHV18腸桿菌。在一個實施例中,此處提供的是包含式(I)化合物的藥物組合物,其作為治療或預防產碳青霉烯酶細菌所引起的感染的活性成分。在另一實施方案中,本文所提供的是包含式(I)化合物的藥物組合物,其與以下組分一起作為治療或預防產碳青霉烯酶細菌所引起的感染的活性成分:a.一種或多種式(Ⅰ)化合物;b.一種或多種抗生素,和c.一種或多種藥學上可接受的載體。在還另一實施例中,該抗生素選自β-內酰胺抗生素類。在還另一實施例中,本文提供的是以下化合物:(2S,3S,5R)-3-甲基-3-(3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜雙環[3.2.0]庚烷-2-羧酸酯和(2S,3S,5R)-3-甲基-3-(4-甲基-3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸酯,它們的衍生物、類似物,互變異構形式,立體異構體,多晶型物,溶劑合物,代謝物,前藥,藥學上可接受的鹽和酯。在還另一方面,化合物(2S,3S,5R)-3-甲基-3-(3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜雙環[3.2.0]庚烷-2-羧酸酯;(2S,3S,5R)-3-甲基-3-(4-甲基-3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸酯及其衍生物,類似物,互變異構形式,立體異構體,多晶型物,溶劑合物,代謝物,前藥,藥學上可接受的鹽和酯,其用于抑制β-內酰胺酶,該β-內酰胺酶不限于,碳青霉烯酶,頭孢菌素酶,青霉素酶,ESBL和抑制劑抗性β-內酰胺酶的用途。在還另一些方面中,本文所描述的是式(I)化合物,其用于治療和/或預防耐受抗生素的細菌。附圖說明:圖1:檢測KPCβ-內酰胺酶的雙紙片協同試驗。具體實施方式式(I)的β-內酰胺化合物,其衍生物,類似物,互變異構形式,立體異構體,多晶型物,溶劑合物,其藥學上可接受的組合物,其藥學上可接受的鹽和酯,它們用于抑制由細菌產生的碳青霉烯酶;增強/恢復抗生素活性,其中:Het為三至七元雜環,該雜環可具有合適的取代基,優選的雜環基如吡咯基,吡咯啉基,咪唑基,吡唑基,吡啶基,嘧啶基,吡嗪基,哌啶基,呋喃基,噻吩基,吡咯烷基,哌嗪基,噁唑烷基,噻唑基,噠嗪基,四唑基(例如1H-四唑基,2H-四唑基等),咪唑基,三唑基,1,2,4-噁二唑基,1,3,4-噁二唑基,1,2,5-噁二唑基,1,2,3-噻二唑基,1,2,4-噻二唑基,1,3,4-噻二唑基和1,2,5-噻二唑基。所定義的雜環基可任選地被一個或多個取代基取代,合適的取代基例如:低級烷基(C1-C4烷基,如甲基,乙基和丙基),低級烷氧基(C1-C4烷氧基如甲氧基,乙氧基和丙氧基),低級烷硫基(C1-C4烷硫基,如甲硫基和乙硫基),低級烷氨基(C1-C4烷氨基如甲氨基,乙氨基和丙氨基),環(低級)烷基(C5-C6環烷基,如環戊基和環己基);環(低級)烯基(C5-C6環烯基如環己烯基和環己二烯基),羥基,鹵素(氯,溴,氟和碘);氨基;保護的氨基;氰基;硝基;羧基;保護的羧基,氨磺酰基;亞氨基;氧代基;氨基(低級)烷基(氨基甲基,氨基乙基和氨基丙基);鹵素和三鹵甲基(-CF3)。優選的取代基為C1-C4烷基,C1-C4烷氧基,C1-C4烷硫基,C1-C4烷氨基,羥基,鹵素和三鹵甲基。該取代物任選進一步被取代。通常情況下,基團Het是未取代的或帶有一個或多個如上文所定義的取代基。優選地,Het表示包含一個或兩個雜原子(包括季銨化的氮)的五到六元雜環。更優選Het選自吡咯基、吡咯啉基、咪唑基、三唑基、吡唑基、吡啶基、嘧啶基、吡嗪基、哌啶基、呋喃基、噻吩基、吡咯烷基、哌嗪基、噁唑烷基、噻唑基、噠嗪基、吡咯烷基和咪唑烷基。優選地,Het是芳環。更優選地,Het表示五元雜環;R1代表羧酸根陰離子或-COOR4,其中R4表示氫,-C6烷基,C6-C10芳基,C6-C10芳基C1-C6烷基,甲氧基苯甲基,硝基苯甲基,甲硅烷基,二苯基甲基,普塞基,醋氧乙基、環庚塞基、匹伏基、海替基、達羅塞特根(daloxate)或其藥學上可接受的鹽;R2和R3各自獨立地表示氫,鹵素,氨基,如三苯甲基氨基的保護的氨基,如苯基乙酰氨基的酰氨基,苯氧基乙酰氨基和苯甲酰基氨基,任選取代的烷基,烯基或炔基;優選地,R選自-(CH2)n-CH3,-(CH2)nC6H5,-(CH2)n-CH=CH2,-CH2-CONH2,包括-CH2COOBut的-CH2-COO-(C1-C4烷基),-(CH2)nCO-雜環基,-CH2-CONH-(CH2)n-COOEt,其中n是從0到5的整數。更優選地,R為-(CH2)n-CH3,-(CH2)nC6H5,-(CH2)n-CH=CH2,-CH2-CONH2或-CH2COOBut。本文所使用的,C1-C6烷基基團或部分為直鏈或支鏈的含1至6個碳原子的烷基基團或部分。通常地,C1-C6烷基基團或部分為C1-C4烷基或部分。C1-C4烷基基團或部分是包含1至4個碳原子的直鏈或支鏈的烷基或部分。C1-C6烷基基團和部分的實例包括,但不限于、甲基、乙基、正丙基、異丙基、正丁基、異丁基、叔丁基、3-甲基-丁基、戊基和己基。C1-C4烷基基團和部分的實例包括,但不限于,甲基、乙基、正丙基、異丙基、正丁基、異丁基和叔丁基。為免生疑問,在一組中存在兩個烷基部分時,該烷基部分可以是相同或不同的,其可任選地被一個或多個取代基取代。術語“C2-C6烯基”是指含有碳-碳雙鍵,并且可以為具有約2至6個碳原子的直鏈或支鏈的脂肪族烴基,其可任選地被一個或多個取代基取代。優選的烯基包括,但不限于,乙烯基、1-丙烯基、2-丙烯基、異丙烯基、2-甲基-1-丙烯基、1-丁烯基和2-丁烯基。本文所使用的,C6-C10芳基基團或部分通常是苯基或萘基。苯基為優選的。術語“C6-C10芳基C1-C6烷基”指直接鍵合至烷基的芳基,其可以任選被一個或多個取代基取代。優選的芳烷基包括,但不限于,-CH2C6H5,-C2H4C6H5,-CH(CH3)C6H5等。本文所用的,術語“雜環基”指5至10元雜環基團或部分為單環的非芳族,飽和或不飽和的C5-C10的碳環,其中一個或多個,例如1,2,3或4個碳原子被選自N,O,S,S(O)和S(O)2的雜原子取代。通常情況下,它是5至6元環。合適的雜環基團和部分包括吡唑烷基,哌啶基,哌嗪基,硫代嗎啉基,S-氧代-硫代嗎啉基,S,S-二氧代-硫代嗎啉基,嗎啉基,吡咯烷基,吡咯啉基,咪唑烷基,咪唑啉基,1,3-二氧戊環基,1,4-二氧雜環戊烯基和吡唑啉基和部分。吡唑烷基,哌啶基,哌嗪基,吡唑烷基,嗎啉基和咪唑基和部分是優選的。術語“雜環基烷基”指與烷基直接鍵合的雜環基,其可以被取代或未被取代。術語“C3-C12環烷基”指約3至12個碳原子的非芳族單環或多環系統,其可任選地被一個或多個取代基取代。優選的環烷基包括,但不限于,環丙基,環丁基,環戊基,環己基,環辛基和十氫萘基。術語“類似物”包括通過一個或多個C,N,O或S原子與母體結構不同的化合物。因此,某一化合物中母體結構的N原子之一被S原子取代后為該化合物的類似物。術語“衍生物”指從式(I)的化合物利用簡單的化學處理過程,例如通過氧化,氫化,烷基化,酯化,鹵化等轉化一個或多個的官能團得到的化合物,類似物,互變異構形式,立體異構體,多晶型物,水合物,其藥學上可接受的鹽或藥學上可接受的溶劑合物。術語“立體異構體”包括在原子的空間排列上彼此不同但其化學式和結構都相同的異構體。立體異構體包括對映異構體和非對映異構體。術語“互變異構體”包括可容易地相互轉換的處于平衡狀態的化合物的異構體形式。酮-烯醇互變異構現象是一個示例。術語“多晶型物”包括晶型上不同形式,而在化學上具有相同結構的化合物。術語“藥學上可接受的溶劑合物”包括溶劑分子與溶質化合物的分子或離子的組合。具有β-內酰胺酶抑制性質的代表性的化合物(1-13)包括但不限于:1.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-1-氮雜雙環[3.2.0]庚-3-基]甲基}-3-甲基-1H-1,2,3-三唑-3-鎓;2.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-l-氮雜雙環[3.2.0]庚-3-基]甲基}-3-乙基-1H-1,2,3-三唑-3-鎓;3.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-l-氮雜雙環[3.2.0]庚-3-基]甲基}-3-正丙基-1H-1,2,3-三唑-3-鎓;4.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-l-氮雜雙環[3.2.0]庚-3-基]甲基}-3-烯丙基-1H-1,2,3-三唑-3-鎓;5.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-l-氮雜雙環[3.2.0]庚-3-基]甲基}-3-(2-氨基-2-氧代乙基)-1H-1,2,3-三唑-3-鎓和對應的酸;6.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-l-氮雜雙環[3.2.0]庚-3-基]甲基}-3-(2-叔丁氧基-2-氧代乙基)-1H-1,2,3-三唑-3-鎓和對應的酸;7.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-l-氮雜雙環[3.2.0]庚-3-基]甲基}-3-(2-嗎啉-4-基-2-氧代乙基)-1H-1,2,3-三唑-3-鎓和對應的酸;8.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-l-氮雜雙環[3.2.0]庚-3-基]甲基}-3-{2[(2-乙氧基-2-氧代乙基)氨基]-2-氧代乙基}-1H-1,2,3-三唑-3-鎓和對應的酸;9.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-l-氮雜雙環[3.2.0]庚-3-基]甲基}-3-{2-[(3-乙氧基-3-氧丙基)氨基]-2-氧乙基}-1H-1,2,3-三唑-3-鎓和對應的酸;10.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-l-氮雜雙環[3.2.0]庚-3-基]甲基}-3-(2-{[1-(乙氧基羰基)-2-羥基丙基]氨基}-2-氧代乙基)-1H-1,2,3-三唑-3-鎓和對應的酸;11.l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-l-氮雜雙環[3.2.0]庚-3-基]甲基}-3-苯甲基-1H-1,2,3-三唑-3-鎓和對應的酸;12.(2S,3S,5R)-3-甲基-3-(3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜雙環[3.2.0]庚烷-2-羧酸酯和對應的酸;13.(2S,3S,5R)-3-甲基-3-(4-甲基-3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸酯和對應的酸。這些化合物(1至11)通過US7,687,488(印度同族IN1217CHE2006)提供的如下方法制備。化合物12和13根據如下所示反應方案制備:其中Het為式(IV)化合物通過在步驟1中將式(VI)化合物與式(V)化合物的反應獲得。在步驟2中,式(IV)化合物轉化為式(III)化合物。式(III)化合物向式(I)化合物的轉化可使用選自六甲基二硅氮烷(HMDS),三甲基氯硅烷(TMCS),三甲基碘硅烷(TMSI),N,O-雙-(三甲基甲硅烷基)-乙酰胺(BSA),甲基三甲基甲硅烷基三氟乙酰胺(MSTFA),Ν,Ο-雙(三甲基甲硅烷基)三氟乙酰胺(BSTFA),甲基二氯硅烷,二甲基二氯硅烷,二苯基二氯硅烷,N-甲基甲硅烷基乙酰胺(MSA),雙三甲基甲硅烷基脲等的甲硅烷基化劑,在試劑存在下進行,該試劑例如丙酮,甲醇,四氫呋喃,氯仿,二氯甲烷,二氯乙烷,乙酸乙酯,N,N-二甲基甲酰胺(DMF),二甲基乙酰胺(DMAc)等或其混合物。式(I)化合物通過將式(III)化合物與合適的R-X(X=鹵素)反應獲得。本文所描述的β-內酰胺化合物優選形成為內鹽。當R上的代表性取代為羧酸或氨基時,它可被進一步轉化成藥學上可接受的鹽。用于制造羧酸基團的鹽的堿選自以下的堿:氫氧化鈉,甲醇鈉,碳酸氫鈉,碳酸鈉,碳酸氫鉀,碳酸鉀,氫氧化鈣,氫氧化鎂等,在如醚,四氫呋喃,甲醇,叔丁醇,二噁烷,異丙醇,乙醇等溶劑中。也可使用溶劑的混合物。也可以使用合適的酸制備酸加成鹽。形成本發明的一部分的化合物的立體異構體可通過使用以其單一對映體形式的反應物,以所有可能的工藝制備,或通過將該反應在單一對映體形式的試劑或催化劑存在下進行,或利用常規方法將立體異構體的混合物解析。一些優選的方法包括利用微生物拆分(resolution),解析手性酸如扁桃酸,樟腦磺酸,酒石酸,乳酸等只要是可適用的手性酸形成的非對映異構體鹽,或通過使用手性堿如馬錢子堿,金雞納生物堿,它們的衍生物及其類似物進行。式(I)化合物的前藥也是本發明所考慮的。前藥是一種有活性的或無活性的化合物,在向患者施用后其經體內生理學活性進行化學改性,如水解,代謝等處理成本發明的化合物。在制造,使用前藥方面的適用性和涉及的技術為本領域技術人員熟知。通式(I)的化合物的各種多晶型物可以通過將式(I)化合物在不同條件下的結晶制備,這些條件在現有技術中為已知。例如,使用不同的常用溶劑或它們的混合物進行重結晶,在不同溫度下結晶,各種模式的冷卻,其范圍包括結晶過程中從非常快至非常慢的冷卻。多晶型物也可以通過以下方式獲得,將化合物加熱或使其熔化,然后逐漸冷卻或快速冷卻。多晶型的存在可通過固體探針NMR光譜,紅外光譜,差示掃描量熱法,粉末X射線衍射或此類其他技術檢測。式(I)化合物的藥學上可接受的溶劑合物可通過常規方法制備,如將式(I)化合物溶解在溶劑,例如水,甲醇,乙醇中,以及以下的溶劑的混合物中,如丙酮:水,二噁烷:水,N,N-二甲基甲酰胺:水等,優選為水,并通過使用不同的結晶方法重結晶。應注意,本文所描述的化合物可含有可以互變異構形式存在的基團,并且雖然本文中一種形式被命名,說明,顯示和/或要求保護,但所有的形式應認為固有地包括在這樣的名稱,說明,顯示和主張中。本文公開的β-內酰胺化合物與β-內酰胺抗生素組合可用于治療人和其他溫血動物的微生物感染,它們可同時經腸胃外,局部和/或口服給藥。除了式(I)化合物,該藥物組合物也可包含一種或多種已知藥物或與之共同施用,其中該已知藥物選自其它臨床上有用的抗生素制劑,如青霉素類(哌拉西林,替卡西林等),頭孢菌素類(頭孢他定,頭孢美唑,頭孢噻肟等),青霉烯類(法羅培南,美羅培南,厄他培南等),碳頭孢烯(洛拉卡比等),氧頭孢烯(拉氧頭孢,拉他頭孢,氟氧頭孢等),頭霉素類(頭孢替坦等)單酰胺菌素類(氨曲南、替吉莫南等),氨基糖苷類(鏈霉素,慶大霉素,阿米卡星等),細菌素類(大腸桿菌素,小菌素等),喹諾酮類(環丙沙星,莫西沙星等),磺胺類(磺胺甲噁唑等),大環內酯類(紅霉素,羅紅霉素,阿奇霉素等),四環素類(多西環素,米諾環素等),甘氨酰環素類(替加環素(Tigecycline)等),噁唑烷酮類(利奈唑來,特里唑來(Torezolid),雷得唑來(Radezolid)等),脂肽類(達托霉素等),多肽類(放線菌素,桿菌肽,粘菌素,多粘菌素B等),多烯抗真菌劑類(那他霉素,制霉菌素,兩性霉素B等),利福霉素類(利福平,利福布汀,利福噴汀等),氯霉素等,或它們的衍生物。抗生素包括青霉素類,頭孢菌素類,碳頭孢烯類,氧頭孢烯類、碳青霉烯類,青霉烷類,頭霉素類,表霉烯(penem)類、單酰胺菌素類或它們的組合。青霉素類包括,但不限于,氮卓西林(美西林)、阿莫西林,氨芐西林,戊青霉素、阿帕西林,阿撲西林,阿度西林,阿洛西林,巴氨西林,羧芐青霉素,卡茚西林、氯甲西林、氯唑西林、環西林(環己西林),雙氯西林,依匹西林、芬貝西林、氟氯青霉素(氟氯西林),海他西林,侖氨西林、美坦西林,甲氧西林,美洛西林,萘夫西林,苯唑西林,培那西林、青霉素G乙胺酯(Penethecillin),青霉素G(普魯卡因青霉素),青霉素N,青霉素O,青霉素V(苯氧甲基青霉素),青霉素B、哌拉西林,匹氨西林,丙匹西林、喹那西林、磺芐西林、酞氨西林、替莫西林,替卡西林,匹美西林,芐星青霉素,芐青霉素,復合阿莫西林克拉維酸(Co-amoxiclav)、侖氨西林或它們的組合。頭孢菌素類包括,但并不限于頭孢噻啶,頭孢雷定,頭孢西丁,頭孢乙腈,頭孢哌酮,頭孢甲肟(Cefinenoxime),頭孢甘酸(Cephaloglycin),頭孢尼西,頭孢地嗪,頭孢匹羅,頭孢匹胺,頭孢唑蘭,頭孢噻利,頭孢瑞南、頭孢咪唑、頭孢克定、頭孢泊肟酯,頭孢特侖,頭孢卡品,頭孢吡普(Ceftobiprole),頭孢洛林(ceftaroline)、頭孢喹肟,頭孢噻呋,頭孢維星(Cefovecin),頭孢羥氨芐,頭孢洛寧,頭孢吡肟,頭孢噻肟,頭孢他啶,頭孢他美,頭孢托侖,頭孢噻啶,頭孢他啶,頭孢曲松、頭孢拉宗,頭孢噻吩,頭孢唑林,頭孢匹林,頭孢替唑,頭孢孟多,頭孢替安,頭孢替安己酯,頭孢呋辛,頭孢唑肟,頭孢甲肟,頭孢唑喃,頭孢磺啶,頭孢美唑,頭孢米諾,頭孢氨芐,頭孢拉定,頭孢克洛,頭孢羥氨芐,頭孢洛寧,頭孢丙烯,頭孢呋肟酯,頭孢克肟,頭孢泊肟酯,頭孢布烯,頭孢地尼,CXA-101(FR264205)或它們的組合;青霉烯類包括,但不限于,法羅培南和碳青霉烯類包括但不限制于美羅培南,厄他培南(Ertapenem),多利培南,比阿培南,帕尼培南,利替培南、替比培南、頭茂培南(Tomopenem)、硫培南、阿祖培南(Razupenem),亞胺培南,ME1036、SM216601,或它們的組合。單酰胺菌素類包括但不限于,氨曲南、卡蘆莫南、替吉莫南BALI9764,BAL30072或它們的組合。與式(I)化合物組合使用的β-內酰胺類抗生素也可與氨基糖苷類、桿菌素類,喹諾酮類,磺胺類,大環內酯類,四環素類,甘氨酰環素類,噁唑烷酮類,脂肽類,多肽類,利福霉素,氯霉素,多烯抗真菌劑類和它們的衍生物共同給藥。式(I)化合物也可包含殺菌性/通透性增加蛋白產物(BPI)或流出泵抑制劑或與之共同給予,以改善抗革蘭氏陰性菌和耐抗微生物劑的細菌的活性。抗病毒劑,抗寄生蟲劑,抗真菌劑和其他抗生素也可與式(I)化合物組合給予。以合適的抗生素的組合方式的式(I)化合物可用于治療患者的細菌感染,術前患者,術后患者,重癥監護病房(ICU)患者的,醫院感染患者和獸醫的患者。該藥物組合物可以為常用的形式,如片劑,膠囊劑,丸劑,顆粒劑,散劑,糖漿劑,錠劑,溶液,懸浮液,氣霧劑,透皮貼劑,外用藥膏,軟膏等,可在合適的固體或液體載體或稀釋劑中包含矯味劑,甜味劑等,,或在適宜的無菌介質中包含上述物質以形成可注射溶液或懸浮液。該藥物組合物還可包含現有技術中已知的藥學上可接受的載體。本發明化合物可以單獨或與如上所述包含任何試劑的抗生素化合物/試劑一起冷凍干燥。該試劑包括配位劑或抗凝血劑,抗氧化劑,穩定劑,氨基糖苷類,藥學上可接受的鹽等或它們的混合物。可對稀釋的溶液或濃縮的溶液進行冷凍干燥,這根據最終產品所要求的品質進行。在冷凍干燥或凍干或解凍之前,可將冷凍干燥物進行脫氣以達到最佳氣體濃度。該化合物可以在無菌條件下過濾。也可使用適當的過濾器,如超濾,以充分減少半乳甘露聚糖的水平。式(I)化合物也可與合適的抗菌劑物理共混。式(I)化合物也可用于治療產β-內酰胺酶(特別是KPC-2)細菌引起的感染。除了式(I)化合物,該藥物組合物還可能包含緩沖液,如檸檬酸鈉,乙酸鈉,酒石酸鈉,碳酸鈉,碳酸氫鈉,嗎啉丙磺酸,其他的磷酸鹽緩沖液等,和螯合劑,如乙二胺四乙酸(EDTA),二亞乙基三胺五乙酸,羥基乙二胺三乙酸,次氮基三乙酸,1,2-二氨基環己烷四乙酸,雙(2-氨基乙基)乙二醇四乙酸,1,6-丙二胺四乙酸等或它們的藥學上可接受的鹽。式(I)化合物可用于治療或預防宿主中的細菌感染,該宿主通常是動物且最典型為人,包括向宿主給予治療量的式(I)化合物或其藥學上可接受的鹽和/或其前藥,以及β-內酰胺抗生素。術語“預防”或“防止”是指防止疾病,即,使疾病的臨床癥狀不發展。術語治療(“treatment'/'treating”)是指對于哺乳動物疾病的任何治療,包括:(a)抑制疾病,即,減緩或阻止臨床癥狀的發展,和/或(b)緩解疾病,即,引起臨床癥狀消退。術語“治療有效量”或“有效量”是指,如下文定義的,在單獨或與其他治療方法組合施用于需要這種治療的哺乳動物時,足以有效治療的式(I)化合物的化合物或混合物的量。術語“增強”是指由一種試劑增強另一種試劑的作用效果,使得總體效果大于兩種試劑的任一種的效果總和。本文使用的術語“用于使用的化合物”包含任何一個或多個以下的情況:(1)化合物的使用,(2)化合物的使用方法,(3)用于治療的用途,(4)制造用于治療的藥物組合物/藥劑的用途或(5)治療/預防/減少/抑制的方法,其包括向有需要的受試者給予有效量的式(I)化合物。術語“受試者”是指有細菌感染的患者,術前患者,術后患者,處于ICU的患者,醫院內感染的患者,社區獲得的感染和獸醫。從前面的描述中,本領域技術人員可以很容易地確定本發明的本質特征而在不會脫離本發明的精神和范圍的情況下對本發明進行各種變化和修改,以使其適應各種用途和癥狀。術語一旦被描述,則對于該術語的相同含義適用于整個專利。參考化合物1(化合物1)l-{[(2S,3S,5R)-2-羧基-3-甲基-4,4,7-三氧代-4-硫雜-1-氮雜雙環[3.2.0]庚-3-基]甲基}-3-甲基-1H-1,2,3-三唑-3-鎓;于25-30℃下,向(2S,3S,5R)-3-甲基-7-氧代-3-(1H-1,2,3-三唑-1-基甲基)-4-硫雜-l-氮雜雙環-[3.2.0]庚烷-2-羧酸4,4-二氧化物(25g)的丙酮(100mL)懸液中在攪拌條件下緩慢加入N,O-雙(甲硅烷基)乙酰胺(18.6g)。將反應混合物在該溫度(25-30℃)下攪拌15-20分鐘。向所得的澄清溶液中以15分鐘的時長加入甲基碘(100ml),并在25-30℃攪拌24小時。通過過濾分離沉淀的固體,然后用丙酮(25mL)洗滌。得到的固體的濕重為30g。上述濕固體用純化水(300mL)在10-15℃下攪拌2.5小時。向所得的反應混合物中加入硫代硫酸鈉(0.1g),并在10-15℃下攪拌10-15分鐘。向該反應混合物中加入二氯甲烷(300mL),攪拌并分離有機層。將水層用安伯萊特(Amberlite)LA-2樹脂溶液(在二氯甲烷中的5%的溶液)洗滌兩次,然后用二氯甲烷洗滌兩次。向該水溶液中,加入活性炭(1g),攪拌15分鐘,過濾,并用純化水(25mL)洗滌。將該溶液過濾并冷凍干燥以得到純的形式的標題化合物(10g)。1HNMR(400MHz,DMSO-d6)δppm:1.39(s,3H),3.14(dd,J=16.0,1.3Hz,1H),3.55(dd,J=16.0,4.2Hz,1H),3.97(s,1H),4,34(s,3H),5.05(dd,J=4.2,1.3Hz,1H),5.29(d,J=14.7Hz,1H),5.42(d,J=14.7HZ,1H),8,91(d,J=1.3Hz,1H),8.99(d,J=1.3Hz,1H).質量m/z:M+1峰于315處。或者可對該溶液進行噴霧干燥以得到標題化合物。化合物-12(2S,3S,5R)-3-甲基-3-(3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜雙環[3.2.0]庚烷-2-羧酸酯步驟1:(2S,3S,5R)-3-(咪唑-1-基甲基)-3-甲基-7-氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯的制備向咪唑(1.696g,24.9mmol)的乙腈(75mL)和水(25mL)的攪拌溶液中加入碳酸氫鈉(4.18g,49.8mmol),并將所得物質攪拌15分鐘。將(2S,3S,5R)-3-氯甲基-3-甲基-7-氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯(10g,24.8mmol)加入到上述混合物中,并在25-30℃下攪拌24小時。反應完成后,將反應物用乙酸乙酯和水的混合液稀釋。分離有機層。將水層再次用乙酸乙酯提取。用無水硫酸鈉干燥合并的有機層,并在真空條件下濃縮以得到粗品(2S,3S,5R)-3-(咪唑-1-基甲基)-3-甲基-7-氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯。產量:10g。步驟2:制備(2S,3S,5R)-3-(咪唑-1-基甲基)-3-甲基-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯在先前步驟中得到的粗品(2S,3S,5R)-3-(咪唑-1-基甲基)-3-甲基-7-氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯(10g)溶解于乙腈(50mL)中。將乙酸和水的混合液加入到上述溶液中,并冷卻至0-5℃。向該均相反應混合物中加入高錳酸鉀(14.59g,92.3mmol)。在0-5℃下再連續攪拌2小時。將反應物用偏亞硫酸氫鈉溶液驟冷。將反應物用乙酸乙酯和水的混合液稀釋。分離有機層,將水層用乙酸乙酯提取。將合并的有機層用飽和的碳酸氫鈉溶液中和。將有機層用無水硫酸鈉干燥,并減壓濃縮。向得到的殘余物中加入丙酮,并攪拌30分鐘。有白色固體析出,將其過濾并干燥。產量:2.60g(22.4%)。1HNMR(400MHz,DMSO-d6)δppm:1.09(s,3H),3.35(d,J=16.0Hz,1H),3.76(dd,J=16.0,2.0Hz,1H),4.42(d,J=15.6Hz,1H),4.90(d,J=15.6Hz,1H),5.10(s,1H),5,26(m,1H),6.89(s,2H),6.98(s,1H),7.33-7.50(m,11H).質量m/z:466(M+1).步驟3:制備(2S,3S,5R)-3-(咪唑-1-基甲基)-3-甲基-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸(化合物-M)向(2S,3S,5R)-3-(咪唑-1-基甲基)-3-甲基-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯(900mg,1.9mmol)的甲醇(20mL)溶液中加入10%的Pd/C(900mgw/w)并在氫氣氣氛下攪拌2小時。將反應物過濾,并用甲醇洗滌。將濾液在減壓下蒸發。向殘余物中加入乙醚(30mL),并攪拌15分鐘。將析出的白色固體過濾并用乙醚洗滌。產量:530mg(91.3%)。1HNMR(400MHz,DMSO-d6)δppm:1.38(s,3H),3.28(d,J=16,4Hz,1H),3.68(dd,J=16.4,4.4Hz,1H),4.51(d,15.2Hz,1H),4.53(s,1H),4.84(d,J=15.2Hz,1H),5.14-5.15(m,1H),7.02(s,1H),7.25(s,1H),7.85(s,1H)·質量m/z:300(M+1).步驟4:制備(2S,3S,5R)-3-甲基-3-(3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜雙環[3.2.0]庚烷-2-羧酸酯向(2S,3S,5R)-3-(咪唑-1-基甲基)-3-甲基-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸(450mg,1.5mmol)在無水丙酮(1.8mL)中的懸液中緩慢加入N,O-雙(甲硅烷基乙酰胺)(0.93mL,3.7mmol),同時攪拌。將反應物再攪拌15分鐘。向得到的澄清溶液中加入甲基碘(1.8mL)并在25-30℃下攪拌2天。將反應物濃縮,并用二氯甲烷-水稀釋。分離有機層。將水層用安伯萊特LA-2樹脂溶液(在二氯甲烷中的30%溶液)洗滌,接著用二氯甲烷洗滌。將水層進行脫氣,并冷凍干燥得到標題化合物。熔點:161.37℃。1HNMR(400MHz,D2O)δppm:1.53(s,3H),3.47(dd,J=16.7,1.36Hz,1H),3.70(dd,J=16.7,4.2Hz,1H),3.94(s,3H),4.41(s,1H),4.99(ABquartet,J=15.4Hz,2H),5.09(m,1H),7.53(s,1H),7.64(s,1H),8.99(s,1H).質量m/z:314(M+1),化合物13(2S,3S,5R)-3-甲基-3-(4-甲基-3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸酯。步驟1:制備(2S,3S,5R)-3-(4-甲基-咪唑-1-基甲基)-3-甲基-7-氧代-4-硫雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯向(2S,3S,5R)-3-氯甲基-3-甲基-7-氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯(3g,7.4mmol)在乙腈(22.5mL))的攪拌溶液中加入碳酸氫鈉(628mg,7.4mmol),水(7.5mL)和4-甲基-咪唑(1.22g,7.4mmol)。將所得物在25-30℃下攪拌42小時。將反應物用乙酸乙酯和水的混合液稀釋。分離有機層。將水層再次用乙酸乙酯提取。對合并的有機層用無水硫酸鈉干燥,并真空濃縮,得到粗(2S,3S,5R)-3-(4-甲基咪唑-1-基甲基)-3-甲基-7-氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯。產量:3.5g。步驟2:制備(2S,3S,5R)-3-(4-甲基-咪唑-1-基甲基)-3-甲基-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯。將前一步驟獲得的粗(2S,3S,5R)-3-(4-甲基-咪唑-1-基甲基)-3-甲基-7-氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯(3.5g,7.8mmol)溶解于乙腈(18mL)中。然后向上述溶液中加入乙酸(18mL)和水(9mL)混合液并冷卻至0-5℃。向該均質反應混合物中加入高錳酸鉀(2.47g,15.6mmol)。0-5℃再繼續攪拌2小時。然后將反應物用偏亞硫酸氫鈉溶液淬火,并用乙酸乙酯和水稀釋。分離有機層,將水層用乙酸乙酯提取。將合并的有機層用飽和的碳酸氫鈉溶液中和。將有機層用無水硫酸鈉干燥并減壓濃縮。使用硅膠柱色譜法(用40-50%乙酸乙酯的己烷溶液梯度洗脫)純化粗化合物得到純化合物,為無色固體。產量:350mg(10%)。1HNMR(400MHz,CDCl3,δppm):1.00(s,3H),2.17(s,3H),3.50(dd,J=16.2Hz,1.8Hz,1H),3.57(dd,J=16.2Hz,4.1Hz,1H),4.24(d,J=15.3Hz,1H),4.50(s,1H),4.61-4.62(m,1H),6.53(s,1H),6.99(s,1H),7.05(s,1H)7.32-7.49(m,10H).步驟3:制備(2S,3S,5R)-3-甲基-3-(4-甲基-3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯向(2S,3S,5R)-3-(4-甲基-咪唑-1-基甲基)-3-甲基-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯(350mg,0.6mmol)在無水丙酮(4mL)中的懸液中加入碘甲烷(4mL)在25-30℃下攪拌15小時。將反應物濃縮并用硅膠柱色譜純化(用0-10%MeOH的二氯甲烷溶液梯度洗脫)得到產物,為淺黃色固體,產量:320mg(96%)。1HNMR(400MHz,CDCl3,δppm):1.35(s,3H),2.30(s,3H),3.47(dd,J=16.4Hz,1.7Hz1H),3.58(dd,J=16.4Hz,4.4Hz1H),3.89(s,3H),4.6(s,1H),4.69(m,1H),4.89(ABquartet,J=15.9Hz,2H),7.01(s,1H),7.26(s,1H),7.32-7.49(m,10H),9.83(s,1H).步驟4:制備(2S,3S,5R)-3-甲基-3-(4-甲基-3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸酯向(2S,3S,5R)-3-甲基-3-(4-甲基-3-甲基-咪唑-3-鎓-1-基甲基)-4,4,7-三氧代-4-硫雜-1-氮雜-雙環[3.2.0]庚烷-2-羧酸二苯甲基酯(310mg,0.62mmol)的懸液中加入間甲酚(3mL),并在室溫攪拌過夜。向反應混合物中加入己烷(3×25mL)并攪拌5分鐘,然后傾析。向其中加入乙醚(15mL)中。將得到的固體用水稀釋,并用安伯萊特LA-2樹脂(在二氯甲烷中的30%溶液)處理,接著用二氯甲烷處理。將水層冷凍干燥得到產物,為淺黃色固體。產量:130mg(75%)。1HNMR(400MHz,D2O)δppm:1.52(s,3H),2.31(s,3H),3.47(dd,J=16.7Hz,1.3Hz1H),3.71(dd,J=16.7Hz,4.1Hz1H),3.80(s,3H),4.39(s,1H),4.92(ABquartet,J=15.4Hz,2H),5.08(m,1H),7.38(s,1H),8.86(s,1H).質量m/z:328(M+1).以下示例僅以說明性方式提供,且不應被視為限制本發明的范圍。對于本領域技術人員顯而易見的變動和改變將處于本發明的范圍和性質中。生物學:產KPC/ESBL腸桿菌的檢測在本實驗中,化合物-1用作診斷試劑,用于檢測屬于KPC&ESBL家族(例如,SHV18)的β-內酰胺酶生產腸桿菌的診斷試劑。一套簡單的在瓊脂培養基上的浸漬有抗生素的吸收紙盤用于該檢測。當該菌株表達β-內酰胺酶時,與化合物-1組合的抑菌圈將明顯大于單獨的抗生素時的情況。方法1:·0.5麥克法蘭的試驗菌以1:10稀釋接種于穆勒-海頓瓊脂平板上試驗菌:肺炎克雷伯菌(Klebsiellapneumoniae)(K.p)ATCCBAA-1705,肺炎克雷伯菌(Klebsiellapneumoniae)(K.p)ATCC700603,大腸桿菌(E.c)Ecoli233·碳青霉烯(例如,亞胺培南[IPM]10μg)和頭孢菌素(例如,頭孢他啶[CAZ]30μg)紙盤(7mm)放置在接種的瓊脂平板上。·化合物-1(60μg)盤放置在距離碳青霉烯和頭孢菌素紙盤為7和10mm處。·由于化合物-1存在的協同作用亞胺培南或頭孢他啶的抑菌圈擴大,以此測量表達的碳青霉烯酶或ESBL的存在。結果:觀察到協同作用,因為鄰近含化合物-1紙盤的亞胺培南或頭孢他啶抑菌圈增加(圖1)。方法2:除了以下改變,該方法與方法1相同:·向相同的紙盤上加入化合物-1(60μg)與碳青霉烯(例如,亞胺培南10μg)或頭孢菌素(例如,頭孢他定30μg)的組合并放在接種的瓊脂平板上。·以亞胺培南或頭孢他啶與10化合物1組合的抑菌圈直徑與單獨的抗生素情況的比較的增加來測量表達的碳青霉烯酶或ESBL的存在。結果化合物-1對碳青霉烯酶或ESBL的抑制活性通過亞胺培南或頭孢他啶與化合物-1的組合與單獨抗生素相比抑菌圈直徑(表1)增加來證明(圖1)。圖(A),(B)及(C)中的方法1顯示了在位于10mm和7mm的距離時鄰近含化合物-1的盤的亞胺培南或頭孢他啶的抑菌圈增加。圖(A),(B)和(C)中的方法2顯示了亞胺培南或頭孢他啶與化合物-1(IT&CT)組合而不是單獨的抗生素(I&C)的抑菌圈的增加。(D)中的兩種方法都沒有顯示抑菌圈的增加,且化合物-1不顯示任何的抑菌圈,這是由于菌株中沒有β-內酰胺酶。有KPC酶的分離株(isolate)的結果顯示于表1中。表1:具有A類碳青霉烯酶和ESBL的臨床分離株的抑菌圈(ZOI)·化合物-1增加了頭孢他啶分別抗測試的產KPC2和KPC3菌株的抑菌圈,分別從12增加至18.5mm,從11增加至22.5mm。·化合物-1增加了亞胺培南分別抗測試的產KPC2和KPC3菌株的抑菌圈,分別從14.5增加至20mm,且從14mm增加至20mm。·化合物-1增加了頭孢他啶抗測試的產SHV18菌株的抑菌圈,從12mm增加至23mm,而在有或沒有化合物-1存在的亞胺培南的直徑沒有變化,這表明亞胺培南自身具有抗這種菌株的活性。·對β-內酰胺酶陰性菌株的抗性,化合物-1對頭孢他啶或亞胺培南都沒有任何影響,因為這兩種抗生素自身都具有抗這種菌株的活性。結論:化合物-1可以用作一種診斷工具,用于檢測包括KPC的β-內酰胺酶。體外試驗本文描述的式(I)的β-內酰胺化合物與β-內酰胺抗生素類組合用于對它作為抗碳青霉烯酶的β-內酰胺酶抑制劑的作用進行評估。在此對本文所述化合物進行了體外評估,對于抗例如產KPC及表達KPC細菌的革蘭氏陰性菌株的抗菌活性進行了評估,用這些酶進行了β-內酰胺酶抑制測定。在雜環氮原子上被取代的β-內酰胺化合物顯示出顯著的β-內酰胺酶抑制性。對于對比研究,他唑巴坦,克拉維酸和舒巴坦與β-內酰胺抗生素類一起使用。碳青霉烯類,頭孢菌素類,單酰胺菌素和青霉烯類(包括獸醫使用的那些)被選中作為抗菌試劑。通過確定最小抑制濃度(MIC)進行的體外抗菌試驗:肉湯微稀釋法通過肉湯微量稀釋或瓊脂稀釋法對β-內酰胺化合物針對體外抗菌活性進行測試,該方法于美國臨床和實驗室標準化研究所(CLSI),(原NCCLS)公布的文件中描述。批準的標準M7-A7,2006年1月,CLSI,Wayne,賓夕法尼亞州,美國和M100-S18,2008年1月,CLSI,Wayne,賓夕法尼亞州,美國。協同肉湯微量稀釋MIC以棋盤格形式進行,采用一系列濃度的抗菌劑與幾種濃度的BLI化合物和其他比較BLI試劑在96孔微量滴定板中進行。簡要地說,β-內酰胺抗生素類的儲液(例如,2560&1280μg/mL)是由水,0.1M的磷酸鹽緩沖液,pH6.0或pH7.0或相應的合適的溶劑制成。同樣地,制備了包含化合物-1的BLI試劑的儲液,β-內酰胺抗生素濃度設定為0.06-128μg/mL。包含BLI化合物的BLI試劑在濃度為1-64μg/mL的范圍內被測試。所有的工作溶液都用陽離子調整的穆勒海頓肉湯(caMHB)進行適當的稀釋。在96孔微量滴定板的孔中連續地用caMHB從工作溶液對抗菌劑進行2倍稀釋。含有BLI化合物的BLI劑也被連續稀釋然后將各待測試的濃度加入到每個不同的抗菌濃度中。BLI化合物,其他比較BLI和所有的抗菌劑也單獨進行測試。通過挑選3至5個孔具有相同形態外觀的菌落制備細菌接種物,該菌落來自于18-24h時長培養基,并調整生理鹽水懸浮液的濁度為0.5麥氏濁度標準,其相當于細菌數量為1x108菌落形成單位(CFU)每mL懸浮液。用caMHB對懸浮液以1:100稀釋以得到約lxl06CFU/mL的菌群作為接種物。將該細菌接種物加入到含caMHB以及抗菌劑或抗菌劑+BLI劑的微量滴定板的孔中,并且細菌接種物體積與caMHB以及抗菌劑或抗菌劑+BLI劑的總體積相同。因此,最終接種物變成一半(約5x105CFU/mL)并且所測試的抗菌劑和組合的濃度也變成一半。將接種的板在35℃在環境氣氛下孵育18-20小時。在光學鏡輔助下用肉眼觀察孵育后的板,并將MIC記錄為濃度,其顯示了接種培養物沒有生長或視覺的濁度。在簡要瓊脂稀釋法中,用于獸醫用途(例如,2mg/mL)的頭孢菌素的儲液用水,0.1M磷酸鹽緩沖劑或合適的溶劑制備,并將溶液連續2倍稀釋。化合物-1溶解于水中且他唑巴坦(比較BLI)溶解于0.1M磷酸鹽緩沖液中,其pH為6.0,以得到1mg/mL的溶液。頭孢菌素濃度限定為0.5-32μg/mL。對于組合,本文所述的他唑巴坦或化合物-1以固定的4μg/mL的濃度,與濃度范圍為0.5至32μg/mL的頭孢菌素類一起測試。將單獨的頭孢菌素和與化合物-1或各濃度的他唑巴坦組合的頭孢菌素加入至20mL的熔融的已冷卻至40-50℃的穆勒海頓瓊脂中,并倒在陪替氏(petri)培養皿中。式(I)化合物和他唑巴坦也單獨進行了測試。通過從18-24h時長培養物中選取3至5孔具有相同的形態外觀的分離的菌落制備細菌接種物,并將生理鹽水懸液的濁度調節至0.5麥克法蘭濁度標準,其相當于約1×108CFU/mL懸液。用鹽水將該懸液以1:10稀釋,得到約1x107CFU/mL的菌群作為接種物。將該細菌接種物用多點接種器接種到所制備的陪替氏培養皿上,其中每個接種點含有1xl04CFU的菌株。接種的陪替氏培養皿在35℃環境氣氛下孵育18-20小時。孵育后,將該陪替氏培養皿放置在暗的非反射表面,且MIC記錄為濃度,其顯示接種的培養沒有生長。表2:亞胺培南與β-內酰胺酶抑制劑(BLI)化合物-12組合時抗肺炎克雷伯氏菌碳青霉烯酶(KPC)生產菌株的最小抑菌濃度(MIC)NA:不能獲得*表型上觀察到AmpC的存在化合物-12顯示了在與化合物-1類似的范圍內具有增強的抗KPC(2&3)產生菌株的活性,而化合物-M僅有中等活性活性,且不在預期活性范圍內。表3a:青霉烯類或單菌霉素/化合物-1抗產KPC-2肺炎克雷伯菌(ATCCBAA-1705)的MICIMP:亞胺培南,MER:美羅培南,ERT:厄他培南,FAR:法羅培南&AZT:氨曲南。在≥4μg/mL濃度時化合物-1與亞胺培南和美羅培南協同作用優于他唑巴坦或克拉維酸或舒巴坦抗產KPC-2菌株ATCCBAA1705。與上述比較物相比,在64μg/mL的濃度,它也表現出與厄他培南,法羅培南和氨曲南的更好的協同作用(表3a)。同樣地,該系列中以下化合物顯示了恢復亞胺培南和美羅培南的抗菌活性的作用(表3b)。表3b:青霉烯類BLI化合物抗KPC-2生產肺炎克雷伯菌(ATCCBAA-1705)表4:人頭孢菌素/化合物-1對產KPC-2肺炎克雷伯菌(ATCCBAA-1705-L)抗性CEF:頭孢吡肟,CTX:頭孢噻肟,CTZ:頭孢他啶&CTB:頭孢吡普在>16μg/mL濃度時,化合物-1與頭孢吡肟協同作用,比他唑巴坦或克拉維酸或舒巴坦更好地抗產KPC-2菌株ATCCBAA1705。它也表現出與頭孢噻肟和頭孢他啶在64μg/mL時的協同作用比以上比較物更好的效果。頭孢吡普在該測試濃度對所有的對比化合物相比并未顯示出任何的協同效應(表4)。表5:獸醫的頭孢菌素/化合物-1抗產KPC-2肺炎克雷伯菌(ATCCBAA-1705)CFQ:頭孢噻呋,CFF:頭孢喹肟,CFD:頭孢羥氨芐&CFL:頭孢洛寧(Cefalonium)在≥32g/mL的濃度時化合物-1與獸醫用頭孢菌素頭孢噻呋和頭孢喹肟協同比他唑巴坦更好地抗產KPC-2菌株ATCCBAA1705。頭孢羥氨芐和頭孢洛寧在測試的濃度沒有顯示所需的協同效應(表5)。表6a:碳青霉烯類&人頭孢菌素/化合物-1抗表達KPC-3大腸桿菌(J53R6206)IMP:亞胺培南,MER:美羅培南,CEF:頭孢吡肟,CTX:頭孢噻肟,CTZ:頭孢他啶&CTB:頭孢吡普在≥2μg/mL的濃度,化合物-1與亞胺培南,美羅培南,頭孢吡肟,頭孢噻肟,頭孢他啶和頭孢吡普協同比他唑巴坦或克拉維酸或舒巴坦更好地抗表達KPC-3大腸桿菌菌株J53R6206(表-6a)。同樣地,該系列中的下列化合物顯示了對于亞胺培南和美羅培南的抗菌活性的恢復(表6b)。表6b:碳青霉烯類BLI化合物抗表達KPC-3大腸桿菌(J53R6206)表-7:獸用頭孢菌素/化合物-1抗表達KPC-3表達大腸桿菌(J53R6206)CFQ:頭孢噻呋,CFF:頭孢喹肟,CFD:頭孢羥氨芐&CFL:頭孢洛寧在4μg/mL濃度時,化合物-1與獸用頭孢菌素類頭孢喹肟、頭孢噻呋和頭孢洛寧協同作用比他唑巴坦更好地抗表達KPC-3大腸桿菌菌株J53R6206。在測試濃度時頭孢羥氨芐沒有顯示所需的協同作用(表7)。用碳青霉烯酶類對β-內酰胺酶抑制分析對化合物1進行β-內酰胺酶抑制分析,以測定IC50值,并將其與比較物BLI劑進行比較,如其他地方所描述(Bebrone等人,Antimicrob.Agents.Chemother,2001,45(6):1868-1871;Jamieson等人,Antimicrob.Agents.Chemother,2003,47(5):1652-1657)。簡要地說,來自產KPC-2和表達KPC-3細菌的革蘭氏陰性菌株的酶提取物用于研究β-內酰胺酶的抑制活性,并使用CENTA作為β-內酰胺酶的底物測定IC50值。表8:化合物-1及碳青霉烯酶類的β-內酰胺酶抑制分析化合物-1的IC50低于抗粗KPC-2&3酶提取物的比較BLI,這表明式(I)的化合物1的BLI的優越的結合后效力(表8)。表9:哌拉西林與標準泰舒(Tazo)組合與新型抑制劑化合物抗來自ATCC的特定的產廣譜β-內酰胺酶(ESBL)革蘭氏陰性分離物抗性的比較化合物-1抗產KPC碳青霉烯酶菌株的體內作用化合物1是ESBL的有效抑制劑,其抗KPC酶的抑制活性已經在體外被證明。在此評估了在小鼠全身性感染和大腿感染的藥學模型中化合物-1對產KPC2肺炎克雷伯菌ATCCBAA1705的抗性,用于體內轉換為其對KPC2的抑制活性。在這些模型中,由于KPC2介導的水解,β-內酰胺類作為單一試劑的療效衰退。通過將化合物-1與β-內酰胺類組合,對其恢復或增強β-內酰胺類的作用效果進行了評估。方法:小鼠全身感染模型雌性瑞士小白鼠,重量為18-22g,它們用于所有的研究。對于每個劑量組,都包括5或6只小鼠。研究方案被研究院動物倫理委員會,蘭花研究實驗室有限公司審查和批準。將小鼠單獨放置在通風籠中,在整個研究期間隨意供應食物和水。從腦心浸液瓊脂培養基的過夜培養物中,用含豬胃粘蛋白的常規生理鹽水制備具有所需的細菌密度的檢驗接種物。在涉及多利培南的研究中,使用洗滌過的細菌細胞。每只小鼠腹腔注射檢驗接種物以使其感染。哌拉西林與β-內酰胺酶抑制劑(BLI)組合:用水性瓊脂(細菌用瓊脂)制備增加濃度的哌拉西林和BLI(化合物-1或他唑巴坦)作為單一試劑或哌拉西林與BLI以1:1的比例的組合。對感染的小鼠在感染后三個不同的時間點用藥物制劑皮下給藥。亞胺培南與BLI的組合:增加濃度的亞胺培南作為單一試劑或與固定濃度的BLI組合使用,用于向感染的小鼠皮下給藥。在這個實驗中,亞胺培南總是與西司他汀一起施用。多利培南與BLI組合:增加濃度的多利培南作為單一試劑或與固定濃度的BLI組合用于向感染的小鼠皮下給藥。經過處理的小鼠的存活每天監測兩次,直到感染后7天。用Reed和Muench法計算有效劑量50(ED50)(Reed,L.J.;Muench,H..“一種估計百分之五十端點的簡單方法”。TheAmericanJuournalofHygiene,1938,27:493-497)。中性粒細胞減少小鼠大腿感染模型(人類適用的模型)雌性瑞士小白鼠,重24-30g,用于所有研究。研究方案經研究院動物倫理委員會,蘭花研究實驗室有限公司審查和批準。通過腹腔注射環磷酰胺使小鼠出現中性粒細胞減少的情況。將腦心浸液肉湯中的對數期培養物注入到小鼠大腿中。亞胺培南或多利培南單獨或以組合形式以減少的分開(fractionated)劑量每15分鐘皮下給藥,總時間為5.5h((Flückiger,U.等人.“IntegrationofpharmacokineticsandpharmacodynamicsofImipeneminahuman-adaptedmousemodel'.AntimicrobialAgentsandChemother,1991,35(9):1905-1910)。在給藥的開始將化合物-1或他唑巴坦皮下大劑量給藥。療效終點為:亞胺培南研究為6小時,多利培南研究為8小時。在小鼠全身感染模型中化合物-1恢復的哌拉西林的抗KPC2肺炎克雷伯菌ATCCBAA1705抗性的功效哌拉西林單獨沒有什么功效,甚至高達800mg/kg。化合物-1恢復了哌拉西林的功效,因為哌拉西林與化合物-1以1:1的比例的組合表現出ED50為50mg/kg。因為化合物-1單獨沒有功效,因此哌拉西林以組合方式的功效歸因于化合物-1的KPC2酶抑制活性。然而,臨床使用的他唑巴坦不能恢復哌拉西林的功效,因為它與哌拉西林以1:1的比例結合時高至>200:>200mg/kg仍未顯示功效(表10)。表10:與化合物-1組合的哌拉西林對比他唑巴坦功效的比較劑量組ED50(mg/kg)哌拉西林>800化合物-1>64他唑巴坦>200哌拉西林∶化合物-1以1∶1比例50∶50哌拉西林∶他唑巴坦以1∶1比例>200∶>200在小鼠全身感染模型中化合物-1增強亞胺培南的抗KPC2肺炎克雷伯菌ATCCBAA1705抗性的功效亞胺培南單獨顯示出ED50為8.9mg/kg。結合固定的64mg/kg的化合物-1使得功效增強,其ED50為2.2mg/kg。他唑巴坦與亞胺培南以相同的劑量組合添加得到的ED50為4mg/kg。化合物-1引起亞胺培南療效的顯著增加是由于其對于KPC2酶的抑制活性(表11)。表11:亞胺培南與化合物1的組合對比他唑巴坦的功效比較劑量組ED50(mg/kg)亞胺培南8.9亞胺培南+化合物-1(64mg/kg)2.2亞胺培南+他唑巴坦(64mg/kg)4在小鼠全身感染模型中化合物-1增強的多利培南抗KPC2肺炎克雷伯菌ATCCBAA1705的功效對多利培南單獨或多利培南與化合物-1或他唑巴坦組合進行評估。化合物-1或他唑巴坦在20mg/kg和64mg/kg進行測試。多利培南單獨具有的ED50為14.14mg/kg。其功效被20mg/kg的化合物-1顯著提高至ED50為1.4mg/kg,且被64mg/kg的化合物-1顯著提高至ED50為1.62mg/千g。他唑巴坦略微提高了多利培南的功效,其中他唑巴坦的劑量分別為20和64mg/kg時,其ED50分別為11.89mg/kg和6.48mg/kg(表12)。這些結果表明,化合物-1對于KPC2的有效抑制活性導致防止多利培南被KPC2介導的水解分解,從而恢復多利培南的功效。表12:多利培南與化合物-1的組合對比他唑巴坦的功效的比較劑量組ED50(mg/kg)多利培南14.14多利培南+化合物-1(20mg/kg)1.4多利培南+化合物-1(64mg/kg)1.62多利培南+他唑巴坦(20mg/kg)11.89多利培南+他唑巴坦(64mg/kg)6.48在中性粒細胞減少小鼠大腿感染模型中化合物-1增強的亞胺培南抗KPC2肺炎克雷伯菌ATCCBAA1705的抗性在治療開始時的平均初始細菌負荷為1.8E+06CFU/大腿。亞胺培南140mg/kg,以分開的劑量給藥,總時間為5.5h,其沒有效果;6小時的治療后細菌生長至6.8E+06CFU/大腿。將亞胺培南與化合物-1以140mg/kg大劑量組合恢復了功效,此時細菌負荷減少至2.1E+05CFU/大腿(表13)。該實驗結果表明,化合物-1在強韌的小鼠大腿感染模型中表現出抑制的能力。表13:亞胺培南與化合物-1的組合的體內藥效學(大腿感染模型)劑量組細菌負荷(CFU/大腿)初始細菌負荷1.81E+06感染對照4.6E+07亞胺培南140mg/kg處理6.8E+06亞胺培南(140mg/kg)+化合物-1(140mg/kg)2.1E+05在中性粒細胞減少小鼠大腿感染模型中通過化合物-1增強的多利培南抗KPC2肺炎克雷伯菌ATCCBAA1705的功效進行了三個實驗,對多利培南單獨或與化合物-1或他唑巴坦組合(兩個實驗)進行評估。多利培南70mg/kg以分開的劑量經5.5h時長給予(Flückiger,U.等人."IntegrationofpharmacokineticsandpharmacodynamicsofImipeneminahuman-adaptedmousemodel'.AntimicrobialAgentsandChemother,.1991,35(9):1905-1910))。化合物-1或他唑巴坦在治療開始時以大劑量給予。治療終點是開始治療后8小時。最初的細菌負荷范圍為從1.4E+07-3.1E+07CFU/大腿。多利培南70mg/kg對于細菌負荷單獨發揮抑制效果。用多利培南單獨處理的小鼠的細菌負荷為5.4E+06-2.6E+07CFU/大腿。將35mg/kg的化合物-1與多利培南組合使細菌負荷下降到7.9E+05-1.3E+06CFU/大腿。在兩個實驗中還將多利培南與35mg/kg的他唑巴坦結合。他唑巴坦對多利培南的功效沒有影響,因為小鼠細菌負荷顯示為1.2E+07-1.6E+07CFU/大腿(表14)。表14:多利培南與化合物-1的組合(大腿感染模型)的體內藥效學劑量組細菌負荷(范圍)(CFU/大腿)初始細菌負荷1.4E+07-3.1E+07感染對照7.3E+07-1.6E+08多利培南70mg/kg處理的5.4E+06-2.6E+07多利培南(7Omg/kg)+化合物-1(35mg/kg)7.9E+05-1.4E+06多利培南(70mg/kg)+他唑巴坦(35mg/kg)1.19x107-1.6x107結論在所有這些實驗中,作為單一試劑的β-內酰胺類的功效下降,因為他們對于KPC2是不穩定的。作為KPC2的抑制劑,化合物-1恢復或顯著增強了β-內酰胺類的功效。
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1