自身免疫性疾病中的褪黑激素的制作方法
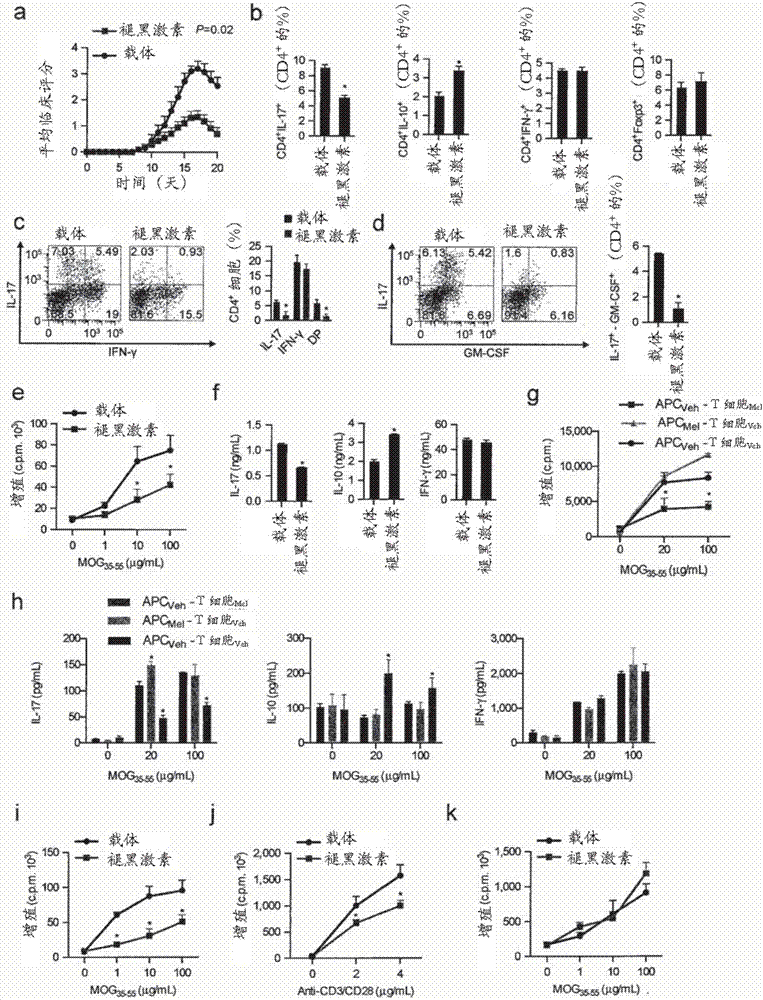
優先權聲明這一申請要求于2014年11月12日提交的美國臨時申請序列號62/078,473的權益。以上文獻的全部內容通過引用結合在此。聯邦資助的研究或進展本發明在受美國國立衛生研究院(nationalinstitutesofhealth)授予的政府支持下完成,批準號為ai093903和ns087867。美國政府享有本發明的一定的權利。在此描述了用于在患有多發性硬化癥(ms)的受試者中治療ms的季節性惡化或減少其發展的風險的方法,該方法包括向受試者給予褪黑激素激動劑。發明背景認為多發性硬化癥(ms)是由于自體反應性t細胞所致的髓鞘破壞引起的中樞神經系統(cns)的免疫介導性疾病。cd4+t細胞特征在于ifn-γ(th1細胞)或il-17(th17細胞)的產生被認為是ms免疫病理的重要促成因素(miossec等人,2009;sospedra和martin,2005;steinman,2014)。foxp3+調節性t細胞(foxp3+)和il-10分泌型1調節性t細胞(tr1)調節效應t細胞的活性,相應地tregs和tr1細胞的不足已經描述于ms中(astier等人,2006;sakaguchi等人,2010;viglietta等人,2004)。因此,效應t細胞和調節性t細胞之間的平衡控制ms疾病活性(miossec等人,2009;sospedra和martin,2005;steinman,2014)。已經將遺傳多態性與ms風險和/或發病機理關聯(beecham等人,2013;sawcer等人,2011)。然而,環境因素,例如感染(ascherio等人,2001;correale和farez,2007;correale等人,2006)、鈉攝入(farez等人,2014)、吸煙(hernan,2005)和維生素d水平(ascherio等人,2014)也影響ms發展和進程。例如,較低水平的維生素d與較高復發率相關聯(runia等人,2012;simpson等人,2010)。作為維生素d合成受日照調節的結果,在多數地點觀察到維生素d水平的顯著季節性波動,其中在春夏達到峰值,并且在秋季和冬季達到最低點(rosecrans和dohnal,2014)。因此,基于維生素d的已報道的抗炎作用(correale等人,2009)(ascherio等人,2010),預計ms復發出現在秋季和冬季期間達到峰值。然而,若干研究,包括薈萃分析(jin等人,2000)和最近的多中心研究(spelman等人,2014)發現ms疾病活性在春季和夏季較高,提示有另外的因素在ms復發季節性方面起作用。發明概述如在此描述的,在秋冬達到峰值的褪黑激素水平示出與ms患者中的臨床疾病活性的負相關。此外,褪黑激素限制了eae的發展并且控制了th17和tr1細胞分化。因此,褪黑激素水平中的季節性變動可能通過至少部分地由效應t細胞和調節性t細胞的調節介導的機理,促成在秋季和冬季觀察到的降低的疾病活性。因此,在此提供了用于在已經患有多發性硬化癥(ms)的受試者中,治療多發性硬化癥(ms)或減少其發展的風險的方法,或用于治療多發性硬化癥(ms)的季節性惡化或減少其發展的風險的方法。這些方法包括向對其有需要的受試者給予治療有效量的褪黑激素激動劑。還提供了用于通過向對其有需要的受試者給予治療有效量的褪黑激素激動劑,在受試者中降低th17細胞水平和/或增加tr1細胞水平的方法。在一些實施例中,受試者患有自身免疫性疾病,例如多發性硬化癥、腸道易激綜合征、克羅恩病、脊柱關節炎、系統性紅斑性狼瘡、白癜風、類風濕關節炎、銀屑病、舍格倫綜合征、或糖尿病(例如1型糖尿病)。在一些實施例中,這些方法包括在來自受試者的樣品中,檢測褪黑激素(例如6-羥基硫酸褪黑激素(6-sm))的水平;將該樣品中的褪黑激素的水平與褪黑激素的參比水平進行比較,該參比水平代表對照受試者(例如患有ms的受試者)中的褪黑激素的水平,該對照受試者具有患有ms的季節性惡化或發展ms的季節性惡化的增加的風險;并且當該樣品中的褪黑激素的水平低于參比水平時,將該受試者鑒定為具有患有ms的季節性惡化或發展ms的季節性惡化的增加的風險。在一些實施例中,褪黑激素的參比水平是或對應于20、20.5、21、21.5、22、22.5、23、23.5、或24ng/mg肌酸酐。在一些實施例中,褪黑激素激動劑是雷美替胺((s)-n-[2-(1,6,7,8-四氫-2h-茚并[5,4-b]呋喃-8-基)乙基]丙酰胺)、阿戈美拉汀(n-[2-(7-甲氧基萘-1-基)乙基]乙酰胺)、他司美瓊((1r,2r)-n-[2-(2,3-二氫苯并呋喃-4-基)環丙基甲基]丙酰胺)、或tik-301(ly-156735)(n-[(2r)-(6-氯-5-甲氧基-1h-吲哚-3-基)丙基]乙酰胺)。在一些實施例中,受試者具有ms的季節性惡化的病史,具有與其ms的季節性惡化相關聯的一個或多個癥狀,具有低褪黑激素水平,生活在低褪黑激素季節正在發生或即將發生的氣候中,或生活在褪黑激素水平通常很低的氣候中。在一些實施例中,這些方法包括給予rev-erb激動劑或ror激動劑。在一些實施例中,褪黑激素激動劑是口服給予的、經鼻給予的、靜脈內給予的、或鞘內給予的。在此還提供了褪黑激素激動劑用于在患有多發性硬化癥(ms)的受試者中治療ms的季節性惡化或減少其發展的風險中的用途。在一些實施例中,該受試者具有低于參比水平的褪黑激素水平,例如,褪黑激素的參比水平是或對應于20、20.5、21、21.5、22、22.5、23、23.5、或24ng/mg肌酸酐。在一些實施例中,褪黑激素激動劑是雷美替胺((s)-n-[2-(1,6,7,8-四氫-2h-茚并[5,4-b]呋喃-8-基)乙基]丙酰胺)、阿戈美拉汀(n-[2-(7-甲氧基萘-1-基)乙基]乙酰胺)、他司美瓊((1r,2r)-n-[2-(2,3-二氫苯并呋喃-4-基)環丙基甲基]丙酰胺)、或tik-301(ly-156735)(n-[(2r)-(6-氯-5-甲氧基-1h-吲哚-3-基)丙基]乙酰胺)。在一些實施例中,受試者具有ms的季節性惡化的病史,具有與其ms的季節性惡化相關聯的一個或多個癥狀,具有低褪黑激素水平,生活在低褪黑激素季節正在發生或即將發生的氣候中,或生活在褪黑激素水平通常很低的氣候中。在一些實施例中,褪黑激素激動劑是在包括rev-erb激動劑或ror激動劑的組合物中。在一些實施例中,褪黑激素激動劑被配制為是口服給予的、經鼻給予的、靜脈內給予的、或鞘內給予的。此外,在此提供了用于鑒定用褪黑激素激動劑進行治療的受試者的方法,該治療用于減少多發性硬化癥(ms)的季節性惡化的發展的風險。這些方法包括選擇患有ms的受試者;在來自該受試者的樣品中,檢測褪黑激素(例如6-羥基硫酸褪黑激素(6-sm))的水平;將該樣品中的褪黑激素的水平與褪黑激素的參比水平進行比較,該參比水平代表對照受試者(例如患有ms的受試者)中的褪黑激素的水平,該對照受試者具有患有ms的季節性惡化或發展ms的季節性惡化的增加的風險;當該樣品中的褪黑激素的水平低于參比水平時,將該受試者鑒定為具有患有ms的季節性惡化或發展ms的季節性惡化的增加的風險;并且任選地給予褪黑激素拮抗劑至受試者。在一些實施例中,褪黑激素的參比水平是或對應于20、20.5、21、21.5、22、22.5、23、23.5、或24ng/mg肌酸酐。在一些實施例中,褪黑激素激動劑是雷美替胺((s)-n-[2-(1,6,7,8-四氫-2h-茚并[5,4-b]呋喃-8-基)乙基]丙酰胺)、阿戈美拉汀(n-[2-(7-甲氧基萘-1-基)乙基]乙酰胺)、他司美瓊((1r,2r)-n-[2-(2,3-二氫苯并呋喃-4-基)環丙基甲基]丙酰胺)、或tik-301(ly-156735)(n-[(2r)-(6-氯-5-甲氧基-1h-吲哚-3-基)丙基]乙酰胺)。在一些實施例中,受試者具有ms的季節性惡化的病史,具有與其ms的季節性惡化相關聯的一個或多個癥狀,具有低褪黑激素水平,生活在低褪黑激素季節正在發生或即將發生的氣候中,或生活在褪黑激素水平通常很低的氣候中。在一些實施例中,這些方法包括給予rev-erb激動劑或ror激動劑。在一些實施例中,褪黑激素激動劑是口服給予的、經鼻給予的、靜脈內給予的、或鞘內給予的。除非另外定義,在此所使用的全部技術術語和科學術語具有與本發明所屬領域之內的普通技術人員通常所理解的相同的意思。在此描述了用于本發明的方法和材料;還可使用本領域已知的其他合適的方法和材料。這些材料、方法、以及實例僅是說明性的,并且不旨在進行限制。在此提及的所有出版物、專利申請、專利、序列、數據庫條目和其他參考文獻通過引用以其整體結合。在有矛盾的情況下,將以本說明書(包括定義)為準。本發明的其他特征和優點將從下列詳述和附圖以及從權利要求中顯而易見。附圖說明圖1.褪黑激素示出與ms臨床復發逆相關。(a)評估每個季節的惡化率,持續隨訪的持續時間,并且在主軸中加以描繪。在每個季節,在首次晨尿中測量的6-羥基硫酸褪黑激素被描繪為在副軸中的平均值±s.e.m。p值對應于泊松回歸模型。缺少惡化率和維生素d(b),報道的呼吸道感染(c)、和布宜諾斯艾利斯城中的uv輻射(d)之間的關聯。還參見表1。圖2.褪黑激素給予改善了eae。(a)在用載體(0.01%dmso)或褪黑激素(5mg/kg)處理的c57/b6中的eae發展。數據代表三次獨立實驗(平均值和s.e.m.)(n≥20只小鼠/組)p值對應于在混合效應模型的重復測量中的治療效果。(b)在疾病誘導后第7天,來自載體或褪黑激素處理的小鼠的脾的il-17+、il10+、ifn-γ+和foxp3+cd4+細胞的流式細胞術分析。每組分析至少4只小鼠,并且數據呈現為平均值±sem。*未配對t檢驗的p<0.05。(c-d)來自處于eae的臨床峰值的對照的或褪黑激素處理的小鼠的cns的il-17+、ifn-γ+、il-17+-ifn-γ+(dp)和il-17+-gm-csf+cd4+t細胞的流式細胞術分析。*未配對t檢驗的p<0.05。(e)載體或褪黑激素處理的小鼠的cd4+t細胞對mog35-55的增殖應答。每組分析至少3只小鼠,并且數據呈現為平均值±s.e.m。*單向方差分析的p<0.05。(f)通過增殖來自載體和褪黑激素處理的小鼠的cd4+t細胞的細胞因子分泌。數據代表三次獨立實驗(平均值和s.e.m.)*未配對t檢驗的p<0.05。(g)在與源自褪黑激素處理的或未處理的小鼠的樹突細胞共培養中的cd4+t細胞的增殖應答和細胞因子譜(h)。數據代表三次獨立實驗(平均值和s.e.m.)。*單向方差分析的p<0.05。(i)在樹突細胞存在下,褪黑激素處理的2d2cd4+t細胞對mog35-55的增殖應答。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(j)褪黑激素處理的2d2cd4+t細胞對僅用抗cd3和抗cd28刺激的mog35-55的增殖應答。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(k)處理的2d2cd4+t細胞對mog35-55刺激的褪黑激素處理的dc的增殖應答。數據代表三次獨立實驗(平均值和s.e.m.)。還參見圖7a-e。圖3.褪黑激素干擾人類th17細胞分化并且促進tr1產生。(a)在褪黑激素(500ng/ml)和阿戈美拉汀(500ng/ml)存在或不存在下,在人類th17分化的cd4+t細胞(il-1β、il-6和tgf-β1)中il-17表達的流式細胞術分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(b).在褪黑激素(500ng/ml)和阿戈美拉汀(500ng/ml)存在或不存在下,通過在人類th17分化的cd4+t細胞中的il-17的elisa進行的細胞因子定量。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(c)如在a.中培養的th17細胞的rt-pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(d)在褪黑激素(500ng/ml)和阿戈美拉汀(500ng/ml)存在或不存在下,在人類th1分化的cd4+t細胞(il-12)中ifn-g表達的流式細胞術分析。數據代表三次獨立實驗(平均值和sem)。(e).在褪黑激素(500ng/ml)和阿戈美拉汀(500ng/ml)存在或不存在下,通過在人類th1分化的cd4+t細胞中的ifn-γ的elisa進行的細胞因子定量。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(f)如在d中培養的th1細胞的rt-pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(g)在褪黑激素(500ng/ml)和阿戈美拉汀(500ng/ml)存在或不存在下,在人類tr1分化的cd4+t細胞中il-10表達的流式細胞術分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(h)如在f中培養的tr1細胞的定量pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)。*單向方差分析的p<0.05。還參見圖8。圖4.褪黑激素經由erk1/2-c/ebpα途徑干擾th17細胞分化。(a)在褪黑激素(2ng/ml)存在或不存在下,通過添加tfg-β、il-6(0h)和il-23(48h)將cd4+初始t細胞分化為th17細胞,并且在72h后通過rt-pcr進行分析。展示的圖片代表五次實驗。*未配對t檢驗的p<0.05。(b)如在a中培養72h后,il-17和il-10的細胞因子分泌分析。數據代表三次獨立實驗(平均值和s.e.m.)*未配對t檢驗的p<0.05。(c)在褪黑激素(2ng/ml)、阿戈美拉汀(20ng/ml,mtnr1a配體)和cgp52608(20ng/ml,ror-α配體)存在或不存在下,在th17分化的cd4+t細胞中的細胞因子分泌。數據代表三次獨立實驗(平均值和s.e.m.)。*單向方差分析的p<0.05。(d)如在c中培養的th17細胞的rt-pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)。*單向方差分析的p<0.05。(e)在野生型小鼠和mtnr1a缺陷小鼠中,如在a中的il-17表達的流式細胞術分析。數據代表三次獨立實驗(平均值和s.e.m.)*未配對t檢驗的p<0.05。(f)如在e中培養的野生型和mtnr1a缺陷小鼠的定量pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)*未配對t檢驗的p<0.05。(g)使用反向蛋白質陣列(reverseproteinarray)進行的信號轉導譜。數據代表兩次獨立實驗(平均值和s.e.m.)*未配對t檢驗的p<0.05。(h)t-和p-erk1/2的免疫印跡分析。數據代表兩次獨立實驗(平均值和s.e.m.)。(i)t-和p-c/ebpα的免疫印跡分析。數據代表兩次獨立實驗(平均值和s.e.m.)。(j)在nr1d1中的c/ebpα的推定的結合位點(左側小圖);用抗c/ebpα進行的染色質免疫沉淀反應(右側小圖)。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(k)用針對nr1d1啟動子的螢光素酶報告基因構建體轉染的hek-293細胞的螢光素酶活性。數據代表三次獨立實驗(平均值和s.e.m.)*未配對t檢驗的p<0.05。(l)在野生型小鼠和c/ebpα缺陷小鼠中,如在a中的il-17表達的流式細胞術分析。數據代表兩次獨立實驗(平均值和s.e.m.)。*單向方差分析的p<0.05。(m)在野生型小鼠和c/ebpα缺陷小鼠中,如在(a)中的il-17表達的流式細胞術分析。數據代表三次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。還參見圖9-10。圖5.褪黑激素通過限制nfil3表達,干擾th17細胞分化。(a)介導褪黑激素對th17細胞分化的作用的建議機制的示意圖。(b)在th0、th17和tr1極化條件下持續3天,在活化的cd4+t細胞中nr1d1表達的rt-pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)。*未配對t檢驗的p<0.05。(c)在th17極化條件下持續3天,用載體、褪黑激素(2ng/ml)或阿戈美拉汀(20ng/ml)處理,活化的cd4+t細胞中nr1d1(左側小圖)和nfil3(右側小圖)表達的rt-pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)。*未配對t檢驗的p<0.05。通過蛋白質印跡(d)進一步確認nfil3表達。數據代表兩次獨立實驗(平均值和s.e.m.)。(e)在褪黑激素(2ng/ml)和/或uo126存在下,在th17極化條件下持續3天,活化的cd4+t細胞中nfil3表達的rt-pcr分析。數據代表五次獨立實驗(平均值和s.e.m.)。*單向方差分析的p<0.05。(f,g)在褪黑激素(2ng/ml)和/或uo126存在下,在th17極化條件下,活化的cd4+t細胞中il-17表達(f)和rorc表達(g)的流式細胞術分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(h,i)在th17極化條件下,在褪黑激素(2ng/ml)存在下,在感染對照或nr1d1編碼逆轉錄病毒后,活化的cd4+t細胞中il-17表達(h)和rorc及il17表達(i)的流式細胞術分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(j,k)在褪黑激素(2ng/ml)存在下,在th17極化條件下,活化的野生型和rev-erbα缺陷cd4+t細胞中il-17表達(j)和rorc及il17表達(k)的流式細胞術分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(l)在rorc和rora中,nfil3的推定的結合位點(左側小圖);在th17極化條件下,在活化的cd4+t細胞中,具有其推定的結合位點的nfil3的相互作用的chip分析(右側小圖)。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(m)在褪黑激素(2ng/ml)存在下,在th17極化條件下,活化的cd4+t細胞中rorc和rora表達的rt-pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)*未配對t檢驗的p<0.05。(n,o)在th17極化條件下,在褪黑激素(2ng/ml)存在下,并且用對照或nfil3編碼逆轉錄病毒轉導,活化的cd4+t細胞中il-17表達(n)和rorc及il17表達(o)的流式細胞術分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(p,q)在褪黑激素(2ng/ml)存在下,在th17極化條件下,在活化的cd4+t細胞中,野生型小鼠和nfil3缺陷小鼠中il-17表達(p)和rorc及il17表達(q)的流式細胞術分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(r)在來自用野生型、mtnr1a-rev-erbα或nfil3缺陷cd4+t細胞重建的、用cfa中的mog35-55免疫的并且用載體或褪黑激素(5mg/kg)處理的rag-1缺陷小鼠的cd4+t細胞中,il-17和ifn-γ表達的流式細胞術分析。*未配對t檢驗的p<0.05。還參見圖11。圖6.褪黑激素促進tr1細胞分化。(a)在褪黑激素(2ng/ml)存在或不存在下,在tr1分化的cd4+t細胞中,il10、ahr和maf表達的rt-pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)。*單向方差分析的p<0.05。(b)體外抑制測定,在與先前標記有csfe的cd4+t細胞一起72h后,將如在a中的處理的或未處理的分化的tr1細胞共培養,并且在48h后,通過流式細胞術測量增殖周期(csfe稀釋)。數據代表兩次獨立實驗(平均值和s.e.m.)。*單向方差分析的p<0.05。(c)在褪黑激素(2ng/ml)、阿戈美拉汀(20ng/ml,mtnr1a配體)和cgp52608(20ng/ml,ror-α配體)存在或不存在下,在tr1分化的cd4+t細胞中的il-10表達的流式細胞術分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(d)如在c中培養的th1細胞的rt-pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(e)在野生型小鼠和mtnr1a缺陷小鼠中,如在c中的il10表達的rt-pcr分析。數據代表三次獨立實驗(平均值和s.e.m.)*單向方差分析的p<0.05。(f)添加或不添加uo126的情況下,褪黑激素處理的tr1細胞中il10的rt-pcr表達。數據代表五次獨立實驗(平均值和s.e.m.)。*對比載體和信號轉導抑制劑對照條件,未配對t檢驗的p<0.05。**對比uo126處理的條件的載體,p<0.05。(g)在野生型小鼠和ror-α缺陷小鼠中,如在c中的il-10表達的流式細胞術分析。(h)ror-α推定的結合位點存在于il10啟動子中(下方小圖),以及用抗ror-α進行的染色質免疫沉淀反應(上方小圖)。數據代表三次獨立實驗(平均值和s.e.m.)。*未配對t檢驗的p<0.05。(i)用針對il10啟動子的螢光素酶報告基因構建體轉染的hek-293細胞的螢光素酶活性。數據代表三次獨立實驗(平均值和s.e.m.)*未配對t檢驗的p<0.05。(j)描繪tr1細胞中的褪黑激素的作用的示意圖。圖7.褪黑激素依賴性eae改善涉及的機制涉及圖2(a)在疾病誘導后第15天開始,用載體(或褪黑激素(5mg/kg))處理的c57/b6中的eae發展。數據代表兩次獨立實驗(平均值和sem)(nr10小鼠/組)。中間小圖中的p值對應于在混合效應模型的重復測量中的治療效果。*未配對t檢驗的p<0.05。(b)在疾病的峰值,來自載體或褪黑激素處理的小鼠的cns的il-17+、il10+、ifn-g+和foxp3+cd4+細胞的流式細胞術分析。每組分析至少4只小鼠,并且數據呈現為平均值±sem。*未配對t檢驗的p<0.05。(c)在疾病的峰值,來自載體或褪黑激素處理的小鼠的脾的cd19+b細胞、gdt細胞和lin-cd90+cd127+il17+il22+先天淋巴細胞(ilc)的流式細胞術分析。每組分析至少4只小鼠,并且數據呈現為平均值±sem。*未配對t檢驗的p<0.05。(d)來自處于eae的臨床峰值的對照或褪黑激素處理的小鼠的cns的il-17+、il-17+-ifn-g+、il-17+-gm-csf+cd4+t細胞的流式細胞術分析(總數)。*未配對t檢驗的p<0.05。(e)在抗原呈遞細胞和mog35-55肽存在下,體外培養的2d2+t細胞的上清液中的il17、il-10、和ifn-g。數據代表兩次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。(f)在載體或褪黑激素存在下,用抗體cd3和cd28刺激3天后,碘化丙啶+和膜聯蛋白v+cd4+t細胞的流式細胞術分析。數據代表兩次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。(g)在載體和褪黑激素20ng/ml存在下,如在(f)中描述的活化的cd4+t細胞中bcl-xl和肌動蛋白的免疫印跡分析。數據代表兩次獨立實驗(平均值和sem)。(h)在褪黑激素和對照或il-10阻斷抗體存在下,用針對cd3和cd28的抗體刺激的cd4+t細胞的增殖應答。數據代表三次獨立實驗(平均值和sem)。單向方差分析的*p<0.05。圖8.褪黑激素干擾人類th17cell細胞分化,涉及圖3(a)在褪黑激素(500ng/ml)和阿戈美拉汀(500ng/ml)存在或不存在下,在人類th17分化的cd4+t細胞(il-1b、il-6和il-23)中il-17表達的流式細胞術分析。數據代表三次獨立實驗(平均值和sem)。單向方差分析的*p<0.05。(b)通過如在a中,在褪黑激素(500ng/ml)和阿戈美拉汀(500ng/ml)存在或不存在下,在人類th17分化的cd4+t細胞中的il-17的elisa進行的細胞因子定量。數據代表三次獨立實驗(平均值和sem)。單向方差分析的*p<0.05。(c)如在a中培養的th17細胞的rt-pcr分析。數據代表三次獨立實驗(平均值和sem)。單向方差分析的*p<0.05。圖9.褪黑激素選擇性地干擾th17細胞分化并且促進tr1產生,涉及圖4(a和b)在載體或褪黑激素(2ng/ml)存在下,在th17(a)或th1(b)極化條件下,活化3天的cd4+t細胞的增殖應答的流式細胞術分析。數據代表三次獨立實驗(平均值和sem)。單向方差分析的*p<0.05。(c)在載體或褪黑激素(2ng/ml)存在下,在th17極化條件下,活化3天的cd4+t細胞的rorgt表達的流式細胞術分析。數據代表三次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。(d)在載體或褪黑激素(2ng/ml)存在下,在th1極化條件下,活化3天的cd4+t細胞的t-bet表達的流式細胞術分析。數據代表三次獨立實驗(平均值和s.e.m.)。(e)添加或不添加褪黑激素(2ng/ml),在有利于th1、th2、th17、tr1和foxp3+itreg細胞的分化的機化條件下,活化3天的cd4+初始t細胞的流式細胞術分析。數據代表三次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。(f)如在(e)中描述的培養的cd4+t細胞中,基因表達的rt-pcr分析。數據代表兩次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。圖10.褪黑激素和相關藥物影響th17細胞分化,涉及圖4(a和b)在褪黑激素(2ng/ml)和對照或il-2阻斷抗體存在下,在th17極化條件下,活化的cd4+t細胞中rorc(a)和il17(b)表達的rt-pcr分析。數據代表兩次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。(c)在褪黑激素(2ng/ml)存在下,在th17或tr1極化條件下持續3天,活化的初始cd4+t細胞中mtnr1a的表達的免疫印跡分析。數據代表兩次獨立實驗(平均值和sem)。(d)在體內分化3天后,不同cd4+t細胞亞群中的rora表達的rt-pcr分析。數據代表五次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。(e)用編碼rora的構建體和針對rora響應性bmal啟動子的螢光素酶報告基因構建體共轉染的hek293細胞中的螢光素酶活性。數據代表兩次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。(f)在載體、褪黑激素(2ng/ml)和雷美替胺(10ng/ml)存在下,在th0或th17極化條件下,活化的鼠cd4+t細胞的上清液中的il17和il-10。(g)如在(f)中活化的cd4+t細胞中的rorc和il17表達的rt-pcr分析。數據代表兩次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。(h和i)在th17極化條件下,并且用載體、褪黑激素(2ng/ml)或阿戈美拉汀(20ng/ml)處理,活化的野生型或mtnr1akocd4+t細胞中的erk1/2磷酸化的流式細胞術分析的磷/總erk比率(h)和mfi比率(i)的百分率。數據代表兩次獨立實驗(平均值和sem)。*未配對t檢驗的p<0.05。圖11.在cd4+t細胞中,eae中的褪黑激素作用是由mtnr1a和nfil3介導的,涉及圖5。在來自用野生型、mtnr1a-或nfil3-缺陷cd4+t細胞重建的、用cfa中的mog35-55免疫的并且用載體或褪黑激素(5mg/kg)處理的rag-1缺陷小鼠的cns的cd4+t細胞中,rorc、il17和csf2表達的rt-pcr分析。*未配對t檢驗的p<0.05。圖12.在rev-erbα激動劑sr9009(5微摩爾)存在或不存在下,通過添加tfg-b、il-6(0hr)和il-23(48hr)將cd4+初始t細胞分化為th17細胞,并且在72h后通過rt-pcr進行分析。*未配對t檢驗的p<0.05。發明詳述強流行病學證據支持維生素d在減少ms復發方面的作用(ascherio等人,2012)。引人注目地,維生素d水平在春季和夏季(此時ms患者復發發生達到峰值)較高。因此,在多個季節中復發的較低發生(特征在于較低的維生素d水平)提出了一個“季節性悖論”:在春季和夏季,維生素d水平較高時,復發頻率較低,這與多數研究中發現的相反(jin等人,2000;spelman等人,2014),只有少數例外(等人,2012)。我們的數據可以通過鑒定褪黑激素(它的水平是由晝長的季節性波動調節,為ms中免疫應答附加調節子)來解決這一悖論。注意到夜班工作(與較低總體褪黑激素水平關聯)(schernhammer等人,2004)增加了發展ms的風險(等人,2011)。這些發現提示褪黑激素還可能是ms危險因素;褪黑激素水平和發展ms的風險之間的關系是正在進行的研究的焦點。最后,在不同地理位置中褪黑激素和已知影響ms的其他季節性環境因素(例如維生素d)之間的相互作用仍然要進一步闡明。在過去50年中,自身免疫障礙的發病率的提高已經達到流行性的比例并且不能僅歸因于遺傳危險性。因此,環境因素及其對免疫應答特別是t細胞分化的影響正不斷引起日益增加的關注。例如,存在于家庭產品中的若干化合物會活化芳烴受體并且同時影響th17細胞和調節細胞的分化(quintana等人,2008);在西化飲食和加工食品中的鈉會增強th17細胞分化(wu等人,2013);共生微生物群的組成影響t細胞分化和應答(lathrop等人,2011);并且缺少日照和飲食習慣會降低維生素d水平并且影響調節性t細胞的功能(correale等人,2009)。這些環境因素中的每一個作用于不同信號傳導途徑,它們之間的復雜相互作用的研究可以闡明環境對免疫系統的影響。促炎性th17細胞被認為促成eae和ms的發病機理(miossec等人,2009)。由ror-α和ror-γt調節th17細胞分化,并且靶向th17細胞的療法目前正在ms和其他自身免疫性疾病中測試,具有初步令人鼓舞的結果(dominiquel.p.baeten和kuchroo,2013)。盡管具有活化ror-α的潛能,褪黑激素經由其膜受體以nfil3依賴性方式抑制th17細胞的產生。有趣地,最近已經示出,在夜間,晝夜節律時鐘通過類似的nfil3依賴性機制,抑制th17發展(yu等人,2013)。我們的工作提示在夜間,除了th17細胞,tr1細胞也以erk1/2-和ror-α依賴性方式受褪黑激素調節。基于褪黑激素由松果體產生及其受日光調節的高度進化保守性(macchi和bruce,2004),可能褪黑激素對免疫應答的晝夜節律的和季節性的影響起到生理學作用,該生理學作用在進化期間驅動其正向選擇。tr1細胞特征在于il-10的產生(pot等人,2011;roncarolo等人,2006)。ahr、c-maf和erk1/2調節tr1細胞發育和il-10表達(apetoh等人,2010;gandhi等人,2010)。本工作示出,褪黑激素通過活化erk1/2信號轉導促進tr1細胞分化,這已經在先前被描述為控制t細胞和dc中的il-10表達(saraiva和o′garra,2010)。我們還將ror-α鑒定為tr1細胞中褪黑激素作用的介體。因此,這些數據提示褪黑激素利用多個途徑來促進tr1細胞分化。促炎性的和調節性的細胞之間的相互作用控制自身免疫性疾病(例如ms)的發展。在此我們報道了褪黑激素(它的水平示出季節變異性)控制了致病性和調節性t細胞之間的平衡。本數據將褪黑激素依賴性信號轉導鑒定為治療性免疫調節的潛在靶點。治療方法如在此所示,褪黑激素(它的水平示出季節變異性)可以控制致病性和調節性t細胞之間的平衡并且改善其中致病性th17t以增加的水平存在和/或具有增加的活性的自身免疫性疾病,例如ms。例如,可以受益于使用在此描述的組合物和方法的治療的其他自身免疫性病癥包括但不限于阿狄森病、脫發、強直性脊柱炎、抗磷脂綜合征、自身免疫性溶血性貧血、自身免疫性肝炎、自身免疫性卵巢炎、白塞氏病、大皰性類天皰瘡、脂瀉病、慢性疲勞免疫功能障礙綜合征(cfids)、慢性炎癥性脫髓鞘性多發性神經疾病、丘-施二氏綜合征、瘢痕性類天皰瘡、冷凝集素病、crest綜合征、克羅恩病、糖尿病(例如i型糖尿病)、家族性植物神經功能不全、子宮內膜組織異位、嗜酸粒細胞增多肌痛綜合征、原發性混合型冷球蛋白血癥、纖維肌痛、綜合征/纖維性肌炎、格雷夫斯氏病、吉蘭-巴雷綜合征、橋本氏甲狀腺炎、特發性肺纖維化、特發性血小板減少性紫癜(itp)、炎癥性腸病(ibd)、扁平苔癬、狼瘡、美尼爾氏病、混合性結締組織病(mctd)、多發性硬化癥、重癥肌無力、天皰瘡、惡性貧血、結節性多動脈炎、軟骨炎、風濕性多肌痛、多發性肌炎和皮肌炎、原發性丙種球蛋白血癥、原發性膽汁性肝硬化、銀屑病、雷諾氏現象、萊特爾綜合征、風濕熱、類風濕關節炎、結節病、硬皮病、舍格倫綜合征、脊椎關節病(脊柱關節炎)、僵體綜合征、大動脈炎、顳動脈炎/巨細胞動脈炎、自身免疫性甲狀腺疾病、潰瘍性結腸炎、自身免疫性眼色素層炎、自身免疫性血管炎、白癜風、以及韋格納氏肉芽腫病。在一些實施例中,自身免疫性疾病是ibd、克羅恩病、脊柱關節炎、系統性紅斑性狼瘡、白癜風、類風濕關節炎、銀屑病、舍格倫綜合征、或糖尿病,例如i型糖尿病,所有這些都已經關系到th17細胞功能障礙(參見例如korn等人,annurevimmunol.[免疫學年鑒]2009;27:485-517dong,cellresearch[細胞研究](2014)24:901-903;zambrano-zaragoza等人,intjinflam.[國際炎癥雜志]2014;2014:651503;waite和skokos,internationaljournalofinflammation;volume2012(2012),articleid819467,10pages[國際炎癥雜志;2012卷(2012),文章id819467,10頁],dx.doi.org/10.1155/2012/819467;han等人,frontiersofmedicine[醫學前沿]9(1):10-19(2015)。在此描述的方法包括使用褪黑激素受體(例如mtnr1a)的激動劑治療自身免疫性疾病,例如多發性硬化癥(ms)。因此,在一些實施例中,該障礙是ms。在春季和夏季的月份期間,當褪黑激素水平較低時,這些方法是特別有用的,而且可以在任何時間使用。在一些實施例中,一旦已經確定某人患有自身免疫性疾病,例如ms,則可以給予包括給予治療有效量的褪黑激素激動劑的治療。這些方法可以包括從受試者獲得樣品,并且評估樣品中褪黑激素的存在和/或水平,并且將該存在和/或水平與一個或多個參比進行比較,這些參比例如是代表褪黑激素的正常水平的對照參比,例如與冬季月份關聯的受試者中的水平,和/或代表與夏季月份關聯的褪黑激素的水平的受影響的參比。低于參比水平的褪黑激素的水平的存在指示受試者應該用褪黑激素激動劑進行處理。這些方法還可以用來預測某人是否將受益于用褪黑激素激動劑進行治療;與具有高于參比水平的褪黑激素的水平的受試者相比,具有低于參比水平的褪黑激素的水平的受試者更可能受益于用褪黑激素激動劑進行的治療。此外,這些方法可以用于為受試者選擇治療;對于具有低于參比水平的褪黑激素的水平的受試者,選擇用褪黑激素激動劑進行的治療。在一些實施例中,受試者具有與其自身免疫性疾病(例如ms)的季節性惡化相關聯的一個或多個癥狀,具有低褪黑激素水平,生活在低褪黑激素季節正在發生或即將發生的氣候中,或生活在褪黑激素水平通常很低的氣候(例如熱帶氣候)中。通常,這些方法包括給予治療有效量的如在此所述的褪黑激素激動劑至需要、或已經被確定為需要此類治療的受試者。如在此上下文中使用的,“治療”意指改善與自身免疫性疾病(例如ms)的季節性惡化相關聯的障礙的至少一個癥狀。治療會導致自身免疫性疾病(例如ms)的一個或多個癥狀(例如抑郁和疲勞、膀胱功能障礙、痙攣狀態、疼痛、共濟失調、和意向震顫)的減少。治療有效量可以是足以預防急性加重的發作,或足以縮短急性加重的持續時間,或足以減小一個或多個癥狀(例如熱敏性、核間性眼肌麻痹、視神經炎、和lhermitte[萊爾米特]癥狀)的嚴重性的量。在一些實施例中,治療有效量是足以預防受試者的腦、視神經、和脊髓中的一個或多個內的脫髓鞘病變的出現,延遲或預防該脫髓鞘病變的生長(即尺寸增加),或促進該脫髓鞘病變的治愈的量,例如,如mri所證明。復發-緩解型和進展型ms多發性硬化癥(ms)是中樞神經系統(cns)的炎性脫髓鞘疾病。ms典型地臨床特征在于由cns中的病變引起的復發的或慢性進展性的神經功能障礙。病理上,這些病變包括影響腦、視神經、和脊髓的多個區域的脫髓鞘。潛在的病因是不確定的,但是ms被廣泛認為至少部分地是自身免疫性的或免疫介導的疾病。在85%的患者中,在最初的、其中急性自身免疫攻擊中樞神經系統(cns)的復發-緩解過程后(rrms),ms完全恢復(compston和coles,lancet[柳葉刀]372,1502-1517(2008))。大部分rrms患者接下來發展繼發進展型ms(spms),其特征在于神經失能的進展型的、不可逆的積累(rovaris等人,lancetneurol[柳葉刀神經病學]5,343-354(2006))。表征spms的進展型的并且不可逆的失能在不存在新炎性病變的情況下發生,提示在ms的這個階段,其他機制可能發揮作用(rovaris等人,lancetneurol[柳葉刀神經病學]5,343-354(2006))。盡管若干療法示出對rrms的積極作用,但是它們通常在spms時無效,并且沒有標記可用于監測到spms的轉換。實際上,阻止適應性炎癥應答的治療示出對rrms管理的積極作用,但是通常在spms中無效(lopez-diego和weiner,natrevdrugdiscov[自然評論藥物發現]7,909-925(2008))。因此,重要的是表征到spms的轉換所涉及的過程,從而鑒定針對進展型ms的療法,并且鑒定用來監測rrms到spms轉換的生物標記。繼發性進展型多發性硬化癥(spms),即多發性硬化癥的四種國際上認可的形式之一(其他形式是復發/緩解型多發性硬化癥、原發性進展型多發性硬化癥和進展型性復發性多發性硬化癥)特征在于伴隨或不伴隨疊加的復發和輕度緩解和平臺期,臨床神經學損傷的穩定進展。發展spms的人將通常先前已經遭受一個時期的復發/緩解型多發性硬化癥(rrms),該病可能已經持續從兩年到40年或更久。偶爾地,在spms的發展后,受試者將具有一些復發和緩解,但是隨著時間發展,這些傾向于變得頻率較低。原發性進展型ms(ppms)相對更罕見(約15%的ms患者群體),并且特征在于從疾病發作開始,能力的緩慢進展型喪失。多數ppms患者患有進展型脊髓病或進展型小腦功能障礙。可以使用本領域已知的方法進行ms的診斷、和亞型的確定,例如基于在空間和時間上播散的cns病變的存在,和替代性診斷的消除(problemsofexperimentaltrialsoftherapyinmultiplesclerosis:reportbythepanelontheevaluationofexperimentaltrialsoftherapyinmultiplesclerosis.annnyacadsci.[多發性硬化癥治療中的實驗性試驗問題:小組評估多發性硬化癥治療中實驗性試驗的報告.紐約科學院學報]122:1965;552-568)。可替代地,可以基于臨床體征和癥狀(包括熱敏性、核間性眼肌麻痹、視神經炎、和lhermitte[萊爾米特]癥狀)的存在來做出診斷(參見例如mcdonald等人,recommendeddiagnosticcriteriaformultiplesclerosis:guidelinesfromtheinternationalpanelonthediagnosisofmultiplesclerosis.ann.neurol.[推薦的多發性硬化癥診斷標準:國際多發性硬化癥診斷小組指導.神經學年報]2001;50:121;和polman等人,diagnosticcriteriaformultiplesclerosis:2005revisionstothe“mcdonaldcriteria.”annneurol[多發性硬化癥的診斷標準:“麥當勞標準”2005年修訂版神經學年報]2005;58:840-846)。量化ms中的失能方法包括庫茨科擴展殘疾狀態量表(edss);mri掃描;臨時神經癥狀測定量表(snrs);克虜伯疲勞嚴重度量表(fss);無行為能力狀態量表(iss);功能獨立性量表(fim);步行指數(ai);劍橋多發性硬化癥基礎評分(cambs);多發性硬化癥的功能評估(fams);心境狀態量表(poms);以及疾病影響量表(sip)。在現有技術中可以找到關于診斷和治療ms,以及進展型ms,例如ppms或smps的另外的信息,例如在hurwitz等人,annindianacadneurol.2009oct-dec[印度神經病學學院年鑒.200910月-12月];12(4):226-230;和spinalcordmedicine,principlesandpractice[脊髓醫學,原理與實踐],lin等人編,(demosmedicalpublishing,inc.[戴蒙醫學出版公司],2003)中,例如,部分v,32章,“multiplesclerosis[多發性硬化癥]”。通常,在此描述的方法可以在任何哺乳動物,優選人類上實踐。褪黑激素激動劑在此描述的方法中有用的褪黑激素激動劑包括例如褪黑激素(n-乙酰-5-甲氧基色胺,cas73-31-4)(西格瑪公司(sigma));治療失眠的circadin/neurin/prm(也稱為延長釋藥的褪黑激素)(neurimpharmaceuticalsltd),用作抗抑郁藥并且是mt1和mt2受體二者的激動劑的阿戈美拉汀/維度新/s-20098((n-[2-(7-甲氧基-1-萘基)乙基]-乙酰胺;cas138112-76-2)(施維雅公司(servierlaboratories);諾華公司(novartis));n-乙酰5-羥色胺(nas);二甲氧基丙酰胺98(百時美施貴寶公司(bristolmyerssquib));治療重性抑郁障礙的tak-375/雷美替胺/rozerem(n-[2-[(8s)-2,6,7,8-四氫-1h-環戊二烯并[e][1]苯并呋喃-8-基]乙基]丙酰胺;cas196597-26-9))(武田藥品工業株式會社(takedapharmaceuticalcompanylimited))、他司美瓊/hetlioz(n-[[(1r,2r)-2-(2,3-二氫-1-苯并呋喃-4-基)環丙基]甲基]丙酰胺)(萬達制藥公司(vandapharmaceuticals))。luzindole(褪黑素抑制劑,n-[2-(2-芐基-1h-吲哚-3-基)乙基]乙酰胺)是具有針對mt2褪黑激素受體的15至25倍較高的親合力的非選擇性配體,并且4p-pdotn-(4-苯基-1,2,3,4-四氫化萘-2-基)丙酰胺或n-[(2s,4s)-4-苯基-1,2,3,4-四氫化萘-2-基]丙酰胺或n-[(2r,4r)-4-苯基-1,2,3,4-四氫化萘-2-基]丙酰胺)是選擇性mt2配體;iik7(n-丁酰基-2-(2-甲氧基-6h-異吲哚[2,1-a]吲哚-11-基)-乙胺(西格瑪公司(sigma))、文拉法辛或郁復伸(1-[2-(二甲氨基)-1-(4-甲氧苯基)乙基]環已-1-醇;鹽酸化物);cas99300-78-4)(西格瑪公司);以及相關的ssri。褪黑激素受體拮抗劑還包括以下項:bms-214778(n-[[(1r,2r)-2-(2,3-二氫-1-苯并呋喃-4-基)環丙基]甲基]丙酰胺);舍曲林4(1s,4s)-4-(3,4-二氯苯基)-n-甲基-1,2,3,4-四氫化萘-1-胺;帕羅西汀(3s,4r)-3-(1,3-苯并二唑-5-基氧甲基)-4-(4-氟苯基)哌啶;氟西汀(n-甲基-3-苯基-3-[4-(三氟甲基)苯氧基]丙-1-胺);ammtc(n-[(6-甲氧基-9-甲基-1,2,3,4-四氫咔唑-4-基)甲基]乙酰胺)。小分子mt1和2特異性受體激動劑的另外的實例可以發現于以下文獻:us20140011849;wo2007148808(褪黑激素(n-乙酰基-5-甲氧色胺));us20090042861;wo2006107019a1((s)-n-[2-(1,6,7,8-四氫-2h-茚并[5,4-b]呋喃-8-基)乙基]丙酰胺);us13/751,011;us14/688,301和us20140357710(n-[[(1r,2r)-2-(2,3-二氫-1-苯并呋喃-4-基)環丙基]甲基]丙酰胺);us20050164987/wo2005063297(ml-23或n-[2-(5-甲氧基-1h-吲哚-3-基)乙基]-2,4-二硝基苯胺);us20050137247(ly-156735;bms-214778);us8859593;us8389544;us20090209638,wo2007137247和wo2011126948。在一些實施例中,褪黑激素激動劑是雷美替胺((s)-n-[2-(1,6,7,8-四氫-2h-茚并[5,4-b]呋喃-8-基)乙基]丙酰胺)、阿戈美拉汀(n-[2-(7-甲氧基萘-1-基)乙基]乙酰胺)、他司美瓊((1r,2r)-n-[2-(2,3-二氫苯并呋喃-4-基)環丙基甲基]丙酰胺)、或tik-301(ly-156735)(n-[(2r)-(6-氯-5-甲氧基-1h-吲哚-3-基)丙基]乙酰胺)。在一些實施例中,這些方法包括給予aa-nat(芳烷基胺n-乙酰轉移酶)和/或hiomt(羥基吲哚-o-甲基轉移酶)的激動劑,除了其他活性,它們在褪黑激素合成中發揮作用。這些可以包括血管緊張素受體激動劑,例如l-162,313(5,7-二甲基-2-乙基-3-[[4-[2(正-丁氧基羰基亞磺酰氨基)-5-異丁基-3-噻吩基]苯基]甲基]-咪唑[4,5-b]吡啶)和[val5]-血管緊張素ii乙酸鹽水合物。rev-erb/ror激動劑在一些實施例中,除了褪黑激素激動劑之外或作為褪黑激素激動劑的替代,這些方法包括給予rev-erb(例如rev-erbα和/或rev-erbβ)的和/或視黃酸受體相關的孤兒受體(ror,例如rorα,rorβ和/或rorγ的激動劑)的激動劑,其中的一些是本領域已知的。例如,這些方法可以包括(或排除)給予天然rev-erb/ror配體,例如血紅素;膽固醇/膽固醇硫酸酯;7α-羥基膽固醇;7β-羥基膽固醇;7-酮基膽固醇;20α-羥基膽固醇;22r-羥基膽固醇;25-羥基膽固醇;24s-羥基膽固醇;24r-羥基膽固醇;24,25-環氧膽固醇;硬脂酸;全反式維甲酸;新魯斯可皂苷元;或(25s)-魯斯可皂苷元。可替代地或此外,這些方法可以包括給予合成的rev-erb配體,例如gsk4112、sr9009;sr9011;gsk2945;gsk0999;gsk5072;和/或gs2667;和/或合成的ror配體,例如t0901317;sr1078;sr3335(也稱為sr3335/ml176);sr1001;sr2211;sr1555;地高辛;熊果酸;ml209;和/或在zhang,w.等人,mol.pharmacol[分子藥理學].82,583-590(2012)(例如化合物1a;化合物1b:n-(4,6-二甲基苯并[d]噻唑-2-基)-3-甲基噻吩-2-甲酰胺;化合物1c:n-(2-(4-乙基苯基)-2h-苯并-[d][1,2,3]三唑-5-基)丙酰胺;和/或抑制劑y:n-(5-苯甲酰基-4-苯基噻唑-2-基)-2-(4-(乙磺酰基)苯基)乙酰胺。參見例如kojetin和burris,naturereviewsdrugdiscovery13,197-216(2014)。標準治療在一些實施例中,在此描述的治療包括結合以下用于ms的標準治療給予褪黑激素激動劑,這些標準治療例如給予皮質類固醇療法、干擾素β-1b、醋酸格拉默、米托蒽醌、芬戈莫德、特立氟胺、富馬酸二甲酯、那他珠單抗、大麻,或其組合。在一些實施例中,在此描述的治療是結合用于ms的一個或多個癥狀的治療進行給予,這些癥狀例如是抑郁和疲勞、膀胱功能障礙、痙攣狀態、疼痛、共濟失調、以及意向震顫;此類治療包括藥理學試劑、鍛煉、以及適當的矯正術。關于ms的診斷和治療的另外的信息可以發現于nationalmssocietywebsite[國家ms協會網站]上,在萬維網上,網址為nationalmssociety.org。在一些實施例中,在受試者被鑒定為在特定時段內,患有或可能發展ms的季節性惡化,例如,被鑒定為具有低于參比水平的褪黑激素的水平的情況下,給予用于進展型ms的治療,包括米托蒽醌或那他珠單抗。藥物組合物在此描述的方法包括制造和使用藥物組合物,這些藥物組合物包含作為活性成分的褪黑激素激動劑。還包含的是藥物組合組分自身。藥物組合物典型地包含藥學上可接受的載體。如在此使用,表達“藥學上可接受的載體”包括與藥物給予可相容的鹽、溶劑、分散介質、涂料、抗細菌的和抗真菌的藥劑、等滲劑和吸收延遲劑等。還可以將補充性活性化合物摻入組合物中。典型地,藥物組合物被配制成與預期的給予途徑相容。在本發明的方法中尤其有用的給予途徑的實例包括腸胃外(例如靜脈內的)、鞘內、口服、以及鼻腔或鼻內(例如通過作為滴劑或吸入劑給予)給予。對于并不跨越血腦屏障的化合物,可以使用直接進入cns或csf的遞送,例如使用植入的鞘內泵(參見例如borrini等人,archivesofphysicalmedicineandrehabilitation[物理醫學與康復檔案]2014;95:1032-8;penn等人,n.eng.j.med.320:1517-21(1989);和rezai等人,painphysician[疼痛醫師]2013;16:415-417),或納米顆粒,例如金納米顆粒(例如葡萄糖包衣的金納米顆粒,參見例如gromnicova等人(2013)plosone8(12):e81043)。配制并且遞送適合的藥物組合物的方法是本領域已知的,參見例如以下系列中的圖書:drugsandthepharmaceuticalsciences:aseriesoftextbooksandmonographs[藥物與藥物科學:教科書和專著系列](dekker,ny);和allen等人,ansel′spharmaceuticaldosageformsanddrugdeliverysystems[安塞爾氏藥物劑型和藥物遞送系統],lippincottwilliams&wilkins出版社;第8版(2004)。適合于可注射使用的藥物組合物可以包括無菌水溶液(在水溶性的情況下)或分散體、以及用于臨時制備無菌可注射溶液或分散液的無菌粉末。對于靜脈內的給予,適當的載體包括生理鹽水、抑菌水、cremophoreltm(basf[巴斯夫公司],帕西波尼(parsippany),新澤西州(n.j.))或磷酸酯緩沖鹽水(pbs)。在所有情況下,該組合物必須是無菌的并且必須具有達到容易注射的程度的流動性。它在制造和儲存條件下應該穩定并且必須抗諸如細菌和真菌的微生物污染作用而保存。該載體可以是包含以下物質的溶劑或分散介質:例如,水、乙醇、多元醇(例如,甘油、丙二醇和液體聚乙二醇等),及其適合的混合物。可以例如通過使用一種包衣(如卵磷脂)、通過在分散情況下維持所需顆粒大小以及通過使用表面活性劑來維持適當的流動性。防止微生物的作用可以通過各種抗細菌劑和抗真菌劑,例如對羥苯甲酸酯、三氯叔丁醇、苯酚、抗壞血酸、硫柳汞等來實現。在許多情況下,優選在組合物中納入等滲劑,例如糖、多元醇如甘露醇、山梨醇、氯化鈉。可以通過在組合物中包含延遲吸收的一種藥劑(例如單硬脂酸鋁和明膠)而使可注射組合物的吸收延長。按照需要,可以通過將活性化合物以需要的量加入具有以上列舉的組分中的一種或多種組合的適當溶劑中,隨后進行無菌過濾來制備無菌注射液。通常,通過將活性化合物加入無菌載體中來制備分散體,該無菌載體包含基礎分散介質以及來自以上列舉的那些所需的其他成分。就用于制備無菌可注射溶液的無菌粉末而言,優選制備方法為真空干燥和冷凍干燥,這些方法產生活性成分的粉末以及來自其以前的無菌過濾溶液的任何另外的所需成分。對于口服給予,可以用惰性稀釋劑或可食用載體來配制組合物。出于口服治療性給藥的目的,可以將活性化合物隨賦形劑一起加入并且以片劑、錠劑或膠囊劑(例如明膠膠囊劑)的形式使用。口服組合物還可以使用一種用作嗽口水的液體載體而被制備。可以包含藥學上相容的粘合劑和/或佐劑材料作為組合物的一部分。片劑、丸劑、膠囊劑、錠劑等可以包含以下成分或具有類似性質的化合物中的任一種:粘合劑,如微晶纖維素、黃芪膠或明膠;賦形劑,如淀粉或乳糖,崩解劑,如海藻酸、primogel、或玉米淀粉;潤滑劑,如硬脂酸鎂或氫化植物油;助流劑,如膠體二氧化硅;甜味劑,如蔗糖或糖精;或調味劑,如薄荷、水楊酸甲酯或橙味調味品。對于通過吸入給藥,化合物可以從加壓容器或分配器(其中包含合適的推進劑,例如氣體(如二氧化碳))、或噴霧器以氣溶膠噴霧形式遞送。此類方法包括美國專利號6,468,798中描述的那些。可以通過適合給予核酸劑,例如dna疫苗的任何方法,來給予是或包含核酸的治療性化合物。這些方法包括基因槍、生物注射器、和皮膚貼劑,連同無針方法,例如美國專利號6,194,389中披露的微顆粒dna疫苗技術,以及如在美國專利號6,168,587中披露的使用粉狀疫苗的哺乳動物透皮無針疫苗接種。另外,鼻內遞送是可能的,如尤其描述于hamajima等人,clin.immunol.immunopathol.[臨床免疫學和免疫病理學],88(2),205-10(1998)中。脂質體(例如,如描述于美國專利號6,472,375中)和微囊包封可以用于遞送在此描述的化合物。還可以使用生物可降解微顆粒遞送系統(例如,如描述于美國專利號6,471,996中)。在一個實施例中,將這些治療性化合物與保護這些治療性化合物免于從體內快速消除的載體一起制備,如控釋配制品,包括植入物和微囊化的遞送系統。可使用生物可降解、生物相容的聚合物,如乙烯醋酸乙烯酯、聚酸酐、聚乙醇酸、膠原、聚原酸酯及聚乳酸。此類配制品可以使用標準技術制備,或例如從alza公司(alzacorporation)和nova制藥公司(novapharmaceuticals,inc.)購買獲得。脂質體懸浮液(包括用細胞抗原的單克隆抗體靶向到選擇的細胞的脂質體)也可以用作藥學上可接受的載體。這些可以根據在本領域中的普通技術人員已知的方法而制備,例如,如在美國專利號4,522,811中所說明的。藥物組合物可以與給藥的說明書一起包括在容器、包裝、或分配器,例如單次劑量分配器中。容器、包裝、或分配器還可以被包括為試劑盒的一部分,該試劑盒可以包含例如用于一天的、一周的、或一個月的治療的足夠的單次劑量分配器。劑量可以例如通過細胞培養或實驗動物中的標準制藥程序來確定化合物的劑量、毒性和治療效果,例如,用于確定ld50(使50%的群體致死的劑量)和ed50(在50%的患者群體中治療有效的劑量)。在毒性和治療效果之間的劑量比為治療指數,它可以表示為比率ld50/ed50。表現出高治療指數的化合物是優選的。盡管可以使用表現出有毒副作用的化合物,但是應該小心設計將此類化合物靶向至受影響的組織的部位的遞送系統,從而將對未感染的細胞的潛在損傷最小化,并且由此減少副作用。從細胞培養測定和動物研究獲得的數據可以用于配制一系列的用于在人類中使用的劑量。優選這些化合物的劑量處于包括ed50在內的有很小毒性或沒有毒性的循環濃度范圍內。該劑量可根據所應用的劑型和所使用的給藥途徑在該范圍內變化。對于用于本發明方法的任何化合物,均可根據細胞培養試驗初步估計治療有效劑量。一種劑量可以在動物模型中被配制以達到在細胞培養中確定的一種循環血漿濃度范圍,該范圍包括ic50(即該測試化合物的完成半最大癥狀的抑制的濃度)。該信息可用于更精確地確定在人中有用的劑量。可以例如通過高效液相色譜法來測量血漿中的水平。“有效量”是足以實現有益的或希望的結果的量。例如,治療量為達到所需療效的量。所述量可與預防上有效量相同或不同,所述預防上有效量為預防疾病或疾病癥狀的發作所需的量。可以在一次或多次施用或應用或給藥時施用有效量。組合物的治療上有效量取決于所選的組合物。可以從每天一次或多次至每周一次或多次來給予組合物;包括每隔一天一次。技術人員將理解,某些因素可以影響有效治療受試者所需的劑量和時程,包括但不限于疾病或障礙的嚴重性、先前的治療、受試者的一般健康狀況和/或年齡,以及存在的其他疾病。此外,用治療有效量的在此描述的組合物對受試者進行的治療可以包括單一治療或一系列治療。實例本發明在以下實例中進一步說明,這些實例不得限制權利要求書中所描述的本發明的范圍。實驗程序在以下所示的實例中使用以下材料和方法。患者。在同一年的9月和11月之間,從位于勞爾卡雷亞神經研究所(raúlcarreainstituteforneurologicalresearch)(fleni)的ms診所募集根據mcdonald[麥克唐納]標準(polman等人,2011),患有復發-緩解型ms的連續患者。所有患者都住在布宜諾斯艾利斯市(buenosairescity)(緯度34.6°s,經度58.4°w)。在2011-2012年期間,在上午8和9點之間,每個季節收集血清和首次晨尿,并且儲存在-80℃。在2015年的1月和2月之間,募集第二群組的26名復發-緩解型ms患者,并且在上午8和9點之間收集血清和全血,用于cd4+t細胞分離和褪黑激素測量。對于每個樣品,記錄嚴格的收集日期和時間,以及處理。如下根據南半球定義季節:夏季(1月-3月),秋季(4月-6月),冬季(7月-9月),春季(10月-12月)。由研究所倫理委員會批準研究實驗方案,并且所有受試者都簽署了知情同意書。動物和eae。如下誘導eae:用100μgmog35-55和500μg結核分枝桿菌提取物h37ra(difco公司)免疫小鼠。在第0天和第2天,用200ng百日咳毒素對小鼠進行腹膜內注射。在下午7:00,每天給予褪黑激素(5mg/kg)或載體(0.01%dmso)。流式細胞術染色和獲取對于細胞內細胞因子染色,在37℃,用佛波醇12-豆蔻酸酯13-乙酸酯(50ng/ml;西格瑪公司)、離子霉素(1μg/ml;西格瑪公司)和莫能菌素(golgistop;1μg/ml;bd生物科學公司(bdbiosciences))刺激細胞4h。在表面標記被染色后,根據制造商的說明書(bd生物科學公司),將細胞固定并且使其可滲透。針對細胞因子的所有抗體都來自biolegend公司。所有實驗都在同一時間開始(上午8-9點)。用lsrii或facsaria(bd生物科學公司)收集數據,然后用flowjo軟件(treestar)進行分析。細胞因子的測量。在72-96h后,通過如先前描述的酶聯免疫吸附測定,在組織培養上清液中測量分泌的細胞因子(farez等人,2009)。定量rt-pcr。用rnaeasy柱(凱杰公司(qiagen),美國)提取rna,然后根據制造商的說明書(美國應用生物系統公司(appliedbiosystems))制備cdna,并且將其用作用于實時pcr的模板。所有引物和探針都是由美國應用生物系統公司(appliedbiosystems)提供的,并且將它們在viia7實時pcr系統(美國應用生物系統公司)上使用。表達被標準化為管家基因gapdh的表達。免疫印跡分析。對于免疫印跡分析而言,用補充有蛋白酶抑制劑“雞尾酒(cocktail)”(西格瑪-奧德里奇公司(sigma-aldrich))的放射免疫沉淀反應緩沖液裂解細胞。用電泳,通過4%-12%bis-trisnupage凝膠(英杰公司(invitrogen),美國)分解不同t細胞亞群的總裂解液,并且將其轉移到pvdf膜(密理博公司(millipore))上。使用以下第一抗體:抗ror-α(艾博抗公司(abcam));抗mtnr1a(圣克魯茲生物技術公司(santacruz))、抗總的和磷酸化的erk1/2(cellsignalling)、抗總c/ebpα(cellsignaling公司)、抗磷酸化c/ebpα(cellsignaling公司)、抗nfil3(圣克魯茲生物技術公司)、以及抗gadph(艾博抗公司)。如制造商(pierce公司)提示的,用supersignalwestfemto最高靈敏度底物使印跡顯色。臨床數據。從我們的ms患者數據庫檢索臨床數據。將從2007年直至2012年發生的復發次數用于計算每月的和季度的惡化率。惡化被定義為由神經學檢查確認的新癥狀的發展或現存癥狀的加劇,持續至少48小時,并且之前是持續至少30天的穩定性或改善。褪黑激素、維生素d、uvb和感染評估。在勞爾卡雷亞神經研究所的(raúlcarreainstituteforneurologicalresearch)(fleni)的臨床實驗室,將維生素d水平量化。通過如先前描述的elisa(graham等人,1998)(genwaybiotech公司),測量為主要褪黑激素代謝物并且已經與夜間褪黑激素水平良好相關的6-羥基硫酸褪黑激素(6-sm)(graham等人,1998)。對于一些實驗而言,使用競爭elisa試劑盒(genwaybiotech公司)測量血清褪黑激素。由政府官員提供研究的時段期間,在布宜諾斯艾利斯市中,上呼吸道感染的官方報告。通過giovanni系統(ht中://disc.sci.gsfc.nasa.gov/giovanni),從nasa衛星獲得布宜諾斯艾利斯位置的uv入射。動物和eae。mtnr1a和ror-α基因敲除小鼠購買自杰克遜實驗室(jacksonlaboratories)。c57bl/6野生型購買自拉普拉塔大學的獸醫學院(facultyofveterinaryinlaplatauniversity)和杰克遜實驗室。nfil3缺陷小鼠由chenzhu提供;rev-erbα缺陷小鼠由mitchlazar(賓夕法尼亞大學(universityofpennsylvania),費城(philadelphia),美國)提供,并且c/ebpα基因敲除小鼠由danieltehen(貝斯以色列女執事醫療中心(bethisraeldeaconessmedicalcenter),波士頓(boston),美國)提供。如下誘導eae:用100μgmog35-55(mevgwyrspfsrvvhlyrngk)和500μg結核分枝桿菌提取物h37ra(difco公司)免疫小鼠。在第0天和第2天,用200ng百日咳毒素對小鼠進行腹膜內注射。在下午7:00,每天給予褪黑激素(5mg/kg)或載體(0.01%dmso)。所有實驗都是根據哈佛大學醫學院(harvardmedicalschool)的研究機構動物護理和使用委員會(iacuc)和ibyme規定的指南進行的。cns浸潤液的分離。如所述分離cns浸潤液(mascanfroni等人,2013)。用冰冷的pbs灌注小鼠。取出腦和脊髓,并且在包含iii型膠原酶(2mg/ml;worthington公司)和dna酶(20單位/ml;西格瑪-奧德里奇公司)的pbs中孵育。然后將組織勻漿,并且上樣到30%-37%-70%percoll梯度上,用于cns浸潤液的富集。體外小鼠t細胞分化。使用磁珠(cd4+t細胞分離試劑盒,美天旎公司(miltenyibiotec)),初始cd4+t細胞(cd4+cd44locd62lhicd25-)來自c57bl/6野生型、mtnr1a-、nfil3-、rev-erbα、c/ebpα-缺陷的或rorα缺陷的小鼠的脾和淋巴結。所有實驗都在上午7和9點之間開始。用板結合的抗cd3(2μg/ml;14-0031-86;億生物科技(ebioscience))和抗cd28(2μg/ml;16-0281-86;億生物科技)活化細胞。添加小鼠il-27(30ng/ml;34-8271;biolegend公司),用于產生tr1細胞。添加il-6(30ng/ml;406-ml-025;r&d系統公司(r&dsystems))、tgf-β1(15ng/ml;130-095-067;美天旎公司)、抗il-4(2.5μg/ml;c17.8;biolegend公司)以及抗ifn-γ(5μg/ml;xmg1.2;biolegend公司),用于產生th17細胞。在第2天添加重組小鼠il-23(30ng/ml;1887-ml-010;r&d系統公司)。對于一些實驗,作為替代,使用il-6和il-1β(10ng/ml;401-ml-025;r&d系統公司)或tgf-β1和il-21(100ng/ml;594-ml-010;r&d系統公司),用于th17細胞分化。使用il-12(30ng/ml;419-ml-010;r&d系統公司)和抗il-4(2.5μg/ml;c17.8;biolegend公司),用于產生th1細胞。添加il-4(30ng/ml;404-ml-010;r&dsystems)和抗ifn-γ(5μg/ml;xmg1.2;biolegend公司),用于產生th2細胞。使用tgf-β1(15ng/ml;130-095-067;美天旎公司),用于產生foxp3+tregs。在培養開始時和在第2天,以2-20ng/ml的終濃度,添加褪黑激素(gador,阿根廷)、阿戈美拉汀、和cgp-52608(西格瑪-奧德里奇公司)。體外人類t細胞分化。對于th17分化,用磁珠(初始人類cd4+t細胞分離試劑盒ii,美天旎公司)從pbmc分離初始cd45ra+cd4+t細胞,并將其以5×105個細胞/ml的密度接種在涂覆有抗cd3(2μg/ml)以及可溶性抗cd28的24孔板中,并且在以下細胞因子(il-1β(25ng/ml)、il-6(50ng/ml)、和tgf-β1(2ng/ml))與中和抗體存在下培養至ifn-g(10mg/ml)和il-4(10微克/ml)。可替代地,通過使用il-1β(25ng/ml)、il-6(50ng/ml)、和il-23(50ng/ml)與中和抗體將th17細胞分化至ifn-g(10mg/ml)和il-4(10微克/ml)。對于th1分化,在il-12(20ng/ml)和抗il-4(10μg/ml)存在下,培養cd4+t細胞。細胞因子的測量。在72-96h后,通過如先前描述的酶聯免疫吸附測定,在組織培養上清液中測量分泌的細胞因子(farez等人,2009)。定量rt-pcr。用于小鼠實驗的引物-探針混合物如下(來自美國應用生物系統公司;括號中為標識符):rorc(mm01261022_ml)、il23r(mm00519942_ml)、il10(mm0043614_ml)、i117(mm00439619_ml)、il21(mm00517640_m1)、rora(mm01173766_m1)、rorc(mm00441144_g1)、foxp3(mm00475156_m1)、tbx21(mm00450960_ml)、gata3(mm00484683_m1)、nrld1(mm00520708_m1)、nfil3(mm00600292_s1)和gapdh(mm99999915_g1)。用于人類實驗的引物-探針混合物如下(來自美國應用生物系統公司;括號中為標識符):rorc(hs01076122_m1)、il17a(hs00174383_m1)、il17f(hs00369400_m1)、il10(hs00961622_m1)、ifng(hs00989291_m1)和18s(hs03003631_g1)。染色質免疫沉淀反應。用4%多聚甲醛交聯細胞中的dna-蛋白質復合物,并且用包含1×蛋白酶抑制劑“雞尾酒”(rochemolecularbiochemicals公司)的0.35ml裂解緩沖液(1%sds,10mmedta和50mmtris-hcl,ph8.1)進行裂解。通過超聲處理剪切染色質,并且將離心后收集的上清液稀釋于緩沖液(1%tritonx-100,2mmedta,150mmnacl和20mmtris-hcl,ph8.1)中。將5μg抗體預先結合至蛋白a和蛋白gdynal磁珠(英杰公司)持續最少6h,并且用包含5%bsa的冰冷的pbs洗滌樣品三次,然后添加至稀釋的染色質,隨后進行免疫沉淀反應過夜。然后在放射免疫沉淀反應緩沖液(50mmhepes,ph7.6,1mmedta,0.7%na脫氧膽酸鹽,1%np-40和0.5mlicl)中洗滌磁珠染色質復合物三次,隨后用tris-edta緩沖液洗滌兩次。然后用1%sds和0.1mnahco3的溶液提取免疫沉淀的染色質,并且在65℃下加熱至少6h,用于逆轉多聚甲醛交聯。用qiaquickdna純化試劑盒(凱杰公司)純化dna片段,并且用sybr綠實時pcr(寶生物工程有限公司(takarabio))進行分析。信號轉導測定。在72-96h期間,用載體(dmso0.001%)、褪黑激素(2-10ng/ml)、阿戈美拉汀(2-10ng/ml)和cgp-52608(2-10ng/ml)處理極化條件下活化的細胞,并且進行裂解。將裂解液轉移至384孔聚丙烯板,并且用裝有固體點樣針的機器人微陣列點樣器(genetix公司)點樣到superepoxi片(telechem公司)上。然后如所述對這些片進行探測、處理和分析(farez等人,2009)。增殖測定。在用mog35-55進行免疫后10天,自載體或褪黑激素處理的wt小鼠獲得脾細胞,并且在mog35-55存在下,將這些細胞在體外重新刺激3天。將細胞用[3h]胸苷(1μci/孔)脈沖處理最后24h。通過流式細胞術評估產生il-17(億生物科技)、ifn-γ(biolegend公司)或il-10(bdpharmingen公司)的t細胞和foxp3+t細胞(億生物科技)的頻率。對于基于cfse的增殖測定,用1μmcfse(羧基熒光素乙酰乙酸琥珀酰亞胺酯;molecularprobes公司)標記cd4+t細胞。在lsriii(bd生物科學公司)或macsquants(美天旎公司)上獲取數據,并且用flowjo軟件(treestar)進行分析。質粒。il-10啟動子報告基因和c-maf與ahr載體如先前所描述(apetoh等人,2010),表達ror-α的載體購買自哈佛大學醫學院的plasmid。編碼c/ebpα(44627)和bmal報告基因(46824)的載體購買自addgene。由laurahooper(西南醫學中心(utsouthwestern),德克薩斯州,美國)友好地提供了用于在t細胞中的nfil3過量表達的逆轉錄病毒。由bartstaels(巴斯德研究所(institutpasteur),里爾(lille),法國,美國)友好地提供了用于在t細胞中的nr1d1過量表達的逆轉錄病毒。由vincentlaudent(巴黎高等師范大學(ecolenormalesupérieure),里昂(lyon),法國)友好地提供了nr1d1啟動子報告基因。轉染和螢光素酶測定。根據制造商的說明書(羅氏公司(roche)),在補充有10%fbs的dmem中生長hek293細胞,并且用fugenehd轉染試劑和2μg的各種質粒進行轉染。在轉染48h后,并且在用雙螢光素酶測定試劑盒(普洛麥格公司(promega))處理24h后,分析螢火蟲螢光素酶和海腎螢光素酶的活性。逆轉錄病毒轉導。將逆轉錄病毒表達構建體與eco和gag-pol病毒包膜構建體一起轉染進人胚腎hek293t細胞。在轉染72h后收集病毒上清液。通過在32℃,在聚凝胺(8μg/ml;西格瑪公司)存在下,在1200g下的離心感染細胞的方法,進行慢病毒轉導。t細胞轉移和免疫。將來自c57bl/6、mtnr1a-、rev-erbα和nfil3缺陷小鼠的經分類的脾cd4+t細胞經腹腔內注射(i.p.)轉移進rag-1缺陷小鼠中(每個小鼠10x106個細胞)。轉移十天后,檢查小鼠的cd4+t細胞重建并且用cfa中的mog35-55免疫。免疫20天后,分離t細胞并且將細胞因子染色。統計分析。使用泊松回歸模型來評估季節、6-sm水平和臨床復發次數的影響,產生發病率比率(irr)和相應的95%置信區間(ci)。使用重復測量混合模型來評估治療的作用及其與eae實驗中的時間的相互作用。使用線性回歸模型來分析血清褪黑激素水平和il-17或il-10基因表達之間的關系。適當時,使用學生t檢驗、曼-惠特尼檢驗、單向方差分析或威爾科克森秩和檢驗來分析兩種或更多種條件之間的差異。小于0.05的p值視為顯著的。除非另外指明,所有數據呈現為平均值±sem。使用statav12(statacorplp公司(statacorplp),德克薩斯州,美國)進行所有統計分析。實例1.褪黑激素水平與ms臨床復發負相關我們首先在我們的139名復發-緩解型ms患者的群組中建立了ms復發的季節性(表1)。使用泊松回歸模型,我們在發生在秋季和冬季的復發次數中檢測到32%降低(發病率比率,irr0.682,95%ci0.49-0.95,p=0.02)。因此,在此研究中使用的ms患者群組示出先前針對其他群組描述的ms復發的季節性(jin等人,2000;spelman等人,2014)。褪黑激素產生受黑暗刺激并且伴隨季節性模式,其中在秋季和冬季期間具有較高水平(brzezinski,1997)。褪黑激素影響若干生物過程,包括晝夜節律時鐘和免疫應答(brzezinski,1997)。因此,我們通過測量復發-緩解型ms患者中的6-羥基硫酸褪黑激素(6-sm)水平,研究了褪黑激素和ms疾病活性之間的關系。因為6-sm是主要褪黑激素代謝物,其在首次晨尿中的水平與夜間褪黑激素分泌強相關,支持其用于流行病學研究(graham等人,1998;mcmullan等人,2013)。與先前報告(morera和abreu,2007;ueno-towatari等人,2007)一致,我們檢測到在秋季和冬季期間增加的褪黑激素分泌,其在春季和夏季期間具有較低水平(圖1a和表1)。此外,我們發現了6-sm水平和ms惡化率之間的顯著負相關(p<0.01史匹曼(spearman)相關)。在年齡與性別調節的泊松回歸模型中進一步確認了這一點,對于每6-sm單位增加,具有復發次數中的3%降低(irr0.97,95%ci0.95-0.99,p=0.007)。最后,為了檢驗褪黑激素水平和惡化率之間的關系是否是同步的,我們延遲了復發的發生1個月(irr1.01,95%ci0.97-1.05;p=0.7)、2個月(irr1.03,95%ci0.99-1.07;p=0.1)、和3個月(irr1.03,95%ci0.99-1.07;p=0.7),其中沒有復發發生中的延遲效果的證據。我們還評估了維生素d水平,并且如先前針對我們的地區中的健康對照和ms患者所報告的(correale等人,2009;fassi等人,2003),貫穿全年,總體水平很低,其中在夏季期間具有較高水平,但是與ms復發無顯著相關(圖1b)。最后,我們并沒有檢測到ms復發和另外的環境因素(例如,如分別通過國家注冊庫和nasa衛星所確定的,報道的上呼吸道感染和uv入射)之間的關聯(圖1c、d)。因此,在秋季和冬季期間的較高褪黑激素水平與臨床復發的減少相關聯。表1.研究群體的基線和臨床特征實例2.褪黑激素改善了實驗性自身免疫性腦炎基于我們的流行病學發現,我們使用ms的實驗性自身免疫性腦炎(eae)模型,研究了褪黑激素對于cns炎癥的影響。用mog35-55免疫初始c57bl/6野生型小鼠,并且每天用褪黑激素(5mg/kg,腹膜內地)或載體處理這些小鼠。褪黑激素給予改善了eae臨床癥狀(圖2a,表2和圖7a)。eae的改善與脾、淋巴結和cns中的th17細胞的減少的個數和頻率相關聯;還在已經關聯至eae的發病機理的il-17+ifnγ+和il-17+gm-csf+cd4+t細胞中檢測到這一減少(codarri等人,2011;el-behi等人,2011;lee等人,2012a)(圖2c、d)。我們還檢測到il-10分泌cd4+t細胞中的伴隨性增加;在其他t細胞亞群、b細胞、γδt細胞或先天淋巴細胞(ilc)的個數或頻率方面,沒有檢測到顯著變化(圖2b和圖7b-d)。為了進一步表征褪黑激素對致腦炎t細胞應答的作用,我們分析了對mog35-55的回憶應答。來自褪黑激素處理的小鼠的脾細胞示出對mog35-55的降低的增殖應答(伴隨il-10產生的增加,il-17減少),然而,沒有檢測到對ifn-γ產生的顯著影響(圖2e、f)。因此,褪黑激素阻止可致腦炎性th17細胞應答。為了研究褪黑激素是否直接作用于t細胞或者它通過其對抗原遞呈細胞的影響間接控制t細胞應答,我們將來自褪黑激素處理的或對照的小鼠的、分類的cd4+t細胞與處理轉換的樹突細胞(dc)共孵育。當與分離自載體處理的小鼠的對照相比時,與分離自對照小鼠的脾dc共孵育的來自褪黑激素處理的小鼠的cd4+t細胞示出減少的增殖和il-17分泌,伴隨增加的il-10產生(圖2g、h)。相反地,當我們使用分離自褪黑激素或載體處理的小鼠的dc來活化來自對照處理的小鼠的cd4+t細胞時,我們并沒有檢測到顯著性差異。支持褪黑激素對t細胞的直接影響,褪黑激素抑制了使用mog35-55和dc的對初始2d2+轉基因t細胞的體外活化(圖2i,圖7e),或在dc不存在的情況下,抑制了使用針對cd3和cd28的抗體的對初始2d2+轉基因t細胞的體外活化(圖2j)。在mog35-55存在下,用褪黑激素預處理dc并沒有影響其活化2d2+t細胞的能力(圖2k)。褪黑激素并沒有增加用針對cd3和cd28的抗體刺激的cd4+t細胞中的凋亡,如通過以下項所示:膜聯蛋白v的分析,和通過流式細胞術的碘化丙啶染色或bcl-x1的表達水平(圖7f、g)。然而,il-10阻斷、消除了褪黑激素對t細胞增殖的抑制作用(圖7h)。表2.eae的臨床特征,涉及圖2a*p=0.05**p<0.05實例3.褪黑激素影響人類t-細胞分化然后我們研究了褪黑激素對人類cd4+t細胞的影響。此外,我們還分析了阿戈美拉汀的作用,它能活化褪黑激素依賴性信號轉導(hickie和rogers,2011)。基于在eae期間褪黑激素給予對t細胞的影響,我們將我們的研究聚焦在人類th17和tr1細胞。褪黑激素和阿戈美拉汀減少了在th17極化條件下,通過活化的人類cd4+t細胞的il-17、rorc和il17a表達的產生(圖3a-e和圖8),沒有檢測到對人類th1細胞的分化的影響(圖3d-f)。伴隨地,褪黑激素和阿戈美拉汀增加了il10表達。實際上,在tr1極化條件下,通過活化的人類cd4+t細胞,褪黑激素和阿戈美拉汀還增加了il-10的產生(圖3g、h)。為了進一步研究褪黑激素對ms中的免疫應答的作用,我們分析了血清褪黑激素水平和在26名rrms患者的外周cd4+t細胞中的il17與il10表達之間的關聯(表3)。使用經年齡與性別調節的線性回歸模型,我們檢測到了血清中的褪黑激素和外周cd4+t細胞中的il17表達之間的負相關(p=0.012):較高血清褪黑激素水平與較低il17表達相關聯(表4)。相反地,線性回歸分析鑒定了外周cd4+t細胞中的較高il10表達和血清中的褪黑激素之間的正相關(p=0.003)。我們并沒有檢測到褪黑激素水平和cd4+t細胞中的rorc、nr1d1或nfil3的表達之間的顯著相關(表4)。因此,褪黑激素體外調節人類th17和tr1細胞的分化,并且內源褪黑激素水平與rrms患者中的外周cd4+t細胞中的il17和il10的表達水平相關聯。表3.將ms群組的基線和臨床特征用于表達研究表4.褪黑激素和分離自ms患者的cd4+細胞中的il10與il17f之間的關聯。變量系數標準誤差95%cip值il100.0090.000530.007-0.0110.003il17-3.920.89-6.4--1.40.012rorc0.0010.0011-0.004-0.0030.387nr1d10.000009510.0000625-0.0002-0.00010.882nfil30.000130.000080.00006-0.00030.163實例4.褪黑激素干擾th17產生與th1細胞一起,th17細胞被認為促成ms和eae的發病機理(kom等人,2009)。基于褪黑激素對eae和通過cd4+t細胞的il-17產生的抑制作用,我們研究了褪黑激素對鼠th17細胞分化的影響。如通過對于th17細胞分化為完全致病細胞而言所必需的rorc、il-17、和il-23的表達所示,褪黑激素干擾th17細胞的體外分化;沒有檢測到對foxp3+itregs、th1或th2細胞的分化的影響。(圖4a、b和圖9)(lee等人,2012b)。褪黑激素還增加了與非致病th17細胞關聯的il-10的表達(lee等人,2012b;mcgeachy等人,2007)(圖4a、b)。已經示出ifnγ和il-2限制th17細胞分化(korn等人,2009)。然而,在我們的研究中,在ifnγ阻斷抗體存在下,th17細胞發生分化,并且il-2阻斷抗體不能消除褪黑激素對th17分化的抑制(圖10a、b)。因此,褪黑激素通過獨立于ifnγ或il-2的機制,抑制了th17細胞分化。褪黑激素的生理濃度導致了受細胞膜和細胞核受體控制的信號傳導途徑的活化(brzezinski,1997)。由多種組織,包括免疫系統的細胞表達褪黑激素膜受體mtnr1a(jockers等人,2008;pozo等人,1997)。此外,褪黑激素結合細胞核類視黃醇相關的孤兒受體α(ror-α),該受體還由免疫細胞表達(pozo等人,2004),并且在th17發育中發揮作用(yang等人,2008)。我們檢測到th17細胞上的mtnr1a和ror-α兩者的表達(圖10c、d)。為了研究關于褪黑激素對th17細胞的影響,mtnr1a信號轉導的作用,我們使用mtnr1a特異性激動劑阿戈美拉汀和雷美替胺(karim等人,2006)(圖10e)。類似于我們關于褪黑激素的觀察,通過阿戈美拉汀或雷美替胺的mtnr1a活化抑制了th17細胞的分化(圖4c、d和圖10f、g)。相反地,褪黑激素不能抑制使用的mtnr1a缺陷的(mtnr1ako)th17細胞的分化(圖4e、f)。因此,mtnr1a介導了褪黑激素對th17細胞分化的抑制作用。實例5.褪黑激素經由erk1/2和c/ebpα活化抑制了th17細胞分化rev-erbα(由nr1d1編碼)是通過限制nfil3(rorc轉錄的直接抑制劑)的表達促進th17分化的晝夜節律時鐘的組分(yu等人,2013)。褪黑激素調節了晝夜節律的和季節性的時鐘二者的活性(pévet,2003)。實際上,褪黑激素水平示出與nr1d1表達的晝夜節律逆相關,提示褪黑激素影響rev-erbα表達(kojetin和burris,2014)。因此,我們研究了褪黑激素是否作用于rev-erbα,從而抑制th17細胞分化。使用反向蛋白質陣列(farez等人,2009),我們分析了在t細胞中由褪黑激素觸發的信號傳導途徑,并且檢測了在erk1/2的活化中,mtnr1a依賴性增加(圖4g、h;圖10h、i)。應注意,erk1/2抑制已經先前示出增強了th17細胞分化(tan和lam,2010),并且erk1/2磷酸化已經與rev-erb蛋白的減少的表達相關聯(castellano等人,2014;kojetin和burris,2014),但是尚未表征涉及的機制及其針對t細胞的相關性。通過nr1d1啟動子的生物信息學分析,我們鑒定了用于caat/增強子結合蛋白α(c/ebpα,在細胞分化的調節中涉及的一種亮氨酸拉鏈轉錄因子)的結合位點(lekstrom-himes和xanthopoulos,1998)。c/ebpα是由磷酸化活化的erk1/2的下游靶標(johnson,2005)。因此,我們分析了erk1/2是否以c/ebpα依賴性方式調節nr1d1啟動子的轉錄活性。在褪黑激素存在下,th17細胞分化導致c/ebpα磷酸化和c/ebpα向nr1d1啟動子的募集(圖4i、j)。在mtnr1akot細胞中并且在erk1/2抑制劑uo216存在下,抑制了c/ebpα磷酸化和向nr1d1啟動子的募集(圖4i、j)。因此,褪黑激素以mtnr1a-和erk1/2依賴性方式,觸發了c/ebpα向nr1d1啟動子的募集。為了分析c/ebpα對nr1d1啟動子的轉錄活性的影響,我們使用了其中nr1d1啟動子控制螢光素酶表達的受體構建體。用褪黑激素或阿戈美拉汀處理nr1d1受體轉染的hek293細胞,導致降低的螢光素酶活性,并且通過c/ebpα過量表達實現了類似的效果(圖4k)。最后,為了研究c/ebpα對褪黑激素抑制th17細胞分化的作用,我們使用了c/ebpα缺陷t細胞(yang等人,2005)。c/ebpα缺陷消除了由褪黑激素誘導的nr1d1表達的降低和th17分化的抑制(圖4l、m)。因此,褪黑激素通過mtnr1a、erk1/2和c/ebpα介導的機制,抑制了th17的分化。此外,在rev-erbα激動劑sr9009(5微摩爾)存在或不存在下,通過添加tfg-b、il-6(0hr)和il-23(48hr)將cd4+初始t細胞分化為th17細胞,并且在72h后通過rt-pcr進行分析。*未配對t檢驗的p<0.05。示于圖12中的結果示出,rev-erb激動劑抑制了向th17細胞的分化。實例6.褪黑激素通過誘導nfil3,抑制了th17細胞中的ror-γt和ror-α表達。nfil3通過抑制ror-γt的表達,限制了th17細胞分化(yu等人,2013)。rev-erbα抑制了nfil3表達(yu等人,2013)。因此,我們假設由褪黑激素誘導的nr1d1表達的降低導致rorc表達的nfil3依賴性抑制(圖5a)。我們檢測了在th17細胞中,而不是在th0或tr1細胞中的nr1d1表達(圖5b)。在th17細胞分化期間,褪黑激素抑制了nr1d1表達,導致ror-γt受體nfil3的表達的伴隨增加(圖5c、d)。與我們關于th17細胞分化的結果一致,由褪黑激素調節rev-erbα和nfil3表達是通過其膜受體mtnr1a和erk1/2介導的(圖5c-g)。在nr1d1過量表達實驗中并且通過使用rev-erbα缺陷t細胞,確認了rev-erbα表達的調節與通過褪黑激素調節th17細胞分化的相關性。nr1d1過量表達和rev-erbα缺陷消除了褪黑激素對th17細胞分化的影響(圖5h-k)。因此,由褪黑激素觸發的mtnr1a依賴性信號轉導通過調節rev-erbα表達抑制了th17細胞分化。ror-α促進了th17細胞分化(yang等人,2008)。因此,通過特異性激動劑cgp52608的ror-α活化,促進了th17細胞分化(圖4c、d)。由褪黑激素直接活化了ror-α(brzezinski,1997)。實際上,褪黑激素促進了mtnr1a缺陷th17細胞的分化(圖4e),提示褪黑激素觸發的mtnr1a信號轉導干擾了由ror-α促進的th17細胞分化。基于nfil3對ror-γt表達和th17細胞分化的抑制作用(yu等人,2013),我們還研究了nfil3是否還抑制ror-α表達。生物信息學分析鑒定了rora和rorc啟動子中的nfil3結合位點。因此,在褪黑激素存在下,在th17極化條件下,伴隨ror-α和ror-γt二者的減少的表達,我們檢測了在活化的cd4+t細胞中,nfil3向rora和rorc啟動子的募集(圖5l、m)。然后我們研究了nfil3表達的調節與th17細胞分化的調節的相關性。nfil3的過量表達(圖5n、o)和nfil3缺陷(圖5p、q)消除了褪黑激素對th17細胞分化的抑制作用。因此,由褪黑激素調節nfil3表達介導了其對體外th17細胞的分化的抑制作用。為了評估mtnr1a和nfil3對體內褪黑激素對th17細胞分化的抑制的作用,我們使用了用野生型、mtnr1a、rev-erbα或nfil3缺陷cd4+t細胞重建的并且用cfa中的mog35-55免疫的rag-1缺陷小鼠。與我們的體外觀察一致,mtnr1a、rev-erbα和nfil3缺陷消除了體內褪黑激素對th17細胞分化的抑制(圖5r、圖11)。實際上,我們檢測到響應于用mtnr1a-、rev-erbα或nfil3-缺陷t細胞重建的小鼠的治療,th17細胞分化的增加最可能反映了褪黑激素對ror-α的非對抗激動活性,及其對th17細胞的分化的促進作用。總之,這些數據提示褪黑激素經由通過nfil3依賴性機制抑制ror-γt和ror-α表達,干擾了th17細胞分化。實例7.褪黑激素經由erk1/2和ror-α促進tr1細胞分化產生cd4+il-10的tr1細胞在調節免疫應答中發揮重要作用(pot等人,2011;roncarolo等人,2006)。通過褪黑激素給予改善eae與產生il-10的t細胞的增加相關(圖2)。因此,我們研究了在tr1極化條件下,褪黑激素對初始cd4+t細胞的活化的影響。我們發現,褪黑激素促進il-10和tr1相關分子il21、ahr和cmaf的表達(apetoh等人,2010)(圖6a)。此外,褪黑激素促進體外tr1細胞的抑制活性(圖6b)。然后我們研究了褪黑激素影響tr1調節細胞的潛在機制。通過tr1細胞,我們檢測到mtnr1a和ror-α兩者的表達(圖10c、d)。實際上,阿戈美拉汀和cgp52608兩者分別是mtnr1a和ror-α的特異性激動劑,促進了tr1細胞分化(圖6c、d)。與這些結果一致,mtnr1a缺陷或由uo126抑制mtnr1a活化的erk1/2通過褪黑激素干擾了tr1分化的促進(圖6e、f)。應注意,報道erk1/2活化通過cd4+t細胞促進了cmaf依賴性il-10生產(saraiva等人,2009)。此外,ror-α缺陷通過褪黑激素抑制了由il-27誘導的tr1細胞的分化及其促進(圖6g)。ror-α通過結合靶基因中的ror反應元件(rore)發揮其生物效應(jetten,2009)。生物信息學分析鑒定了il10啟動子中的ror-α結合位點(圖6h),提示褪黑激素可以增加ror-α向il10啟動子的募集,并且因此增加il10轉錄。與這一假設一致,在褪黑激素存在下,在tr1極化條件下,在t-細胞活化后,我們檢測到ror-α與il10啟動子的增加的結合(圖6h)。此外,在報告基因測定中,ror-α反式活化了il10啟動子,并且與芳烴受體(ahr)和c-maf協同促進了其促進il10表達的能力(apetoh等人,2010;gandhi等人,2010)(圖6i)。總之,這些數據提示褪黑激素通過其對mtnr1a和ror-α的影響促進了tr1細胞分化(圖6j)。參考文獻apetoh,l.,quintana,f.j.,pot,c.,joller,n.,xiao,s.,kumar,d.,bums,e.j.,sherr,d.h.,weiner,h.l.,andkuchroo,v.k.(2010).thearylhydrocarbonreceptorinteractswithc-maftopromotethedifferentiationoftype1regulatorytcellsinducedbyil-27.nat.immunol.11,854-861。ascherio,a.,munger,k.l.,lennette,e.t.,spiegelman,d.,hernan,m.a.,olek,m.j.,hankinson,s.e.,andhunter,d.j.(2001).epstein-barrvirusantibodiesandriskofmultiplesclerosis:aprospectivestudy.jama286,3083-3088。ascherio,a.,munger,k.l.,andlünemann,j.d.(2012).theinitiationandpreventionofmultiplesclerosis.naturereviewsneurology8,602-612。ascherio,a.,munger,k.l.,andsimon,k.c.(2010).vitamindandmultiplesclerosis.thelancetneurology9,599-612。ascherio,a.,munger,k.l.,white,r.,k.,simon,k.c.,polman,c.h.,freedman,m.s.,hartung,h.-p.,miller,d.h.,montalban,x.,etal.(2014).vitamindasanearlypredictorofmultiplesclerosisactivityandprogression.jamaneurol71,306。astier,a.l.,meiffren,g.,freeman,s.,andhafler,d.a.(2006).alterationsincd46-mediatedtr1regulatorytcellsinpatientswithmultiplesclerosis.journalofclinicalinvestigation116,3252-3257。beecham,a.h.,patsopoulos,n.a.,xifara,d.k.,davis,m.f.,kemppinen,a.,cotsapas,c.,shah,t.s.,spencer,c.,booth,d.,goris,a.,etal.(2013).analysisofimmune-relatedlociidentifies48newsusceptibilityvariantsformultiplesclerosis.natgenet45,1353-1360。brzezinski,a.(1997).melatonininhumans.nengljmed336,186-195。castellano,i.,ercolesi,e.,andpalumbo,a.(2014).nitricoxideaffectserksignalingthroughdown-regulationofmapkinasephosphataselevelsduringlarvaldevelopmentoftheascidiancionaintestinalis.plosone9,e102907。codarri,l.,gyülvészi,g.,tosevski,v.,hesske,l.,fontana,a.,magnenat,l.,suter,t.,andbecher,b.(2011).rorγtdrivesproductionofthecytokinegm-csfinhelpertcells,whichisessentialfortheeffectorphaseofautoimmuneneuroinflammation.nat.immunol.12,560-567。correale,j.,ysrraelit,m.c.,andgaitan,m.i.(2009).immunomodulatoryeffectsofvitamindinmultiplesclerosis.brain132,1146-1160。correale,j.,andfarez,m.(2007).associationbetweenparasiteinfectionandimmuneresponsesinmultiplesclerosis.ann.neurol.61,97-108。correale,j.,fiol,m.,andgilmore,w.(2006).theriskofrelapsesinmultiplesclerosisduringsystemicinfections.neurology67,652-659。dominiquel.p.baeten,andkuchroo,v.k.(2013).interleukin-17andataleoftwoautoimmunediseases.naturemedicine19,824-825。el-behi,m.,ciric,b.,dai,h.,yan,y.,cullimore,m.,safavi,f.,zhang,g.-x.,dittel,b.n.,androstami,a.(2011).theencephalitogenicityoft.nat.immunol.12,568-575。farez,m.f.,fiol,m.p.,gaitan,m.i.,quintana,f.j.,andcorreale,j.(2014).sodiumintakeisassociatedwithincreaseddiseaseactivityinmultiplesclerosis.journalofneurology,neurosurgery&psychiatry。farez,m.f.,quintana,f.j.,gandhi,r.,izquierdo,g.,lucas,m.,andweiner,h.l.(2009).toll-likereceptor2andpoly(adp-ribose)polymerase1promotecentralnervoussystemneuroinflammationinprogressiveeae.nat.immunol.10,958-964。fassi,j.,russopicasso,m.f.,furci,a.,sorroche,p.,jáuregui,r.,andplantalech,l.(2003).[seasonalvariationsin25-hydroxyvitamindinyoungandelderlyandpopulationsinbuenosairescity].medicina(baires)63,215-220。gandhi,r.,kumar,d.,burns,e.j.,nadeau,m.,dake,b.,laroni,a.,kozoriz,d.,weiner,h.l.,andquintana,f.j.(2010).activationofthearylhydrocarbonreceptorinduceshumantype1regulatorytcell-likeandfoxp3(+)regulatorytcells.nat.immunol.11,846-853。graham,c.,cook,m.r.,kavet,r.,sastre,a.,andsmith,d.k.(1998).predictionofnocturnalplasmamelatoninfrommorningurinarymeasures.jpinealres24,230-238。a.k.,t.,hillert,j.,olsson,t.,andalfredsson,l.(2011).shiftworkatyoungageisassociatedwithincreasedriskformultiplesclerosis.ann.neurol.70,733-741。hernan,m.a.(2005).cigarettesmokingandtheprogressionofmultiplesclerosis.brain128,1461-1465。hickie,i.b.,androgers,n.l.(2011).novelmelatonin-basedtherapies:potentialadvancesinthetreatmentofmajordepression.lancet378,621-631。jetten,a.m.(2009).retinoid-relatedorphanreceptors(rors):criticalrolesindevelopment,immunity,circadianrhythm,andcellularmetabolism.nuclreceptsignal7,e003。jin,y.,depedro-cuesta,j.,m.,stawiarz,l.,andlink,h.(2000).seasonalpatternsinopticneuritisandmultiplesclerosis:ameta-analysis.journaloftheneurologicalsciences181,56-64。jockers,r.,maurice,p.,boutin,j.a.,anddelagrange,p.(2008).melatoninreceptors,heterodimerization,signaltransductionandbindingsites:what'snew?britishjournalofpharmacology154,1182-1195。johnson,p.f.(2005).molecularstopsigns:regulationofcell-cyclearrestbyc/ebptranscriptionfactors.j.cell.sci.118,2545-2555。karim,a.,tolbert,d.,andcao,c.(2006).dispositionkineticsandtoleranceofescalatingsingledosesoframelteon,ahigh-affinitymt1andmt2melatoninreceptoragonistindicatedfortreatmentofinsomnia.jclinpharmacol46,140-148。kobayashi,t.,steinbach,e.c.,russo,s.m.,matsuoka,k.,nochi,t.,maharshak,n.,borst,l.b.,hostager,b.,garcia-martinez,j.v.,rothman,p.b.,etal.(2014).nfil3-deficientmicedevelopmicrobiota-dependent,il-12/23-drivenspontaneouscolitis.thejournalofimmunology192,1918-1927。kojetin,d.j.,andburris,t.p.(2014).rev-erbandrornuclearreceptorsasdrugtargets.natrevdrugdiscov13,197-216。korn,t.,bettelli,e.,oukka,m.,andkuchroo,v.k.(2009).il-17andth17cells.annu.rev.immunol.27,485-517。lathrop,s.k.,bloom,s.m.,rao,s.m.,nutsch,k.,lio,c.-w.,santacruz,n.,peterson,d.a.,stappenbeck,t.s.,andhsieh,c.-s.(2011).peripheraleducationoftheimmunesystembycoloniccommensalmicrobiota.nature478,250-254。lee,y.,awasthi,a.,yosef,n.,quintana,f.j.,xiao,s.,peters,a.,wu,c.,kleinewietfeld,m.,kunder,s.,hafler,d.a.,etal.(2012a).inductionandmolecularsignatureofpathogenicth17cells.nat.immunol.1-11。lee,y.,awasthi,a.,yosef,n.,quintana,f.j.,xiao,s.,peters,a.,wu,c.,kleinewietfeld,m.,kunder,s.,hafler,d.a.,etal.(2012b).inductionandmolecularsignatureofpathogenicth17cells.nat.immunol.13,991-999。lekstrom-himes,j.,andxanthopoulos,k.g.(1998).biologicalroleoftheccaat/enhancer-bindingproteinfamilyoftranscriptionfactors.j.biol.chem.273,28545-28548。-amsrud,k.i.,t.,bakke,s.j.,beiske,a.g.,bjerve,k.s.,b.t.,hovdal,h.,f.,midgard,r.,pedersen,t.,etal.(2012).vitamindanddiseaseactivityinmultiplesclerosisbeforeandduringinterferon-βtreatment.neurology79,267-273。macchi,m.m.,andbruce,j.n.(2004).humanpinealphysiologyandfunctionalsignificanceofmelatonin.frontneuroendocrinol25,177-195。mcgeachy,m.j.,bak-jensen,k.s.,chen,y.,tato,c.m.,blumenschein,w.,mcclanahan,t.,andcua,d.j.(2007).tgf-βandil-6drivetheproductionofil-17andil-10bytcellsandrestrainth-17cell-mediatedpathology.nat.immunol.8,1390-1397。mcmullan,c.j.,schernhammer,e.s.,rimm,e.b.,hu,f.b.,andforman,j.p.(2013).melatoninsecretionandtheincidenceoftype2diabetes.jama309,1388-1396.miossec,p.,korn,t.,andkuchroo,v.k.(2009).interleukin-17andtype17helpertcells.nengljmed361,888-898。morera,a.l.,andabreu,p.(2007).daytime/night-timeandsummer/wintermelatoninandmalondialdehyderhythms:aninverserelationship.jpinealres43,313-314。pévet,p.(2003).melatonin:fromseasonaltocircadiansignal.j.neuroendocrinol.15,422-426。polman,c.h.,reingold,s.c.,banwell,b.,clanet,m.,cohen,j.a.,filippi,m.,fujihara,k.,havrdova,e.,hutchinson,m.,kappos,l.,etal.(2011).diagnosticcriteriaformultiplesclerosis:2010revisionstothemcdonaldcriteria.ann.neurol.69,292-302。pot,c.,apetoh,l.,awasthi,a.,andkuchroo,v.k.(2011).inductionofregulatorytr1cellsandinhibitionofth17cellsbyil-27.seminarsinimmunology23,438-445。pozo,d.,delgado,m.,fernandez-santos,j.m.,calvo,j.r.,gomariz,r.p.,martin-lacave,i.,ortiz,g.g.,andguerrero,j.m.(1997).expressionofthemel1a-melatoninreceptormrnaintandbsubsetsoflymphocytesfromratthymusandspleen.fasebj.11,466-473。pozo,d.,garcía-s.,guerrero,j.m.,andcalvo,j.r.(2004).mrnaexpressionofnuclearreceptorrzr/roralpha,melatoninmembranereceptormt1,andhydroxindole-o-methyltransferaseindifferentpopulationsofhumanimmunecells.jpinealres37,48-54。quintana,f.j.,basso,a.s.,iglesias,a.h.,korn,t.,farez,m.f.,bettelli,e.,caccamo,m.,oukka,m.,andweiner,h.l.(2008).controloftregandth17celldifferentiationbythearylhydrocarbonreceptor.nature453,65-71。roncarolo,m.-g.,gregori,s.,battaglia,m.,bacchetta,r.,fleischhauer,k.,andlevings,m.k.(2006).interleukin-10-secretingtype1regulatorytcellsinrodentsandhumans.immunol.rev.212,28-50。rosecrans,r.,anddohnal,j.c.(2014).clinicalbiochemistry.clinicalbiochemistry47,670-672。runia,t.f.,hop,w.c.j.,derijke,y.b.,buljevac,d.,andhintzen,r.q.(2012).lowerserumvitamindlevelsareassociatedwithahigherrelapseriskinmultiplesclerosis.neurology79,261-266。sakaguchi,s.,miyara,m.,costantino,c.m.,andhafler,d.a.(2010).foxp3+regulatorytcellsinthehumanimmunesystem.naturereviewsimmunology10,490-500。saraiva,m.,ando'garra,a.(2010).theregulationofil-10productionbyimmunecells.naturereviewsimmunology10,170-181。saraiva,m.,christensen,j.r.,veldhoen,m.,murphy,t.l.,murphy,k.m.,ando'garra,a.(2009).interleukin-10productionbyth1cellsrequiresinterleukin-12-inducedstat4transcriptionfactoranderkmapkinaseactivationbyhighantigendose.immunity31,209-219。sawcer,s.,hellenthal,g.,pirinen,m.,spencer,c.c.a.,patsopoulos,n.a.,moutsianas,l.,dilthey,a.,su,z.,freeman,c.,hunt,s.e.,etal.(2011).geneticriskandaprimaryroleforcell-mediatedimmunemechanismsinmultiplesclerosis.nature476,214-219。schernhammer,e.s.,rosner,b.,willett,w.c.,laden,f.,colditz,g.a.,andhankinson,s.e.(2004).epidemiologyofurinarymelatonininwomenanditsrelationtootherhormonesandnightwork.cancerepidemiol.biomarkersprev.13,936-943。simpson,s.,taylor,b.,blizzard,l.,ponsonby,a.-l.,pittas,f.,tremlett,h.,dwyer,t.,gies,p.,andvandermei,i.(2010).higher25-hydroxyvitamindisassociatedwithlowerrelapseriskinmultiplesclerosis.ann.neurol.68,193-203。sospedra,m.,andmartin,r.(2005).immunologyofmultiplesclerosis.annu.rev.immunol.23,683-747。spelman,t.,gray,o.,trojano,m.,petersen,t.,izquierdo,g.,lugaresi,a.,hupperts,r.,bergamaschi,r.,duquette,p.,grammond,p.,etal.(2014).seasonalvariationofrelapserateinmultiplesclerosisislatitudedependent.ann.neurol。steinman,l.(2014).immunologyofrelapseandremissioninmultiplesclerosis.annu.rev.immunol.32,257-281。tan,a.h.m.,andlam,k.p.(2010).pharmacologicinhibitionofmek-erksignalingenhancesth17differentiation.thejournalofimmunology184,1849-1857。ueno-towatari,t.,norimatsu,k.,blazejczyk,k.,tokura,h.,andmorita,t.(2007).seasonalvariationsofmelatoninsecretioninyoungfemalesundernaturalandartificiallightconditionsinfukuoka,japan.jphysiolanthropol26,209-215。viglietta,v.,baecher-allan,c.,weiner,h.l.,andhafler,d.a.(2004).lossoffunctionalsuppressionbycd4+cd25+regulatorytcellsinpatientswithmultiplesclerosis.j.exp.med.199,971-979。wu,c.,yosef,n.,thalhamer,t.,zhu,c.,xiao,s.,kishi,y.,regev,a.,andkuchroo,v.k.(2013).inductionofpathogenicth17cellsbyinduciblesalt-sensingkinasesgk1.nature1-5。yang,j.,croniger,c.m.,lekstrom-himes,j.,zhang,p.,fenyus,m.,tchen,d.g.,darlington,g.j.,andhanson,r.w.(2005).metabolicresponseofmicetoapostnatalablationofccaat/enhancer-bindingproteinalpha.j.biol.chem.280,38689-38699。yang,x.o.,pappu,b.p.,nurieva,r.,akimzhanov,a.,kang,h.s.,chung,y.,ma,l.,shah,b.,panopoulos,a.d.,schluns,k.s.,etal.(2008).thelper17lineagedifferentiationisprogrammedbyorphannuclearreceptorsrorαandrorγ.immunity28,29-39。yu,x.,rollins,d.,ruhn,k.a.,stubblefield,j.j.,green,c.b.,kashiwada,m.,rothman,p.b.,takahashi,j.s.,andhooper,l.v.(2013).th17celldifferentiationisregulatedbythecircadianclock.science342,727-730。其他實施方案應理解,雖然已經結合其詳細描述,對本發明進行了描述,但前面的描述旨在說明而非限制本發明的范圍,本發明的范圍由所附的權利要求書的范圍限定。其他方面、優點以及修改都在以下權利要求書的范圍之內。當前第1頁12
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1