豬流行性腹瀉病毒滅活疫苗及其制備方法與流程
本發明屬于生物
技術領域:
,具體屬于獸用生物制藥領域,涉及豬流行性腹瀉病毒滅活疫苗及其制備方法。
背景技術:
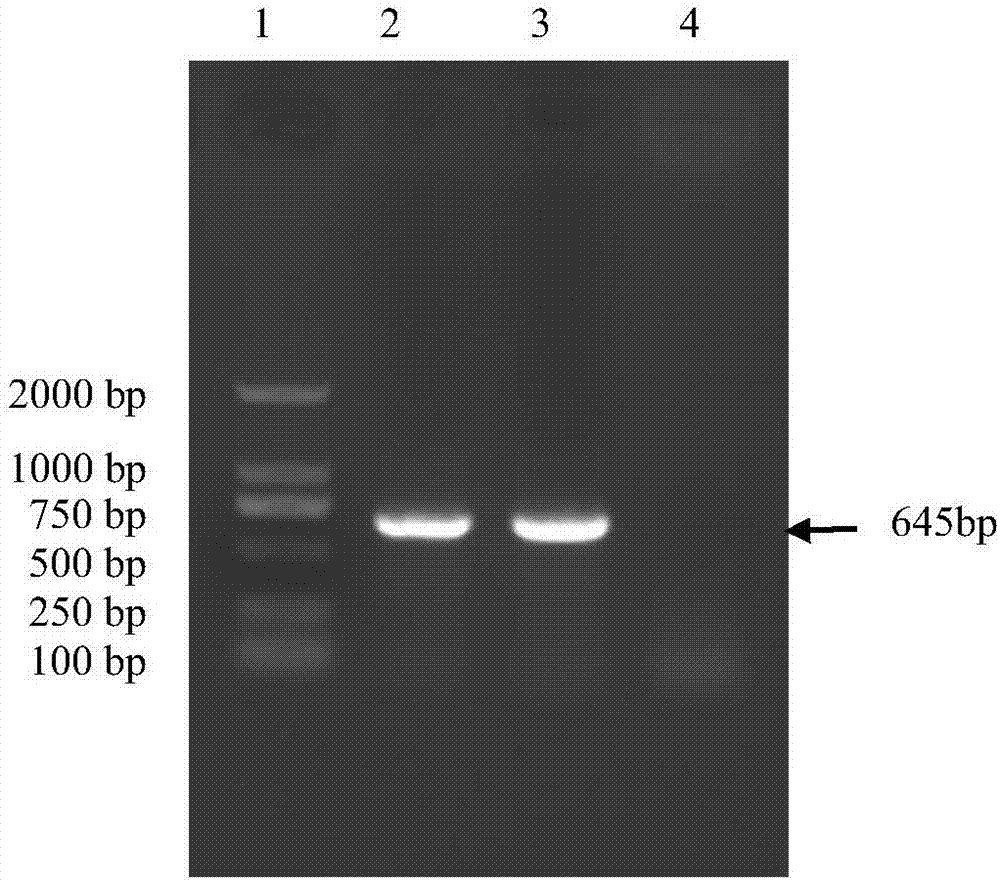
:豬流行性腹瀉(porcineepidemicdiarrhea,ped)是由豬流行性腹瀉病毒(porcineepidemicdiarrheavirus,pedv)引起一種急性、接觸性病毒性腸道傳染病,其病癥以嘔吐、水樣腹瀉、食欲下降和脫水為主,是常見的豬腸道傳染性疾病。豬流行性腹瀉病毒(pedv)系冠狀病毒科冠狀病毒屬成員,豬流行性腹瀉病毒(pedv)經口鼻感染后直接進入小腸,在小腸上皮細胞增殖,引起小腸絨毛吸收上皮細胞病變、損傷、脫落和小腸絨毛萎縮,導致腸內酶活性降低,吸收功能障礙,腸道內滲透壓增高,引發滲透性腹瀉,最終造成掉膘、降低飼料吸收利用率。pedv嚴重影響了我國的養豬業,其感染性強、危害性大,是影響全球養豬業的最重要病毒之一,哺乳仔豬感染后死亡率可達100%,母豬常以帶毒而不表現癥狀形式出現。近幾年我國多省爆發ped,給養豬業造成了嚴重的經濟損失。目前尚無治療豬流行性腹瀉的特效藥物,常規治療效果不佳,因此仍以疫苗預防為主,而病毒株及其培養的成功與否是疫苗研制的關鍵因素。目前,國外使用的疫苗主要為韓國弱毒株,國內主要是哈爾濱獸醫研究所研制的豬流行性腹瀉、豬傳染性胃腸炎二聯滅活苗等,此疫苗中使用的毒株為豬流行性腹瀉病毒pedvcv777株,該毒株分離年代較早,通過對現流行毒株的基因分析,發現流行毒株與二十世紀70年代分離到的cv777毒力基因發生了較大的改變,所以這也許是用含有原始毒株的疫苗免疫失敗的原因之一。因此篩選新毒株,制備行豬流行腹瀉疫苗用于預防豬流行性腹瀉是十分必要的。技術實現要素:為解決上述問題,本發明旨在提供一種豬流行性腹瀉病毒滅活疫苗及其制備方法,其采用本公司分離保藏的豬流行性腹瀉病毒毒株(pedv-kb2013-4株),其微生物保藏編號為cgmccno.12663作為病毒毒株,該毒株遺傳穩定,免疫原性能好,用其制備的滅活疫苗對于豬流行性腹瀉具有良好的保護效力。為解決以上技術問題,達成本發明的目的,本發明采用如下技術方案:一種豬流行性腹瀉病毒滅活疫苗,含有滅活的豬流行性腹瀉病毒和佐劑,其中佐劑是由以重量百分含量計5%角鯊烷、1%油酸、1%吐溫80、92%0.005m檸檬酸鈉緩沖溶液和1%的β-葡聚糖組成,所述豬流行性腹瀉病毒是由豬流行性腹瀉病毒毒株(pedv-kb2013-4株)經滅活制備得到,其微生物保藏編號為cgmccno.12663;分類命名:豬流行性腹瀉病毒(porcineepidemicdiarrheavirus,pedv);保藏時間是2016年08月23日;保藏單位:中國微生物菌種保藏管理委員會普通微生物中心;保藏地址:北京市朝陽區北辰西路1號院3號,中國科學院微生物研究所。本發明還請求保護豬流行性腹瀉病毒滅活疫苗在制備治療豬流行性腹瀉病毒感染藥物中的應用。本發明還提供所述豬流行性腹瀉病毒滅活疫苗的制備方法,包括如下步驟:a.按照常規方法制備vero細胞(vero細胞購自美國atcc),生長液為含10%新生牛血清的dmem,培養至細胞長成單層時接種pedv-kb2013-4病毒;b.取pedv-kb2013-4毒株(5×105tcid50/ml)按1%接種長勢良好的vero單層細胞,置37℃吸附1小時,棄去吸附液,補加含有10μg/ml胰蛋白酶的dmem作為維持液繼續培養;c.接毒后,每日觀察2次,記錄細胞病變情況,細胞病變達80%以上時收獲病毒,將收獲的病毒在-80℃,反復凍融三次,6000rpm離心20min,收集上清液,即為病毒液;d.病毒液經20倍濃縮后,加入0.2%甲醛37℃滅活24小時得到pedv-kb2013-4疫苗原液;e.配制佐劑,所述佐劑的配方含5%角鯊烷、1%油酸、1%吐溫80、92%0.005m檸檬酸鈉緩沖溶液和1%的β-葡聚糖,其配制方法為:將處方量的吐溫80、β-葡聚糖與檸檬酸鈉緩沖液攪拌混勻,再加入處方量的油酸、角鯊烷,高壓均質機1200bar,進行5個循環,然后收集料液,0.22μmptfe膜過濾除菌。f.將步驟d制得的pedv-kb2013-4株疫苗原液和佐劑按1.5:1的體積比,無菌環境中,攪拌混合均勻,即制得豬流行性腹瀉滅活疫苗。作為優選的技術方案,本發明的豬流行性腹瀉病毒滅活疫苗還含有豬白細胞介素-4(il-4),即得到一種免疫增強型豬流行性腹瀉病毒滅活疫苗,即還提供了如下技術方案:一種豬流行性腹瀉病毒滅活疫苗,含有滅活的豬流行性腹瀉病毒、佐劑和豬白細胞介素-4(4),其中佐劑是由以重量百分含量計5%角鯊烷、1%油酸、1%吐溫80、92%0.005m檸檬酸鈉緩沖溶液和1%的β-葡聚糖組成,所述豬流行性腹瀉病毒是由豬流行性腹瀉病毒毒株(pedv-kb2013-4株)經滅活制備得到,其微生物保藏編號為cgmccno.12663;分類命名:豬流行性腹瀉病毒(porcineepidemicdiarrheavirus,pedv);保藏時間是2016年08月23日;保藏單位:中國微生物菌種保藏管理委員會普通微生物中心;保藏地址:北京市朝陽區北辰西路1號院3號,中國科學院微生物研究所。以上含有豬白細胞介素-4(il-4)的免疫增強型豬流行性腹瀉病毒滅活疫苗的制備方法如下:a.按照常規方法制備vero細胞(vero細胞購自美國atcc),生長液為含10%新生牛血清的dmem,培養至細胞長成單層時接種pedv-kb2013-4病毒;b.取pedv-kb2013-4毒株(5×105tcid50/ml)按1%接種長勢良好的vero單層細胞,置37℃吸附1小時,棄去吸附液,補加含有10μg/ml胰蛋白酶的dmem作為維持液繼續培養;c.接毒后,每日觀察2次,記錄細胞病變情況,細胞病變達80%以上時收獲病毒,將收獲的病毒在-80℃,反復凍融三次,6000rpm離心20min,收集上清液,即為病毒液;d.病毒液經20倍濃縮后,加入0.2%甲醛37℃滅活24小時得到pedv-kb2013-4疫苗原液;e.配制佐劑,所述佐劑的配方含5%角鯊烷、1%油酸、1%吐溫80、92%0.005m檸檬酸鈉緩沖溶液和1%的β-葡聚糖,其配制方法為:將處方量的吐溫80、β-葡聚糖與檸檬酸鈉緩沖液攪拌混勻,再加入處方量的油酸、角鯊烷,高壓均質機1200bar,進行5個循環,然后收集料液,0.22μmptfe膜過濾除菌。f.將步驟d制得的pedv-kb2013-4株疫苗原液和佐劑按1.5:1的體積比,無菌環境中,攪拌混合均勻,進一步按照20萬iu/頭份(即每份疫苗中添加20萬iu的豬白細胞介素-4)的量向疫苗制劑中添加豬白細胞介素-4,即制得免疫增強型豬流行性腹瀉滅活疫苗。基于以上技術方案,本發明具有如下優點和有益效果:(1)與現有的商品化疫苗毒株相比,本發明所篩選的豬流行性腹瀉病毒pedv-kb2013-4株具有免疫原性好,抗體產生快,產生的抗體滴度高且維持時間長,免疫劑量小,在產前42天前進行滅活疫苗的免疫注射可使懷孕母豬所產仔豬獲得較好的被動免疫,能夠有效抵抗強毒株的攻擊,提高仔豬的存活率。(2)本發明在疫苗佐劑制備中添加了角鯊烷、油酸、吐溫80、檸檬酸鈉緩沖溶液和β-葡聚糖,其中葡聚糖的添加使用能夠顯著地提高動物對疫苗中抗原的免疫應答,縮短免疫窗口期,顯著延長抗pedv抗體產生持續期,提高抗體產生水平。(3)作為本發明優選的技術方案,其進一步在疫苗制劑中添加了20萬iu/頭份的豬白細胞介素-4,其中il-4il-4對于b細胞、t細胞、肥大細胞、巨噬細胞和造細胞都有免疫調節作用,與pedv滅活病毒聯合免疫能夠顯著提高豬的細胞免疫水平,提高免疫接種后的抗體水平,降低豬只的發病率和死亡率。附圖說明:圖1:pedv-kb2013-4株接種vero細胞在不同時期的cpe圖片,其中圖1-a、圖1-c、圖1-e分別為未接種病毒的vero細胞培養24h、36h、48h后的細胞圖像;圖1-b、圖1-d、圖1-f分別為接種pedv-kb2013-4株24h、36h、48h后的cpe圖像。圖2:pedvrt-pcr檢測結果,通道1:takaradnamaker;通道2:陽性對照;通道3:第9代病毒液;通道4:陰性對照。圖3:母豬免疫不同疫苗后的抗體水平檢測結果(實施例4)。圖4:母豬免疫不同疫苗后的抗體水平檢測結果(實施例7)。具體實施方式:實施例1:豬流行性腹瀉病毒pedv-kb2013-4株的分離鑒定(1)豬流行性腹瀉病毒pedv-kb2013-4株的分離在流行病學調查時,陜西某豬場送檢腹瀉仔豬小腸,刮取腸粘膜和內容物,按照1:5的比例(重量:體積)加入pbs,反復凍融3次,離心取上清,0.22μm濾膜過濾,濾液中加入終濃度為20μg/ml的胰酶,37℃處理1.5小時。按常規方法接種長滿單層的vero細胞(接種前用ph7.4的pbs洗三次),按照10%的比例接種病毒,37℃吸附1小時,補足細胞維持液(含10μg/ml的胰酶),37℃溫箱培養。如此操作盲傳至第10代,觀察是否產生cpe,同時設置空白細胞作為對照。盲傳傳至第5代時細胞出現輕微的cpe變化,傳至第9代時則出現明顯、穩定的cpe變化,細胞圓縮,顆粒增加,聚堆呈葡萄串樣,細胞出現損傷和脫落,即分離得到pedv-kb2013-4株。說明書附圖圖1展示了pedv-kb2013-4株接種vero細胞在不同時期的cpe圖片,其中圖1-a、圖1-c、圖1-e為對照組,其圖像分別為未接種病毒的vero細胞培養24h、36h、48h后的細胞圖像,由圖可知,直到vero細胞培養到48h,細胞仍保持致密單層,僅有少量細胞脫落;圖1-b、圖1-d、圖1-f分別為接種pedv-kb2013-4株24h、36h、48h后的cpe圖像,圖1-b是接種pedv-kb2013-4株24h產生的病變,其中有少量的細胞開始圓縮、脫落,圖1-d是接種pedv-kb2013-4株36h后產生的病變,有較多的細胞開始脫落,細胞間的空隙變大;圖1-f是接種pedv-kb2013-4株48h后產生的病變,細胞開始大量脫落,達到75%以上,且細胞間聚堆呈葡萄串樣,表現為典型的網狀cpe癥狀。(2)病毒pt-pcr檢測按照omega試劑盒的說明進行rna的提取,產品立即進行反轉錄或貯存于-80℃備用。并合成檢測引物pedvf:5’-aacggttctattcccgttgatg-3’;pedvr:5’-taaatgaagcactttctcactatc-3’。取總rna5.25μl,5×buffer2μl,dntp(10mmeach)0.5μl,下游引物(pedv-r)1μl,amv反轉錄酶0.5μl,rna酶抑制劑0.25μl,總體積10μl。反應條件:37℃10min,42℃反轉錄1h,冰浴2min。取rt產物1μl,2×promegamix12.5ul,引物pedv-f、pedv-r各1ul,高壓滅菌水9.5ul,總體積25ul。反應條件:94℃3min,94℃30s,60℃45s,72℃45s,35個循環,72℃7min。擴增后的產物,進行瓊脂糖凝膠電泳,擴增出目的條帶645bp,參見說明書附圖圖2,經測序鑒定,所述病毒分離毒株為pedv。(3)病毒滴毒測定取第10代病毒,用細胞維持液進行10倍系列稀釋,取10-4、10-5、10-6、10-7四個稀釋度,每個稀釋度分別接種長滿vero細胞單層的96孔細胞板6孔,100μl/孔,同時設陰性對照細胞6孔,37℃5%co2培養箱培養72~120小時,觀察細胞病變,細胞顆粒增多,圓縮,細胞破損,脫落判為感染。同時陰性對照組細胞孔應不出現細胞病變。采用reed-muench法,計算tcid50。經測定,病毒含量為5×105tcid50/ml。(4)動物回歸試驗取pedv中和抗體均小于1:8的母豬所產的3~5日齡仔豬10頭,每頭口服2ml第10代病毒,觀察7天,統計接種豬的發病情況,對試驗豬進行剖檢,觀察病理變化。刮取發病豬腸粘膜和內容物,提取rna,按實施例1第2步提到的檢測引物,進行rt-pcr檢測,并將pcr產物進行序列測定。結果仔豬8/10發病,發病豬表現為腹瀉,個別豬出現嘔吐,剖檢觀察發現胃和小腸出現典型的病理變化。從發病豬的腸粘膜及內容物中可擴增出645bp的片段,經序列分析為pedvs基因。經實驗室分離鑒定,已成功的從陜西某豬場腹瀉豬小腸內容物中分離到豬流行性腹瀉病毒,命名為pedv-kb2013-4株,其微生物保藏編號為cgmccno.12663;分類命名:豬流行性腹瀉病毒(porcineepidemicdiarrheavirus,pedv);保藏時間是2016年08月23日;保藏單位:中國微生物菌種保藏管理委員會普通微生物中心;保藏地址:北京市朝陽區北辰西路1號院3號,中國科學院微生物研究所。實施例2:用pedv-kb2013-4株制備疫苗(1)pedv疫苗的制備a.按照常規方法制備vero細胞(vero細胞購自美國atcc),生長液為含10%新生牛血清的dmem,培養至細胞長成單層時接種pedv-kb2013-4病毒;b.取pedv-kb2013-4毒株(5×105tcid50/ml)按1%接種長勢良好的vero單層細胞,置37℃吸附1小時,棄去吸附液,補加含有10μg/ml胰蛋白酶的dmem作為維持液繼續培養;c.接毒后,每日觀察2次,記錄細胞病變情況,細胞病變達80%以上時收獲病毒,將收獲的病毒在-80℃,反復凍融三次,6000rpm離心20min,收集上清液,即為病毒液;d.病毒液經20倍濃縮后,加入0.2%甲醛37℃滅活24小時得到pedv-kb2013-4疫苗原液;e.配制佐劑,所述佐劑的配方含5%角鯊烷、1%油酸、1%吐溫60、92%0.005m檸檬酸鈉緩沖溶液和1%β-葡聚糖,其配制方法為:將處方量的吐溫80、β-葡聚糖與檸檬酸鈉緩沖液攪拌混勻,再加入處方量的油酸、角鯊烷,高壓均質機1200bar,進行5個循環,然后收集料液,0.22μmptfe膜過濾除菌。f.將pedv-kb2013-4株疫苗原液和佐劑按1.5:1的體積比,無菌環境中,攪拌混合均勻,即制得豬流行性腹瀉滅活疫苗。(2)疫苗檢驗方法及結果按照上述方法制備出3批疫苗,批號分別為20140101、20140102、20140103。2.1性狀檢驗3批滅活疫苗外觀呈粉紅色乳膠狀。2.2無菌檢驗3批滅活疫苗按照現《中華人民共和國獸藥典》2010年版第三部附錄進行檢驗,t.g、g.p管和g.a斜面培養基均未觀察到菌落。2.3支原體檢驗3批滅活疫苗按照《中華人民共和國獸藥典》2010年版第三部附錄進行檢驗,未發現小瓶和小管培養物顏色出現明顯變化,移植的液體培養物在固體培養基上無“煎蛋”狀支原體菌落。2.4外源病毒檢驗3批滅活疫苗按照《中華人民共和國獸藥典》2010年版第三部附錄進行檢驗,均無豬瘟病毒、牛病毒性腹瀉病毒、豬細小病毒、豬偽狂犬病毒、輪狀病毒、豬傳染性胃腸炎病毒等污染。證明毒種是純凈的。2.5安全檢驗取豬流行性腹瀉中和抗體、抗原均為陰性的3日齡豬24頭,隨機分成4組,每組6頭,肌注10頭份疫苗,臨床觀察14日,均100%健活,未見不良反應發生。表1:3批豬流行性腹瀉滅活疫苗檢驗結果檢驗項目201401012014010220140103性狀檢驗粉紅色乳液粉紅色乳液粉紅色乳液無菌檢驗無菌生長無菌生長無菌生長支原體檢驗無支原體生長無支原體生長無支原體生長外源病毒檢驗無外源病毒污染無外源病毒污染無外源病毒污染安全性檢測100%健活,未見不良反應100%健活,未見不良反應100%健活,未見不良反應實施例3豬流行性腹瀉病毒pedv-kb2013-4株滅活苗的安全試驗1.材料與方法1.1對妊娠母豬的單劑量試驗取產前5-6周豬流行性腹瀉中和抗體、抗原均為陰性的妊娠母豬10頭,隨機分成2組,每組5頭,第一組肌肉注射20140101批豬流行性腹瀉病毒pedv-kb2013-4株滅活苗1頭份/頭,第二組不進行注射作為對照組,觀察至母豬產仔。1.2對妊娠母豬的單劑量重復試驗取產前5-6周豬流行性腹瀉中和抗體、抗原均為陰性的妊娠母豬10頭,隨機分成2組,每組5頭,第一組肌肉注射20140101批豬流行性腹瀉病毒pedv-kb2013-4株滅活苗1頭份/頭,第二組不進行注射免疫。免疫后2周第1組肌肉注射20140101批豬流行性腹瀉病毒pedv-kb2013-4株滅活苗1頭份/頭,觀察至母豬產仔。1.3對妊娠母豬的超劑量試驗取產前5-6周豬流行性腹瀉中和抗體、抗原均為陰性的妊娠母豬16頭,隨機分成4組,第1、2、3組分別肌肉注射20140101、20140102、20140103批豬流行性腹瀉病毒pedv-kb2013-4株滅活苗各2頭份/頭,第4組不進行注射作對照組,觀察至母豬產仔。2.結果2.1單劑量試驗結果免疫組5頭妊娠母豬與對照組比較,采食、飲水、妊娠產仔均未見異常,注射部位均未見不良反應。2.2單劑量重復試驗結果免疫組5頭妊娠母豬與對照組比較,采食、飲水、妊娠產仔均未見異常,注射部位均未見不良反應。2.3超劑量試驗結果3批疫苗免疫組12頭妊娠母豬與對照組比較,采食、飲水、妊娠產仔均未見異常,注射部位均未見不良反應。實施例4母豬注射豬流行性腹瀉滅活疫苗后的抗體水平檢測試驗1材料與方法取產前42天豬流行性腹瀉中和抗體、抗原均為陰性的妊娠母豬20頭,隨機分成4組,每組5頭,第1組肌肉注射20140101批豬流行性腹瀉病毒pedv-kb2013-4株滅活苗1頭份/頭,第2組、第3組分別注射市場上現有的商品化pedv-tgev二聯疫苗(分別標記為疫苗a、疫苗b),第4組不進行注射作為對照組。各組于免疫后第1周、第2周、第3周、第4周、第5周、第6周采血,分離血清進行病毒中和試驗。2結果實驗結果表明,本發明所制備的疫苗,產生抗體快,且產生的抗體滴度高,維持時間長,參見說明書附圖3。實施例5豬流行性腹瀉病毒pedv-kb2013-4株滅活疫苗的效力試驗1材料與方法取產前5-6周豬流行性腹瀉中和抗體、抗原均為陰性的妊娠母豬30頭,隨機分成3組,每組10頭,第1組肌肉注射20140101批豬流行性腹瀉病毒pedv-kb2013-4株滅活苗1頭份/頭,第2組注射pedv弱毒疫苗株cv777制備的弱毒疫苗1頭份/頭(市購,1ml/頭份,病毒含量105tcid50/ml),第3組注射相同量的生理鹽水作為對照組,母豬產仔后,3日齡、7日齡、14日齡仔豬各取24頭,隨機分成3組,每組8頭,均口服豬流行性腹瀉強毒5ml,觀察攻毒后仔豬的臨床表現。2結果第1組pedv-kb2013-4株滅活苗免疫母豬所產的仔豬,3日齡攻毒后,8頭免疫仔豬哺乳、精神、糞便未見異常,均健活;第2組pedv弱毒疫苗株cv777弱毒疫苗免疫母豬所產的仔豬,3日齡攻毒后,3頭表現出典型的豬流行性腹瀉癥狀,而后死亡,5頭仔豬哺乳、精神、糞便未見異常,均健活,即5/8表現出ped癥狀;第3組的8頭對照仔豬攻毒后,8/8表現典型的豬流行性腹瀉癥狀,8/8死亡。7日齡攻毒后,第1組的8頭免疫仔豬哺乳、精神、糞便未見異常,均健活;第2組的8頭仔豬,8頭對照組仔豬攻毒后,3頭表現出ped癥狀病死亡,即死亡率為3/8;第3組的仔豬全部表現典型的豬流行性腹瀉癥狀,8/8死亡。14日齡攻毒后,第1組的8頭免疫仔豬哺乳、精神、糞便未見異常,均健活;第2組的8頭仔豬,8頭對照組仔豬攻毒后,2頭表現出ped癥狀病死亡,即死亡率為2/8;第3組8頭對照組仔豬攻毒后,8/8表現典型的豬流行性腹瀉癥狀,5/8死亡。表2免疫母豬所產的仔豬攻毒保護率由表2的結果可知,本發明獲得的pedv-kb2013-4株具有良好的免疫原性,其對動物的保護率接近100%,高于市售的弱毒疫苗。本發明所篩選的豬流行性腹瀉病毒pedv-kb2013-4株制備的疫苗免疫原性好,抗體產生快,產生的抗體滴度高且維持時間長,免疫劑量小,在產前42天前進行免疫注射可使懷孕母豬所產仔豬獲得較好的被動免疫,能夠有效抵抗強毒株的攻擊,提高仔豬的存活率。實施例6:用pedv-kb2013-4株制備含有豬白細胞介素-4(il-4)的免疫增強型豬流行性腹瀉病毒滅活疫苗的制備方法如下:a.按照常規方法制備vero細胞(vero細胞購自美國atcc),生長液為含10%新生牛血清的dmem,培養至細胞長成單層時接種pedv-kb2013-4病毒;b.取pedv-kb2013-4毒株(5×105tcid50/ml)按1%接種長勢良好的vero單層細胞,置37℃吸附1小時,棄去吸附液,補加含有10μg/ml胰蛋白酶的dmem作為維持液繼續培養;c.接毒后,每日觀察2次,記錄細胞病變情況,細胞病變達80%以上時收獲病毒,將收獲的病毒在-80℃,反復凍融三次,6000rpm離心20min,收集上清液,即為病毒液;d.病毒液經20倍濃縮后,加入0.2%甲醛37℃滅活24小時得到pedv-kb2013-4疫苗原液;e.配制佐劑,所述佐劑的配方含5%角鯊烷、1%油酸、1%吐溫80、92%0.005m檸檬酸鈉緩沖溶液和1%的β-葡聚糖,其配制方法為:將處方量的吐溫80、β-葡聚糖與檸檬酸鈉緩沖液攪拌混勻,再加入處方量的油酸、角鯊烷,高壓均質機1200bar,進行5個循環,然后收集料液,0.22μmptfe膜過濾除菌。f.將步驟d制得的pedv-kb2013-4株疫苗原液和佐劑按1.5:1的體積比,無菌環境中,攪拌混合均勻,進一步按照20萬iu/頭份(即每份疫苗中添加20萬iu的豬白細胞介素-4)的量向疫苗制劑中添加豬白細胞介素-4,即制得免疫增強型豬流行性腹瀉滅活疫苗。實施例7:母豬注射豬流行性腹瀉滅活疫苗后的抗體水平檢測試驗1材料與方法取產前42天豬流行性腹瀉中和抗體、抗原均為陰性的妊娠母豬20頭,隨機分成4組,每組5頭,第1組肌肉注射實施例3的20140101批豬流行性腹瀉病毒pedv-kb2013-4株滅活苗1頭份/頭,第2組、第3組分別注射市場上現有的商品化pedv-tgev二聯疫苗(分別標記為疫苗a、疫苗b),第4組不進行注射作為對照組,第5組注射實施例6制備的免疫增強型豬流行性腹瀉病毒滅活疫苗1頭份/頭,各組于免疫后第1周、第2周、第3周、第4周、第5周、第6周采血,分離血清進行病毒中和試驗。2結果實驗結果表明,本發明實施例6所制備的疫苗,產生抗體快,且產生的抗體滴度高,維持時間長,參見說明書附圖4。當前第1頁12
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1