胺基二硫代甲酸鹽衍生物在抗菌領(lǐng)域的應(yīng)用的制作方法
本發(fā)明屬于藥物化學(xué)
技術(shù)領(lǐng)域:
,涉及胺基二硫代甲酸鹽衍生物作為新型金屬β-內(nèi)酰胺酶抑制劑在抗菌領(lǐng)域的應(yīng)用。
背景技術(shù):
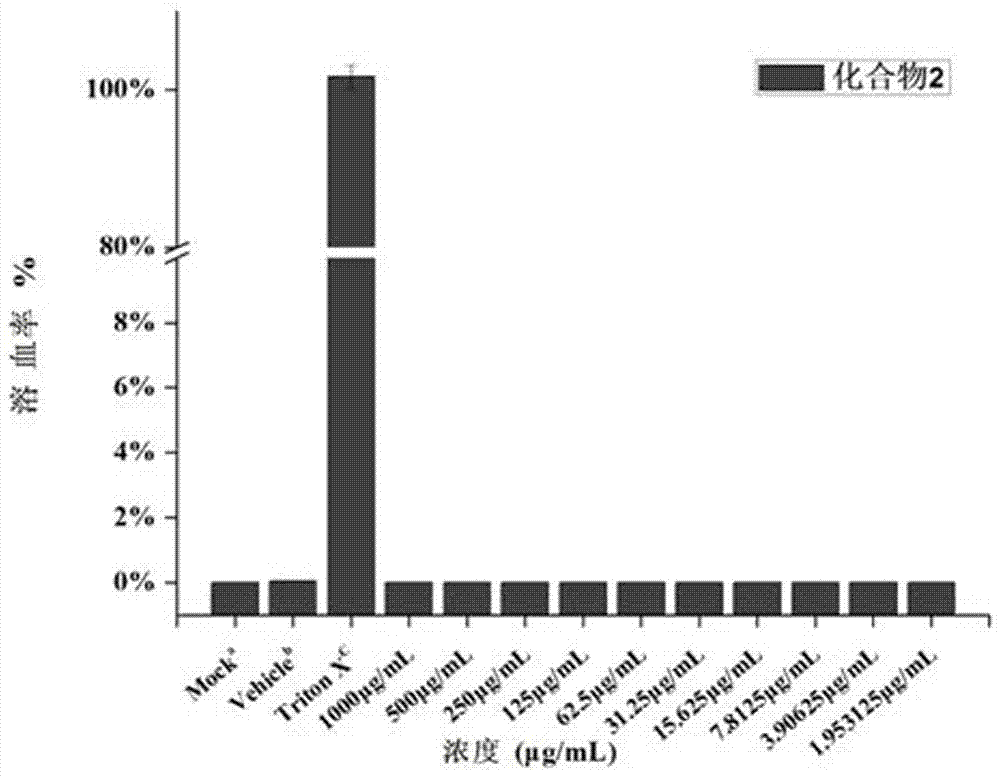
:抗生素耐藥(antimicrobialresistance,amr)趨勢如同幽靈一般不知不覺的侵襲了全球(microbiologyandmolecularbiologyreviews2010,74,417.)。抗生素產(chǎn)生耐藥性已經(jīng)成為公共衛(wèi)生安全的主要威脅(naturereviewsmicrobiology2015,13,42.)。細菌耐藥的原因可以歸結(jié)為細菌染色體突變和耐藥基因水平傳播兩個方面。其中,細菌固有耐藥是細菌自身所具備的本能。而由耐藥基因的水平傳播而導(dǎo)致的獲得性耐藥的產(chǎn)生(nature2004,430,242.)是導(dǎo)致耐藥性播散和多重耐藥菌產(chǎn)生的重要原因。β-內(nèi)酰胺類抗生素(青霉素,頭孢菌素,碳青霉烯類和單環(huán)內(nèi)酰胺類)是多年來臨床廣泛使用治療細菌感染的重要抗生素。β-內(nèi)酰胺酶的出現(xiàn)是目前臨床上使用β-內(nèi)酰胺類抗生素受限的主要問題,β-內(nèi)酰胺酶可以通過水解β-內(nèi)酰胺環(huán),使β-內(nèi)酰胺類抗生素失效(biochemistry,1999,38,10013.)。在臨床用藥以及動物生產(chǎn)中β-內(nèi)酰胺類抗生素的不規(guī)范使用和濫用,造成耐藥性問題更加嚴(yán)重(emerginginfectiousdiseases2002,8,347.)。碳青霉烯類β-內(nèi)酰胺抗生素(如亞胺培南和美羅培南)被認為是治療嚴(yán)重感染和全身感染最有效的藥物,因為它們對絕大多數(shù)β-內(nèi)酰胺酶高度穩(wěn)定。然而,隨著碳青霉烯類藥物的消費量在過去二十年中一直在穩(wěn)步增長,能夠水解碳青霉烯類抗生素的酶已經(jīng)出現(xiàn),并且主要在革蘭氏陰性細菌中傳播,導(dǎo)致細菌對這一類藥物產(chǎn)生抗性,嚴(yán)重威脅臨床抗感染治療。根據(jù)氨基酸序列同源性差異,β-內(nèi)酰胺酶按照ambler分類法被分為a,b,c和d類。其中絲氨酸-β-內(nèi)酰胺酶包含a,c和d三類,它們通過絲氨酸殘基與β-內(nèi)酰胺抗生素通過共價結(jié)合而使抗生素失活(biologicalsciences1980,289,321-331)。臨床上所使用的β-內(nèi)酰胺酶抑制劑為絲氨酸-β-內(nèi)酰胺酶抑制劑,如克拉維酸,舒巴坦和他唑巴坦等。金屬β-內(nèi)酰胺酶(mbls,amblerb類)在其活性位點含有一個或兩個鋅離子,其通過極化水分子促進β-內(nèi)酰胺的親核攻擊(biochemicaljournal1998,331(pt44),703)。mbls對絲氨酸-β-內(nèi)酰胺酶抑制劑不敏感,并且可以水解在臨床中應(yīng)用的大多數(shù)β-內(nèi)酰胺抗生素,針對其有效的抑制劑目前在臨床中還沒有應(yīng)用。2014年,gerardd.wright等人報道了從真菌中得到的一種天然的化合物ama,它可以快速、有效的抑制含有ndm-1型金屬β-內(nèi)酰胺酶的活性,與美羅培南聯(lián)合用藥的情況下可使產(chǎn)ndm-1酶菌株對美羅培南恢復(fù)敏感(nature2014,510,503.)。2015年,sabihay.essack等人報道了兩種鋅離子螯合劑nota和dota,此兩種螯合劑可以攜帶金屬β-內(nèi)酰胺酶的菌株恢復(fù)對碳青霉烯類抗生素的敏感性(journalofantimicrobialchemotherapy2015,70,1594.)。2015年,西北大學(xué)楊科武課題組報道了一系列巰基乙酸硫酯氨基酸衍生物,其對于金屬β-內(nèi)酰胺酶l1的ic50最小可以達到18nm,但是其體外活性實驗證明其恢復(fù)美羅培南敏感性效果并不理想(acsmedicinalchemistryletters2015,6,660.)。二硫代甲酸鹽是一類運用非常廣泛的有機物。其廣泛應(yīng)用于農(nóng)業(yè)、工業(yè)、環(huán)境污染、醫(yī)藥等領(lǐng)域。其醫(yī)藥領(lǐng)域的研究目前處于發(fā)展期,例如,二乙基二硫代氨基甲酸鈉(ddtc)被臨床用于免疫調(diào)節(jié)劑用來治療艾滋病(中國專利,專利號:93100610);ddtc可以抑制細胞超氧化酶的活性,導(dǎo)致細胞缺氧達到治療癌癥的目的(biochemicalpharmacology1979,28,27.);由于其分子中的硫原子帶負電可以結(jié)合金屬離子,所以又作為解毒劑用于人體金屬中毒,針對二硫代氨基甲酸鹽(dtc)作為碳酸酐酶抑制劑被報道,其中(ibu)2-dtc對于hcai、hcaii和hcaix碳酸酐酶的ki分別為0.97、0.95和4.5(bioorganicmedicinalchemistry2013,21,1516.)。通過小分子藥物來進行疾病相關(guān)酶的活性干預(yù),是一種對于人類疾病具有前景的藥理學(xué)干預(yù)方法。目前未見胺基二硫代甲酸鹽衍生物作為金屬β-內(nèi)酰胺酶抑制劑在抗菌領(lǐng)域的應(yīng)用。技術(shù)實現(xiàn)要素:本發(fā)明目的在于提供胺基二硫代甲酸鹽衍生物作為新型金屬β-內(nèi)酰胺酶抑制劑在抗菌領(lǐng)域的應(yīng)用。為實現(xiàn)本發(fā)明目的,技術(shù)方案如下:首先合成了10個胺基二硫代甲酸鹽衍生物,并對它們進行了核磁共振氫譜和碳譜的確證。在隨后的抗菌生物評價過程中,發(fā)現(xiàn)該類化合物可以提升美羅培南對于耐藥菌株的敏感性,它們的結(jié)構(gòu)如下:測試了該類化合物1-10與抗生素美羅培南(mem)的聯(lián)用實驗數(shù)據(jù);對部分化合物1,2和7體外紅細胞溶血進行了實驗;對化合物1,2和7體外hela(海拉癌細胞株)細胞毒進行了實驗;對化合物1,2和7體外對于大腸埃希菌(blaimp)的殺菌動力學(xué)進行了實驗;并進行了化合物1,2,7和nota在體外與美羅培南(mem)、zn2+協(xié)同用藥對比實驗。結(jié)果發(fā)現(xiàn),化合物1-10作為胺基二硫代甲酸鹽衍生物,可以不同程度上恢復(fù)產(chǎn)金屬β-內(nèi)酰胺酶菌株對美羅培南的敏感性。可以作為新型金屬β-內(nèi)酰胺酶抑制劑在抗菌領(lǐng)域應(yīng)用。本發(fā)明優(yōu)點及創(chuàng)新點在于:發(fā)現(xiàn)胺基二硫代甲酸鹽衍生物的新用途,將用于抑制碳酸酐酶的抑制劑,作為新型金屬β-內(nèi)酰胺酶抑制劑在抗菌領(lǐng)域得到應(yīng)用,并且發(fā)現(xiàn)該類化合物與美羅培南協(xié)同用藥具有很好的殺菌效果。由鋅離子參與的協(xié)同用藥所引起結(jié)果的改變推測,化合物可能是由于和金屬β-內(nèi)酰胺酶中的鋅離子結(jié)合導(dǎo)致該酶失活。該應(yīng)用將有利于開發(fā)新型金屬β-內(nèi)酰胺酶抑制劑。附圖說明圖1為本發(fā)明化合物1、2和7的紙片擴散法藥敏實驗結(jié)果,選用乙二胺四乙酸(edta)作為對照藥物,美羅培南(mem)作為抗菌化合物,選取產(chǎn)ndm-1或imp酶的菌株14-50(大腸埃希菌,攜帶blandm-4基因)和15-101(陰溝腸桿菌,攜帶blaimp基因)進行測試,藥敏實驗結(jié)果的判斷與操作遵循美國臨床和實驗室標(biāo)準(zhǔn)協(xié)會(clinicalandlaboratorystandardsinstitute,clsi-m07-a9)規(guī)定。使用藥敏紙片直徑為6mm。1-a圖中,a-mem,b-mem和本發(fā)明化合物1,c-mem和本發(fā)明化合物2,d-mem和edta;1-b圖中,a-mem,b-mem和edta,c-mem和本發(fā)明化合物7;由圖可知,化合物1、2和7在與mem協(xié)同用藥后使得mem敏感性增大,抑菌圈隨之增大。圖2為本發(fā)明化合物1,2和7體外紅細胞溶血性的實驗結(jié)果,其中,2a-本發(fā)明化合物1,2b-本發(fā)明化合物2,2c-本發(fā)明化合物7。由圖可知,本發(fā)明化合物1,2和7在1000μg/ml時紅細胞的溶血率仍舊小于1%。由此可以證明,本發(fā)明化合物1,2和7對紅細胞在1000μg/ml的范圍內(nèi)幾乎不存在毒性。圖3為本發(fā)明化合物1,2和7在體外對于hela細胞毒性的實驗結(jié)果,其中,3a-本發(fā)明化合物1,3b-本發(fā)明化合物2,3c-本發(fā)明化合物7。由圖可知,化合物1,2和7在1000μg/ml時對hela細胞的抑制率分別為54.05±1.24%,67.59±1.03%和30.21±1.00%。由此可以初步證明,在體外實驗過程中,化合物1,2和7具有較小的細胞毒性。圖4為本發(fā)明化合物1,2和7在體外對于hela細胞毒性的活死細胞熒光實驗結(jié)果,圖中,a–c陰性對照(不加藥組),d–f本發(fā)明化合物1(64μg/ml),g–i本發(fā)明化合物2(64μg/ml),j–l本發(fā)明化合物7(64μg/ml),m-o為陽性對照組0.1%tritonx-100。圖中比例尺為20μm。由圖可以顯著的觀察到,本發(fā)明化合物1,2和7于64μg/ml作用于hela細胞24小時后,對于細胞維持正常形態(tài)的生長幾乎沒有影響。圖5為本發(fā)明化合物1,2,7和nota在體外與美羅培南(mem)、zn2+聯(lián)用后的結(jié)果柱狀圖,由圖可知,化合物1,2,7和nota與mem聯(lián)用16-18h之后幾乎可以達到100%的抑制率,但是與鋅離子聯(lián)合使用后藥物失效,說明化合物1,2,7和nota與金屬β-內(nèi)酰胺酶中的鋅離子結(jié)合導(dǎo)致該酶失活,具有可逆性。圖6、本發(fā)明化合物1,2和7與mem聯(lián)用后在體外對于大腸埃希菌(菌株編號16,blaimp)的殺菌動力學(xué)結(jié)果。圖中,6a為本發(fā)明化合物1,6b為本發(fā)明化合物2,6c為本發(fā)明化合物7,6d為對照化合物nota。由圖可知,當(dāng)本發(fā)明化合物1、2、7和nota在4×mic(本發(fā)明化合物與nota終濃度為4×64μg/ml,mem為4×0.03125μg/ml)和8×mic(本發(fā)明化合物與nota終濃度為8×64μg/ml,mem為8×0.03125μg/ml)兩個濃度作用24h后,對于對數(shù)生長初期的細菌有很好的殺菌活性。由圖6a可知,當(dāng)本發(fā)明化合物1在4×mic和8×mic兩個濃度作用24h后,對于對數(shù)生長初期的細菌有很好的殺菌活性。與陽性對照nota的活性相對較優(yōu)。圖7為本發(fā)明化合物1,2,7和nota在體外對于大腸埃希菌(菌株編號16,blaimp)的殺菌動力學(xué)結(jié)果對比圖,圖中,7a,7b,7c和7d分別為本發(fā)明化合物1,2,nota和7與mem協(xié)同作用24小時后的菌管照片。其中,7a中,a-空白,b-化合物1的4×mic,c-化合物1的8×mic;7b中,a-空白,b-化合物2的4×mic,c-化合物2的8×mic;7c中,a-空白,b-化合物7的4×mic,c-化合物7的8×mic;7d中,a-空白,b-nota的4×mic,c-nota的8×mic;從7a-d圖中,24h后的外觀可以清楚地看到,化合物1,2,nota和7作用后的菌液濁度很低,而空白對照組濁度明顯大。具體實施方式下面結(jié)合具體實施例,進一步闡述本發(fā)明。這些實施例僅用于說明本發(fā)明而不用于限制本發(fā)明要求保護的范圍。應(yīng)用例1本發(fā)明化合物藥敏實驗具體操作步驟:實驗用品:一次性無菌培養(yǎng)皿、濾紙片(經(jīng)過高壓滅菌)、mha培養(yǎng)基、美羅培南(mem)、乙二胺四乙酸(edta)、打孔器。實驗操作步驟:(1)藥物紙片的制備:用打孔機將濾紙剪裁成直徑為6mm左右的圓型濾紙,收集50張,裝入小西林瓶中,高壓滅菌,烘干備用。根據(jù)美國臨床和實驗室標(biāo)準(zhǔn)協(xié)會(clsi)所規(guī)定的藥物含量要求和50片藥敏紙片所需總含量,制備藥敏紙片。于生物安全柜中,將配置好的mem以及本發(fā)明抗菌化合物加入到滅過菌的西林瓶中,牛皮紙密封瓶口。放置到37℃恒溫培養(yǎng)箱中烘干待用。待紙片烘干后,取載藥不同藥敏紙片加入到滅菌后肉湯中,檢查是否存在細菌污染,并用西林瓶蓋將西林瓶密封,置于4℃冰箱保存。(2)菌液的制備與實驗操作:麥?zhǔn)蠞岫葐挝粸?.5的耐藥菌株用mhb肉湯稀釋10倍后用滅菌過的棉棒,均勻涂于制備好的無菌mha瓊脂平板上,涂布菌液的平板于生物安全柜內(nèi)晾干后于背面標(biāo)記相應(yīng)的菌株編號,化合物編號等。用滅菌過的鑷子取相應(yīng)藥物的藥敏紙片貼于mha瓊脂平板表面,盡量貼平。陽性對照組滴加10μl0.1mol/ledta溶液,陰性對照組滴加10μl0.1mol/l金屬酶抑制劑,37℃過夜培養(yǎng)。(3)結(jié)果的判定:抑菌圈直徑>20mm為極度敏感,15~20mm為高度敏感,10~14mm為中度敏感,10以下為低度敏感,0為不敏感。實驗結(jié)果見表1和表2。表1:本發(fā)明化合物1和2與mem協(xié)同用藥后藥敏實驗結(jié)果化合物編號抑菌圈直徑(14-55)化合物編號抑菌圈直徑(15-101)mem9.6mmmem9.8mmmem+edta22.9mmmem+edta20.3mm本發(fā)明化合物1+mem23.9mm本發(fā)明化合物1+mem24.28mm本發(fā)明化合物2+mem22.1mm本發(fā)明化合物2+mem22.84mm表2:本發(fā)明化合物7與mem協(xié)同用藥后藥敏實驗結(jié)果化合物編號抑菌圈直徑(14-55)化合物編號抑菌圈直徑(101)mem0mmmem0mmmem+edta15.8mmmem+edta11.8mm本發(fā)明化合物7+mem18.9mm本發(fā)明化合物7+mem17.2mm由表1可知,藥物聯(lián)用結(jié)果表明,本發(fā)明化合物1、2、7和edta的聯(lián)用結(jié)果都證明了,與mem聯(lián)用之后,mem對耐藥細菌恢復(fù)敏感性,并且結(jié)果指明該測試菌株對于聯(lián)用藥物高度敏感。表2比表1中數(shù)據(jù)表示敏感性降低,但是菌株14-55對本發(fā)明化合物7和mem聯(lián)用后依舊為高度敏感。應(yīng)用例2本發(fā)明化合物體外抗菌聯(lián)合用藥活性測試:實驗方法微量肉湯稀釋法:(1)抗菌藥物貯存液制備:制備抗菌藥物貯備液的濃度為5120μg/ml,溶解度低的抗菌藥物可稍低于上述濃度。所需抗菌藥物溶液量或粉劑量可公式進行計算。配制好的抗菌藥物貯存液應(yīng)貯存于-20℃以下環(huán)境,保存期不超過6個月。(2)待測菌的制備:用接種環(huán)挑取過夜培養(yǎng)的mh(a)培養(yǎng)皿上的單菌落于mh(b)培養(yǎng)基中,校準(zhǔn)為0.5麥?zhǔn)媳葷針?biāo)準(zhǔn),約含菌數(shù)1×108cfu/ml,然后稀釋100倍,即得到約含菌數(shù)1.0×106cfu/ml的菌液,備用。(3)分別將抗菌藥物(美羅培南mem)貯備液母液(5120μg/ml)稀釋160倍,得到濃度為32μg/ml的抗菌藥物溶液。取無菌的96孔板,第一孔加入200μl的抗菌藥物,第二至十孔分別加入100μl的mh肉湯培養(yǎng)基,從第一孔吸取100μl加入第二孔,混勻,再吸取100μl至第三孔,依次類推,第十孔吸取100μl棄去。此時各孔藥物濃度依次為:16、8、4、2、1、0.5、0.25、0.125、0.0625、0.03125μg/ml,第十二孔加入200μlmh(b)培養(yǎng)基(陰性對照)。(4)然后將稀釋好的菌液分裝于ep管中,計算需要固定待測化合物的濃度(64μg/ml或32μg/ml),將其加入菌液中,使待測化合物的終濃度為64或32μg/ml。自稀釋好mem的96孔板的第1孔至第10孔分別加入菌液和待測化合物的混合溶液。將加完藥的96孔板放置37℃培養(yǎng)箱進行培養(yǎng),16-18h觀察菌液生長情況,根據(jù)美國臨床與實驗室標(biāo)準(zhǔn)協(xié)會(clsi)的判定標(biāo)準(zhǔn),肉眼觀測完全不長菌的那一孔為抗菌藥物的mic。同時用標(biāo)準(zhǔn)株做質(zhì)控。實驗結(jié)果見表3-6。表3:本發(fā)明化合物1,2,7和nota對含有ndm的菌株的mic(μg/ml)及其與美羅培南(mem)聯(lián)合用藥的mic結(jié)果本發(fā)明化合物1、2和nota單獨用藥的結(jié)果均為>128μg/ml。a表示mem單獨使用情況下,對于菌株的最小抑菌濃度(mic);b表示,在nota濃度為32μg/ml的條件下,mem對于菌株的mic;c表示,在本發(fā)明化合物1為64μg/ml條件下,mem對于菌株的mic;d表示,在本發(fā)明化合物2為64μg/ml條件下,mem對于菌株的mic。表4:本發(fā)明化合物3至10對含有ndm的菌株的mic(μg/ml)及其與美羅培南(mem)聯(lián)合用藥的mic結(jié)果本發(fā)明化合物3至10單獨用藥的結(jié)果均為>128μg/ml,ni表示聯(lián)合用藥結(jié)果>16μg/ml。a本表中的菌株編號與表3菌株編號一樣的為同一株臨床分離耐藥細菌,b-i表示本發(fā)明化合物3至10在濃度為64μg/ml的條件下,mem對于菌株的mic。表3和表4為本發(fā)明化合物1-10使用微量肉湯稀釋法所測定的與mem聯(lián)用后最小抑菌濃度(mic)的測定結(jié)果。如表3所示的作用結(jié)果,從中可看出,本發(fā)明化合物1和2對于mem的作用結(jié)果均有提高。并且有幾組與陽性對照nota相比,提高效力高于陽性對照組。從菌株的種屬來看,對于大腸埃希菌的作用效力來講,nota依舊可以將mem的mic恢復(fù)至耐藥折點左右,但是對于其它菌株卻沒有此效果。而反觀本發(fā)明化合物1和2,無論是針對大腸埃希菌還是肺炎克雷伯菌等,均對mem具有一定的提高效力,最大可以提高2560倍。表4所展示結(jié)果中,這一組化合物也可以提高mem的效果,但是相對沒有表3的化合物效果好。在表4中,活性最好的是化合物7,可以將部分菌株中mem的mic降低至0.03125μg/ml以下。表5:本發(fā)明化合物1,2和nota對產(chǎn)imp酶菌株的mic(μg/ml)及其與美羅培南(mem)聯(lián)合用藥的結(jié)果本發(fā)明化合物1、2和nota單獨用藥的結(jié)果均為>128μg/ml。a表示mem單獨使用情況下,對于菌株的最小抑菌濃度(mic);b表示,在nota濃度為32μg/ml的條件下,mem對于菌株的mic;c表示,在本發(fā)明化合物1為64μg/ml條件下,mem對于菌株的mic;d表示,在本發(fā)明化合物2為64μg/ml條件下,mem對于菌株的mic。表6:本發(fā)明化合物3至10對含有imp的菌株的mic(μg/ml)及其與美羅培南(mem)聯(lián)合用藥的mic結(jié)果菌株編號amembmemcmemdmemememfmemgmemhmemi1188ni16216<0.03125<0.031251224ni20.5810.513nininini4ni841488ni16<0.0312588815816nini<0.0312516111648ni16<0.03125820.5171616nini<0.0312516<0.03125<0.03125181616ni8<0.0312516421988nini4844201616nini16421本發(fā)明化合物3至10單獨用藥的結(jié)果均為>128μg/ml,ni表示聯(lián)合用藥結(jié)果>16μg/ml。a本表中的菌株編號與表5菌株編號一樣的為同一株臨床分離耐藥細菌,b-i表示本發(fā)明化合物3至10在濃度為64μg/ml的條件下,mem對于菌株的mic。表5與表6所展示的結(jié)果為在含有imp基因的菌株中,化合物1-10與mem聯(lián)用后的mic結(jié)果。其中,表5為本發(fā)明化合物1和2以及陽性對照藥物nota與mem的作用結(jié)果。從表中不難看出,除了13與20號菌株的結(jié)果改變較小以外,其余的結(jié)果都證明了在含有imp耐藥基因的菌株測試中,本發(fā)明化合物1和2對于mem的恢復(fù)作用力較好,最大可以提高2560倍。表6中結(jié)果的提高力度依舊不明顯,但是本發(fā)明化合物7在此次的作用結(jié)果中表現(xiàn)良好,16-18號菌株中mem的作用結(jié)果都小于0.03125μg/ml。應(yīng)用例3本發(fā)明化合物體外紅細胞溶血性實驗實驗材料:10mlep管,96孔板,新鮮脫脂羊血、磷酸鹽緩沖液(ph7.2-7.4)、抗菌藥物儲備液。質(zhì)量百分含量5%紅細胞懸浮液的制備:將新鮮的脫纖維羊血保存于4℃冰箱中,配置好的pbs緩沖液放置于37℃水浴鍋中,即用即取。實驗于生物安全柜內(nèi)進行操作,取10mlep管置于試管架,使用單孔道移液器吸取5700μl的1×pbs加入ep管中,小心緩慢的吸取300μl無菌綿羊血,緩慢加入到pbs溶液中,上下緩慢顛倒混勻,放入離心機1500rmp離心10min,取出ep管,小心移除上清。再重新分別加入5~7mlpbs溶液,重復(fù)上述操作。直至離心后上清液不再渾濁。最后一次離心過后,棄掉上清液,紅細胞沉積物留置待用。另取10mlep管,向其中加入5700μl的1×pbs(37℃),然后小心緩慢于液面下加入300μl的紅細胞沉積物。上下緩慢顛倒混勻,如此,便配置好質(zhì)量百分含量5%的紅細胞懸液。樣品溶液的配置:用少量的dmso溶解樣品(dmso終濃度不能大于質(zhì)量百分含量0.5%),并且用相同體積的dmso做陰性對照。溶解后的dmso儲備藥液,需用pbs于ep管中梯度稀釋。操作步驟:取96孔細胞培養(yǎng)板,記錄實驗編號,藥品代碼,日期。用單孔道移液器吸取配置好的質(zhì)量百分含量5%紅細胞懸浮液,每孔150μl加入。然后將梯度稀釋過后的藥物(每個藥物平行做三個副孔)對應(yīng)加入96孔板中。制備完成后放置于37℃恒溫箱內(nèi)孵育1h。最后,將培養(yǎng)板置于-4℃離心機內(nèi)離心(3500rpm,5min)。離心完畢,另取一塊96孔細胞培養(yǎng)板,做好標(biāo)注。然后對應(yīng)地吸取100μl上清液(孔孔對應(yīng))。吸取完畢后,與酶標(biāo)儀中測取od540nm值,分析數(shù)據(jù),得到hc50。應(yīng)用例4本發(fā)明化合物體外細胞毒性測試1、鋪板:將培養(yǎng)中狀態(tài)良好的hela細胞自培養(yǎng)箱中取出,于生物安全柜中操作。倒掉上清培養(yǎng)基,用2ml1×pbs洗細胞一次,除去殘留的培養(yǎng)基。取1ml胰蛋白酶沿壁打入培養(yǎng)皿中,于37℃培養(yǎng)箱,體積百分比0.5%co2中孵育1-2min。取出細胞消化后的培養(yǎng)皿,加入1ml培養(yǎng)基終止消化。將終止消化后的細胞混懸液轉(zhuǎn)移至10mlep管中,800rpm3min離心。緩慢棄掉上清,加入2-4ml培養(yǎng)基,反復(fù)吹打50次。從中取10μl細胞混懸液打入細胞計數(shù)板中,于顯微鏡下計數(shù)。計算好需要細胞的數(shù)目,配置為5000個/孔的細胞混懸液。每孔100μl依次加入96孔板中,于恒溫培養(yǎng)箱中孵育24h。2、加藥:將待測藥物在4mlep管中梯度稀釋好后,取出已貼壁生長的96孔板,棄掉上清,將稀釋好的待測藥物每個濃度三個副孔,每孔200μl加入板中,操作完成后將96孔板放入恒溫培養(yǎng)箱中。24h后,使用cck-8試劑盒,每孔7μl依次加入板中,放入37℃恒溫培養(yǎng)箱中培養(yǎng)4h后,于酶標(biāo)儀讀取od450nm值,計算抑制率,回歸其ic50。應(yīng)用例5本發(fā)明化合物體外活死細胞雙染測試熒光染液的配置:由于熒光染液都是生物級別,所以操作于生物安全柜內(nèi)進行(熒光染液大多數(shù)都強致癌,所以操作需謹慎)。鈣黃綠素-am的配置參照說明書配置,用dmso進行溶解,分裝后錫箔紙包裹外層,保存于-20℃冰箱內(nèi),即用即取。碘化丙啶需用ddh2o進行稀釋,操作同鈣黃綠素。操作步驟:操作同應(yīng)用例4細胞毒篩選實驗相同,區(qū)別在于將細胞置于24孔細胞培養(yǎng)板中培養(yǎng),加藥。藥物作用24h后,取出,分別收集各個孔上清于ep管中,將ep管好標(biāo)記,3500rpm5min離心,棄掉上清,1×pbs洗一次,再次棄掉上清。將24孔板用1×pbs每孔各洗一次。用配置好的染料每孔500μl先吹打收集該孔的死細胞,然后將其混合液加入到12孔板的孔中。操作完成后,于37℃恒溫培養(yǎng)箱孵育15min。接著,尼康熒光顯微鏡下拍照,記錄。應(yīng)用例6本發(fā)明化合物鋅離子敏感性實驗此實驗操作前期步驟同應(yīng)用例2,不同之處如下。待測藥物的添加:計算需要固定待測化合物的濃度(64μg/ml或32μg/ml),將其加入菌液中,使待測化合物的終濃度為64或32μg/ml,然后加入等摩爾量的zncl2。自稀釋好美羅培南的96孔板的第1至第10縱排分別加入菌液和待測化合物的混合溶液。將加完藥的96孔板放置37℃培養(yǎng)箱進行培養(yǎng),16-18h后,于酶標(biāo)儀讀取od600的吸光度,記錄。計算不同濃度下的細菌生長率,使用origin8.0生成柱狀圖。同時用標(biāo)準(zhǔn)菌株大腸埃希菌做質(zhì)控。應(yīng)用例7本發(fā)明化合物體外殺菌動力學(xué)測試實驗材料:mhb培養(yǎng)基,mha培養(yǎng)基,1.5ml無菌ep管,96孔板,pbs緩沖液。操作步驟:實驗操作于生物安全柜內(nèi)完成。取兩支10mlep管分別加入3ml的mhb培養(yǎng)基,用接種環(huán)分別挑取培養(yǎng)皿中的單克隆菌株,放置恒溫搖床中,37℃250rpm過夜生長。次日,將兩支管中的菌液分別都按1:10000倍進行稀釋,將稀釋好的菌液分為兩批,分別于恒溫搖床37℃250rpm繼續(xù)分別生長2h和5h。待到達生長時間,取出菌液,加入不同濃度mic的抗菌藥物和美羅培南。此時,分別從每個樣品管里面取出100μl的樣品液,于低溫離心機內(nèi)10000g離心,棄掉上清,用1×pbs稀釋。取無菌96孔板,每孔180μl加入1×pbs。從上述用1×pbs稀釋好的菌液中取出20μl加入第一孔,依次往后倍比稀釋。從稀釋好的孔中取出10μl的樣品液滴加于mha固體培養(yǎng)基上,做好標(biāo)記,此為0h時的菌落計數(shù)。此后的時間點取樣方法,依舊依照上述方法,分別對1h、2h、3h……24h等進行菌落計數(shù),使用origin8.0繪制出時間殺菌曲線。當(dāng)前第1頁12
相關(guān)技術(shù)
網(wǎng)友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1
- 丁基橡膠硫化劑預(yù)分散母膠粒及其制備方法
- 含羧酸酰胺類、二硫代氨基甲酸酯類殺菌劑和生防菌的菌藥組合物、制劑及應(yīng)用
- 新型二硫代氨基甲酸鹽類重金屬螯合劑的生產(chǎn)工藝的制作方法
- 含苯基酰胺類、二硫代氨基甲酸酯類殺菌劑和生防菌的菌藥組合物、制劑及應(yīng)用
- 一種錫硫鍵構(gòu)建的三(o-溴芐基)錫二乙基二硫代氨基甲酸酯配合物及其制備方法與應(yīng)用
- 電化學(xué)還原二氧化碳為甲酸或其鹽的催化劑及其制備方法
- 二硫代氨基甲酸銅衍生物及其制備與應(yīng)用
- 二硫代氨基甲酸銅衍生物及其制備與應(yīng)用
- 二乙基二硫代氨基甲酸碲的制備方法
- 基于控制干燥時間的二硫代氨基甲酸鹽的合成工藝的制作方法
- 具有增強的穩(wěn)定性和發(fā)光效率的量子點納米粒子的制作方法
- 新型二硫代氨基甲酸鹽類重金屬螯合劑的生產(chǎn)工藝的制作方法
- 含苯基酰胺類、二硫代氨基甲酸酯類殺菌劑和生防菌的菌藥組合物、制劑及應(yīng)用
- 一種錫硫鍵構(gòu)建的三(o-溴芐基)錫二乙基二硫代氨基甲酸酯配合物及其制備方法與應(yīng)用
- 一種兩端含金剛烷基團的raft鏈轉(zhuǎn)移劑及其制備方法和應(yīng)用
- 二硫代氨基甲酸銅衍生物及其制備與應(yīng)用
- 一種兩端含金剛烷基團的raft鏈轉(zhuǎn)移劑及其制備方法和應(yīng)用
- 二硫代氨基甲酸銅衍生物及其制備與應(yīng)用
- 二乙基二硫代氨基甲酸碲的制備方法
- 控制反應(yīng)時間的二硫代氨基甲酸鹽合成工藝的制作方法
- 一種澳洲茄胺衍生物在制備抗腫瘤藥物增敏劑中的應(yīng)用的制作方法與工藝
- 野八角中新苯甲酸衍生物及其制備方法、應(yīng)用和藥物組合物與流程
- 一種含噻吩基苯二胺衍生物合Zn(II)的聚合金屬配合物及其制備方法與用途與流程
- E?3?(苯基衍生物?次甲基)?吡喃并二氫黃酮衍生物及制備及應(yīng)用的制作方法與工藝
- 一種二苯甲酸碘苯類衍生物的制備方法及裝置與流程
- 手性2,5?二取代的環(huán)戊烷甲酸衍生物及其用途的制作方法與工藝
- 炔基吲唑衍生物及其用途的制作方法與工藝
- 1,2,4?噁二唑苯甲酸的藥物組合物和鹽的制作方法與工藝
- 娃兒藤堿含三氟甲基衍生物及其制備方法與流程
- 作為TTX?S 阻滯劑的芳胺衍生物的制作方法與工藝
- 一種水基農(nóng)藥增效劑的制造方法與工藝
- 用二硫代氨基甲酸鹽處理有機反應(yīng)中殘留重金屬離子的方法
- 洗煤污水處理藥劑的制作方法
- 含羧酸酰胺類、二硫代氨基甲酸酯類殺菌劑和生防菌的菌藥組合物、制劑及應(yīng)用
- 具有增強的穩(wěn)定性和發(fā)光效率的量子點納米粒子的制作方法
- 膜形成用組合物的制作方法
- 新型二硫代氨基甲酸鹽類重金屬螯合劑的生產(chǎn)工藝的制作方法
- 含苯基酰胺類、二硫代氨基甲酸酯類殺菌劑和生防菌的菌藥組合物、制劑及應(yīng)用
- 一種錫硫鍵構(gòu)建的三(o-溴芐基)錫二乙基二硫代氨基甲酸酯配合物及其制備方法與應(yīng)用
- 組合物、組合物的制造方法、不飽和化合物及不飽和化合物的制造方法