用于浸提金屬和貯存金屬提取期間的熱能的系統、裝置和方法與流程
相關申請的交叉引用
本應用性申請基于2014年9月9日提交的美國臨時專利申請序列號62/047,731且要求其優先權。該申請的整個內容作為參考引入本文。
本公開涉及從熔渣和礦石提取金屬的環境友好的浸提方法、其中進行該方法的一鍋法裝置、和用于該浸提方法的大規模生產的系統。
背景技術:
用于如銅、銀和金等的傳統金屬開采操作的主要目的為從礦石提取純金屬。為此,開采操作使用用于各種開采和提取步驟的很多不同的容器或鍋。例如,在銅礦開采中,銅礦石通過破碎(crush)接著焙燒來濃縮。在焙燒步驟期間,將破碎的銅礦石在暴露于空氣(例如,在開放空氣容器中)的同時加熱。空氣中的氧和水使銅硫化物轉換為銅氧化物,其示意性地在以下反應中示出:
cus+2o2+h2o→cuo+h2so4
接著,將銅氧化物通過在化學還原劑的存在下再加熱而熔煉(smelt),這使銅金屬與不期望的元素分離。
這些不期望的元素作為有害氣體而放出,或者它們作為稱為熔渣的材料漂浮在熔煉容器中。
熔渣通常被傾倒或用作道渣(roadballast)、回填材料、噴砂劑、水泥添加劑、或屋頂紙板用材料(materialforroofingshingles)。然而,熔渣會滲入河水、溪流、土壤、和環境中,這對于環境會是危險的,因為熔渣包含重金屬污染物。同時,熔渣包含沒有提取且浪費了的賤金屬(例如鋅和鐵)和一些錢幣金屬(例如,銅)。
不存在通過開采產生的熔渣的短缺。例如,對于生產的每一噸銅,粗略地產生2.2噸的熔渣。并且每年,全世界由于銅礦開采和精煉,粗略地產生2500萬噸的銅熔渣。該熔渣的大部分在水中具有低的溶解性,因此其為化學惰性物質,這使其難以加工。
熔渣也非常熱(例如,高達約1650攝氏度)。熔渣通常傾入渣坑并且使其冷卻。如果來自正冷卻的熔渣的熱能可以用于浸提過程(例如,經由熱轉移)以使金屬提取過程中加熱所需的成本和設備最少化,則會非常有益。
已經越來越關注用于從在銅的熔煉期間形成的熔渣回收高價值金屬的濕法冶金法。研究已經著重于使用如酸、堿和鹽等浸提劑(lixiviant)的在大氣壓下的浸提方法,還著重于高壓氧化性酸浸提。熔渣中的如銅、銀和金等金屬可以使用這些浸提方法來回收,但這些酸和堿對于環境非常有害。
氰化物法也用于從礦石和熔渣提取金屬,例如金、銅、銀和金。不幸地是,由于氰化物的高度有毒的性質,金屬提取的氰化物法是不期望的。結果,氰化物法在很多國家和地區是被禁止的。
因此,在采礦工業中存在的需要是經濟、有效
技術實現要素:
本公開的各種實施方案包括用于使用如熔融鹽或離子液體等低蒸汽壓液體從礦石和/或熔渣提取金屬的系統、裝置和方法。該環境友好的浸提方法是使用酸、堿或氰化物的金屬提取的傳統方法的替代。本文公開的系統和方法能夠從熔渣和/或礦石提取金屬。在實施方案中,熔渣為從使用利用酸、堿等的浸提方法的傳統采礦提取方法得到的副產物。
在另一個實施方案中,本文公開的系統和方法也可以用于從礦石和從作為礦石的副產物而產生的熔渣提取金屬。這些從礦石和熔渣的提取可以同時或循序(即,礦石,然后熔渣)進行。因此,在實施方案中,從礦石和熔渣的金屬提取的本公開可以完全代替依賴于使用酸、堿、氰化物等的有毒浸提方法的開采操作。在實施方案中,將礦石和熔渣使用低蒸汽壓試劑的環境友好的浸提方法同時地處理。在另一個實施方案中,將礦石和來源于礦石的熔渣使用如熔融鹽或離子液體等低蒸汽壓液體循序地處理。
本文公開的系統和方法也能夠使來自預加熱的熔渣的熱能轉移和利用或貯存,而不失去。將通過傳統浸提方法生產的熔渣預加熱至大約1650攝氏度。在
本文公開的環境友好的浸提方法包括將如熔融鹽或離子液體等低蒸汽壓液體用于溶解和從礦石和/或熔渣提取金屬并且通過電沉積回收它們。在一個以上的實施方案中,例如對于小規模操作,提取和電沉積步驟循序在相同的容器(例如,坩堝、鍋、釜、容器等)中進行。另外,本公開涵蓋大規模采礦操作,其中金屬提取和電沉積以彼此緊密接近的方式,但在分開的容器中進行,或共置于相同的設施中。
用于本公開的熔融鹽或離子液體具有非常低的蒸汽壓,例如在500攝氏度的操作溫度下的約2磅每平方英寸表壓(2psig)至在800攝氏度下的約1/2個大氣壓(即,7psig)以下、至在高達1400攝氏度的溫度下的1個大氣壓以下。該鹽也具有低的熔融溫度(即,在低至200攝氏度且高達400攝氏度下,將從固體轉換為液相)。將該鹽加氣(即,在開放容器內暴露于空氣)以將氧和水從空氣溶解至熔融鹽或離子液體中,從而形成將礦石或熔渣中的全部金屬和金屬離子提取為作為離子性金屬氯化物的鹽的混合物。金屬和金屬氧化物是不穩定的并且通過其中金屬和金屬離子轉換為金屬鹵化物的過程而溶解在加氣熔融的鹵化物鹽中,依序然后可以作為金屬在相同的鍋中電沉積在陰極上。
用于本公開的熔融鹽或離子液體不具有可觀的蒸汽壓,所以直到溫度遠高于1000攝氏度后,它們也幾乎不能夠從液相轉換為氣相,這是因為鹽蒸汽的形成受固體鹽(bulksalt)的靜電吸引(electrostaticattraction)的抑制。相反地,使用酸和堿電解質水溶液的傳統浸提方法在這樣的高溫下會不適合,這是因為水在100攝氏度下沸騰。
本文公開的方法和系統的優勢為能夠節約原本從熔渣損失的能量。如本文記載的用于處理銅熔渣的熔融鹽在高溫(例如,例如在一鍋法系統中,約400-500攝氏度,并且對于大規模操作為高達1000攝氏度)下使用。這些
固體熔渣的k-1至在1200-1300攝氏度下的熔融熔渣的0.1-0.3wm-1k-1。該非常高的溫度說明了氣冷礦渣保持數天的液體的原因[8]。有色金屬熔渣占據與熔渣相關的可得能量的90%,這使其對于儲液器來說為提供加熱熔融鹽或離子液體可轉移的熱能的巨大潛質。本文記載的使用熔融鹽來進行從這些熔渣回收金屬開辟了不僅回收金屬還回收有價值的熱能的新方法。
本文記載的方法的實施方案包括用于熔渣材料的熱轉移方法和系統。因此,本文公開的從礦石或熔渣浸提金屬的方法包括從礦石提取金屬或從熔渣提取金屬的更好的應用性,以及通過在系統中使用熱轉移方法保存能量而獲取和利用在傳統加工期間浪費的熱量的應用性。
可以認為本文公開的方法和系統不僅為從熔融的礦石提取金屬,也為借由鹽槽系統的獨特設計而貯存能量的粗略(robust)的解決方案。
熔融鹽和離子液體可以為用于從熔渣回收熱能的非常有用的熱載體。該最近的開發是由于以下事實:在高溫(高達1300攝氏度)下,這些種類的液體鹽可以用作熱轉移流體,而沒有其它已知的傳統熱載體可以在這樣的溫度下起效,例如,熔渣為約1650攝氏度,因而對熔渣使用酸、堿或氰化物的傳統的金屬提取方法不能起效,并且非熔融鹽不會與熔渣一起起效。
已經開發了幾種方法來回收熔渣的廢能量,但已經顯示幾乎沒有可行的。然而,本文記載的浸提方法和能量回收循環可以使用相同的熔融鹽和設備用材料而組合。
基于熔渣廢熱的溫差電勢(thermoelectricpower)的產生可以可能地結合至本文記載的浸提方法。從熔融鹽至儲水器的熱交換也可以產生使渦輪發電機發電的蒸汽流。
一鍋法裝置和方法
本公開的一個以上的實施方案包括用于一鍋法金屬提取和電沉積裝置的容器。該裝置或系統包括:1)耐高溫、耐腐蝕的外坩堝,其中外坩堝包括無孔玻璃質碳材料、或無孔陶瓷填充石墨、或石英、或無孔陶瓷材料;2)位于外坩堝的底部中央的耐高溫、耐腐蝕的內坩堝,其中內坩堝為陰極的(即,在電路中用作陰極),并且內坩堝包括多孔石墨、或無孔玻璃質碳材料、或無孔陶瓷填充石墨;3)通過將低熔融的加氣氯化物鹽與金屬礦石或熔渣組合生產的在內坩堝內的熔融鹽;4)垂直地位于內坩堝內的陽極棒;5)可操作地連接至內坩堝陰極和陽極棒的電源;和6)用于持續地混合內坩堝內的熔融鹽和熔渣/礦石的攪拌手段。
在使用該裝置的方法期間,將熔渣和/或礦石投入內坩堝中并且攪拌至熔融鹽或離子液體中以形成混合物,從其首先提取金屬其次電沉積純金屬。環繞內坩堝外壁的外坩堝內的區域包括用于加熱內坩堝的高溫的材料(例如,熔融熔渣等)。
在實施方案中,在一鍋法金屬提取和電沉積裝置中,內坩堝內的熔融鹽保持小于100厘泊的粘度。典型地,這通過溫度保持在約400和500攝氏度之間、或使混合物的粘度為小于100厘泊的任意其它溫度來實現。對于特定的金屬或鹽,更高的溫度對于實現該粘度會是必要的。
同時,在一鍋法金屬提取和沉積裝置中,熔融鹽為低熔融加氣氯化物鹽組合物。在優選的實施方案中,該氯化物鹽可以
2),或還有本領域技術人員會典型地已知和使用的其它這樣的氯化物鹽。
同時,在一個以上的實施方案中,金屬礦石或熔渣可以包括約20-30%的要提取并且電沉積至電極上、接著作為"純金屬"回收的例如銅金屬等金屬。
一鍋法:在一個以上的實施方案中,從礦石或熔渣提取金屬的方法包括:提供一鍋法裝置的第一步驟,所述一鍋法裝置包括:1)耐高溫、耐腐蝕的外坩堝;2)位于外坩堝的底部中央的耐高溫、耐腐蝕的內坩堝,其中內坩堝為陰極并且貯存通過將低熔融的加氣氯化物鹽與金屬礦石或熔渣組合生產的加氣熔融鹽;3)在外坩堝內且環繞內坩堝、并且能夠使內坩堝保持在約400-500攝氏度的溫度的加熱材料;和4)垂直地位于內坩堝內的陽極棒。盡管優選約400-500攝氏度的溫度,但該方法可以包括其中熔融鹽和礦石或熔渣的混合物的粘度小于100厘泊的任意溫度。在實施方案中,內坩堝包括多孔石墨、無孔玻璃質碳材料、或無孔陶瓷填充材料,并且外坩堝包括無孔玻璃質碳材料、或無孔陶瓷填充石墨、或石英、或無孔陶瓷材料。
在第二步驟中,將加氣熔融鹽在內坩堝中與熔渣和/或礦石混合直至熔融鹽內的金屬經由氧化并且氯離子與金屬氧化物中的氧陰離子交換以形成金屬氯化物來提取。在實施方案中,混合加氣熔融鹽在約400-500攝氏度的溫度下進行約1小時。
在第三步驟中,電源連接至電極,并且在陰極內坩堝與陽極棒之間施加電流。
并且在通過電還原進行的第四步驟中,來源于金屬氯化物的致密的金屬下沉并且沉積至內坩堝陰極的底部上。該純金屬為從坩堝排出、刮掉或者除去的最終產物。
在一鍋法方法的實施方案中,加氣熔融鹽是約為以下的組合物:13.4%氯化鈉、33.7%氯化鉀和52.9%氯化鋅(2),并且所述組合物的熔融溫度為約204攝氏度。
具有過濾或傾析的多坩堝系統
本公開的各種實施方案還包括在使用多個坩堝、器皿、反應器、容器等的同時從礦石和/或熔渣提取和沉積金屬的環境友好的浸提系統和方法。該多坩堝系統和方法適合于從礦石和/或熔渣提取和沉積大量金屬的全面的制造操作。
多坩堝系統:多坩堝系統的各種實施方案包括以下組件:能夠加熱和溶解金屬在與低蒸汽壓的熔融鹽或離子液體需氧地混合的熔渣和/或礦石中的混合坩堝;從混合物除去未溶解的熔渣或礦石(例如,通過過濾或傾析)的機構;能夠進行電沉積以通過沉積在陰極電極上而從液體溶液移出純金屬的電化學反應器。
電化學反應器包括:貯存液體溶液的耐高溫的坩堝;上端連接至直流電源并且底端浸漬在液體溶液中的陰極電極和陽極電極(例如,石墨);和使通電的液體溶液從所述反應器坩堝排出且排入可移動回收槽中的一個以上的閥。
可移動回收槽能夠首先接收致密的金屬(例如,銅),然后由用于接收包括熔融鹽或離子液體的耗盡金屬的液體溶液的空槽置換,其然后可以用于將通電的液體鹽溶液輸送回混合坩堝和/或熱交換單元。在實施方案中,回收槽為熱量和液體封閉的以防止熱量和使用的液體溶液的明顯損失。
浸提系統可以進一步包括將回收的通電的液體溶液(即,使用的熔融鹽或離子液體)再加熱的熱交換單元。熱交換單元包括在傾回至混合坩堝中之前將其熱量轉移至通電的液體溶液的來自礦石熔爐的高溫熔融熔渣。
多坩堝方法:在一個實施方案中,該方法的第一步驟包括:在約400和500攝氏度之間的溫度下在開放空氣坩堝中將金屬礦石或熔渣加熱、混合和溶解至非揮發性低蒸汽壓液體中以生產富金屬的液體溶液。非揮發性低蒸汽壓液體包括需氧性熔融鹽或離子液體,例如低粘度的nacl-kcl-zncl2。如以下式中公開,混合加氣熔融鹽能夠經由氧化和/或氯離子與金屬氧化物或金屬硫化物中的氧離子或硫離子交換得到金屬氯化物而從礦石和/或熔渣提取金屬。
cus+2o2+h2o→cuo+h2so4
cuo+2nacl→cucl2+na2o
該方法的第二步驟包括經由過濾或傾析將液體溶液與混合坩堝中的未溶解的礦石或熔渣分離。過濾的液體溶液包括金屬離子,并且將殘留的礦石/熔渣貯存或回收至熱交換器。
該方法的第三步驟包括:將具有金屬離子的液體溶液轉移至電化學反應器中。該反應器包括:耐高溫的外殼(例如,坩堝);上端連接至直流電源并且底端浸漬在液體溶液中的陰極電極和陽極電極;和使反應器中的可回收的熔融鹽排出的一個以上的閥。
第四步驟包括當在陰極與陽極電極之間施加電流時,將金屬從液體溶液的金屬離子電沉積在陰極電極上。
第五步驟包括首先排出致密的金屬,其次排出耗盡金屬的鹽,以通過使液體溶液經過包括將液體溶液再加熱的來自礦石熔爐的熔融熔渣的熱交換器來回收通電的液體鹽溶液。
本公開可以使用各種金屬礦石和熔渣,例如銅、金和銀,或其任意組合。另外,熔融鹽或離子液體可以包括:幾種共熔組成的nacl-kcl-zncl2、在共熔組成中混合有na和k的氯化物的2-鋁的氯化物和3-錳的氯化物、和4-具有各種陽離子和氯陰離子的穩定的離子液體。
附圖說明
不認為附圖和步驟是無遺漏的,但為涉及的方法的簡單說明。
圖1表明用于將金屬離子提取至需氧性熔融鹽(或離子液體)和從溶解在熔融鹽中的金屬離子電沉積金屬的系統和方法的一個實施方案的示意圖。非揮發性低蒸汽壓液體鹽是可再使用的并且熱量可以從熔融熔渣回收以加熱熔融鹽或離子液體。不使用酸、堿或氰化物。
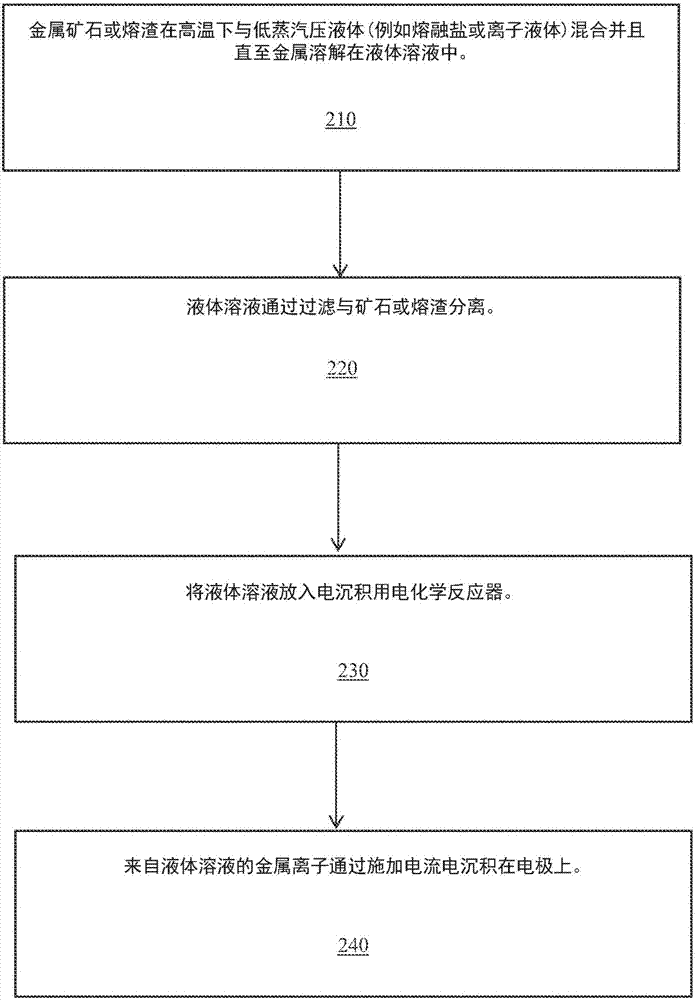
圖2為本文記載的方法的一般步驟的流程圖。
圖3表明使用熔融鹽作為低蒸汽壓液體并且使用熱交換器來貯存和提供熱能的本文記載的方法的示意圖。
圖4表明用于將金屬離子提取至熔融鹽中并且從溶解在熔融鹽中的金屬離子電沉積金屬的試驗工廠的示意圖。
圖5是示出在銅金屬在300℃下從包含3gm添加的cucl2·2h2o的熔融的nacl-kcl-zncl2鹽電沉積時電流密度隨時間的變化的圖。we:石墨。ce:石墨。re:sse。對we的施加電壓為-0.5vvs.ag/agcl。
圖6是示出使用本文記載的一鍋法方法的示例性實施方案中提取和沉積銅的主要步驟的流程圖。
圖7是圖6的一鍋法裝置的圖示。
具體實施方式
本文的各種實施方案的大規模制造操作可以包括借由以下非限制性實例的各種實施方案:具有用于從液體溶液移除熔渣殘留物的過濾器的多坩堝系統(例如,參見圖1、3、4);沒有過濾但具有陰極和陽極電極棒的單坩堝系統;和其中坩堝的底部用作陰極電極并且陽極電極棒懸浮在液體溶液中的沒有過濾的單坩堝系統(例如,圖6和7)。
具有過濾的多坩堝系統和方法
圖1示出本公開的系統和方法的一個實施方案的示意圖。雖然這是實驗室規模設施,但本領域技術人員可以容易地轉換本公開用于中試工廠。
金屬礦石和/或熔渣110(例如,包括銅、金、銀或其任意組合)添加至包含高溫的從槽150回收的熔融鹽(ms)或離子液體(il)的坩堝120并且在其中攪拌。坩堝120暴露于空氣,意味著坩堝的頂部保持敞開,或將空氣攪拌至液體溶液中。在實施方案中,熔融鹽包括作為分別為0.5/0.5/1摩爾比的混合物的氯化鈉和氯化鉀和氯化鋅共熔體(eutectic)(即,nacl-kcl-znc12)。該nacl-kcl-znc12熔融鹽在約200℃熔融并且具有非常低的蒸汽壓(7psig)并且在空氣中在超過1000℃是化學穩定的。
將礦石或熔渣借由本領域已知的標準機構,例如借由吊車或輸送帶添加至坩堝120。再使用的熔融鹽或離子液體可以從回收槽150泵入或傾入坩堝120中。
在來自礦石或熔渣的金屬溶解至熔融鹽或至離子液體中的同時,向坩堝120施加熱,并且攪拌混合物以吸收金屬礦石或熔渣。這將生產包含金屬氯化物(例如,cucl2)的液體溶液。雖然其它溫度預期在本發明的范圍內并且隨著使用的熔融鹽或離子液體和提取的金屬的種類而改變,但施加熱的適當的溫度范圍是約500至1100攝氏度。熱源130可以是來自礦石熔爐的熔融熔渣(例如,高達1650攝氏度)和/或本領域技術人員已知的標準生熱的電-機械設備。
在一個實施方案中(如圖1中示出),液體溶液通過重力或真空泵170經過過濾器140。將過量的熔渣殘留物通過將坩堝借由使用例如吊車或其它機械方法反轉而丟棄。剩余溶液進入借由熱源132進行加熱的坩堝106。坩堝106包括一對電極108(陽極)和109(陰極)。坩堝106進一步包括壓力釋放機構105作為坩堝內的壓力變得太高時的安全機構。坩堝106進一步包括閥107,閥107首先將熔融的金屬排入回收槽150,然后
在金屬電鍍步驟期間,可以使用各種類型的電極108、109(例如,石墨、玻璃質碳、或任意穩定的難熔(refractory)金屬)。金屬形成在石墨陰極109上。隨著金屬形成在陰極109上,石墨陽極108將由于與空氣接觸的熔融鹽中的微量水的存在而氧化為二氧化碳。水基本上來自空氣:
c+h2o→co2+4h++4e-
在圖1的系統的另一個實施方案中,可以省略坩堝130。將加氣低粘度的熔融鹽或離子液體直接傾入或泵入坩堝106并且借由吊車添加熔渣和/或礦石。手動地或自動地進行混合,并且將坩堝106在132處借由機械手段加熱,直至礦石和/或熔渣中的金屬溶解并且轉換為金屬鹽(例如,如cucl2等金屬氯化物)。
電源然后連接至電極108和109并且在其間施加電流以將金屬鹽(金屬氯化物)轉換為金屬。殘留的礦石-熔渣(未溶解)和鹽漂浮,而分離的金屬(cu)沉入坩堝106的底部,其中在閥107處排出至槽150從而形成銅錠(例如,30英尺長、直徑約8英寸)。
陽極(-)電極108然后提起(機械地或手動地)并且將耗盡金屬的殘留液體鹽借由閥105傾入容器中從而變為回收的熔融鹽或離子液體。
將陽極(-)電極108和陰極(+)電極109提起并且將坩堝106使用吊車反轉以丟棄殘留的熔渣。坩堝106然后回復直立并且再填充;并且將陽極(-)電極108和陰極(+)電極109放回原位。
然后,重復加熱、和混合、和施加電流以從礦石或熔渣提取金屬的過程,并且其中提取的金屬下沉并且排出坩堝以外。
具有過濾或傾析的多坩堝方法的流程
圖2示出本文公開的各種實施方案的使用低蒸汽壓、加氣熔融鹽或離子液體的金屬浸提方法的一般步驟的概要,并且圖3是圖2的一個示例性實施方案。
在步驟210中,將金屬礦石或熔渣與低蒸汽壓熔融鹽或離子液體混合以形成混合物。借由例如沒有蓋上的坩堝,將混合物加氣。坩堝的溫度控制為能夠使全部金屬和金屬氧化物從礦石或熔渣提取出并且在混合物中形成溶解在液體溶液中的金屬離子。
在步驟220中,將具有金屬離子的液體溶液通過過濾或傾析(從剛高于耗盡金屬的固體的水平面傾出),或其它工業分離方法從耗盡金屬的固體礦石或熔渣分離。耗盡金屬的固體可以例如通過反轉容器而在此處丟棄,其可以然后再使用以將熱量轉移至富金屬的礦石或熔渣和熔融鹽或離子液體的新的液體溶液。
在步驟230中,將富金屬的熱的液體溶液放入用于電沉積的電化學反應器。在該步驟中,非常熱的液體(1000℃左右或高于1000℃)可以從鍋起經過金屬管(熱交換器至水浴)并且冷卻的(500℃)液體回到用作陰極的石墨鍋以制成金屬。交換的熱量可以用于使來自水的蒸汽驅動渦輪發電機以發電。
在步驟240中,在使用電流在碳陽極處形成二氧化碳的同時,來自液體溶液的金屬離子在碳陰極處作為純金屬電沉積。
金屬比鹽致密并且可以從反應容器(像石墨坩堝)的底部傾出,在電化學反應器中殘留在上部的耗盡金屬的低蒸汽壓液體然后可以回收至初始步驟以從礦石或熔渣再次提取金屬。
在圖2的流程的第一步驟中,將礦石或熔渣投入容器中,
從用作熱轉移流體的低蒸汽壓液體獲得,以從熔渣取得熱能。低蒸汽壓液體可以保持貯存在分離槽(圖3,320)中。當礦石或熔渣中的金屬和金屬的離子達到平衡時,該混合物準備好通過過濾或傾析(例如,圖3,350)來分離。為了有助于過濾方法,可以通過在實驗室規模中施加真空、或通過重力、或通過設定要傾析的容器的相對垂直位置(上部)利用壓力差將液體排出至收集液體的容器(下部)。后者是對于工業方法更實用的構造。隨著將液體通過將水經過管以產生水蒸汽而從上部用管輸送至下部容器,可以除去熱量。從分離過程獲得的全部低蒸汽壓液體貯存在容器(例如,圖3,360)中。該后者容器不僅具有低蒸汽壓液體,其也具有可以電沉積為金屬的在攪拌過程中溶解的全部金屬離子。
將低蒸汽壓液體通過使用電阻加熱器或在使液體與熱熔渣接觸時用作熱轉移流體且由熔融熔渣加熱的液體本身而保持在恒定溫度下。
電鍍可以使用石墨電極等來進行。隨著金屬形成在陰極上,石墨陽極將由于電流和供給了空氣的熔融離子性流體中的微量水或分子氧的存在而氧化為二氧化碳。水和分子氧基本上來自空氣。金屬和熔融鹽具有不同的密度。金屬下沉并且鹽漂浮。當低蒸汽壓溶液中的金屬離子的大多數電沉積時,打開閥以從熔融鹽分離金屬。金屬和鹽的分離還通過以下來進行:將底層金屬傾出具有金屬和離子性流體的容器的底部以外,或將金屬層上方的離子性流體釋放至分離容器中;該容器可以是可移動的(例如,圖3,370)以將低蒸汽壓液體回收至其中其與新的礦石或熔渣混合的初始步驟。
圖3是用于將金屬離子提取至熔融鹽中(例如,使用熔融鹽從熔渣浸提金屬)的方法和系統的示例性實施方案的示意圖。來自熱的熔融熔渣305的熱量經過熱交換器315。熱交換器315將熱量提供至熔融鹽并且該最后的熱的鹽貯存在分離槽320中。經過熱交換器315的熔融熔渣305進給至造粒機330;其中在造粒機330中生產小的熔渣的顆粒。將熔渣的顆粒與熔融鹽混合;然后將熔渣和熔融鹽在槽340中攪拌。熔融鹽和熔渣殘留物的分離通過傾析或過濾350來進行。在攪拌過程期間生產的需氧性熔融鹽溶解金屬離子并且離子在石墨電極360上還原且電沉積為金屬層,其中從石墨回收金屬。在電沉積金屬之后,熔融鹽釋放出金屬離子并且其沉積在槽370中,現在其準備用于回收。回收的熔融鹽進給至初始熱交換器315用于再次加熱并且用作熱轉移流體。
圖4示出基于圖2和3的方法和系統用于使用熔融鹽從礦石或熔渣提取金屬離子的示例性生產工廠系統400的示意圖。該工廠可以由本領域技術人員成比例變為各種尺寸。
在槽405中,熔融熔渣從礦石熔爐分離,并且經過熱交換器410,在熱交換器410中熔融熔渣將熱能提供至從軸475落下經過熱交換器410進入槽420的回收的熔融鹽。熔融熔渣由于熱交換器而降低其溫度并且進給至其中在槽415處獲得小顆粒的造粒過程。回收的全部熔融鹽沉積在熱絕緣槽420中,在熱絕緣槽420中,將回收的全部熔融鹽與新鹽混合用于彌補在該過程中消耗的鹽。從熱絕緣槽420取得熔融鹽并且其與來自造粒機系統415的熔渣在槽425處混合。混合物借由裝置430在保持在攪拌下一些時間,直至其達到熱力學平衡。在該方法的本部分中,將金屬離子提取至熔融鹽中。
為了從殘留的熔渣分離包含金屬離子的熔融鹽,攪拌終止并且在等待一些時間之后,進行殘留的熔渣的沉淀;殘留的熔渣進給至435處的槽的底部。在435處的槽的底部中為用于熔融鹽的傾析或過濾而打開的閘門。在分離過程中,將殘留的熔渣使用循環臂取出并且熔融鹽越過熔渣或經過過濾器
在從熔渣分離熔融鹽之后,熔融鹽進給至其中金屬離子通過在石墨電極上電沉積金屬而從熔融鹽分離的具有在450處的兩個石墨電極的容器455。隨著金屬形成在石墨陰極處,在陽極上,石墨將由于陽極電流和與空氣接觸的熔融鹽中的微量水的存在而氧化為二氧化碳。水基本上來自空氣。將其中進行電沉積的容器在管開口460處使用與來自熱絕緣槽420的熔融鹽交換的熱量保持在高溫下(大于400攝氏度)。當幾乎全部金屬離子通過電沉積從熔融鹽分離時,閘門打開并且耗盡金屬的熔融鹽傾入第二熱絕緣槽470并且借由管465用管輸送。從該第二絕緣槽470,將熔融鹽借由用管輸送至開口475和/或通過使用可移動的容器回收至熱交換器,以在熱交換器410處再次加熱。
認識到的是,圖4中表明的系統是一個示例性實施方案,以及本領域技術人員可以容易地改造示意圖以達成用于從熔融熔渣提取金屬的大型設施的等效系統。
沒有過濾的一鍋法裝置和系統
以下公開是圖5-7中示出的用于小規模的操作,例如實驗室。在該實施方案中,使用沒有過濾或傾析(例如,圖6和7)的一鍋法系統(例如,圖7中的一鍋法裝置)。
示出一鍋法系統中提取和沉積如銅等金屬的主要步驟的流程圖在圖6中示出。在步驟610中,包括nacl-kcl-znc12的熔融鹽在石墨坩堝中保持在400與500攝氏度之間。在步驟620中,將約20至30%銅熔渣的銅精礦(copperconcentrate)添加至熔融鹽以形成液體溶液。在步驟630中,將液體溶液在400至500攝氏度下在暴露于空氣的同時混合約1小時從而吸收熔渣中的銅。在步驟640中,銅金屬通過電鍍溶解在熔融鹽中的離子性銅來形成。同時在步驟650中,銅金屬下沉并且沉積在石墨坩堝的底部
在圖7中示出的一鍋法實施方案中,承裝加熱的熔融鹽或離子液體的石墨內坩堝720用作陰極電極,而垂直地浸漬在鹽中的一個以上的石墨棒750用作陽極電極。這提供了清潔、有效且相對于傳統的金屬精煉相對地安全得多的替代。單坩堝實施方案進一步包括:內坩堝720,其位于填充有如熔煉熔渣等的熱源730以用于加熱內坩堝720內的熔融鹽或離子液體和礦石/熔渣的外坩堝710內的中央;可以用于內坩堝和外坩堝(720,710)二者中的手動或自動的攪拌手段740;以及用于在內坩堝720的壁與陽極棒750之間施加電流(例如,通過將電極應用至二者)的電源(未示出)。內坩堝和外坩堝(720,710)二者由耐高溫、耐腐蝕的材料,例如無孔玻璃質碳材料或無孔陶瓷填充石墨制成。內坩堝也可以由多孔石墨制成。外坩堝也可以由石英或無孔陶瓷材料制成。
該臺式實施方案使用較低溫度的離子液體,然而,也可以使用其中熔融鹽包含混合物中分別為0.5/0.5/1摩爾比的氯化鈉和氯化鉀和氯化鋅共熔體的更實用的市售大規模系統。該nacl-kcl-znc12熔融鹽在200℃下熔融并且在空氣中在超過1000℃是穩定的。另外,該熔融的氯化物混合物在加氣時在空氣的存在下且在大于500℃的溫度下將以迅速的速度溶解金屬和金屬氧化物。在全部的金屬和金屬氧化物轉換為金屬氯化物(幾小時)之后,金屬氯化物的金屬形式在相同的鍋中通過電沉積而形成。來自空氣的氧基本上為驅動金屬溶解的氧化劑。
實施例
以下實施例為一鍋法裝置和方法(圖6和7)。
實驗設計
使用的試劑為氯化鈉(nacl)、氯化鉀(kcl)、氯化鋅(zncl2)、氯化銀、99.99%銀線(alfaaesar,premion等級)和來自sigmaaldrich(試劑等級)的氯化銅。銅精礦礦石(concentratedcopperore)和銅熔渣樣品由mexicanadecobre提供。使用的裝置為加熱套(mantle)(glascol)、99.9%石墨坩堝(wangxueping,singapore)、玻璃質碳坩堝(spisupplies/structureprobe,inc.,westchester,pa)、石墨棒(mcmastercarr)、電源(circuitspecialists,tempe,az)、biologic穩壓器(oakridge,tn)。在氧化鋯棒密封至石英的浸漬熔融鹽的容器側以制得彎曲的離子流路的石英容器中的氯化鉀中,自制的參考電極由銀線在氯化銀的溶液中制成,并且發現該ag/agcl電極(sse)相對于nhe具有0.2v的電壓,參考電極的細節記載于作為參考并入的(.h.h.elsentriecy[5])。
三元熔融鹽混合物在“一鍋”中用作浸提劑并且電鍍電解質具有熔點(tm)為204℃的13.4摩爾%nacl-33.7%kcl-52.9%zncl2的組成(參見[6,7])。該提取和電鍍池(cell)是石墨棒作為陽極插入的填充有熔融鹽和銅精礦的作為陰極的導電性的碳坩堝。電源用于在陽極棒與陰極偏向(biased)負的陰極坩堝之間施加電壓。將根據熱力學計算的約2.0v的最小電位差施加在陽極(石墨棒)與陰極(石墨坩堝)之間,并且根據電解槽的幾何形狀(電極面積和分隔(separation))調節以得到期望的電流水平。因為銅是熔體中的最致密的材料,銅下沉并且在石墨坩堝(陰極)的底部上收集。為了分析的目的,將從熔融鹽(上方)電沉積的銅從石墨坩堝的底部收集并且使用去離子水(di水)清洗幾次以除去全部鹽和可溶性雜質,稱重,然后用于元素分析。元素分析通過galbraithlaboratories,knoxville,tn,usa來進行。
結果和討論
銅提取和金屬形成為使用nacl、kcl和zncl2的熔融共熔混合物的“一鍋法”方法,該nacl、kcl和zncl2的熔融共熔混合物同時作為浸提劑(用于溶解銅和銅
a)從熔融鹽中的氯化銅(ii)電沉積銅金屬
將氯化銅添加至熔融的nacl-kcl-znc12共熔鹽,然后嘗試電沉積銅金屬。這作為第一步驟來進行以檢驗銅離子是否溶解在熔融的nacl-kcl-znc12共熔鹽中并且該熔融鹽混合物是否可以用作用于使這些離子還原電沉積為銅金屬的電解質。將精確稱量的量(3gm)的氯化銅二水合物(cucl2·2h2o)添加至石英坩堝中的熔融的nacl-kcl-znc12鹽。看到氯化銅二水合物容易地溶解在熔融鹽中。在350℃下相對于浸漬在相同的鹽混合物中的銀/氯化銀參考電極(sse)測量nacl-kcl-znc12鹽中銅金屬線電極與cucl2之間的開路電壓(ocv)。銅線與sse參考之間的ocv初始地顯示為-0.14v,但緩慢地轉移至更正的值,并且幾分鐘后為約-0.12v。因此,估計熔融鹽混合物中的cu/cu2+耦合電位相對于sse為約-0.12v。
下一步,將用作陽極和陰極的兩個石墨棒與sse參考電極一起放入使用電阻加熱帶(resistiveheatingtape)來加熱的石英坩堝中的具有3gm的cucl2·2h2o的熔融的naci-kcl-zncl2鹽中。因為發現銅線在氯化銅鹽中的ocv相對于sse為-0.12v左右,將相對于sse為-0.5v的恒定電位施加至工作石墨棒(陰極),并且約60ma/cm2的電池電流在石墨工作(陰極)電極與對(陽極)電極之間產生。
下一步,試圖進行用于使用簡單電源電沉積銅金屬的實用電解槽設計。將石墨棒狀電極浸漬至石墨坩堝中的銅鹽(3gm的cucl2·2h2o)和熔融的nacl-kcl-znc12鹽的新混合物中。通常的電源用于在石墨坩堝陰極(負極)與石墨棒陽極(正極)之間施加恒定電壓(2.0v)。
當施加電壓時,產生40與60ma/cm2的電流。將電壓在范圍為250℃-300℃的溫度下施加2h,并且銅金屬電鍍在石墨坩堝的底部上。電沉積的銅的測量量為1.09gm,這表明在實驗誤差內,銅離子向銅金屬的轉換率有效地為100%。從該實驗的主要結論為:銅金屬可以在使用熔融氯化物鹽作為反應介質(電解質)并且使用如上所述的電解槽設計時從離子性銅化合物定量地提取。
b)使用熔融金屬鹵化物鹽從銅精礦提取銅
在驗證用于從溶解了cucl2離子的熔融的nacl-kcl-znc12鹽沉積銅金屬的新方法的可行性之后,下一步驟是檢驗銅是否可以從富銅土提取和提取的銅是否可以電鍍為金屬銅。這里研究的富銅土為從mexicanadecobre獲得的共熔的銅精礦和銅熔渣。
認為本實驗中的成功為其中使用熔融鹽并且從該熔融鹽電沉積純銅金屬而從銅精礦(或熔渣)提取銅的新的“綠色”技術的概念的驗證。
該新的方法使用便宜的氯化物鹽(nacl、kcl和znc12),
將使從裝入有氯化銅的熔融鹽電沉積金屬銅優化的相同的設置和條件用于從包含礦物樣品的實際的銅提取銅并且將提取的銅電沉積為銅金屬的第一嘗試中。然而,當使用實際的銅精礦樣品時,可見的是需要進一步的優化。例如,在處理銅精礦樣品期間,將銅沉積在坩堝壁和坩堝底部上,甚至在多孔石墨的壁中。另外,電沉積的銅的外觀是暗淡的,說明雜質的存在。
進行銅提取(時間、溫度)和電沉積條件(電位、溫度、時間)的改變,以在形成的銅金屬的實驗測定百分比相對于富銅土(精礦或熔渣)中鑒定(assay)的銅方面使銅精礦的處理條件最優化。目標是改變條件并且提高作為用于確定條件的改變是改善的標準的轉換效率(從銅精礦礦石或熔渣回收的銅金屬的程度)。
在很多試驗和誤差之后,發現了用于以高效率處理銅的提取和金屬銅的沉積的適當的電解槽。該電解槽從純(但多孔)石墨改變為無孔玻璃質導電性碳坩堝,以用于保持熔融的nacl-
在處理富銅土(cu精礦或熔渣)之后,銅不在坩堝的壁中,但可以清楚地看到沉積在作為罐的坩堝的壁和底部二者上。
銅使用玻璃質碳坩堝作為陰極來形成并且收集和轉移至玻璃燒杯,然后使用di水來洗滌。將銅在高過電位下電鍍,所以其它元素在提取和電鍍過程中與銅共電鍍。
為了確定從富銅樣品提取的銅的程度,將未處理的樣品材料傳送至第三方(galbraithlaboratories,inc.,tn,usa)用于化學分析。分析提供了作為接收的未處理樣品(cu精礦)中和處理之后收集的材料(提取的材料)中銅的百分比。分析銅精礦和提取的材料的三個重復樣品。估算銅轉換率。表1示出銅精礦礦石和對應的電沉積銅的試驗。如表1中示出,實驗地確定的銅從銅礦石的轉換率為98.36%。
表1
c)使用金屬鹵化物鹽從銅熔渣提取銅
使用從cu精礦提取銅金屬的優化的相同過程,從包含銅的熔渣提取銅金屬。熔渣的起始量為50gm。提取的材料為1.3gm。將該量(l.3gm)傳送至相同的公司(galbraithlaboratories,inc.,tn,usa)用于分析。表2示出在從50gm熔渣提取的1.3gm材料中的銅的百分比(%cu)。
表2
從表2中的結果,清楚的是,從1.3gm(從50gm熔渣提取的)中,存在25.22mg的cu。對于每100gm熔渣,可以回收50.44mg的cu,考慮到每年從傳統的銅提取方法產生百萬噸熔渣[1],認為這是具有可觀的經濟價值和影響的顯著的量。
這些示例性實施方案為可以用于從富銅精礦或熔渣提取銅且將提取的銅沉積為銅金屬的對于傳統方法的替換方法的積極的概念驗證。使用熔融的nacl-kcl-znc12鹽作為銅提取流體(浸提劑)和用于電沉積銅金屬的電解質二者,在一鍋中進行該新的方法。nacl-kcl-znc12鹽是環境良好的,因為其由無毒元素制成并且不釋放有毒蒸汽。
當這些添加至包含在石墨或玻璃質碳坩堝中的需氧性共熔熔融的氯化物鹽時,銅從精礦或熔渣完全地溶解。在吸收銅精礦或熔渣之后,將石墨陽極插入熔融鹽混合物中。將電源連接至石墨棒陽極和用作陰極的石墨坩堝,然后熔融鹽中的銅離子還原并且沉積為下沉至石墨坩堝的底部的銅金屬。在大規模上,打開閥
從熔融的nacl-kcl-znc12鹽電沉積銅基本上再生成熔融的nacl-kcl-znc12鹽。因為可以再生成nacl-kcl-znc12鹽,新的方法不僅環境良好,也可以同時是可持續且經濟的。該方法良好地適用于處理富有銀和金以及銅的土質材料和全部三種金屬的混合物。
雖然結果非常新,但看起來傳統濕法冶金方法沒有理由不被此時看起來為更經濟、有效、可持續且環境良好的替代的新的熔融鹽方法替換。
結論
術語“多種”可以在說明書中使用以記載兩種以上的組分、裝置、元素、單元或參數等。除非另有說明,本文記載的方法實施方案不限定為特定的順序或序列。另外,記載的方法實施方案或其元素中的一些可以在相同的時刻發生或進行。
雖然本公開的各種特征可以記載于單一實施方案的內容中,但這些特征也可以分開地或以任意適當的組合提供。相反地,雖然各種實施方案可以記載于本文中的用于說明的分開實施方案的內容中,但它們也可以在單一實施方案中實施。
要理解的是,本文采用的措辭和術語不構成為限制性的并且僅用于描述目的。
要理解的是,本文記載的細節不解讀為對各種實施方案的應用的限制。
另外,要理解的是,本公開的各種實施方案可以以各種方式進行或實施,以及本發明可以在除了以上說明書中表明的那些以外的實施方案中實施。
參考文獻
l.markeschlesinger,matthewj.king,kathrync.sole,williamgdavenport,extractivemetallurgyofcopper,fifthedition(201l),elsevier,printedandboundingreatbritain,isbn:978-0-08-096789-9.
2.jianmingluanddaviddreisinger,"solventextractionofcopperfromchloridesolutioni:extractionisotherms",hydrometallurgy137(2013)13-17.
3.s.ayataandh.yildiran,"copperextractionfromgoldbearingcopper(ii)sulphidewithoutthermalprocesstoobtaingoldconcentrate",mineralsengineering18(2005)901-904.
4.ionelabirloaga,idademichelis,francescoferella,mihaibuzatuandfrancescovegliò,"studyontheinfluenceofvariousfactorsinthehydrometallurgicalprocessingofwasteprintedcircuitboardsforcopperandgoldrecovery",wastemanagement33(2013)935-941.
5.h.h.elsentriecyandd.f,gervasio,"establishingelectrodepotentialsinmoltensalts",manuscriptinpreparation(2015).
6.dominicgervasio,hassanh.elsentriecy,luisphillipidasilva,a.m.kannan,xinhaixu,"materialschallengesforconcentratingsolarpower",chapter4,innanoscalematerialsanddevicesforelectronics,photonicsandsolarenergy,isbn9783319186320,stephengoodnick,anatolikorkin,androbertnemanich,editors,inthe"nanostructurescienceandtechnology"series,editor:davidlockwoodspringereditor:davidpacker,springer,ny,ny(2015).
7.k.vignarooban,p.pugazhendhi,c.tucker,d.gervasioanda.m.kannan,"corrosionresistanceofhastelloysinmoltenmetal-chlorideheat-transferfluidsforconcentratingsolarpowerapplications",solarenergy,103,pp.62-69(2014).
8."materialschallengesforconcentratingsolarpower",h.h.elsentriecyetal.,nanoscalematerialsanddevicesforelectronics,photonicsandsolarenergyin"nanostructurescienceandtechnology",springer,ny,ny,stephengoodnick,anatolikorkin,androbertnemanich,:davidlockwood,davidpacker,editorsinpress(2015).
- 還沒有人留言評論。精彩留言會獲得點贊!