抗LOX?1人源單鏈抗體及其制備方法和應用與流程
本發明涉及基因工程
技術領域:
,特別涉及一種抗lox-1人源單鏈抗體及其制備方法和應用。
背景技術:
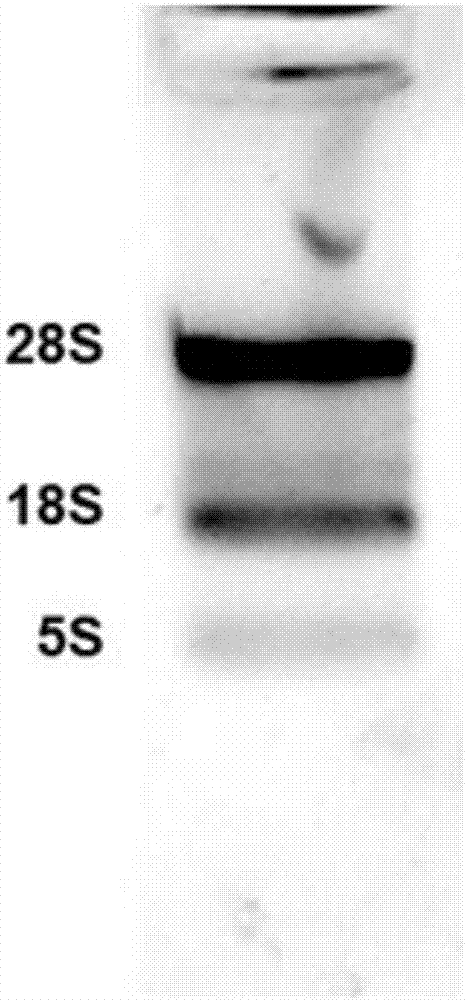
:2016年10月8日的柳葉刀雜志公布的全球疾病負擔最新數據顯示,從1990年到2015年主要死因的排位發生了變化,2015年的主要死因,缺血性心臟病和腦血管疾病分別排在第一和第二位,也就是說,心腦血管疾病已經成為人類的第一殺手。我國心血管病患病率及死亡率處于上升階段,“中國心血管病報告2015”中指出,心血管病占居民疾病死亡構成的40%以上,為我國居民的首位死因。心血管病負擔日漸加重,已成為重大的公共衛生間題,防治心血管病刻不容緩。心腦血管疾病的前身是動脈粥樣硬化(arteriosclerosis,as)。多項研究顯示:as是經多年無癥狀發展而突然致殘致死的疾病,70%-80%的冠狀動脈血栓的形成是繼發于as斑塊的破裂。特別是最近的臨床調查顯示,30歲以下卻已經出現動脈硬化的病例已有很多。對人類而言,隨年齡的增長動脈硬化幾乎是不可避免的,但是發病危險因素的有無是疾病進展的關鍵。as在形成脂紋這種初級階段的時候是可逆的,經治療,內腔狹窄和斑塊可以回縮;但是隨著病變的發展,將逐漸成為不可逆性改變。as的發生始于血管內皮損傷,氧化型低密度脂蛋白(oxidizedlowdensitylipoprotein,ox-ldl)是導致血管內皮細胞激活、損傷和功能失調的主要危險因子,是as的主要致病因素。而ox-ldl必須通過其存在于血管內皮細胞的特異性受體,即植物凝集素樣氧化型低密度脂蛋白受體-1(lectin-likeoxidizedlowdensitylipoproteinreceptor-1,lox-1)的介導才能發揮作用。近來研究發現:眾多因素能調控lox-1的病理表達,內皮細胞吞噬與lox-1結合ox-ldl后觸發一系列信息通路,調控轉錄因子的表達,使黏附分子、炎癥因子等表達上調,活性氧表達降低,導致內皮損傷、as等疾病形成。lox-1是as眾多事件的初始階段,已成為抗as藥物研發的強有力新靶點。目前,已經成功開發出鼠源和雞源抗lox-1單克隆抗體(monoclonalantibody),而且一系列的動物模型試驗結果表明,抗lox-1單克隆抗體不但能夠抑制lox-1介導的動脈粥樣硬化類疾病的發生發展,還可以作為靶向載體用于動脈粥樣硬化斑塊的顯像。雖然抗lox-1單克隆抗體在動物模型的研究中顯示了優越的診療效果,但是動物源性單克隆抗體應用于人體治療時存在諸多問題:一是不能有效地激活人體中補體和fc受體相關的效應系統;二是被人體免疫系統所識別,產生人抗鼠抗體(humanantigenmouseantibody,hama),造成諸多毒副作用;三是在人體循環系統中被很快清除掉,難以達到理想的治療效果。與單克隆抗體相比,單鏈抗體(single-chainfragmentvariable,scfv)顯示了其獨特的優越性,它是在基因水平上將免疫球蛋白的重鏈可變區(thevariableregionofheavychain,vh)和輕鏈可變區(thevariableregionoflightchain,vl)通過一段連接肽連接而成,它不僅具備單克隆抗體可與抗原特異結合的特征,更因其具有分子量小、組織穿透性好、免疫原性低、易于基因工程操作和構建抗體融合蛋白等諸多優點而凸顯其在醫學應用中的價值。目前,關于抗lox-1單鏈抗體的研究報道很少,只有一株源于鼠源單克隆抗體(#10-1)的單鏈抗體。雖然動物源性單鏈抗體由于缺少了fc段,免疫原性顯著降低,但仍存在很大的隱患。為了盡可能減少藥用抗體的免疫原性,研究者嘗試利各種抗體人源化技術對現有動物源抗體進行改造,但是人源化改造也面臨很大的困境,一方面不可能完全去除抗體的免疫原性,另一方面在抗體改造過程中,抗體空間構型可能發生改變,親和力往往會下降,很難達到預期的作用效果。因此,開發人源單鏈抗體,減少異源抗體的免疫原性,成為抗體研究的重點和難點。技術實現要素:為了解決現有技術的問題,本發明實施例提供了一種抗lox-1人源單鏈抗體及其制備方法和應用。所述技術方案如下:一方面,一種抗lox-1人源單鏈抗體,包括輕鏈和重鏈,所述抗體包含一組cdr:hcdr1、hcdr2、hcdr3、lcdr1、lcdr2和lcdr3;該組cdr與下述序列至少具有30%的同源性:hcdr1的氨基酸序列如seqidno.1所示;hcdr2的氨基酸序列如seqidno.2所示;hcdr3的氨基酸序列如seqidno.3所示;lcdr1的氨基酸序列如seqidno.4所示;lcdr2的氨基酸序列如seqidno.5所示;lcdr3的氨基酸序列如seqidno.6所示。進一步的,所述抗體的重鏈氨基酸序列如seqidno.7所示,所述抗體的輕鏈氨基酸序列如seqidno.8所示。進一步的,所述抗體的輕鏈可變區和重鏈可變區通過柔性序列連接,所述柔性序列的氨基酸序列如seqidno.9所示。進一步的,所述抗體c末端連接6個組氨酸序列,所述組氨酸序列如seqidno.10所示。另一方面,一種多核苷酸,所述多核苷酸能夠編碼上述抗lox-1人源單鏈抗體。具體的,所述多核苷酸序列如seqidno.11所示。再一方面,一種載體,含有上述多核苷酸。具體的,所述載體為pny-scfv質粒。再一方面,一種宿主細胞,所述宿主細胞含有上述的載體。具體的,所述宿主細胞為短小芽孢桿菌(brevibacilluschoshinensis)sp3。再一方面,上述抗lox-1人源單鏈抗體在制備治療心血管疾病藥物中的應用。再一方面,上述抗lox-1人源單鏈抗體的制備方法,包括以下步驟:以seqidno.11所示的序列為模板,通過pcr反應在所示序列的n端和c端分別接入末端酶切位點salⅰ和hindⅱ;然后連接到載體的多克隆位點,構筑得到表達載體;將表達載體轉化至宿主細胞中;挑選含有表達載體的宿主細胞陽性單菌落接種到mt液體培養基中,37℃振蕩培養過夜,次日按稀釋度1:100接種到tm培養液中,30℃、150rpm振蕩培養60小時;取上清液通過鎳柱親和層析得到回收液,回收液經過分子篩過濾分離,得到純化的抗lox-1人源單鏈抗體。本發明實施例提供的技術方案帶來的有益效果是:①提供了一種從人的外周血中獲得抗lox-1人源scfv的有效方法。②確定了在scfv的c末端加入組氨酸標簽的可行性。加入的6個組氨酸標簽不僅簡化了表達后的scfv純化方法,也確定了該標簽不影響scfv的親和力。這一成果為本發明的人源scfv在今后的融合載藥開發方面提供了有力支持。③本發明提供的scfv表達體系與方法,為以后該人源scfv的量產提供有力保障,是今后以lox-1為靶點的診斷試劑和基因工程抗體藥物開發和推廣的重要基礎。④本發明可為動脈粥樣硬化早期診斷試劑的開發,特別是靶向載藥材料及其治療藥物的開發提供了可以消除外源蛋白對人體免疫系統影響的理想材料。附圖說明為了更清楚地說明本發明實施例中的技術方案,下面將對實施例描述中所需要使用的附圖作簡單地介紹,顯而易見地,下面描述中的附圖僅僅是本發明的一些實施例,對于本領域普通技術人員來講,在不付出創造性勞動的前提下,還可以根據這些附圖獲得其他的附圖。圖1是從心血管病人外周血單核細胞提取的總rna結果的電泳圖;圖2是從cdna文庫中擴增出的vh-ch,vκ-cl和vλ-cl片段的電泳圖;圖3是通過重疊延伸pcr方法獲得的vh-vκ和vh-vλ片段的電泳圖;圖4是構筑的含有人源單鏈抗體片段的噬菌體質粒示意圖;圖5是多克隆噬菌體三輪淘篩的elisa結果圖;圖6是單克隆噬菌體篩選后10個陽性克隆的elisa結果圖;圖7是抗lox-1人源單鏈抗體的氨基酸序列及cdr區域圖;圖8是抗lox-1人源單鏈抗體表達載體pny-scfv的構建示意圖;圖9是抗lox-1人源單鏈抗體在短小芽孢桿菌中分泌表達的經時變化sds-page電泳圖;圖10是分泌表達的抗lox-1人源單鏈抗體純化過程的sds-page電泳圖;圖11是抗lox-1人源單鏈抗體和人源lox-1蛋白親和力測定結果圖。具體實施方式為使本發明的目的、技術方案和優點更加清楚,下面將結合附圖對本發明實施方式作進一步地詳細描述。實施例1:人源單鏈抗體(single-chainantibodyfragment/single-chainvariablefragment,scfv)噬菌體展示文庫的構建實驗材料:載體pcantab5e,菌株tg1均購自pharmacia公司。淋巴細胞分離液,hank’s液購自amresco公司。anti-m13antibody(hrp)購自abcam公司。高純質粒小量制備試劑盒,bsa和多功能dna純化回收試劑盒均購自bioteke。限制性內切酶sfiⅰ和notⅰ,t4dna連接酶,rtaq和lataq購自takara。qrt-pcr的m-mlv第一鏈合成系統試劑盒購自invitrogen,bstnⅰ購自neb公司。蛋白胨,酵母浸粉,瓊脂粉和蛋白胨購自安琪公司。氨芐青霉素,鹽酸硫胺素,iptg和卡那霉素購自北京鼎國昌生物技術有限責任公司。naco3,nahco3,kcl,na2hpo4,kh2po4,nh4cl,naoh,nacl和葡萄糖購自北京化工廠。hepes,tmb購自solarbio公司。血樣來自20名心腦血管疾病患者志愿者,由吉林大學中日聯誼醫院提供。建庫用引物見表1。表1建庫用引物序列表1中斜體堿基為sfiⅰ和notⅰ的酶切位點;帶有下劃線標注的堿基為linker(g4s)3的堿基序列。基本的分子生物學操作和使用的培養基及試劑等的配制,依據《分子生物學實驗技術手冊》執行。使用試劑盒的操作,按試劑盒使用說明執行。人外周血單核細胞(peripheralbloodmononuclearcell,pbmc)的分離按下述步驟實施:(1)將新鮮的抗凝血與等體積hank’s液均勻混合,再小心地加入已裝有淋巴細胞分離液的離心管中。(2)1500rpm離心15-20min。(3)用移液槍移取離心管中第二層的環狀乳白色單核細胞層。(4)采用血球計數板對單核細胞進行計數。(5)將單核細胞分裝后于-80℃冷凍保存。總rna從人外周血pmbc提取獲得,電泳檢查結果見圖1;電泳結果表明總rna提取質量良好,可以用于反轉錄合成cdna文庫。我們以oligo(dt)20為引物,利用rt-pcr試劑盒,以上述提取的總rna為模板,反轉錄為cdna,從而獲得cdna文庫。以合成的cdna文庫為模板,用表1中的引物,采用半巢式pcr方法擴增vh和vλ/vκ片段,結果見圖2,圖中m為dnamaker,1為vh-ch,2為vκ-cl,3為vλ-cl,結果顯示在大約700bp附近獲得了目的片段。隨后通過overlappingpcr,將vh和vλ/vκ片段分別組裝成scfv(vh-vλ/vκ),結果見圖3,圖中m為dnamaker,4為vh-vλ,5為vh-vκ,組裝后的scfv大小在750bp附近,且特性很好;至此,人源scfv文庫構建成功,為下一步利用噬菌體展示系統篩選特異性親和lox-1的scfv奠定了材料基礎。取噬菌體質粒pcantab5e,利用限制性內切酶位點將scfv片段連接到質粒中(如圖4所示),并通過電轉化方法將質粒pcantab5e-scfv導入tg1細胞中,從而建立人源scfv噬菌體展示文庫。進而對文庫的陽性率、多樣性和庫容量進行鑒定。構建的人源scfv噬菌體展示文庫的陽性率大于98%,多樣性為90%。采用梯度稀釋涂板計數文庫菌落,并結合文庫陽性率和多樣性結果計算得出單鏈抗體scfv(vh-vλ)和scfv(vh-vκ)噬菌體展示文庫的庫容量分別為2.7×1011和3.5×1011,噬菌體展示文庫的總容量為6.2×1011。實施例2:抗lox-1人源scfv淘篩抗lox-1人源scfv的淘篩采用免疫管淘篩法。淘篩操作按下述程序執行:一、輔助噬菌體m13ko7的制備(1)采用2×ty培養基在37℃,200rpm條件下培養tg1培養液至od600為0.4,分裝至1.5ml無菌離心管內,200μl/管。(2)將m13ko7逐級梯度稀釋至10-4、10-6、10-8、10-10和10-12倍。分別取10μl不同數量級的m13ko7侵染該200μltg1,37℃水浴靜止放置30min。將侵染完畢的200μltg1全部加入3ml溶解狀態的約42℃的瓊脂中,平鋪在預先溫浴好的2×ty平板上(不含抗生素),37℃培養過夜。(3)挑取一個小的噬菌斑于5ml處于對數中期的tg1菌液中,于37℃,200rpm條件下培養2h。(4)將培養好的tg1全部加入含有500ml2×yt的3l搖瓶中,37℃震蕩培養1h,然后加入卡那霉素使終濃度為50μg/ml,30℃震蕩過夜培養。(5)將過夜培養物10800g離心15min。將100ml含有2.5mnacl的10%peg加入400ml上清中,冰浴1h。(6)10800g離心30min,棄上清。(7)采用8mlpbs緩沖液重懸沉淀,并加入2mlnacl/peg混勻,冰浴20min。(8)10800g離心30min,棄上清。(9)5mlpbs緩沖液重懸沉淀,11600g離心10min徹底除去細菌殘片。(10)分裝m13ko7,200μl/管,并保存于4℃冰箱備用。長期保存的m13ko7加入10%甘油于-80℃保存。(11)輔助噬菌體滴度測定。將m13ko7逐級梯度稀釋至10-18、10-20、10-20、10-22倍。取梯度稀釋的噬菌體50μl加入1mltg1(od600為0.4)菌液,混勻后加入3ml融化的瓊脂(42℃)中,均勻平鋪于2×yt平板。(12)根據平板上的噬菌體斑數計算噬菌體滴度(cfu/ml)。二、重組噬菌粒的制備(1)向裝有20ml2×yt-ag培養基中加入scfv(vh-vλ/κ)噬菌體展示文庫甘油保存液,在37℃,250rpm條件下培養1h。(2)向文庫培養液中加入4×1010pfum13ko7,37℃水浴30min,分別取出10μl于90μl的2×yt-g培養基,混勻后涂布于2×yt-ag和2×yt-kg平板,用于鑒定感染效率。(3)37℃,250rpm培養30min。(4)1000g離心10min,小心去除上清。(5)將沉淀細胞用20ml2×yt-ak培養基(不含葡萄糖)重懸,于100ml搖瓶中,37℃、250rpm,過夜培養。(6)1000g離心20min。(7)轉移上清(含有重組噬菌粒)至50ml無菌離心管中。三、濃縮重組噬菌粒(1)向20ml重組噬菌粒中加入4mlnacl/peg,混勻冰浴放置1h。(2)10800g,4℃離心30min,徹底去除上清。(3)用4ml的pbs緩沖液重懸沉淀,并用0.45μm濾膜去除菌體以用于淘篩。四、免疫管淘篩法(1)取3.5ml緩沖液稀釋的50μglox-1ecd于免疫管,4℃過夜包被。(2)采用3.5ml的pbst震蕩洗滌免疫管3次,每次5min。(3)采用含有2%bsa的pbs溶液封閉免疫管,37℃放置2h。pbst震蕩洗滌免疫管3次,每次5min。(4)將重組噬菌粒與含有2%bsa的pbs溶液按體積比3:2進行混合,于室溫放置20min。(5)向封閉好的免疫管中加入混合重組噬菌粒3.5ml,37℃緩和震蕩孵育2h。(6)去除免疫管中的重組噬菌粒,并采用3.5ml的pbst震蕩洗滌免疫管3次,每次5min。(7)向免疫管中加入4ml新鮮宿主菌tg1(od600為0.5)。37℃、150rpm震蕩培養1h。(8)取震蕩培養的菌液10μl按照“一、輔助噬菌體m13ko7的制備”的方法確定淘篩輸出的噬菌體量。(9)將剩余的菌液全部轉移至50ml離心管中,加入終濃度為100μg/ml的氨芐青霉素和4×1010pfu的m13ko7。(10)37℃水浴靜置30min后,于37℃、250rpm震蕩培養30min。(11)1000g離心10min,小心去除上清。(12)將沉淀細胞用20ml2×yt-ak培養基(不含葡萄糖)重懸于50ml搖瓶中,于37℃、250rpm條件下過夜培養。(13)1000g離心20min。(14)轉移上清約20ml(含有重組噬菌體)至50ml無菌離心管中。(15)按“三、濃縮重組噬菌粒”的方法濃縮噬菌體,用于下一輪陶篩。五、多克隆phageelisa(1)包被,每孔包被2μglox-1ecd蛋白,100μl/孔,包被條件為4℃過夜。采用bsa作為陰性對照孔。(2)洗滌,pbst震蕩洗滌3次,每次5min。(3)封閉,每孔加入100μl含有2%bsa的pbs溶液,37℃封閉2h。(4)洗滌,pbst震蕩洗滌3次,每次5min。(5)加樣,取100μl重組噬菌體加入抗原包被孔,37℃反應2h。(6)洗滌,pbst震蕩洗滌3次,每次5min。(7)采用2%bsa的pbs緩沖液以1:5000稀釋anti-m13antibody(hrp),每孔加入100μl,37℃孵育1h。(8)洗滌,pbst震蕩洗滌3次,每次5min。(9)顯色,每孔加入100μltmb顯色液,37℃反應30min。(10)終止反應,采用2mh2so4終止反應5min。(11)采用酶標儀測定a450吸光度值。每個樣品作兩2個平行,取平均值。六、單克隆phageelisa(1)包被,每孔包被2μglox-1ecd蛋白,100μl/孔,包被條件為4℃過夜。采用bsa作為陰性對照孔。(2)洗滌,pbst震蕩洗滌3次,每次5min。(3)封閉,每孔加入100μl含有2%bsa的pbs溶液,37℃封閉2h。(4)洗滌,pbst震蕩洗滌3次,每次5min。(5)加樣,取100μl單克隆濃縮重組噬菌體加入抗原包被孔,37℃反應2h。(6)洗滌,pbst震蕩洗滌3次,每次5min。(7)采用2%bsa的pbs緩沖液以1:5000稀釋anti-m13antibody(hrp),每孔加入100μl,37℃孵育1h。(8)洗滌,pbst震蕩洗滌3次,每次5min。(9)顯色,每孔加入100μltmb顯色液,37℃反應30min。(10)終止反應,采用2mh2so4終止反應5min。(11)酶標儀測定a450吸光度值。a450值與陰性對照孔比值大于2.0的為陽性樣品,每個樣品作兩2個平行,取平均值。通過三輪淘篩后,特異性噬菌體一共被成功富集142.5倍。多克隆phageelisa結果(圖5)表明,在第二輪陶篩中,已經有了大幅度的提高,在第三輪淘篩后,信號值提高幅度較小。經過三輪淘篩后使lox-1特異性結合的scfv得到充分富集。從淘篩富集后的文庫中挑取1000個單克隆,并分別制備每個單克隆的重組噬菌體,再進行單克隆phageelisa鑒定。s/n值大于2的陽性克隆共200個,典型的10個陽性克隆結果見圖6,10個陽性克隆中有7個與lox-1蛋白親和力較強,其中以39號親和力最高。實施例3:抗lox-1人源scfv分子鑒定及功能區分析從200個陽性克隆中選取與lox-1親和活性顯著高的7株單克隆,提取制粒,將質粒委托華大基因公司測序,測序后的結果,利用(http://www.imgt.org)的imgt軟件對scfv序列進行分析,確定scfv序列是否具有人源vh和vl區序列的基因特征。并確定scfv的cdr和fr序列區域。此外,分別采用expasy網站的sopma工具、genetyx軟件對scfv的結構特征、物理性質進行預測。圖7是本發明的抗lox-1人源scfv氨基酸序列及相關功能圖。抗lox-1人源scfv含有的如下的結合片段,包含一組cdr:hcdr1、hcdr2、hcdr3、lcdr1、lcdr2和lcdr3,氨基酸序列如下:hcdr1的氨基酸序列如seqidno.1;hcdr2的氨基酸序列如seqidno.2;hcdr3的氨基酸序列如seqidno.3;lcdr1的氨基酸序列如seqidno.4;lcdr2的氨基酸序列如seqidno.5;lcdr3的氨基酸序列如seqidno.6。圖7中抗lox-1人源scfv由768個核苷酸編碼而成,如seqidno.11所示。實施例4:抗lox-1人源scfv的原核表達及純化本發明的抗lox-1人源scfv的編碼核苷酸序列(見序列表中的seqidno.11所示),以該序列為模板,通過pcr反應在n端和c端分別接入末端酶切位點salⅰ和hindⅱ;之后連接到表達載體pny326的多克隆位點中,見附圖8,構筑好的質粒被命名為pny-scfv;接下來將pny-scfv電轉化至宿主短小芽孢桿菌sp3(brevibacilluschoshinensissp3)中。挑選含有pny-scfv重組質粒的brevibacilluschoshinensissp3陽性單菌落接種到mt液體培養基中,37℃振蕩培養過夜,次日按稀釋度1:100接種到tm培養液中,30℃、150rpm振蕩培養96小時。每隔12小時取培養液,進行sds-page電泳,經過染色、脫色,發現brevibacilluschoshinensissp3的表達產物在約30kda處有明顯的條帶,與預期的目的蛋白帶大小一致,表明抗lox-1人源scfv基因獲得了表達,見圖9。在tm培養基中,30℃振蕩培養60小時,目的蛋白達到較大表達量。抗lox-1人源scfv基因在brevibacilluschoshinensissp3宿主菌中表達主要以可溶的形式存在上清液中。為方便表達,在抗lox-1人源scfv的c末端加上了6個組氨酸標簽,表達后的蛋白可以通過鎳柱親和層析得到回收,在經過分子篩過濾分離,可以得到純化的抗lox-1人源scfv蛋白。圖10是重組的抗lox-1人源scfv經兩步法純化的結果。sds-page可以看到經分子篩純化后的蛋白為單一條帶,說明經親和層析和分子篩層析純化后,能夠得到較高純度的目的抗lox-1人源scfv蛋白。實施例5:抗lox-1人源scfv的鑒定采用生物分子相互作用系統(bio-layerinterferometry,bli)測定抗lox-1人源scfv片段與抗原lox-1的親和活性。整個實驗在octetred96(fortebio)操作系統下進行,溫度設定在30℃。將人源lox-1蛋白(sinobiologicalinc.)溶于pbs緩沖液中,用生物素化試劑盒ezlinksulfo-nhs-biotin(pierce)進行生物塑化;生物塑化的lox-1蛋白與鏈霉親和素傳感器(sasensor)于pbs緩沖液中進行孵育600秒;結合有lox-1的sasensor移至pbs緩沖液中平衡60秒;然后移至含有不同濃度抗體(分別為400,200,100,50,25nmol/l)的pbs溶液中,使sasensor上的抗原lox-1與抗體孵育結合600秒;將上述反應后的sasensor移至pbs溶液中,進行解離600秒;結果使用軟件dataanalysis7.0進行數據分析。bli測定圖譜見圖11,隨著scfv濃度的增加,納米位移深度增加;在解離過程中,scfv濃度大于200nmol/l時,解離度有所增強。通過該圖譜利用軟件dataanalysis7.0分析得表2的動力學參數,其中kno為結合動力學常數;kdis為解離動力學常數,kd為解離平衡常數(kd=kdis/kno)。kd是scfv同lox-1親和力的表征參數,其數值越小,說明scfv與lox-1的親和力越強。表2中的結果表明,本發明的人源抗lox-1scfv的kd為6.69×10-9,是一個特異性較強的抗lox-1人源scfv。表2基于bli的抗lox-1人源scfv動力學參數kd(m)kno(1/ms)kdis(1/s)6.69e-096.98e+034.67e-05本發明提供了一種從人的外周血中獲得抗lox-1人源scfv的有效方法。確定了在scfv的c末端加入組氨酸標簽的可行性。加入的6個組氨酸標簽不僅簡化了表達后的scfv純化方法,也確定了該標簽不影響scfv的親和力。這一成果為本發明的人源scfv在今后的融合載藥開發方面提供了有力支持。本發明提供的scfv表達體系與方法,為以后該人源scfv的量產提供有力保障,是今后以lox-1為靶點的診斷試劑和基因工程抗體藥物開發和推廣的重要基礎。本發明可為動脈粥樣硬化早期診斷試劑的開發,特別是靶向載藥材料及其治療藥物的開發提供了可以消除外源蛋白對人體免疫系統影響的理想材料。上述本發明實施例序號僅僅為了描述,不代表實施例的優劣。以上所描述的系統實施例僅僅是示意性的,其中所述作為分離部件說明的單元可以是或者也可以不是物理上分開的,作為單元顯示的部件可以是或者也可以不是物理單元,即可以位于一個地方,或者也可以分布到多個網絡單元上。可以根據實際的需要選擇其中的部分或者全部模塊來實現本實施例方案的目的。本領域普通技術人員在不付出創造性的勞動的情況下,即可以理解并實施。以上所述僅為本發明的較佳實施例,并不用以限制本發明,凡在本發明的精神和原則之內,所作的任何修改、等同替換、改進等,均應包含在本發明的保護范圍之內。當前第1頁12
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1