一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的化學(xué)發(fā)光試劑盒及其制備方法、檢測(cè)方法、評(píng)價(jià)方法與流程
本發(fā)明涉及免疫分析技術(shù)領(lǐng)域,具體涉及到一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的化學(xué)發(fā)光試劑盒及其制備方法、檢測(cè)方法、評(píng)價(jià)方法。
背景技術(shù):
結(jié)核病在全世界仍為危害人類健康和生命的主要傳染病之一。目前全世界結(jié)核病患者約有2000萬(wàn)人,每年新增結(jié)核病患者800萬(wàn)人左右,每年因結(jié)核病死亡人數(shù)約300萬(wàn)人。我國(guó)僅次于印度,位居世界第二。通過(guò)近幾年的流行病學(xué)抽樣調(diào)查初步結(jié)果表明,我國(guó)約5億人口感染結(jié)核分枝桿菌,現(xiàn)有結(jié)核病人約500萬(wàn)人,每年約10萬(wàn)人死亡于結(jié)核病,在我國(guó)傳染病中位居第一。面對(duì)如此嚴(yán)峻的形勢(shì),結(jié)核病的預(yù)防和控制已經(jīng)引起國(guó)內(nèi)外政府和學(xué)者的高度重視。因此結(jié)核病的早期診斷和治療對(duì)結(jié)核病控制尤為重要。
機(jī)體對(duì)結(jié)核分枝桿菌的免疫應(yīng)答主要體現(xiàn)為細(xì)胞免疫。因此對(duì)于結(jié)核分枝桿菌的檢測(cè)只有通過(guò)對(duì)細(xì)胞免疫應(yīng)答進(jìn)行,近年來(lái),一種用于診斷結(jié)核分枝桿菌的新方法進(jìn)入人們視線,其利用特異性刺激蛋白對(duì)已感染結(jié)核桿菌的細(xì)胞進(jìn)行刺激培養(yǎng),機(jī)體細(xì)胞會(huì)分泌大量的r干擾素,利用免疫手段對(duì)分泌的特異性的r干擾素進(jìn)行檢測(cè),間接的體現(xiàn)機(jī)體細(xì)胞的結(jié)核分枝桿菌的受感染情況,該檢測(cè)原理被稱為r干擾素釋放試驗(yàn)(IGRA)技術(shù)。
在該檢測(cè)原理基礎(chǔ)上衍生出了多種檢測(cè)方法學(xué),目前市場(chǎng)上所擁有的包括酶聯(lián)免疫斑點(diǎn)(ELISPOT)法、酶聯(lián)免疫(ELISA)法。ELISPOT檢測(cè)的檢測(cè)靈敏度較高,但因該檢測(cè)方法在抽取病人血樣后需要做淋巴細(xì)胞分離計(jì)數(shù)后再進(jìn)行后期的刺激培養(yǎng)過(guò)夜及免疫檢測(cè)程序,操作復(fù)雜,專業(yè)門檻較高,大大限制了檢測(cè)通量,另外因其涉及的配套設(shè)備和試劑較多,也大大增加了檢測(cè)成本及操作過(guò)程中的錯(cuò)誤率發(fā)生。ELISA檢測(cè)因使用全血培養(yǎng),節(jié)省了較多操作時(shí)間,在檢測(cè)通量上也彌補(bǔ)了ELISPOT的缺陷,但因?yàn)闄z測(cè)方法學(xué)的限制,其檢測(cè)靈敏度較低,對(duì)于低免疫力或淋巴細(xì)胞數(shù)量偏低的人群,其檢測(cè)結(jié)果的不確定性較高,無(wú)法做到精確的診斷,且因其檢測(cè)低靈敏度的原因,所需檢測(cè)血樣量也較高,需要不低于每個(gè)培養(yǎng)管1ml的血量。
技術(shù)實(shí)現(xiàn)要素:
為了解決上述不足的缺陷,本發(fā)明提供了一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的化學(xué)發(fā)光試劑盒及其制備方法、檢測(cè)方法、評(píng)價(jià)方法,可以實(shí)現(xiàn)檢測(cè)靈敏度高、特異性好、操作簡(jiǎn)便,檢測(cè)通量高,檢測(cè)成本低,檢測(cè)樣本量少且不需要太多復(fù)雜的輔助設(shè)備。
本發(fā)明提供了一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的試劑盒,包括血樣刺激系統(tǒng)和免疫檢測(cè)系統(tǒng),所述血樣刺激系統(tǒng)包括培養(yǎng)管、血樣刺激用對(duì)照品、結(jié)核特異性刺激蛋白;所述免疫檢測(cè)系統(tǒng)包括包被有r干擾素克隆抗體的化學(xué)發(fā)光板、生物素標(biāo)記的r干擾素克隆抗體、鏈霉親和素標(biāo)記的酶底物和酶促發(fā)光底物。
上述的試劑盒,其中,所述血樣刺激用對(duì)照品包括血樣刺激用陰性對(duì)照品和血樣刺激用陽(yáng)性對(duì)照品;所述包被有r干擾素克隆抗體的化學(xué)發(fā)光板包括包被有r干擾素單克隆抗體或r干擾素多克隆抗體的化學(xué)發(fā)光板;所述生物素標(biāo)記的r干擾素克隆抗體包括生物素標(biāo)記的r干擾素單克隆抗體或r干擾素多克隆抗體;所述鏈霉親和素標(biāo)記的酶底物包括辣根過(guò)氧化物酶或堿性磷酸酶。
上述的試劑盒,其中,所述血樣刺激用陰性對(duì)照品中包括AIM-V培養(yǎng)液。
上述的試劑盒,其中,所述結(jié)核特異性刺激蛋白包括AIM-V培養(yǎng)液和結(jié)核分枝桿菌特異性刺激蛋白ESAT6和CFP10的獨(dú)立蛋白混合或ESAT6和CFP10融合蛋白。
上述的試劑盒,其中,所述血樣刺激用陽(yáng)性對(duì)照品中包括AIM-V培養(yǎng)液、磷酸鹽緩沖液、植物血凝素或CD3細(xì)胞因子。
上述的試劑盒,其中,所述生物素標(biāo)記的r干擾素單克隆抗體或r干擾素多克隆抗體的緩沖液為磷酸鹽緩沖液和蛋白保護(hù)劑。
上述的試劑盒,其中,所述鏈霉親和素標(biāo)記的辣根過(guò)氧化物酶或堿性磷酸酶的緩沖液為磷酸鹽緩沖液和蛋白保護(hù)劑。
同時(shí)在另一種實(shí)施例中,本發(fā)明還提供了一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的試劑盒的制備方法,包括以下步驟:
r干擾素單克隆抗體或多克隆抗體包被化學(xué)發(fā)光板的制備;
生物素標(biāo)記的r干擾素單克隆抗體或r干擾素多克隆抗體及工作夜的制備;
鏈霉親和素標(biāo)記的辣根過(guò)氧化物酶或堿性磷酸酶及工作液的制備;
校準(zhǔn)品的制備;
洗滌液的制備。
本發(fā)明的另一面,本發(fā)明還提供了一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的試劑盒的檢測(cè)方法,包括以下步驟:
血樣培養(yǎng);
r干擾素檢測(cè)。
本發(fā)明的再一面,本發(fā)明還提供了一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的試劑盒的評(píng)價(jià)方法,包括以下步驟:
根據(jù)試劑盒的檢測(cè)結(jié)果繪制標(biāo)準(zhǔn)曲線;
根據(jù)上述的標(biāo)準(zhǔn)曲線計(jì)算最低檢出限和精密性值;
根據(jù)上述最低檢出限和精密性值來(lái)判定檢測(cè)樣本的陰陽(yáng)性。
本發(fā)明具有以下優(yōu)點(diǎn):采用酶促化學(xué)發(fā)光法,將r干擾素單克隆抗體或r干擾素多克隆抗體包被于化學(xué)發(fā)光板中,利用酶促催化發(fā)光底物,并利用生物素放大系統(tǒng),提高了試劑盒的靈敏度和準(zhǔn)確性;同時(shí)對(duì)于樣本使用量為3.0ml以下;實(shí)驗(yàn)證明,化學(xué)發(fā)光法配合生物素放大系統(tǒng)是一種檢測(cè)r干擾素的有效方法,且進(jìn)一步證明了對(duì)3.0ml以下的血樣量的檢測(cè)結(jié)果也有效的符合于臨床評(píng)判。
具體優(yōu)點(diǎn)包括:
1、化學(xué)發(fā)光法配合生物素放大系統(tǒng)檢測(cè)系統(tǒng),對(duì)于T淋巴細(xì)胞偏少的樣本的檢測(cè)結(jié)果與市面上ELISA試劑盒做了比對(duì),本發(fā)明試劑盒的檢測(cè)靈敏度明顯高于ELISA試劑盒,能夠?qū)LISA檢測(cè)結(jié)果不確定的樣本,做出很好的結(jié)果判斷;
2、本發(fā)明試劑盒在血樣處理上,沒(méi)有T淋巴細(xì)胞分離過(guò)程,為全血直接培養(yǎng),在此操作上與市面上的ELISPOT試劑盒比較,減少了操作程序,避免了更多的操作失誤,也節(jié)省了更多的操作時(shí)間,降低了操作所需試劑耗材的成本損耗;且因本發(fā)明試劑盒無(wú)需做太多血樣處理,操作簡(jiǎn)便,對(duì)于所需設(shè)備也無(wú)很高要求,可實(shí)現(xiàn)大通量檢測(cè),免疫診斷部分可實(shí)現(xiàn)半自動(dòng)化或全自動(dòng)化批量操作。
3、目前市場(chǎng)上的ELISA試劑盒所需樣本量為3ml以上;ELISPOT試劑盒所需樣本量為5ml以上,對(duì)于低免疫人群的樣本量需求更高,甚至達(dá)到8-10ml,本發(fā)明試劑盒對(duì)于血樣樣本量的最高要求僅為3.0ml,大大減少了病人的血樣抽取量。
附圖說(shuō)明
通過(guò)閱讀參照以下附圖對(duì)非限制性實(shí)施例所作的詳細(xì)描述,本發(fā)明及其特征、外形和優(yōu)點(diǎn)將會(huì)變得更明顯。在全部附圖中相同的標(biāo)記指示相同的部分。并未刻意按照比例繪制附圖,重點(diǎn)在于示出本發(fā)明的主旨。
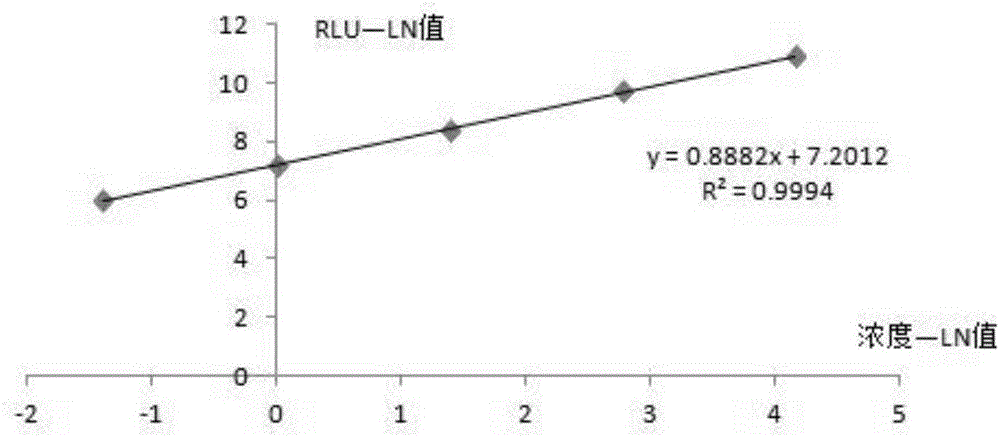
圖1為本發(fā)明提供的化學(xué)發(fā)光檢測(cè)試劑盒的標(biāo)準(zhǔn)曲線。
具體實(shí)施方式
在下文的描述中,給出了大量具體的細(xì)節(jié)以便提供對(duì)本發(fā)明更為徹底的理解。然而,對(duì)于本領(lǐng)域技術(shù)人員而言顯而易見(jiàn)的是,本發(fā)明可以無(wú)需一個(gè)或多個(gè)這些細(xì)節(jié)而得以實(shí)施。在其他的例子中,為了避免與本發(fā)明發(fā)生混淆,對(duì)于本領(lǐng)域公知的一些技術(shù)特征未進(jìn)行描述。
為了徹底理解本發(fā)明,將在下列的描述中提出詳細(xì)的步驟以及詳細(xì)的結(jié)構(gòu),以便闡釋本發(fā)明的技術(shù)方案。本發(fā)明的較佳實(shí)施例詳細(xì)描述如下,然而除了這些詳細(xì)描述外,本發(fā)明還可以具有其他實(shí)施方式。
本發(fā)明提供了一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的試劑盒,包括血樣刺激系統(tǒng)和免疫檢測(cè)系統(tǒng),所述血樣刺激系統(tǒng)包括培養(yǎng)管、血樣刺激用對(duì)照品、結(jié)核特異性刺激蛋白;所述免疫檢測(cè)系統(tǒng)包括包被有r干擾素克隆抗體的化學(xué)發(fā)光板、生物素標(biāo)記的r干擾素克隆抗體、鏈霉親和素標(biāo)記的酶底物和酶促發(fā)光底物。其中培養(yǎng)管中血樣需求量在1.0ml及以下,也即每個(gè)檢測(cè)樣本量所需樣本量在3ml以下,目前市場(chǎng)上的ELISA試劑盒所需樣本量為3ml以上;ELISPOT試劑盒所需樣本量為5ml以上,對(duì)于低免疫人群的樣本量需求更高,甚至達(dá)到8-10ml,本發(fā)明試劑盒對(duì)于血樣樣本量的最高要求僅為3.0ml,大大減少了病人的血樣抽取量。
在本發(fā)明一優(yōu)選但非限制的實(shí)施例中,血樣刺激用對(duì)照品包括血樣刺激用陰性對(duì)照品和血樣刺激用陽(yáng)性對(duì)照品;包被有r干擾素克隆抗體的化學(xué)發(fā)光板包括包被有r干擾素單克隆抗體或r干擾素多克隆抗體的化學(xué)發(fā)光板,進(jìn)一步,包被于化學(xué)發(fā)光板中的r干擾素單克隆抗體或r干擾素多克隆抗體的濃度在于1~3ug/ml;生物素標(biāo)記的r干擾素克隆抗體包括生物素標(biāo)記的r干擾素單克隆抗體或r干擾素多克隆抗體;鏈霉親和素標(biāo)記的酶底物包括辣根過(guò)氧化物酶或堿性磷酸酶。其中鏈霉親和素標(biāo)記的酶底物并不限于辣根過(guò)氧化物酶或堿性磷酸酶,進(jìn)一步,辣根過(guò)氧化物酶為辣根過(guò)氧化氫酶。
在本發(fā)明一優(yōu)選但非限制的實(shí)施例中,血樣刺激用陰性對(duì)照品中包括AIM-V培養(yǎng)液。
在本發(fā)明一優(yōu)選但非限制的實(shí)施例中,結(jié)核特異性刺激蛋白包括AIM-V培養(yǎng)液和結(jié)核分枝桿菌特異性刺激蛋白ESAT6和CFP10的獨(dú)立蛋白混合或ESAT6和CFP10融合蛋白。
在本發(fā)明一優(yōu)選但非限制的實(shí)施例中,血樣刺激用陽(yáng)性對(duì)照品中包括AIM-V培養(yǎng)液、磷酸鹽緩沖液、植物血凝素或CD3細(xì)胞因子。
在本發(fā)明一優(yōu)選但非限制的實(shí)施例中,生物素標(biāo)記的r干擾素單克隆抗體或r干擾素多克隆抗體的緩沖液為磷酸鹽緩沖液和蛋白保護(hù)劑。
在本發(fā)明一優(yōu)選但非限制的實(shí)施例中,鏈霉親和素標(biāo)記的辣根過(guò)氧化物酶或堿性磷酸酶的緩沖液為磷酸鹽緩沖液和蛋白保護(hù)劑,其中保護(hù)蛋白劑可以為酪蛋白、牛血清白蛋白、明膠、動(dòng)物血清或人血清。
在本發(fā)明一優(yōu)選但非限制的實(shí)施例中,酶促發(fā)光底物為辣根過(guò)氧化物酶、堿性磷酸酶的酶促發(fā)光底物。
在本發(fā)明一優(yōu)選但非限制的實(shí)施例中,試劑盒中還包含r干擾素校準(zhǔn)品。本發(fā)明的另一面,一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的試劑盒的制備方法,包括以下步驟:
步驟S1:r干擾素單克隆抗體或多克隆抗體包被化學(xué)發(fā)光板的制備,具體包括,利用磷酸鹽緩沖液或碳酸鹽緩沖液將r干擾素單克隆抗體或多克隆抗體稀釋至1~3ug/ml,按照100ul/孔加入化學(xué)發(fā)光板中,并于4℃放置16~20小時(shí)后,取出化學(xué)發(fā)光板,甩干殘液,利用如牛血清白蛋白、酪蛋白、明膠、動(dòng)物或人血清等進(jìn)行封閉處理,按照120ul~200ul/孔加樣,37℃放置2小時(shí)或4℃放置16~20小時(shí),甩干殘液,干燥保存于4℃?zhèn)溆谩?/p>
步驟S2:生物素標(biāo)記的r干擾素單克隆抗體或r干擾素多克隆抗體及工作夜的制備,具體包括步驟S2a:生物素標(biāo)記的r干擾素單克隆抗體或r干擾素多克隆抗體制備,具體為利用0.1M PBS pH7.2配制10mM NHS-DPEG4-Biotin工作溶液。將r干擾素單克隆抗體或多克隆抗體加入適量的10mM NHS-DPEG4-Biotin工作溶液中,于室溫反應(yīng)1小時(shí),利用葡聚糖凝膠分離純化,去除游離生物素,加入0.1%BSA,放置4℃?zhèn)溆茫徊襟ES2b:生物素標(biāo)記的r干擾素單克隆抗體或r干擾素多克隆抗體工作液的制備,具體包括:稀釋液的制備:0.01M PB緩沖液(pH7.4),1%酪蛋白或1%BSA,0.1%proclin300;工作液的制備:用稀釋液稀釋生物素標(biāo)記好的r干擾素單克隆抗體或r干擾素多克隆抗體后得到生物素標(biāo)記的r干擾素單克隆抗體或r干擾素多克隆抗體工作液,其稀釋比例在1:500~1:5000,優(yōu)選比例比例為1:1000。
步驟S3:鏈霉親和素標(biāo)記的辣根過(guò)氧化物酶或堿性磷酸酶及工作液的制備,具體包括步驟S3a:鏈霉親和素標(biāo)記的辣根過(guò)氧化物酶或堿性磷酸酶的制備,其中包括采用戊二醇法,將辣根過(guò)氧化物酶或堿性磷酸酶配置成50IU/ml,取適量,加入含1.25%戊二醛的pH6.8的PBS溶液中,混勻至室溫下反應(yīng)過(guò)夜。收集反應(yīng)液,利用PBS(pH7.2)透析4次,取適量SA溶于1mol/L碳酸鹽緩沖液(pH9.5)中,與透析后的反應(yīng)液混勻,于4℃反應(yīng),并加入適量0.2mol/L賴氨酸溶液。混勻,室溫反應(yīng)2小時(shí),利用0.05mol/L PBS(pH7.2)透析4次。離心取上清液,至4℃?zhèn)溆谩2襟ES3b:鏈霉親和素標(biāo)記的辣根過(guò)氧化物酶或堿性磷酸酶工作液的制備,其中包括,稀釋液的制備:0.1M TB緩沖液(pH7.4),1%酪蛋白或1%BSA,0.1%proclin300;工作液的制備:用稀釋液稀釋鏈霉親和素標(biāo)記的辣根過(guò)氧化物酶或堿性磷酸酶后得到鏈霉親和素標(biāo)記的辣根過(guò)氧化物酶工作液或鏈霉親和素標(biāo)記的堿性磷酸酶工作液,其稀釋比例在1:500~1:5000,優(yōu)選稀釋比例為1:1000。
步驟S4:校準(zhǔn)品的制備,具體包括:r干擾素校準(zhǔn)品抗原為基因重組的濃度≥95%的人r干擾素蛋白或國(guó)際(WHO/NIBSC)和國(guó)家中檢院提供的人r干擾素標(biāo)準(zhǔn)品物質(zhì),本發(fā)明試劑盒中涉及的r干擾素校準(zhǔn)品的稀釋液為AIM-V或含1%BSA的PB緩沖液,內(nèi)含0.1%proclin300。稀釋濃度梯度為:0IU/ml、0.25IU/ml、1.0IU/ml、4.0IU/ml、16.0IU/ml、64.0IU/ml,用于制作檢測(cè)標(biāo)準(zhǔn)曲線,制作的標(biāo)注曲線如圖1所示的其中一種實(shí)施例。
步驟S5:洗滌液的制備,具體包括:洗滌液為0.01M PBST溶液,配制1L的洗滌液:二水磷酸二氫鈉9.75g、十二水磷酸氫二鈉51g、氯化鈉155g、Tween20 10ml,內(nèi)含0.1%proclin300,使用時(shí)利用超純水20倍稀釋。
本發(fā)明的還提供了一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的試劑盒的檢測(cè)方法,具體包括以下步驟:
步驟a:血樣培養(yǎng),具體包括,肝素抗凝血樣管抽取血樣3.0ml量;在血樣離體6-8小時(shí)內(nèi),按照1.0ml/管血樣分別加入陰性對(duì)照培養(yǎng)管、特異性刺激培養(yǎng)管、陽(yáng)性對(duì)照培養(yǎng)管;血樣管上下顛倒8-10次或5秒時(shí)間,使血樣與培養(yǎng)管中的物質(zhì)充分混勻,此階段若產(chǎn)生氣泡對(duì)后續(xù)檢測(cè)無(wú)影響;將血樣培養(yǎng)管豎直放置37℃培養(yǎng)箱中,孵育20~24小時(shí)。
步驟b:r干擾素檢測(cè)階段,具體包括20倍稀釋濃縮洗滌液至工作濃度;按照稀釋梯度進(jìn)行標(biāo)準(zhǔn)品濃度稀釋,并加入化學(xué)發(fā)光板中,50ul/孔,做好標(biāo)示;取出培養(yǎng)管,抽取上清液作為檢測(cè)樣本;也可離心機(jī)離心獲取上清液;按照50ul/孔加入對(duì)應(yīng)板孔,做好標(biāo)示;取生物素標(biāo)記的r干擾素抗體工作液,按照50ul/孔加入對(duì)應(yīng)板孔;37℃孵育2h,取出,每孔200ul洗滌液,洗滌4次,拍干;取鏈霉親和素標(biāo)記的過(guò)氧化物酶工作液或鏈霉親和素標(biāo)記的堿性磷酸酶工作液,按照50ul/孔加入對(duì)應(yīng)反應(yīng)孔;50ul/孔,放置37℃反應(yīng)30min取出發(fā)光板,每孔200ul洗滌液,洗滌4次,拍干;每孔加入50ul酶發(fā)光底物,讀取發(fā)光值;分別取校準(zhǔn)品梯度的濃度值和發(fā)光值的對(duì)數(shù)值,制作標(biāo)準(zhǔn)曲線,獲得曲線方程;將待測(cè)樣本的發(fā)光值取對(duì)數(shù)值代入,計(jì)算出待測(cè)樣本濃度值的對(duì)數(shù)值,取指數(shù),即為待測(cè)樣本的濃度值。
本發(fā)明還提供了一種定量檢測(cè)結(jié)核分枝桿菌r干擾素的試劑盒的評(píng)價(jià)方法,具體包括步驟(1):根據(jù)試劑盒的檢測(cè)結(jié)果繪制標(biāo)準(zhǔn)曲線,具體為本發(fā)明試劑盒用校準(zhǔn)品濃度(0IU/ml剔除,該值作為反應(yīng)板本底考慮,不計(jì)入標(biāo)準(zhǔn)曲線范圍內(nèi))的ln值作為X值,對(duì)應(yīng)濃度檢測(cè)的發(fā)光值RLU分別取對(duì)數(shù)做Y值,以此做一元一次方程。如圖1所示,所繪制的標(biāo)準(zhǔn)曲線回歸方程為y=0.8882x+7.2012,R2=0.9994。
步驟(2):根據(jù)上述的標(biāo)準(zhǔn)曲線計(jì)算最低檢出限和精密性值,具體包括本發(fā)明試劑盒在檢測(cè)標(biāo)準(zhǔn)曲線的同時(shí)檢測(cè)最低檢出限參考品(0.1IU/ml)10次,并通過(guò)標(biāo)準(zhǔn)曲線計(jì)算最低檢出限參考品的平均濃度值(x)和標(biāo)準(zhǔn)差(SD)。根據(jù)公式:檢出限=X+2SD,計(jì)算樣品的最低檢出限,結(jié)果如表1,本發(fā)明試劑盒對(duì)血樣檢測(cè)IFN-r的最低檢出限為0.139IU/ml<0.15IU/ml,如表1所示為IFN-r化學(xué)發(fā)光檢測(cè)試劑盒的最低檢出限。同上述最低檢出限的檢測(cè)結(jié)果,本發(fā)明試劑盒利用標(biāo)準(zhǔn)差(SD)/平均濃度值(x)所獲得的比值即為精密性值,即:標(biāo)準(zhǔn)差0.010IU/ml除以平均濃度值0.092IU/ml,乘以100%,為11.11%<15%。
表1 IFN-r化學(xué)發(fā)光檢測(cè)試劑盒的最低檢出限
步驟(3):根據(jù)上述最低檢出限和精密性值來(lái)判定檢測(cè)樣本的陰陽(yáng)性,具體包括,篩選20例新鮮血樣,10例明確結(jié)核感染陽(yáng)性患者,10例明確結(jié)核感染陰性樣本。利用本發(fā)明試劑盒進(jìn)行血樣培養(yǎng)及免疫反應(yīng)檢測(cè)。對(duì)血樣進(jìn)行編號(hào):10例陰性樣本N1~N10;10例陽(yáng)性樣本P1~P10對(duì)標(biāo)準(zhǔn)曲線濃度值及發(fā)光值分別取對(duì)數(shù),擬合標(biāo)準(zhǔn)曲線,同時(shí)將樣本檢測(cè)發(fā)光值取對(duì)數(shù)值,帶入方程式中Y值,計(jì)算出X值,并取X值的指數(shù)值,即為對(duì)應(yīng)樣本發(fā)光值的濃度值。對(duì)該些濃度值進(jìn)行數(shù)據(jù)分析,判定該檢測(cè)樣本的陰陽(yáng)性。其中陰陽(yáng)性結(jié)果判定依據(jù)如下所示:
1.當(dāng)陰性培養(yǎng)管濃度≤8IU/ml:
1.1.T-N<0.35IU/ml,P-N≥0.5IU/ml,結(jié)果為陰性;
1.2.T-N≥0.35IU/ml且<N/4,P-N≥0.5IU/ml,結(jié)果為陰性;
1.3.T-N≥0.35IU/ml且≥N/4,結(jié)果為陽(yáng)性;
1.4.T-N<0.35IU/ml且P-N<0.5IU/ml,結(jié)果為不確定;
1.5.T-N≥0.35IU/ml且<N/4,P-N<0.5IU/ml,結(jié)果為不確定;
2.當(dāng)陰性培養(yǎng)管濃度>8IU/ml:
任何檢測(cè)值都判為不確定性。
使用本發(fā)明的試劑盒檢測(cè)的結(jié)果如表2所示:
表2 IFN-r化學(xué)發(fā)光試劑盒檢測(cè)10例陰性血樣、10例陽(yáng)性血樣的結(jié)果
從表2可以看出,采用本發(fā)明試劑盒檢測(cè)r干擾素與目前市面上所擁有的ELISPOT方法學(xué)檢測(cè)試劑盒以及ELISA檢測(cè)試劑盒相比較,具有操作簡(jiǎn)便、操作靈敏度高、特異性好、檢測(cè)成本低、樣本使用量少,對(duì)于設(shè)備的要求低等的優(yōu)點(diǎn)。
以上對(duì)本發(fā)明的較佳實(shí)施例進(jìn)行了描述。需要理解的是,本發(fā)明并不局限于上述特定實(shí)施方式,其中未盡詳細(xì)描述的設(shè)備和結(jié)構(gòu)應(yīng)該理解為用本領(lǐng)域中的普通方式予以實(shí)施;任何熟悉本領(lǐng)域的技術(shù)人員,在不脫離本發(fā)明技術(shù)方案范圍情況下,都可利用上述揭示的方法和技術(shù)內(nèi)容對(duì)本發(fā)明技術(shù)方案做出許多可能的變動(dòng)和修飾,或修改為等同變化的等效實(shí)施例,這并不影響本發(fā)明的實(shí)質(zhì)內(nèi)容。因此,凡是未脫離本發(fā)明技術(shù)方案的內(nèi)容,依據(jù)本發(fā)明的技術(shù)實(shí)質(zhì)對(duì)以上實(shí)施例所做的任何簡(jiǎn)單修改、等同變化及修飾,均仍屬于本發(fā)明技術(shù)方案保護(hù)的范圍內(nèi)。
- 還沒(méi)有人留言評(píng)論。精彩留言會(huì)獲得點(diǎn)贊!
- 一種敲除c?di?AMP分解酶的重組恥垢分枝桿菌株及其應(yīng)用的制造方法與工藝
- 檢測(cè)結(jié)核分枝桿菌感染的抗原多肽池及其應(yīng)用的制造方法與工藝
- 一種獼猴桃分枝定位器的制造方法與工藝
- 一種xanthone類化合物及其單晶的制備方法與作為抗海分枝桿菌藥物的應(yīng)用與制造工藝
- 一種糖肽類抗生素耐藥基因檢測(cè)試劑盒的制造方法與工藝
- 分枝桿菌快速分離培養(yǎng)方法與制造工藝
- 一種用于檢測(cè)潛在結(jié)核的特異性標(biāo)志物及其應(yīng)用的制造方法與工藝
- 結(jié)核分枝桿菌抗原蛋白R(shí)v2941及其T細(xì)胞表位肽的應(yīng)用的制造方法與工藝
- 一種微流控芯片上基于熒光量子點(diǎn)磁性富集并分離結(jié)核分枝桿菌TB的方法及裝置與制造工藝
- 二肽meso?DAP?D?Ala和/或四肽L?Ala?D?Glu?L?Lys?D?Ala的新用途的制造方法與工藝
- 結(jié)核桿菌CFP10?38kD?19kD融合蛋白構(gòu)建及鑒定的制作方法
- 結(jié)核桿菌16kD?CFP10?19kD融合蛋白構(gòu)建及鑒定的制作方法
- 一種抗結(jié)核分枝桿菌感染的蛋白trim27的制作方法
- 檢測(cè)結(jié)核分枝桿菌耐藥基因的試劑盒及相關(guān)應(yīng)用
- 一種結(jié)核分枝桿菌Rv1768基因微滴數(shù)字PCR絕對(duì)定量檢測(cè)試劑盒的制作方法
- Imb-ny類化合物在制備抗結(jié)核分枝桿菌藥物中的應(yīng)用
- 用于癌癥治療的檢查點(diǎn)抑制劑和分枝桿菌全細(xì)胞的制作方法
- 一種與油菜分枝角度性狀qtl位點(diǎn)緊密連鎖的分子標(biāo)記及應(yīng)用
- 一種結(jié)核分枝桿菌感染診斷試劑盒的制作方法
- 一種基于菊粉-殼聚糖修飾的結(jié)核分枝桿菌亞單位疫苗及其制備方法
- 一種結(jié)核分枝桿菌感染診斷試劑盒的制作方法
- 一種基于菊粉-殼聚糖修飾的結(jié)核分枝桿菌亞單位疫苗及其制備方法
- 結(jié)核分枝桿菌pcr-lfb檢測(cè)試劑盒的制作方法
- 基于高分辨熔解曲線技術(shù)的結(jié)核分枝桿菌耐藥性基因突變檢測(cè)的制作方法
- 一種用于分枝桿菌快速檢測(cè)與分型的引物及方法
- 結(jié)核分枝桿菌Rv0324基因在制備治療結(jié)核分枝桿菌潛伏感染制劑中的用圖
- 結(jié)核分枝桿菌Rv3833基因在制備治療結(jié)核分枝桿菌潛伏感染藥物中的用圖
- 結(jié)核分枝桿菌Rv1909c基因在制備治療結(jié)核分枝桿菌潛伏感染的藥物中的用圖
- Rv3121蛋白在檢測(cè)結(jié)核分枝桿菌感染中的應(yīng)用
- 結(jié)核桿菌篩查系統(tǒng)的制作方法
- 一種結(jié)核分枝桿菌感染診斷試劑盒的制作方法
- 一種基于菊粉-殼聚糖修飾的結(jié)核分枝桿菌亞單位疫苗及其制備方法
- 結(jié)核分枝桿菌pcr-lfb檢測(cè)試劑盒的制作方法
- 基于高分辨熔解曲線技術(shù)的結(jié)核分枝桿菌耐藥性基因突變檢測(cè)的制作方法
- 一種用于分枝桿菌快速檢測(cè)與分型的引物及方法
- 偶發(fā)分枝桿菌在發(fā)酵生產(chǎn)表博醇中的應(yīng)用
- 鑒別結(jié)核分枝桿菌與非結(jié)核分枝桿菌感染的檢測(cè)方法
- 結(jié)核分枝桿菌Rv0324基因在制備治療結(jié)核分枝桿菌潛伏感染制劑中的用圖
- 結(jié)核分枝桿菌Rv3833基因在制備治療結(jié)核分枝桿菌潛伏感染藥物中的用圖
- 結(jié)核分枝桿菌Rv1909c基因在制備治療結(jié)核分枝桿菌潛伏感染的藥物中的用圖
- 結(jié)核分枝桿菌Rv0324基因在制備治療結(jié)核分枝桿菌潛伏感染制劑中的用圖
- 結(jié)核分枝桿菌Rv1909c基因在制備治療結(jié)核分枝桿菌潛伏感染的藥物中的用圖
- 一種快速檢測(cè)結(jié)核分枝桿菌的方法
- 一種多肽抗原檢測(cè)牛結(jié)核分枝桿菌抗體的elisa試劑盒的制作方法
- 結(jié)核分枝桿菌特異性融合蛋白及其編碼基因與應(yīng)用
- 可利霉素在抗結(jié)核分枝桿菌感染中的應(yīng)用
- 一種三抗體雙通道同時(shí)檢測(cè)人核基質(zhì)蛋白和癌胚抗原免疫傳感器的制備方法及應(yīng)用
- T細(xì)胞表位肽p2及其應(yīng)用
- T細(xì)胞表位肽p4及其應(yīng)用
- 一種檢測(cè)結(jié)核分枝桿菌及其耐藥基因突變的試劑盒及應(yīng)用
- 從分枝層壁菌制備環(huán)胞多肽a的方法
- 編碼結(jié)核分枝桿菌細(xì)胞吸收的dna分子的制作方法
- 胞內(nèi)分枝桿菌變態(tài)反應(yīng)原提取方法
- 分枝桿菌細(xì)胞壁中分枝菌酸的檢測(cè)方法
- 結(jié)核分枝桿菌胞內(nèi)二級(jí)信使環(huán)二鳥苷酸合成酶在治療結(jié)核病藥物篩選中的應(yīng)用的制作方法
- 基于焦磷酸測(cè)序的檢測(cè)結(jié)核分枝桿菌已胺丁醇耐藥性的方法
- 利用固定化分枝桿菌細(xì)胞脫除汽油中有機(jī)硫的方法
- 胞內(nèi)分枝桿菌檢測(cè)用引物和探針、以及使用該引物和探針的胞內(nèi)分枝桿菌的檢測(cè)方法
- 利用hbha來(lái)檢測(cè)肺結(jié)核和由結(jié)核分枝桿菌(mycobacteriumtuberculosis)引起的感染的制作方法
- 一種核酸等溫?cái)U(kuò)增檢測(cè)結(jié)核分枝桿菌活菌的方法及試劑盒的制作方法
- 一種利用rna恒溫?cái)U(kuò)增的結(jié)核分枝桿菌核酸檢測(cè)試劑盒的制作方法
- 利用hbha來(lái)檢測(cè)肺結(jié)核和由結(jié)核分枝桿菌引起的感染的制作方法
- 用于檢測(cè)結(jié)核分枝桿菌感染的方法
- 一種檢測(cè)結(jié)核分枝桿菌感染的試劑、方法及應(yīng)用的制作方法
- 用于檢測(cè)結(jié)核分枝桿菌感染的方法
- 人工分枝菌酸膜的制作方法
- 體外檢測(cè)結(jié)核分枝桿菌感染的試劑和方法
- 一種檢測(cè)分枝桿菌屬細(xì)菌存在的方法以及及其所用的試劑盒和抗體的制作方法