痘病毒溶瘤載體的制作方法
本申請是2010年5月18日提交的美國專利申請系列第12/743,402號的部分繼續申請,上述申請是2008年11月17日提交的PCT/EP2008/009720的美國國家階段,其指定美國并以英語于2009年5月28日公開為WO 2009/065546 A1,并根據35U.S.C.§119要求2007年11月19日提交的EP 07301557.0的優先權;在此出于所有目的將各內容均明確整體并入作為參考,每個均轉讓給其受讓人。
發明領域
溶瘤病毒是一類新的用于治療癌癥的治療劑,其具有依賴于腫瘤的自我永存的獨特特性(HERMISTON.A demand for next-generation oncolytic adenoviruses.Current opinion in molecular therapeutics.2006,第8卷,no.4,第322-30頁)。溶瘤病毒能夠選擇性地在惡性腫瘤細胞中復制,因此能夠提供潛在地遠高于常規癌癥治療的效力和特異性水平(FISHER.Striking out at disseminated metastases:the systemic delivery of oncolytic viruses.Current opinion in molecular therapeutics.2006,第8卷,no.4,第301-13頁)。使用這些病毒的益處在于,當它們復制時,它們會溶解其宿主細胞。癌細胞是許多病毒的理想的宿主,因為它們具有失活的抗病毒干擾素路徑,或者具有能夠使病毒復制不受阻礙地進行的突變的腫瘤抑制基因(CHERNAJOVSKY,等人.Fighting cancer with oncolytic viruses.British medical journal.2006,第332卷,no.7534,第170-2頁)。
一些病毒天然地能夠選擇性在腫瘤細胞中復制,但溶瘤病毒也可以通過修飾天然存在的病毒獲得。出于該目的,目前用于修飾病毒的主要策略包括:必要病毒基因中的功能性缺失;用于控制這些病毒基因表達的腫瘤或組織特異性啟動子:和趨性修飾以將腺病毒再導向至癌細胞表面。在不久的將來,溶瘤腺病毒需要加以優化,以充分實現其作為關鍵抗癌工具的潛力,并因此,改善惡性神經膠質瘤患者的預后(JIANG等人Oncolytic adenoviruses as antiglioma agents.Expert review of anticancer therapy.2006,第6卷,no.5,第697-708頁)。
例如,選擇性修飾成在具有p53突變的細胞中復制并將其殺死的腺病毒ONYX-015正在由Onyx Pharmaceuticals開發用于多種實體瘤包括頭頸、胃腸道和胰腺腫瘤的潛在治療。其是在E1B基因座處具有功能喪失突變的重組腺病毒,其產物是與p53腫瘤抑制蛋白結合并使其失活的55kDa蛋白質。因此,認為ONYX-015腺病毒使得正常細胞不感染。p53腫瘤抑制基因的突變是癌癥中遺傳異常最常見的類型,在半數以上所有主要癌癥類型中發生。因此,這些細胞對病毒易感,所述病毒將會很容易復制并導致細胞死亡。ONYX-015正在進行治療復發頭頸癌的III期試驗,結腸直腸、卵巢、胰腺和口腔腫瘤的II期試驗,以及消化系疾病、食道和肝腫瘤的I期試驗(COHEN,等人.ONYX-015.Onyx Pharmaceuticals.Current opinion in investigational drugs.2001,第2卷,no.12,第1770-5頁)。
天然溶瘤病毒是具有選擇性感染腫瘤細胞并將其殺死的先天能力的有復制能力的病毒。盡管五十年前用于用活病毒治療癌癥的最初嘗試,對天然溶瘤病毒的關注落后于對于改造的腺病毒和皰疹病毒用作癌癥治療劑的支持。但是,近年來,重新興起對于這些天然存在的活性劑的高效力和選擇性的關注(ROBERTS等人Naturally oncolytic viruses.Current opinion in molecular therapeutics.2006,第8卷,no.4,第314-21頁)。
在天然溶瘤病毒當中,牛痘病毒(痘病毒)具有許多用于溶瘤病毒療法的理想病毒骨架所必需的關鍵特性。這些包括生命周期短,細胞-細胞傳播迅速,溶解能力強,克隆能力大,以及分子生物學明確。此外,盡管能夠在人細胞中復制,它們并不視作是天然的健康問題,尤其是明確表征在消滅天花運動中已經傳遞至數百萬個體。使用疫苗株或遺傳修飾疫苗株的早期臨床結果已經證實了抗腫瘤效果(THORNE等人Vaccinia virus and oncolytic virotherapy of cancer.Current opinion in molecular therapeutics.2005,第7卷,no.4,第359-65頁)。
相反,痘病毒粘液瘤病毒是新的溶瘤候選物,其沒有直接用于人的歷史,因為其具有明顯和絕對的對兔類動物(兔子)的宿主物種趨性。最近發現粘液瘤病毒也能夠選擇性地感染并殺死人腫瘤細胞——與大多數人癌癥中發現的細胞內信號傳導路徑調節異常有關的獨特趨性。該綜述概述了粘液瘤病毒對于人癌細胞的趨性的現有知識,以及顯示其在癌癥動物模型中能夠感染并清除腫瘤的臨床前數據(STANFORD等人Myxoma virus and oncolytic virotherapy:a new biologic weapon in the war against cancer.Expert opinion on biological therapy.2007,第7卷,no.9,第1415-25頁)。
技術問題
注射實現抗腫瘤效果所需的高劑量痘病毒引起毒性問題。大多數不良事件較小,通常與牛痘病毒有關的不良反應是自限性的,包括發熱、頭痛、疲勞、肌痛、發冷、局部皮膚反應、非特異性皮疹、多形性紅斑、淋巴結病和種痘部位疼痛。其他反應可能需要額外的治療(例如,一線治療VIG和二線治療西多福韋(cidofovir))。可能需要進一步評價或治療的不良反應包括偶然接種、全身性牛痘(GV)、痘性濕疹(EV)、進行性牛痘(PV)、種痘后中樞神經系統疾病和胎兒牛痘(CONO等人Smallpox vaccination and adverse reactions.Guidance for clinicians.MMWR.Recommendations and reports:Morbidity and mortality weekly report.Recommendations and reports/Centers for Disease Control.2003,第52卷,no.RR-4,第1-28頁)。
因此,對于溶瘤活性與其天然對應物同樣好的更加安全的痘病毒存在需求。
背景技術:
US 5364773(VIROGENETICS CORPORATION(TROY,NY))15/11/1994描述了一種修飾的重組痘病毒,更具體地,一種具有失活的非必需病毒編碼的編碼的遺傳功能的牛痘病毒,使得重組痘病毒的毒力減弱,安全性提高。具體地,通過刪除編碼毒力因子的可讀框,或者通過編碼毒力因子的可讀框的插入性失活,使遺傳功能失活。更具體地,該專利描述了其中J2R、B13R+B14R、A26L、A56R、C7L-K1L和I4L可讀框已經失活的牛痘病毒。該病毒(NYVAC)可以改造成為用于外源核酸的載體,并且用作用于在宿主動物中誘導免疫反應的疫苗。但是,NYVAC在大多數哺乳動物細胞中不能有效復制,并且不能用作溶瘤病毒(XIANGZHI等人Vaccinia virus K1L protein supports viral replication in human and rabbit cells through a cell-type-specific set of its ankyrin repeat residues that are distinct from its binding site for ACAP2.Journal of virology.2006,第353卷,no.1,第220-233頁)。
WO 2004/014314(KIRN DAVID(US))描述了一種在其病毒基因組中包括一個或多個突變的變更的牛痘病毒。所描述的突變屬于一種或多種以下多肽分類:1)干擾素調節多肽;2)互補控制多肽;3)TNF或趨化因子調節多肽;4)絲氨酸蛋白酶抑制劑;5)IL-lp調節多肽;6)非感染性EEV形式多肽;和7)作用于抑制感染性病毒從細胞釋放的病毒多肽(抗感染病毒形式的多肽)。此外,還公開了牛痘病毒A41L或C11R中的突變。
本申請更具體地說明了牛痘基因組區,例如A34R、A41L、A53R、B5R、B7R、B8R、B13R、B15R、B18R、B22R、B28R、B29R、CUR、E3L、K2L、N1L、vC12L和vCKBP。本發明的方法涉及使用在此討論的任意痘病毒。發明人還公開了通過給予癌細胞或患者有效量的該變更的牛痘病毒治療癌癥的方法。
技術實現要素:
發明人出人意料地發現,包括缺陷性I4L和/或F4L基因的痘病毒具有提高的安全性譜,但保持著相等的溶瘤活性(與其天然對應物相比較)。
本發明涉及包括缺陷性I4L和/或F4L基因的痘病毒,其條件是所述痘病毒不是NYVAC。
如申請文件通篇所用,除非上下文明顯另外指出,術語“a”和“an”以其表示“至少一種”、“至少第一”、“一種或多種”或“多個”所引組分或步驟的含義使用。例如,術語“細胞”包括多個細胞,包括其混合物。
術語“和/或”在本文任意處使用時均包括以下含義:“和”、“或”和“所述術語相連的元素的所有或任意其他組合”。
如本文所用,術語“大約”或“約”是指在指定值或范圍的20%以內,優選10%以內,更優選5%以內。
如本文所用,術語“包括”和“包括有”是指產品、組成和方法包括所引的組分或步驟,但不排除其他。當定義產品、組成和方法時,“基本上由……組成”應當指排除其他具有任何重要意義的組分或步驟。因此,基本上由所描述組分組成的組合物不排除痕量污染物和可藥用的載體。“由……組成”應當指排除其他組分或步驟的痕量元素。
如本文所用,術語“包括缺陷性基因的痘病毒”是指在缺陷性基因的一個或多個核苷酸中包括刪除、置換或加入或者這些可能性的任意組合的痘病毒,其中所述的修飾導致痘病毒不能產生具有未修飾基因所產生蛋白質的活性的蛋白質。在本發明的優選實施方式中,包括缺陷性基因的痘病毒是指其中全部基因序列被刪除的痘病毒。突變可以使用重組技術以若干種本領域技術人員已知的方式進行。修飾痘病毒基因組的方法在本領域是可獲得的。例如,以下文獻中公開的方法可以用于產生本發明的痘病毒:MCCART等人Systemic cancer therapy with a tumor selective vaccinia virus mutant lacking thymidine kinase and vaccinia growth factor genes..Cancer res..2001,no.61,第8751-57頁;KIM等人Systemic armed oncolytic ans immunologic therapy for cancer with JX-594,a targeted poxvirus expressing GM-CSF.Molecular Therapeutic.2006,no.14,第361-70頁;WO 2004/014314(KIRN DAVID(US))19/02/2004和US 5364773(VIROGENETICS CORPORATION(TROY,NY))15/11/1994。本申請實施例中公開的方法具體地有關產生根據本發明的痘病毒。多種痘病毒基因組的序列是本領域可獲得的,例如,牛痘病毒(vaccinia virus)、牛痘病毒(cowpox virus)、金絲雀痘病毒、鼠痘病毒、粘液瘤病毒基因組可獲自Genbank(編號分別為NC_006998、NC_003663、NC_005309、NC_004105、NC_001132)。
如本文所用,術語“痘病毒”是指屬于痘病毒科家族的病毒。根據優選的實施方式,根據本發明的痘病毒屬于脊椎動物痘病毒(Chordopoxvirinae)亞科,更優選地,屬于正痘病毒(Orthopoxvirus)屬,再更優選地,屬于牛痘病毒物種。
例如,可以使用牛痘病毒Dairen I、IHD-J、L-IPV、LC16M8、LC16MO、Lister、LIVP、Tashkent、WR 65-16、Wyeth、安卡拉(Ankara)、哥本哈根(Copenhagen)、天壇(Tian Tan)和WR株。根據特別優選的實施方式,根據本發明的痘病毒是牛痘病毒哥本哈根株。
痘病毒牛痘含有大的雙鏈DNA基因組(187千堿基對),是唯一在感染的細胞的細胞質中復制的已知DNA病毒家族的成員。由于感染的細胞必須將大量DNA前體遞送至細胞質復制位點,病毒編碼并表達許多DNA代謝和合成所需的酶活性,包括核糖核苷酸還原酶和脫氧尿苷5’-三磷酸核苷酸水解酶(dUTPase)。
核糖核苷酸還原酶(EC 1.17.4.1)催化核糖核苷酸還原成脫氧核糖核苷酸——代表DNA生物合成中第一提交步驟的反應。病毒酶在亞基結構上與哺乳動物酶相似,由兩個稱作R1和R2的異源性亞基組成。編碼病毒核糖核酸還原酶亞基的基因已得以測序,并定位于牛痘基因組上的位置,被35千堿基隔開(SLABAUGH等人.Journal of virology.1988,第62卷,519-27頁;TENGELSEN等人.Virology.1988,no.164,第121-31頁;SCHMITT等人.Journal of virology.1988,no.62,第1889-97頁)。牛痘病毒大的亞基的單體(稱作R1,由I4L基因編碼)是86-kDa的多肽,含有核苷酸底物變構效應器結合位點(SLABAUGH等人.Journal of virology.1984,no.52,第507-14頁;SLABAUGH等人.Journal of virology.1984,no.52,第501-6頁)。小的亞基(稱作R2,由F4L基因編碼)是包括兩個37-kDa多肽的同二聚體;每個多肽含有催化要求的基于鐵穩定化蛋白質的自由基(HOWELL等人.Journal of Biological Chemistry.1992,no.267,第1705-11頁)。I4L和F4L基因的序列及其在多種痘病毒基因組中的位置可獲自公開數據庫,例如,經由登陸號DQ437594、DQ437593、DQ377804、AH015635、AY313847、AY313848、NC_003391、NC_003389、NC_003310、M35027、AY243312、DQ011157、DQ011156、DQ011155、DQ011154、DQ011153、Y16780、X71982、AF438165、U60315、AF410153、AF380138、U86916、L22579、NC_006998、DQ121394和NC_008291。
除非另外指出,本文使用的基因命名是哥本哈根牛痘株,并也用于其他痘病毒科的同源基因。但是,基因命名可以根據痘株而不同。供參考,哥本哈根和MVA基因之間的對應關系可以見于ANTOINE.Virology.1998,no.244,第365-396頁的表1。
根據優選實施方式,本發明的痘病毒還包括缺陷性J2R基因。
J2R基因編碼胸苷激酶(TK),其形成嘧啶脫氧核糖核苷酸合成補救途徑的一部分。由TK催化的反應涉及將γ-磷酰基部分從ATP轉移至2'脫氧-胸苷(dThd),產生胸苷5'-單磷酸(dTMP)。牛痘病毒的TK是2型的。與1型相比較,2型TK具有較小的多肽鏈,為~25KDa,但形成同四聚體。它們對于代謝途徑末端產生的反饋抑制物dTDP或dTTP敏感。與1型TK相比較,2型TK的底物特異性要窄得多,僅磷酸化2'脫氧尿苷(dU)和/或dThd(EL OMARI等人Structure of vaccinia virus thymidine kinase in complex with dTTP:insights for drug design.BMC structural biology.2006,no.6,第22頁)。
J2R區域缺陷性的痘病毒及其獲得方法可獲自本領域。例如,可以使用以下文獻的教導產生J2R區域刪除的痘病毒:MCCART等人Systemic cancer therapy with a tumor-selective vaccinia virus mutant lacking thymidine kinase and vaccinia growth factor genes.cancer research.2001,第61卷,no.24,第8751-7頁;PUHLMANN等人Vaccinia as a vector for tumor-directed gene therapy:biodistribution of a thymidine kinase-deleted mutant.Cancer gene therapy.2000,第7卷,no.1,第66-73頁;GNANT等人Systemic administration of a recombinant vaccinia virus expressing the cytosine deaminase gene and subsequent treatment with 5-fluorocytosine leads to tumor-specific gene expression and prolongation of survival in mice.Cancer Research.1999,第59卷,no.14,第3396-403頁。
根據優選的實施方式,本發明的痘病毒還包括缺陷性F2L基因。
脫氧尿苷5’-三磷酸核苷酸水解酶(dUTP酶,EC 3.6.1.23)在Mg(2+)離子的存在下催化dUTP水解成dUMP和焦磷酸。在從dNTP庫除去dUTP并產生dUMP時,dUTP酶涉及保持DNA復制的保真度以及通過胸苷酸合酶提供產生TMP的前體。牛痘dUTP酶是由F2L基因編碼的15kDa蛋白質(MCGEOGH..Nucleic Acids Research.1990,no.18,第4105-10頁;BROYLES..Virology.1993,no.195,第863-5頁)。牛痘病毒F2L基因的序列可經由登陸號M25392獲自genbank,F2L基因在多種痘病毒基因組中的序列和位置也可以獲自genbank,例如,經由登陸號NC_006998、DQ121394、NC_001611、AY689436、AY689437、NC_008291、DQ437594、DQ437593、AY313847、AY313848、NC_006966、NC_005309、NC_003391、NC_003389、NC_001132、NC_003310、NC_002188、M35027、AY243312、AF170726、DQ011157、DQ011156、DQ011155、DQ011154、DQ011153、X94355、Y16780、AY318871、U94848、AF198100和M34368。
根據優選的實施方式,根據本發明的痘病毒還包括目標核酸。
在優選的實施方式中,目標核酸含有編碼其為治療分子的基因產物的至少一段目標序列(即,治療基因)。“治療分子”是當適當給予患者特別是患有疾病或疾病狀況或者應當針對該疾病或狀況受保護的患者時具有藥理學或保護活性的分子。這樣的藥理學或保護活性是預期與在所述疾病或所述狀況的進程或癥狀方面的有益效果相關的活性。當技術人員在本發明的過程中選擇編碼治療分子的基因時,他通常將其選擇與之前獲得并且可以在沒有過度實驗的情況下合理預期的結果相關聯,而不是實施要求保護的發明,以獲得這樣的藥學特性。根據本發明,目標序列與其導入的目標細胞可以是同源的或異源的。有利地,目標所述序列編碼全部或部分多肽,特別是具有治療或預防特性的治療或預防性多肽。多肽理解成多核苷酸的任意翻譯產物,無論其大小,是否糖基化,并且包括肽和蛋白質。作為主要的例子,治療性多肽包括可以補償動物或人機體中缺陷性或缺乏的蛋白質的多肽,或者通過毒性效果作用以限制有害細胞并將其從體內去除的多肽。它們還可以是免疫性賦予多肽,其起到內源性抗原的作用,以激發體液或細胞反應或者二者。
治療性基因編碼的多肽的例子包括編碼以下的基因:細胞因子(α、β或γ干擾素,白介素特別是IL-2、IL-6、IL-10或IL-12,腫瘤壞死因子(TNF),集落刺激因子GM-CSF、C-CSF、M-CSF…,免疫刺激多肽(B7.1、B7.2等),凝血因子(FVIII、FIX…),生長因子(轉化生長因子TGF、成纖維細胞生長因子FGF等),酶(脲酶、腎素、凝血酶、金屬蛋白酶、一氧化氮合酶NOS、SOD、過氧化氫酶…),酶抑制劑(α1-抗胰蛋白酶、抗凝血酶III、病毒蛋白酶抑制劑、纖溶酶原激活物抑制劑PAI-1),CFTR(囊性纖維化跨膜傳導調節子)蛋白,胰島素,肌萎縮蛋白,I類或II類MHC抗原,可以調控/調節細胞基因表達的多肽,能夠抑制細菌、寄生蟲或病毒感染或其發展的多肽(抗原多肽、抗原表位、通過競爭抑制天然蛋白質作用的反式顯性(transdominant)變體…),細胞凋亡誘導劑或抑制劑(Bax、Bcl2、BclX…),細胞靜止劑(p21、p16、Rb…),載脂蛋白(ApoAI、ApoAIV、ApoE…),血管生成抑制劑(血管抑素、內皮抑素…),血管生成多肽(血管內皮生長因子VEGF家族、FGF家族、CCN家族,包括CTGF、Cyr61和Nov),氧自由基清除劑,具有抗腫瘤效果的多肽,在本領域識別為可用于治療或預防臨床狀況的抗體、毒素、免疫毒素和標記物(β-半乳糖苷酶、熒光素酶…)或任何其他目標基因。
合適的抗腫瘤基因包括但不限于編碼腫瘤抑制物的基因(例如Rb、p53、DCC、NF-1、Wilm腫瘤、NM23、BRUSH-1、p16、p21、p56、p73及其各自的突變體)、自殺基因產物、抑制細胞分裂或轉導信號的抗體、多肽。
根據特別優選的實施方式,本發明的痘病毒還包括自殺基因。
自殺基因是指編碼能夠將藥物前體轉化成細胞毒性化合物的蛋白質的基因。
自殺基因包括但不限于編碼具有胞嘧啶脫氨酶活性、胸苷激酶活性、尿嘧啶磷酸核糖轉移酶活性、嘌呤核苷磷酸化酶活性和/或胸苷酸激酶活性的蛋白質的基因。
自殺基因和包括一個核堿基部分的對應藥物前體的例子公開于下表:
表1
根據本發明的優選實施方式,自殺基因編碼具有至少一種CD酶活性的蛋白質。CD酶涉及嘧啶代謝途徑,通過該途徑外源性胞嘧啶通過水解脫氨的方式轉化成尿嘧啶。盡管CD酶活性已經在原核生物和低等真核生物中得以證明(JUND等人.Journal of Bacteriology.1970,no.102,第607-15頁;BECK等人.Journal of Bacteriology.1972,no.110,第219-28頁;HOEPRICH等人.Journal of Infectious Diseases.1974,no.130,第112-18頁;ESDERS等人.J.biol.chem..1985,no.260,第3915-22頁),它們在哺乳動物中并不存在(KOECHLIN等人.Biochemical pharmacology.1966,no.15,第435-46頁;POLAK等人.Chemotherapy.1976,no.22,第137-53頁)。
CD酶還使胞嘧啶的類似物即5-氟胞嘧啶(5-FC)脫氨,從而形成5-氟尿嘧啶(5-FU),這是當其轉化成5-氟-UMP(5-FUMP)時具有高度細胞毒性的化合物。由于使編碼酶的基因失活的突變或者由于其在該酶中天然缺陷而缺少CD酶活性的細胞,由于是哺乳動物細胞,對5-FC有抗性(JUND等人.Journal of Bacteriology.1970,no.102,第607-15頁;KILLSTRUP等人.Journal of Bacteriology.1989,no.171,第2124-2127頁)。相反,向其中轉移編碼CD酶活性的序列的哺乳動物細胞變得對5-FC敏感(HUBER等人.Cancer Research.1993,no.53,第4619-4626頁;MULLEN等人.Proceedings of the National Academy of Sciences of the United States of America.1992,no.89,第33-37頁;WO 93/01281(US HEALTH))。此外,相鄰的未轉化的細胞也變得對5-FC敏感(HUBER等人.Proceedings of the National Academy of Sciences of the United States of America.1994,no.91,第8302-6頁)。這一現象稱作旁觀者效應(bystander effect),是由于表達CD酶活性分泌5-FU的細胞接著通過跨質膜的直接擴散使相鄰細胞中毒。5-FU在被動擴散中的這一特性代表了與其中旁觀者效應要求與表達tk的細胞有接觸的tk/GCV參考系統相比較的優勢(MESNIL等人.Proceedings of the National Academy of Sciences of the United States of America.1996,no.93,第1831-35頁)。因此,可以很容易地理解CD酶在基因治療特別是抗癌基因治療背景中提供的所有優勢。
分別編碼這兩種生物的CD酶的釀酒酵母(S.cerevisiae)FCY1、白色念珠菌FCA1和大腸桿菌codA基因是已知的,其序列已得到公開(分別是SEQ ID NO:4;SEQ ID NO:5;SEQ ID NO:6)。
在這一方面,根據本發明更優選的實施方式,編碼具有CD酶活性的蛋白質的基因是FCY1、FCA1或CodA或其類似物。這些基因的類似物是指核酸序列與親本基因核酸序列的同一性程度大于70%、有利地大約80%、優選大于90%、最優選大于95%的基因。
專利WO 2005/007857公開了編碼具有提高的CD酶活性的蛋白質的基因。該多肽通過加入氨基酸序列衍生自天然CD酶。根據本發明另一優選實施方式,具有CD酶活性的蛋白質是WO 2005/007857公開的多肽,更優選序列標識符SEQ ID NO:2中表示的FCU1-8多肽及其類似物。
在原核生物和低等真核生物中,尿嘧啶通過尿嘧啶磷酸核糖轉移酶(UPRT酶)的作用轉化成UMP。該酶將5-FU轉化成5-FUMP。根據本發明另一優選實施方式,自殺基因編碼具有UPRT酶活性的蛋白質。
所討論的UPRT酶可以是任何來源的,特別是原核生物、真菌或酵母來源。通過說明的方式,在本發明的上下文中,可以使用編碼來自以下的UPRT酶的核酸序列:大腸桿菌(E.coli)(ANDERSEN等人Characterization of the upp gene encoding uracil phosphoribosyltransferase of Escherichia coli K12.European Journal of Biochemistry.1992,no.204,第51-56頁);乳酸乳球菌(Lactococcus lactis)(MARTINUSSEN等人Cloning and characterization of upp,a gene encoding uracil phosphoribosyltransferase from Lactococcus lactis.Journal of Bacteriology.1994,第176卷,no.21,第6457-63頁);牛分枝桿菌(Mycobacterium bovis)(KIM等人Complete sequence of the UPP gene encoding uracil phosphoribosyltransferase from Mycobacterium bovis BCG.Biochemistry and molecular biology international.1997,vol.41,no.6,p.1117-24);和枯草桿菌(Bacillus subtilis)(MARTINUSSEN等人Two genes encoding uracil phosphoribosyltransferase are present in Bacillus subtilis.Journal of Bacteriology.1995,第177卷,no.1,第271-4頁)。但是,最特別優選使用酵母UPRT酶,特別是由釀酒酵母FUR1基因編碼的酵母UPRT酶,公開于以下文獻中的所述基因的序列在此并入作為參考:KERN等人The FUR1gene of Saccharomyces cerevisiae:cloning,structure and expression of wild-type and mutant alleles.(Gene.1990,第88卷,no.2,第149-57頁)。作為指導,基因序列和對應的UPRT酶的序列可以見于文獻和專業數據庫中(SWISSPROT、EMBL、Genbank、Medline等)。
申請EP 0998568 A說明了在使得合成UPRT酶的編碼部分的5’缺乏105核苷酸的FUR1基因,上述酶在N-端位置處前35個殘基已經被刪除,并以天然蛋白質中36位處的甲硫氨酸開始。突變體基因的表達產物命名為FUR1Δ105,能夠補充釀酒酵母的fur1突變體。此外,截短的突變體表現出比天然酶更高的UPRT酶活性。因此,根據本發明特別有利的實施方式,自殺基因編碼天然UPRT酶的缺失突變體。缺失優選地位于原始UPRT酶N-端區域中。其可以是完全的(影響所述N-端區的所有殘基),或者是部分的(影響一級結構中一個或多個連續或不連續的殘基)。通常,多肽由N-端、中間和C-端部分組成,每個代表分子的大約三分之一。例如,由于釀酒酵母UPRT酶具有251個氨基酸,其N-端部分由位于天然形式第一位處的以所謂的起始子甲硫氨酸開始的前83個氨基酸組成。對于大腸桿菌UPRT酶,其N-端部分包括位置1-69。
優選的具有UPRT酶活性的蛋白質包括基本上如EP 0998568 A的序列標識符SEQ ID NO:1所示的氨基酸序列,以1位上的Met殘基開始,以216位上的Val殘基結束。術語“基本上”是指與所述序列SEQ ID NO:1 EP 0998568 A的同一性程度大于70%,有利地大于80%,優選大于90%,最優選大于95%。再更優選地,其包括序列標識符SEQ ID NO:1 EP 0998568 A中所示的氨基酸序列。如上所述,其可以包括額外的突變。具體可以提及2位(天然UPRT酶中的37位)上的絲氨酸殘基被丙氨酸殘基置換。
根據本發明另一優選實施方式,自殺基因編碼具有至少一種CD酶和至少一種UPRT酶活性的蛋白質。專利申請WO 96/16183和EP 0998568 A描述了使用編碼具有兩種具有CD酶和UPRT酶活性的結構域的酶的融合蛋白,并表明由表達質粒攜帶的雜合基因codA::upp或FCY1::FUR1或FCY1::FUR1Δ105(即FCU1)的轉移增加了轉染的B16細胞對5-FC的敏感性。根據本發明更優選的實施方式,自殺基因編碼包括基本上如序列標識符SEQ ID NO:3(coda::upp)、SEQ ID NO:1(FCU1)或FCY1::FUR1表示的氨基酸序列的多肽。術語“基本上”是指與所述序列的同一性程度大于70%,有利地大于80%,優選大于90%,最優選大于95%。再更優選地,其包括序列標識符SEQ ID NO:3(coda::upp)、SEQ ID NO:1(FCU1)或FCY1::FUR1中所示的氨基酸序列。如上所述,其可以包括額外的突變。
根據使用中的常規技術,核酸序列可以很容易地通過克隆、通過PCR或通過化學合成得到。它們可以是天然基因,或者是通過突變、缺失、置換和/或加入一個或多個核苷酸由后者得到的基因。而且,其序列在本領域技術人員可以查閱的文獻中得以廣泛說明。
本領域技術人員能夠由公開的數據克隆CD酶或UPRT酶序列,進行可能的突變,根據現有技術或者基于申請EP 0998568 A中所示的方案在非細胞或細胞系統中測試突變體形式的酶活性,并且具體地分階段融合具有CD酶和UPRT酶活性的多肽,并因此融合全部或部分的對應的基因。
根據更優選的實施方式,本發明的痘病毒還包含包括編碼通透酶的基因的核酸序列。
通透酶是指涉及包括一個核堿基部分的藥物或其前體通過細胞膜轉移的跨膜蛋白。
通透酶包括但不限于嘌呤通透酶、胞嘧啶通透酶和核苷轉運體。
根據本發明優選的實施方式,通透酶是釀酒酵母嘌呤或胞嘧啶通透酶。釀酒酵母核堿基轉運體由稱作FCY2的嘌呤-胞嘧啶通透酶和稱作FUR4的尿嘧啶通透酶組成。嘌呤-胞嘧啶通透酶FCY2介導質子和腺嘌呤、鳥嘌呤、次黃嘌呤和胞嘧啶跨酵母質膜的同向轉運(Grenson 1969,Jund和Lacroute 1970;Polak和Grenson 1973;Chevallier等人1975;Hopkins等人1988)。FCY2蛋白質還介導胞嘧啶的類似物5-氟胞嘧啶的轉運(Grenson 1969;Jund和Lacroute 1970)。FCY2基因編碼最初預測具有10-12個(Weber等人1990)、現在贊同9個(Ferreira等人1999)跨膜-跨越結構域的533個氨基酸的蛋白質(58kDa)。FCY2對于嘌呤核堿基和胞嘧啶表現出相似的親和性(Brethes等人1992)。尿嘧啶攝取到釀酒酵母中通過尿嘧啶通透酶FUR4介導(Jund和Lacroute 1970;Jund等人1977)。FUR4是尿嘧啶-質子同向轉運蛋白(Hopkins等人1988),其預測是具有10個跨膜結構域和長的細胞質親水性N-和C-端尾部(Jund等人1988;Garnier等人1996)的633個氨基酸的蛋白質(71.7kDa)。FUR4蛋白質還可以介導尿嘧啶的類似物5-氟尿嘧啶的轉運(Jund和Lacroute1970)。
FCY2和Fur4的氨基酸序列尤其可獲自swissprot數據庫(登錄號分別為P17064和P05316)。優選地,通透酶具有選自包含如專利申請WO2006/048768中所公開的氨基酸序列SEQ ID NO:1和SEQ ID NO:2的組的氨基酸序列。
就這一方面,根據本發明優選實施方式,通透酶選自包含FCY2和Fur4的組及其類似物。Fur4和FCY2類似物是指氨基酸序列與本文以上所述的親本蛋白質氨基酸序列具有大于70%,有利地大于80%,優選大于90%,最優選大于95%的同一性程度并且保持穿過細胞膜轉運包括至少一個核堿基部分的藥物的能力的多肽。
本領域技術人員能夠選擇通透酶,其將與藥物或包括一個堿基部分的藥物前體有關。例如,FCY2和Fur4優選地與5-氟胞嘧啶(5-FC)有關。
根據更優選的實施方式,本發明的痘病毒還可以包括目標核苷酸的表達所必需的元件。
根據更優選的實施方式,本發明的痘病毒還可以包含包括編碼通透酶的基因的核酸序列的表達所必需的元件。
目標核酸和/或包括編碼通透酶的基因的核酸的表達所必需的元件包括將所述DNA轉錄為mRNA以及如果需要的話將mRNA翻譯成多肽所要求的元件。適合用于許多脊椎動物系統的轉錄啟動子在文獻中得以廣泛描述。例如,合適的啟動子包括病毒啟動子例如RSV、MPSV、SV40、CMV或7.5k,牛痘啟動子,誘導型啟動子等。優選的啟動子分離自痘病毒,例如,牛痘病毒7.5K、H5R、TK、p28、p11或K1L。另外可選地,可以使用例如CHAKRABARTI.Biotechniques.1997,no.23,第1094-97頁;HAMMOND等人.Journal of Virological Methods.1997,no.66,第135-38頁;和KUMAR.Virology.1990,no.179,第151-8頁中所述的合成啟動子以及早期和晚期痘病毒啟動子之間的嵌合啟動子。
目標核酸序列和包括編碼通透酶的基因的核酸序列還可以包括額外的功能元件,例如內含子序列、靶向序列、轉運序列、分泌信號、核定位信號、IRES、聚A轉錄終止序列、三聯體前導序列和涉及復制或整合的序列。所述序列在文獻中已經報道,本領域技術人員可以很容易地獲得。
本發明還涉及制備根據本發明的痘病毒的方法,其包括:
(i)將根據本發明的痘病毒引入到細胞中,
(ii)將所述細胞在適合于能夠產生所述痘病毒的條件下培養,和
(iii)從細胞培養物中回收所述痘病毒。
盡管痘病毒當然可以從培養物上清液中回收,其也可以自細胞回收。常用的方法之一在于通過連續冷凍/解凍循環的方式溶解細胞,以收集溶解上清液中的病毒體。然后可以將病毒體擴增,并使用本領域技術純化(色譜方法、超離心方法,特別是通過氯化銫梯度等)。
本發明還涉及包括根據本發明的痘病毒與可藥用的賦形劑的組合的組合物。
根據本發明的組合物更加具體地通過基因治療的方式用于疾病的預防或治愈性治療,更具體地目的在于增殖性疾病(癌癥、腫瘤、再狹窄等)或目的在于與破骨細胞活性增加有關的疾病(例如,類風濕性關節炎、骨質疏松癥)。
根據本發明的組合物可以就其局部、腸胃外或消化途徑給藥而言常規制造。具體地,將治療有效量的本發明的重組載體或痘病毒與可藥用的賦形劑組合。可以預期有許多種給藥途徑。可以提到的例子有胃內、皮下、心臟內、肌內、靜脈內、腹膜內、腫瘤內、鼻內、肺內和氣管內途徑。在后三個實施方式的情形中,給藥通過氣溶膠或通過滴注方式進行是有利的。給藥可以作為單一劑量或者作為特定時間間隔后一個或多個時機重復的劑量進行。適當的給藥路徑和劑量取決于許多參數,例如,個體、要治療的疾病或者要轉移的目標基因。基于根據本發明的病毒顆粒的制劑可以配置成劑量104至1014pfu(斑形成單位)、有利地105至1013pfu、優選106至1012pfu、更優選106至107pfu的形式。
組合物可以包括就藥學觀點而言可接受的稀釋劑、佐劑或賦形劑以及增溶劑、穩定劑和防腐劑。在注射給藥的情形中,優選含水、非水或等滲溶液中的制劑。其可以呈現為液體或干燥(粉末、凍干物等)形式的單劑量或多劑量,所述凍干物可以在使用時使用適當的稀釋劑重建。
本發明還涉及根據本發明的痘病毒或組合物用于制備意在通過基因療法用于治療人或動物體的藥物的用途。藥物可以在體內直接給藥(例如,通過靜脈內注射至可接近的腫瘤中,通過氣溶膠方式至肺內,使用適當的導管至血管系統中)。優選的用途在于治療或預防癌癥、腫瘤和有害細胞增殖導致的疾病。可以提及的可想到的應用為乳腺癌、子宮癌(特別是由乳頭狀瘤病毒導致者)、前列腺癌、肺癌、膀胱癌、肝癌、結腸癌、胰腺癌、肺癌、食道癌、喉癌、中樞神經系統癌癥(例如成膠質細胞瘤)和血癌(淋巴瘤、白血病等)。另一優選的用途在于治療或預防類風濕性關節炎、骨質疏松癥和其他與破骨細胞活性增加有關的疾病。也可以用于心血管疾病背景,例如,為了抑制或延遲血管壁平滑肌細胞的增生(再狹窄)。最后,在感染性疾病的情形中,可以預期藥物應用于AIDS。
當使用本發明的痘病毒、組合物或方法用于治療癌癥時,優選的給藥途徑是全身途徑,因為根據本發明的痘病毒能夠特異性地靶向腫瘤細胞。
本發明還延伸至用于治療疾病的方法,其特征在于將根據本發明的痘病毒、組合物給予對該治療有需求的宿主生物或細胞。
根據有利的實施方式,治療用途或治療方法還包括額外的步驟,其中給予宿主生物或細胞可藥用量的前藥,有利地為胞嘧啶類似物,特別是5-FC。例如,可以使用50-500mg/kg/天的劑量,優選200mg/kg/天或100mg/kg/天的劑量。在本發明上下文中,前藥根據標準實踐(例如,口服,全身)給藥。
優選地,給藥在施用根據本發明的治療劑之后進行,優選在施用治療劑之后至少3天,更優選至少4天,再更優選至少5天。根據本發明再更優選的實施方式,前藥的給藥在施用治療劑之后7天進行。優選口服途徑。可以給予單劑量前藥,或者在足夠長能夠使毒性代謝物在宿主生物或細胞內產生的時間內重復給予多劑量。
而且,根據本發明的組合物或方法可以與一種或多種加強5-FU細胞毒性作用的物質組合。具體地可以提及抑制嘧啶從頭生物合成途徑的酶的藥物(例如下文所提及者),例如甲酰四氫葉酸的藥物(Waxman等人,1982,Eur.J.Cancer Clin.Oncol.18,685-692),其在5-FU代謝產物(5-FdUMP)的存在下增加胸苷酸合酶的抑制,導致復制所要求的dTMP庫降低,最后是例如氨甲碟呤(methotrexate)的藥物(Cadman等人,1979,Science 250,1135-1137),其通過抑制二氫葉酸還原酶并增加PRPP(磷酸核糖焦磷酸)庫,使得5-FU摻入到細胞RNA內增加。
根據本發明,抑制嘧啶從頭生物合成路徑的酶的藥物優選地選自PALA(N-(膦酰基乙酰基)-L-天冬氨酸;Moore等人,1982,Biochem.Pharmacol.31,3317-3321);來氟米特(Leflunomide)A771726(來氟米特活性代謝物;Davis等人,1996,Biochem.35,1270-1273)和布喹那(Brequinar)(Chen等人,1992,Cancer Res.52,3251-3257)。
根據本發明的組合物或方法可以與一種或多種抗癌治療有效的物質組合。在可以與根據本發明的組合物聯合或組合使用的抗癌治療有效的藥學物質當中,可以提到的有烷基化劑,例如,如絲裂霉素C、環磷酰胺、白消安、異環磷酰胺(ifosfamide)、異環磷酰胺(isosfamide)、美法侖、六甲嘧胺、噻替派(thiotepa)、苯丁酸氮芥(chlorambucil)或達卡巴嗪(dacarbazine);抗代謝物,例如,如吉西他濱(gemcitabine)、卡培他濱(capecitabine)、5-氟尿嘧啶、阿糖孢苷、2-氟脫氧胞苷、氨甲碟呤、idatrexate、tomudex或三甲曲沙(trimetrexate);拓撲異構酶II抑制劑,例如,如阿霉素、表阿霉素、依托泊苷(etoposide)、替尼泊苷(teniposide)或米托蒽醌(mitoxantrone);拓撲異構酶I抑制劑,例如,如伊力替康(CPT-11)、7-乙基-10-羥基-喜樹堿(SN-38)或拓撲替康;抗有絲分裂藥物,例如,如紫杉醇、多西紫杉醇、長春花堿、長春新堿或長春瑞濱;和鉑衍生物,例如,如順鉑、草酸鉑、順螺鉑(spiroplatinum)和卡鉑(carboplatinum)。
一種或多種抗癌治療中有效的物質和本發明的組合物可以通過本領域技術人員公知的方法一次或數次給藥,包括全身給藥和直接注射到腫瘤中。可以通過團注或灌注進行(例如,0.5-6小時中)。抗癌物質和/或痘病毒組合物的多種給藥可以彼此以適當時間分開,并使用相同或不同的劑量在相同位點或不同位點通過相同途徑或通過不同途徑進行。劑量可以由從業人員鑒于多種參數例如要治療的癌癥的性質、給藥的模式和頻率以及給予藥物常規考慮的其他因素加以調適。
在一實施方式中,本發明的方法或組合物與特別優選伊力替康的拓撲異構酶I抑制劑結合。優選地,伊力替康和痘病毒組合物靜脈內給藥。例如,伊力替康的適當劑量可以從5-100mg/kg/天變化,痘病毒劑量為從1x106至1x109pfu。優選地,痘病毒組合物將靜脈內注射1-3次,伊力替康以適當的周期性(例如一周一次)注射對于一個或多個循環。此外,在首次給予痘病毒組合物之后數天(例如,3-10天)將進行伊力替康治療。
在另一實施方式中,本發明的方法或組合物與特別優選草酸鉑的抗有絲分裂藥物結合。優選地,草酸鉑將腹膜內或靜脈內給藥,并且根據本發明的痘病毒組合物通過靜脈內途徑給藥。例如,草酸鉑的適當劑量可以從0.5-10mg/kg/天變化,痘病毒劑量為從1x106至1x109pfu。優選地,痘病毒組合物將靜脈內注射1-3次,草酸鉑以適當的周期性(例如每兩周)注射,對于一個或多個循環。此外,優選的方法包括首次給予痘病毒組合物,然后在首次痘病毒注射之后數天(例如,3-10天)給予草酸鉑治療。
而且,本發明的方法或組合物還包括額外的步驟,其中如上所述將可藥用量的前藥給予宿主生物或細胞。本發明上下文中優選的前藥是5-FC。
根據本發明的組合物或方法還可以與放療結合使用。
根據本發明的組合物或方法還可以與一種或多種其他藥劑結合使用,其包括但不限于免疫調節劑,例如,如α、β或γ干擾素,白介素(IL-2、IL-6、IL-10或IL-12)或腫瘤壞死因子;影響細胞表面受體調節的藥劑,例如,如表皮生長因子受體抑制劑(特別是西妥昔單抗(cetuximab)、帕尼單抗(panitumumab)、扎魯木單抗(zalutumumab)、尼妥珠單抗(nimotuzumab)、馬妥珠單抗(matuzumab)、吉非替尼(gefitinib)、厄洛替尼(erlotinib)或拉帕替尼(lapatinib))或人表皮生長因子受體-2抑制劑(特別是曲妥珠單抗(trastuzumab));和影響血管生成的藥劑,例如,如血管內皮生長因子抑制劑(特別是貝伐單抗(bevacizumab)或蘭尼單抗(ranibizumab))。
附圖說明
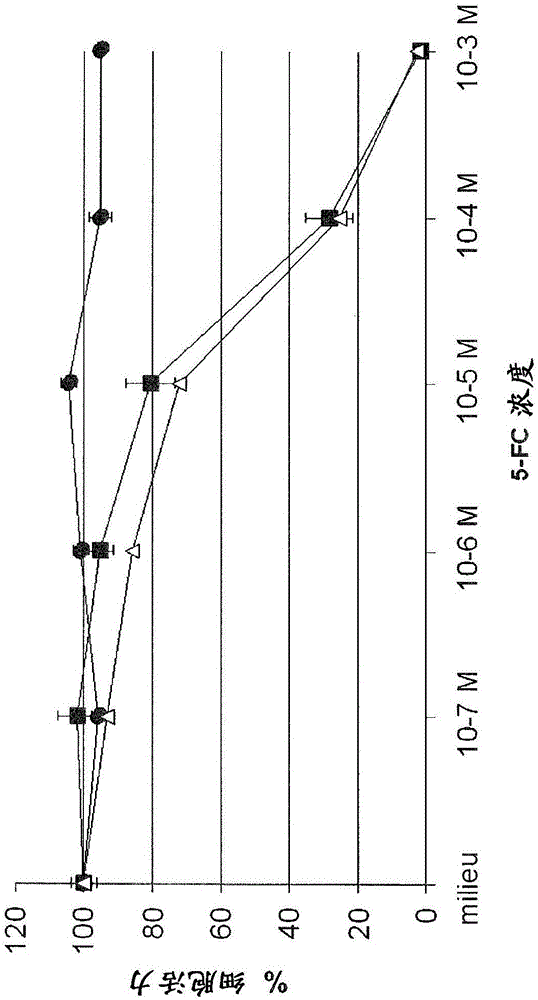
圖1.牛痘病毒感染的人結腸直腸腫瘤細胞(LoVo)對5-FC的體外敏感性。將在0.0001MOI下用所示的病毒(模擬物(●)VVTK-/FCU1(■)或VVTK-I4L-/FCU1(△))感染的LoVo細胞暴露于多個濃度的5-FC。感染后5天測量細胞存活。結果以存在或不存在藥物的情況下細胞存活力的百分比表示。數值以沒有由于病毒復制的細胞死亡的情況下三次獨立測量的平均值±SD表示。
圖2.牛痘病毒感染的人結腸直腸腫瘤細胞(LoVo)對5-FC的體外敏感性。將在0.0001MOI下用所示的病毒(模擬物(●)VVTK-/FCU1(■)或VVTK-F4L-/FCU1(◇)感染的LoVo細胞暴露于多個濃度的5-FC。感染后5天測量細胞存活。結果以存在或不存在藥物的情況下細胞生存力的百分比表示。數值以沒有由于病毒復制的細胞死亡的情況下三次獨立測量的平均值±SD表示。
圖3.在0.0001MOI下用所示病毒感染的LoVo中在感染后第5天VVTK-/FCU1和VVTK-I4L-/FCU1的體外復制效力。數值以三次獨立測量的平均值±SD表示。
圖4.在0.0001MOI下用所示病毒感染的LoVo中在感染后第5天VVTK-/FCU1和VVTK-F4L-/FCU1的體外復制效力。數值以三次獨立測量的平均值±SD表示。
圖5.靜脈注射病毒之后Swiss裸鼠中皮下LoVo的平均腫瘤體積±SEM。接種腫瘤(可觸及腫瘤)之后7天,將小鼠用107pfu緩沖液+鹽水(◇)、緩沖液+5-FC(◆)、VVTK-I4L-/FCU1+鹽水(△)或VVTK-I4L-/FCU1+5-FC(▲)處理。病毒注射后7天在3周時間內,一天兩次將動物用鹽水或5-FC 100mg/kg/j通過口腔喂食處理。一周兩次測量腫瘤體積。
圖6.靜脈注射病毒之后Swiss裸鼠中皮下LoVo的平均腫瘤體積±SEM。接種腫瘤(可觸及腫瘤)之后7天,將小鼠用107pfu緩沖液+鹽水(◇)、緩沖液+5-FC(◆)、VVTK-F4L-/FCU1+鹽水(□)或VVTK-F4L-/FCU1+5-FC(■)處理。病毒注射后7天在3周時間內,一天兩次將動物用鹽水或5-FC 100mg/kg/j通過口腔喂食處理。一周兩次測量腫瘤體積。
圖7.靜脈注射病毒之后Swiss裸鼠中皮下LoVo的平均腫瘤體積±SEM。接種腫瘤(可觸及腫瘤)之后11天,將小鼠用以下處理:緩沖液+H2O(◇),或者緩沖液+5-FC(◆),或者一次注射107pfu VVTK-I4L-/FCU1+H2O(○),或者一次注射107pfu VVTK-I4L-/FCU1+5-FC(病毒注射之后7天并且在3周時間內施用5-FC)(●),或者兩次(第11天和第33天)注射107pfu VVTK-I4L-/FCU1+H2O(□),或者兩次(第11天和第33天)注射107pfu VVTK-I4L-/FCU1+5-FC(從第18天到第32天和從第40天到第54天給予5-FC)(■)。一天兩次將動物用100mg/kg 5-FC通過口腔喂食處理。一周兩次測量腫瘤體積。
圖8.靜脈注射病毒之后Swiss裸鼠中皮下U87-MG(成膠質細胞瘤腫瘤細胞)的平均腫瘤體積±SEM。接種腫瘤(可觸及腫瘤)之后11天,將小鼠用以下處理:緩沖液+H2O(◇),或者緩沖液+5-FC(◆),或者107pfu VVTK-I4L-/FCU1+H2O(○),或者107pfu VVTK-I4L-/FCU1+5-FC(●)。病毒注射之后7天在3周時間內,一天兩次將動物用100mg/kg5-FC通過口腔喂食處理。一周兩次測量腫瘤體積。
圖9.分裂細胞中與匯合細胞中病毒收率的比例。將PANC1(人胰腺腫瘤)、H1299(人肺腫瘤)或U118MG(人膠質瘤腫瘤)細胞用100pfuVVTK-/FCU1或VVTK-I4L-/FCU1感染。感染后48h,測定病毒滴度。數值是分裂細胞中與匯合細胞中病毒收率之間的比例。
圖10.分裂細胞中與匯合細胞中病毒收率的比例。將PANC1(人胰腺腫瘤)、H1299(人肺腫瘤)或U118MG(人膠質瘤腫瘤)細胞用100pfuVVTK-/FCU1或VVTK-F4L-/FCU1感染。感染后48h,測定病毒滴度。數值是分裂細胞中與匯合細胞中病毒收率之間的比例。
圖11.用1x106PFU的VVTK-/FCU1或VVTK-I4L-/FCU1靜脈感染到荷有皮下人腫瘤的Swiss裸鼠中之后的第6天和第21天,器官或腫瘤中的病毒滴度(pfu/mg組織)。
圖12.用1x106PFU的VVTK-/FCU1或VVTK-F4L-/FCU1靜脈感染到荷有皮下人腫瘤的Swiss裸鼠中之后的第6天和第21天,器官或腫瘤中的病毒滴度(pfu/mg組織)。
圖13.通過靜脈注射用1x108pfu的VVTK-/FCU1(■)或VVTK-I4L-/FCU1處理之后Swiss裸鼠的存活。
圖14.通過靜脈注射用1x107pfu(A)或1x108pfu(B)的VVTK-/FCU1(■)或VVTK-I4L-/FCU1(◇)處理之后具有免疫力的B6D2小鼠的存活。
圖15.感染后第13天和感染后第34天在Swiss裸鼠中靜脈注射1x106pfu VVTK-/FCU1或VVTK-I4L-/FCU1之后尾部痘痕的平均數量。
圖16.感染后第13天和感染后第34天在Swiss裸鼠中靜脈注射1x106pfu VVTK-/FCU1或VVTK-F4L-/FCU1之后尾部痘痕的平均數量。
圖17.感染后第15天和感染后第31天在Swiss裸鼠中靜脈注射1x107pfu VVTK-/FCU1或VVTK-I4L-/FCU1之后尾部痘痕的平均數量。
圖18.感染后第15天和感染后第31天在Swiss裸鼠中靜脈注射1x107pfu VVTK-/FCU1或VVTK-F4L-/FCU1之后尾部痘痕的平均數量。
具體實施方式
實施例
構建載體質粒
使用胸苷激酶基因缺失并在牛痘合成啟動子p11K7.5的控制下表達FCU1基因的牛痘病毒哥本哈根株(登陸號M35027)構建缺失I4L的穿梭質粒。通過PCR擴增I4L的DNA側翼區域。I4L的下游側翼區域的引物為5’-TCC CCC GGG TTA ACC ACT GCA TGA TGT ACA-3’(SEQ ID NO:7;SmaI位點加下劃線)和5’-GCC GAG CTC GAG GTA GCC GTT TGT AAT TCT-3’(SEQ ID NO:8;SacI位點加下劃線)。上游區的引物為5’-GCC TGG CCA TAA CTC CAG GCC GTT–3’(SEQ ID NO:9;MscI位點加下劃線)和5’–GCC CAG CTG ATC GAG CCG TAA CGA TTT TCA–3’(SEQ ID NO:10;PvuII位點加下劃線)。將擴增的DNA片段用限制性內切酶SmaI/SacI或MscI/PvuII消化,并連接到PpolyIII質粒中相應的位點中。I4L的下游側翼區域的重復區域通過PCR使用以下引物擴增:5’-GCC GCA TGC ATC CTT GAA CAC CAA TAC CGA–3’(SEQ ID NO:11;SphI位點加下劃線)和5’-GCT CTA GAG AGG TAG CCG TTT GTA ATC TG–3’(SEQ ID NO:12;XbaI位點加下劃線),并插入到PpolyIII質粒中。在缺失的病毒的產生過程中使用重復區域消除選擇盒。將與pH5R牛痘啟動子控制下的GFP/GPT融合基因對應的選擇盒插入到PpolyIII質粒中的SacI/SphI位點中。得到的質粒是缺失I4L基因的稱作pΔI4L的重組穿梭質粒。
使用牛痘病毒哥本哈根株(登陸號M35027)構建缺失F4L的穿梭質粒。通過PCR擴增F4L的DNA側翼區域。F4L的下游側翼區域的引物為5’-CGC GGA TCC TTT GGT ACA GTC TAG TAT CCA-3’(SEQ ID NO:13;BamHI位點加下劃線)和5’-TCC CCC GGG TTA TAA CAG ATG CAG TAT CCA-3’(SEQ ID NO:14;SmaI位點加下劃線)。上游區域的引物為5’-GCC CAG CTGTTC AAT GGC CAT CTG AAA TCC–3’(SEQ ID NO:15;PvuII位點加下劃線)和5’–GAA GAT CTA GTA TCG CAT CTA AAA GAT GG–3’(SEQ ID NO:16;BglII位點加下劃線)。將擴增的DNA片段用限制性內切酶BamHI/SmaI或BglII/PvuII消化,并連接到PpolyIII質粒中相應的位點中。I4L的下游側翼區域的重復區域通過PCR使用以下引物擴增:5’-GCC GAG CTC ACC CAC ACG TTT TTC GAA AAA–3’(SEQ ID NO:17;SacI位點加下劃線)和5’-GCC GCA TGC TTA TAA CAG ATG CAG TAT CAA–3’(SEQ ID NO:18;SphI位點加下劃線),并插入到PpolyIII質粒中。在缺失的病毒的產生過程中使用重復區域消除選擇盒。將與pH5R牛痘啟動子控制下的GFP/GPT融合基因對應的選擇盒插入到PpolyIII質粒中的SacI/SmaI位點中。得到的質粒是缺失F4L基因的稱作pΔF4L的重組穿梭質粒。.
產生重組牛痘病毒
將CEF細胞用VVTK-FCU1(牛痘病毒,J2R激酶基因缺陷性,在合成啟動子p11k7.5的控制下表達FCU1基因)哥本哈根株在0.1MOI下感染,并在37℃下孵育2h,然后用重組穿梭質粒(0.2μg)的CaCl2共沉淀物轉染。將細胞在37℃下孵育48h。然后使用出現的病毒稀釋物在含有最終濃度15μg/ml的次黃嘌呤、最終濃度250μg/ml的黃嘌呤和最終濃度250μg/ml的霉酚酸的選擇培養基中感染CEF細胞。分離熒光(GFP)和陽性(GPT選擇)斑塊,并在GPT選擇培養基的存在下在CEF細胞中進行數輪選擇。使用在缺失區域內的引物通過40個PCR循環確定VVTK-FCU1的存在或不存在。消除親代病毒之后,使用雙缺失病毒在沒有GPT選擇培養基的情況下感染CEF,以消除選擇盒。分離非熒光斑塊,并在CEF中進行2輪選擇。將最終的重組VV病毒在CEF中擴增,提純,并通過斑塊測定在CEF上對病毒儲液進行滴定。
對5-FC的體外細胞敏感性
將人腫瘤細胞由在0.0001MOI的各自的重組VV轉導。將總計3x 105細胞/孔在2ml含有多種濃度5-FC的培養基中在6-孔培養皿中鋪平板。然后將細胞在37℃下培養5天,通過臺盼藍拒染法對活細胞進行記數。圖1、2、3和4所示的結果表示,比起在I4L和J2R基因缺陷性病毒中或者比起在F4L和J2R基因缺陷性病毒中,在J2R基因缺陷性病毒中FCU1活性是等同的。
培養的細胞中的體外復制
將分裂或匯合細胞在6孔斑塊中以100PFU病毒(幾乎MOI 0.0005)感染。對于分裂細胞加入補充有10%FCS、對于匯合細胞加入不補充的2mL培養基。感染后48小時收獲細胞。將細胞在-20℃下儲存,并進行超聲,以釋放病毒,病毒也通過斑塊滴定在CEF細胞上加以量化。分裂細胞與匯合細胞中的復制之間的比例在所有細胞中是類似的。兩種病毒VVTK-/FCU1、VVTK-I4L-/FCU1和VVTK-F4L-/FCU1在分裂細胞中比在匯合細胞中復制得更多。
作為檢驗復制病毒特異性的間接方式,測定分裂相比匯合的腫瘤細胞(人胰腺腫瘤PANC1;人肺腫瘤H1299;人膠質瘤腫瘤U118MG)中產生的病毒的收率。將匯合細胞以1x106細胞/孔平板鋪平板,并在完全培養基中培養7天,然后在感染之前1天,將細胞洗滌,并在無血清培養基中培養。感染之前1天將分裂的細胞以3x105細胞/孔平板鋪平板。為了評價細胞分裂的水平,在細胞鋪平板之后5小時、24小時和48小時測量滴定的胸苷并入到核酸中的量。在該時間過程中,胸苷并入在匯合細胞中相對恒定,而在分裂細胞中隨著時間觀察到并入增加。然后將細胞用100pfu病毒感染,感染后48小時通過CEF上的斑塊滴定測定分裂腫瘤細胞中和匯合腫瘤細胞中產生的病毒收率之間的比例。圖9和圖10中所示的結果說明,兩種病毒VVTK-/FCU1、VVTK-I4L-/FCU1和VVTK-F4L-/FCU1均在分裂細胞中比在匯合細胞中復制得更多。而且,通過與VVTK-/FCU1比較,對于兩種病毒VVTK-I4L-/FCU1和VVTK-F4L-/FCU1,圖9和圖10中所示的結果在所有不同類型的細胞中均表現出比例的增加。所有不同類型細胞中比例的增加是因為兩種病毒VVTK-I4L-/FCU1和VVTK-F4L-/FCU1在匯合細胞中的復制較低。這些結果說明,與VVTK-/FCU1相比較,兩種病毒VVTK-I4L-/FCU1和VVTK-F4L-/FCU1均表現出朝向分裂細胞的增加的特異性。
皮下腫瘤模型
雌性Swiss裸鼠獲自Charles River Laboratories。研究中使用的動物年齡均一(6周),體重范圍23-26g。Swiss裸鼠皮下(s.c.)注射5x106LoVo細胞至側腹中。當腫瘤達到直徑50-70mm3時,以盲模式將小鼠隨機化,并用所示載體處理用于體內實驗。
病毒的生物分布
通過腫瘤和器官樣品中的病毒滴定評價多種病毒的存在。通過尾靜脈注射將1x106PFU VV-FCU1或VVTK-I4L-/FCU1或VVTK-F4L-/FCU1靜脈內(i.v.)注射到荷有建立的皮下LoVo腫瘤的裸鼠中。在所示的時間點將小鼠處死,收集腫瘤和其他器官并稱重。將腫瘤和器官在PBS中均質化,如之前所述在CEF上測定滴度。將病毒滴度標準化至毫克組織。表2、表3、表4和表5中所示的結果(病毒滴度范圍以pfu/mg組織表示)表明,14天之后,根據本發明的病毒主要在腫瘤中發現。圖11和圖12中所示的結果表明,兩種病毒VVTK-/FCU1、VVTK-I4L-/FCU1和VVTK-F4L-/FCU1均靶向腫瘤,在腫瘤中的病毒大約比在其他分析的器官中多1 000至10 000倍,VVTK-/FCU1的情形中尾部除外。在第6天在肺、脾臟、腎臟和淋巴結中檢測到少量VVTK-/FCU1(小于10pfu/mg),在皮膚、尾部和骨髓中更多,在第21天,在皮膚和尾部檢測到。相反,VVTK-I4L-/FCU1和VVTK-F4L-/FCU1具有更高的腫瘤特異性,在第6天僅有少量在淋巴結和尾部,在第21天僅在腫瘤中。
表2
表3
表4
表5
本發明的痘病毒在皮下腫瘤模型中的抗腫瘤活性
將荷有建立的皮下LoVo腫瘤(50-70mm3)的裸鼠分別用所示載體以1.107PFU的劑量靜脈內(通過尾靜脈)處理一次。病毒注射之后第7天開始,通過口服喂食以100mg/kg(0.5ml 5-FC 0.5%水中)一天兩次給予5-FC,給藥3周。使用卡尺每周兩次測量腫瘤大小。使用公式(p/6)(長度x寬度2)以mm3計算腫瘤體積。圖5和圖6中所示的結果表明,多種病毒具有能夠控制腫瘤生長的溶瘤活性的相似的效力(p<0.05),并且給予5-FC的組合的活性(病毒的溶瘤和FCU1基因的治療性)可以進一步提高腫瘤生長的控制(p<0.01)。
根據以下將荷有建立的皮下LoVo腫瘤(50-70mm3)的裸鼠也用1.107PFU劑量的所示載體靜脈內(通過尾靜脈)處理:用腫瘤(可觸及腫瘤)接種之后11天,將小鼠通過以下處理:緩沖液+H2O,或者緩沖液+5-FC,或者注射一次107pfu VVTK-I4L-/FCU1+H2O,或者注射一次107pfu VVTK-I4L-/FCU1+5-FC(病毒注射之后7天給予5-FC,給藥3周),或者注射兩次(第11天和第33天)107pfu VVTK-I4L-/FCU1+H2O,或者注射兩次(第11天和第33天)107pfu VVTK-I4L-/FCU1+5-FC(第18-32天和第40-54天給予5-FC)。一天兩次將動物通過口服喂食用100mg/kg的5-FC處理。使用卡尺一周兩次測量腫瘤大小。使用公式(p/6)(長度x寬度2)計算單位mm3的腫瘤體積。圖7中所示的結果表明,注射一次或兩次之后單獨的病毒沒有抗腫瘤活性。當與載體組以及單獨的病毒(沒有5-FC)直至第50天相比較時,加入5-FC處理表現出統計學上顯著的腫瘤生長的抑制(p<0.05)。正如一次單次注射一樣,與載體組和僅注射兩次病毒(無5-FC)相比較,兩次靜脈內注射VVTK-I4L-/FCU1+5-FC表現出顯著的抗腫瘤活性(p<0.05)。而且,在與5-FC治療組合的一次和兩次注射病毒之間觀察到從第56天起病毒進化方面的顯著差異(p<0.05)。
根據以下將荷有建立的皮下U87-MG(成膠質細胞瘤腫瘤細胞)的裸鼠用1.107PFU劑量的所示載體靜脈內(通過尾靜脈)處理:用腫瘤(可觸及腫瘤)接種之后11天,將小鼠通過以下處理:緩沖液+H2O,或者緩沖液+5-FC,或者107pfu VVTK-I4L-/FCU1+H2O,或者107pfu VVTK-I4L-/FCU1+5-FC。病毒注射后7天在3周時間內,一天兩次將動物通過口服喂食用100mg/kg的5-FC處理。使用卡尺一周兩次測量腫瘤大小。使用公式(π/6)(長度x寬度2)計算單位mm3的腫瘤體積。圖8所示結果表明了VVTK-I4L-/FCU1對U87-MG細胞的高溶瘤活性,其導致強抗腫瘤活性(p<0.0001)。通過口服喂食加入5-FC的組合的活性導致類似的活性(p<0.0001)。
病毒病原性
使用Swiss裸鼠(圖13)和免疫活性B6D2小鼠(圖14)上進行的存活研究對病毒致病性進行評價。將小鼠靜脈內注射每小鼠100μL緩沖液中1.107或1.108PFU的全部VVTK-/FCU1和VVTK-I4L-/FCU1。整個實驗進程中每天觀察小鼠。在Swiss裸鼠(圖13)中,注射1x108PFU VVTK-/FCU1導致注射后3天40%的動物死亡。其余小鼠在注射后50天和80天之間死亡。給予VVTK-I4L-/FCU1致病性較低,大多數動物在65-140天之間死亡(p<0.01)。107pfu下兩種病毒均沒有觀察到毒性證據(圖14(A))。靜脈內注射108pfu VVTK-/FCU1之后所有小鼠均死亡(圖14(B))。與VVTK-/FCU1感染的小鼠相比較VVTK-I4L-/FCU1處理組存活顯著延長至70%(圖14(B))。因此,該結果證明了雙缺失病毒VVTK-I4L-/FCU1毒性的降低。
痘痕尾部損傷模型
將Swiss裸鼠靜脈注射1.106(圖15和16)或1.107(圖17和18)PFU每種病毒。每周一次計算尾部損傷。與注射VVTK-/FCU1的小鼠在感染后第13天小鼠平均8個痘痕相比較,注射1.106PFU VVTK-I4L-/FCU1或VVTK-F4L-/FCU1的小鼠具有小于1痘痕/小鼠(p<0.001),如圖15(A)和圖16(A)所示。注射后第34天結果類似,與VVTK-I4L-/FCU1或VVTK-F4L-/FCU11幾乎1個比較,VVTK-/FCU1平均4個痘痕(p<0.0001),如圖15(B)和圖16(B)所示。感染后第15天,與注射1.107PFU VVTK-/FCU1的小鼠平均10痘痕/小鼠相比較,注射1.107PFU VVTK-I4L-/FCU1或VVTK-F4L-/FCU1的小鼠分別平均3痘痕/小鼠和2痘痕/小鼠(圖17(A)和圖18(A))。感染后第31天,與注射VVTK-/FCU1的小鼠平均7痘痕/小鼠相比較,注射VVTK-I4L-/FCU1或VVTK-F4L-/FCU1的小鼠分別平均1.5痘痕/小鼠和2痘痕/小鼠(圖17(B)和圖18(B))。VVTK-/FCU1與VVTK-I4L-/FCU1和VVTK-F4L-/FCU1二者之間痘痕數的差異在統計學上是顯著的(p<0.01)。痘痕形成與尾部的病毒復制有關,因此與毒力和毒性有關。靜脈注射VVTK-I4L-/FCU1或VVTK-F4L-/FCU1毒性小于單缺失TK病毒。
VVTK-I4L-/FCU1和伊力替康的組合
VVTK-I4L-/FCU1治療與伊力替康組合的治療效果在存在和不存在5FC前藥的情況下在人胰腺癌MiaPaca2細胞系(編號:CRL-1420TM)上在體內評價。更具體地,將裸鼠(n=12小鼠/組)皮下注射5x 106MiaPaca2細胞。當腫瘤具有100-200mm3時,在腫瘤植入后第24、28和30天靜脈注射1x 106PFU VVTK-I4L-/FCU1。在第28、31、35、38、42、45天靜脈給予33mg/kg/天伊力替康。從腫瘤植入后第31天起,每天兩次通過口服喂食給予100mg/kg的5-FC 3周。使用卡尺測量腫瘤大小。使用公式(π/6)(長度x寬度2)以mm3為單位計算腫瘤體積。當腫瘤大小超過體積4000mm3時,將小鼠處死。使用Mann-Whitney U-檢驗確定各組之間的腫瘤體積差異。P值<0.05視作具有顯著性。
在腫瘤植入日后73天時間內全身注射VVTK-I4L-/FCU1+/-5-FC和伊力替康之后,定期(每4-6天)測量人胰腺MiaPaca2植入腫瘤的腫瘤體積。表6提供了植入后第24、39、50、59、63和73天多個小鼠組中測得的以mm3為單位的平均腫瘤體積。“iri”表示伊力替康,“VV”表示VVTK-I4L-/FCU1。
表6
當腫瘤體積>4000mm3時將小鼠安樂死。
在MiaPaca2模型中,就腫瘤生長而言,對照(未處理)組和單獨5-FC組之間沒有差異。在有或沒有5-FC的情況下給予VVTK-I4L-/FCU1導致輕微的抗腫瘤效果。與無處理相比較,在有或沒有5-FC的情況下給予伊力替康表現出顯著的腫瘤生長控制。就腫瘤生長控制而言,在給予或不給予5-FC的情況下VVTK-I4L-/FCU1與伊力替康組合觀察到最大的益處。
總之,與其他組相比較,使用VVTK-I4L-/FCU1與伊力替康的組合(有或沒有5-FC)治療導致腫瘤生長的顯著抑制。
VVTK-I4L-/FCU1與草酸鉑的組合
VVTK-I4L-/FCU1治療與草酸鉑組合的治療效果在存在和不存在5FC前藥的情況下在結腸直腸癌LoVo細胞系上進行體內評價。5FU也在這些條件下測試。
更具體地,將裸鼠(n=11小鼠/組)皮下注射5x 106LoVo細胞。當腫瘤具有100-200mm3時,在腫瘤植入后第21天靜脈注射1x 107PFU VVTK-I4L-/FCU1。在第24、27、31、3/4、38、41天腹膜內給予2.5mg/kg/天草酸鉑。從腫瘤植入后第28天起,每天兩次通過口服喂食給予100mg/kg 5-FC 3周。從腫瘤植入后第23天起,腹膜內給予200mg/kg/天5-FC 3周。使用卡尺測量腫瘤大小。使用公式(π/6)(長度x寬度2)以mm3為單位計算腫瘤體積。當腫瘤大小超過體積4000mm3時,將小鼠處死。使用Mann-Whitney U-檢驗確定各組之間的腫瘤體積差異。P值<0.05視作具有顯著性。
在腫瘤植入日后52天的時間內全身注射VVTK-I4L-/FCU1+/-5-FC和草酸鉑之后定期(每4-6天)測量人結腸直腸LoVo植入腫瘤的腫瘤體積。表7提供了植入后第19、25、32、46、49和52天多個小鼠組中測量的以mm3為單位的腫瘤體積平均值。“oxa”表示草酸鉑,“VV”表示VVTK-I4L-/FCU1。
表7
在LoVo模型中,就腫瘤生長而言,與對照(未處理)小鼠相比較,用單獨的草酸鉑、單獨的5-FC、草酸鉑+5-FC、單獨的5-FU、草酸鉑+5-FU或者單獨的VVTK-I4L-/FCU1處理提供輕微的腫瘤生長控制。與無處理相比較,VVTK-I4L-/FCU1+草酸鉑或VVTK-I4L-/FCU1+5-FC導致顯著的腫瘤生長控制。就腫瘤生長控制而言,VVTK-I4L-/FCU1+5-FC+草酸鉑組合觀察到最大的益處。與無處理、單獨草酸鉑、單獨的5-FC、草酸鉑+5-FC、單獨的VVTK-I4L-/FCU1、VVTK-I4L-/FCU1+草酸鉑或者VVTK-I4L-/FCU1+5-FC相比較,用該組合處理導致顯著的腫瘤生長抑制。而且,與單獨的化療藥物5-FU或者與草酸鉑組合(5-FU以最大耐受濃度腹膜內給予)相比較,用VVTK-I4L-/FCU1+5-FC+草酸鉑組合處理導致顯著的抗腫瘤效果。
總之,與VVTK-I4L-/FCU1和草酸鉑中的每一個以及與標準抗腫瘤藥物5FU相比較,在5-FC的存在下用VVTK-I4L-/FCU1和草酸鉑的組合處理顯著證明提供增強的抗腫瘤效果。
統計學分析
統計學分析使用非參數Mann-Whitney U檢驗和STATISTICA 7.1軟件(StatSoft,Inc.)進行。P<0.05視作在統計學上具有顯著性。
參考文獻
US 5364773(VIROGENETICS CORPORATION(TROY,NY))15.11.1994
WO 2004/014314(KIRN DAVID(US))19.02.2004
WO 2004/014314(KIRN DAVID(US))19.02.2004
US 5364773(VIROGENETICS CORPORATION(TROY,NY))15.11.1994
WO 93/01281(US HEALTH)
WO 2005/007857
WO 2005/007857
EP 0998568 A
EP 0998568 A
EP 0998568 A
EP 0998568 A
WO 96/16183
EP 0998568 A
EP 0998568 A
WO 2006/048768
HERMISTON.A demand for next-generation oncolytic adenoviruses.Current opinion in molecular therapeutics.2006,第8卷,no.4,第322-30頁.
FISHER.Striking out at disseminated metastases:the systemic delivery of oncolytic viruses.Current opinion in molecular therapeutics.2006,第8卷,no.4,第301-13頁.
CHERNAJOVSKY等人.Fighting cancer with oncolytic viruses.British medical journal.2006,第332卷,no.7534,第170-2頁.
JIANG等人.Oncolytic adenoviruses as antiglioma agents.Expert review of anticancer therapy.2006,第6卷,no.5,第697-708頁.
COHEN等人.ONYX-015.Onyx Pharmaceuticals.Current opinion in investigational drugs.2001,第2卷,no.12,第1770-5頁.
ROBERTS等人.Naturally oncolytic viruses.Current opinion in molecular therapeutics.2006,第8卷,no.4,第314-21頁.
THORNE等人.Vaccinia virus and oncolytic virotherapy of cancer.Current opinion in molecular therapeutics.2005,第7卷,no.4,第359-65頁.
STANFORD等人.Myxoma virus and oncolytic virotherapy:a new biologic weapon in the war against cancer.Expert opinion on biological therapy.2007,第7卷,no.9,第1415-25頁.
CONO等人.Smallpox vaccination and adverse reactions.Guidance for clinicians.MMWR.Recommendations and reports:Morbidity and mortality weekly report.Recommendations and reports/Centers for Disease Control.2003,第52卷,no.RR-4,第1-28頁.
XIANGZHI等人.Vaccinia virus K1L protein supports viral replication in human and rabbit cells through a cell-type-specific set of its ankyrin repeat residues that are distinct from its binding site for ACAP2.Journal of virology.2006,第353卷,no.1,第220-233頁.
MCCART等人.Systemic cancer therapy with a tumor selective vaccinia virus mutant lacking thymidine kinase and vaccinia growth factor genes..Cancer res..2001,no.61,第8751-57頁.
KIM等人.Systemic armed oncolytic ans immunologic therapy for cancer with JX-594,a targeted poxvirus expressing GM-CSF.Molecular Therapeutic.2006,no.14,第361-70頁.
SLABAUGH等人.Journal of virology.1988,第62卷,第519-27頁.
TENGELSEN等人.Virology.1988,no.164,p.121-31.
SCHMITT等人.Journal of virology.1988,no.62,第1889-97頁.
SLABAUGH等人.Journal of virology.1984,no.52,第507-14頁.
SLABAUGH等人.Journal of virology.1984,no.52,第501-6頁.
HOWELL等人.Journal of Biological Chemistry.1992,no.267,第1705-11頁.
ANTOINE..Virology.1998,no.244,第365-396頁.
EL OMARI等人.Structure of vaccinia virus thymidine kinase in complex with dTTP:insights for drug design.BMC structural biology.2006,no.6,第22頁.
MCCART等人.Systemic cancer therapy with a tumor-selective vaccinia virus mutant lacking thymidine kinase and vaccinia growth factor genes.cancer research.2001,第61卷,no.24,第8751-7頁.
PUHLMANN等人.Vaccinia as a vector for tumor-directed gene therapy:biodistribution of a thymidine kinase-deleted mutant.Cancer gene therapy.2000,第7卷,no.1,第66-73頁.
GNANT等人.Systemic administration of a recombinant vaccinia virus expressing the cytosine deaminase gene and subsequent treatment with 5-fluorocytosine leads to tumor-specific gene expression and prolongation of survival in mice.Cancer Research.1999,第59卷,no.14,第3396-403頁.
MCGEOGH..Nucleic Acids Research.1990,no.18,第4105-10頁.
BROYLES..Virology.1993,no.195,第863-5頁.
JUND等人.Journal of Bacteriology.1970,no.102,第607-15頁.
BECK等人.Journal of Bacteriology.1972,no.110,第219-28頁.
HOEPRICH等人.Journal of Infectious Diseases.1974,no.130,第112-18頁.
ESDERS等人.J.biol.chem..1985,no.260,第3915-22頁.
KOECHLIN等人.Biochemical pharmacology.1966,no.15,第435-46頁.
POLAK等人.Chemotherapy.1976,no.22,第137-53頁.
JUND等人.Journal of Bacteriology.1970,no.102,第607-15頁.
KILLSTRUP等人.Journal of Bacteriology.1989,no.171,第2124-2127頁.
HUBER等人.Cancer Research.1993,no.53,第4619-4626頁.
MULLEN等人.Proceedings of the National Academy of Sciences of the United States of America.1992,no.89,第33-37頁.
HUBER等人.Proceedings of the National Academy of Sciences of the United States of America.1994,no.91,第8302-6頁.
MESNIL等人.Proceedings of the National Academy of Sciences of the United States of America.1996,no.93,第1831-35頁.
ANDERSEN等人.Characterization of the upp gene encoding uracil phosphoribosyltransferase of Escherichia coli K12.European Journal of Biochemistry.1992,no.204,第51-56頁.
MARTINUSSEN等人.Cloning and characterization of upp,a gene encoding uracil phosphoribosyltransferase from Lactococcus lactis.Journal of Bacteriology.1994,vol.176,no.21,第6457-63頁.
KIM等人.Complete sequence of the UPP gene encoding uracil phosphoribosyltransferase from Mycobacterium bovis BCG.Biochemistry and molecular biology international.1997,vol.41,no.6,第1117-24頁.
MARTINUSSEN等人.Two genes encoding uracil phosphoribosyltransferase are present in Bacillus subtilis.Journal of Bacteriology.1995,vol.177,no.1,第271-4頁.
KERN等人.The FUR1gene of Saccharomyces cerevisiae:cloning,structure and expression of wild-type and mutant alleles.Gene.1990,vol.88,no.2,第149-57頁.
CHAKRABARTI..Biotechniques.1997,no.23,第1094-97頁.
HAMMOND等人.Journal of Virological Methods.1997,no.66,第135-38頁.
KUMAR..Virology.1990,no.179,第151-8頁.
權利要求書(按照條約第19條的修改)
1.組合物,其包含溶瘤痘病毒,所述溶瘤痘病毒包含缺陷性I4L和/或F4L基因并且還包含自殺基因,用于與在抗癌治療中有效的一種或多種物質組合治療癌癥,其中在抗癌治療中有效的一種或多種物質選自伊力替康和草酸鉑。
2.根據權利要求1的用于治療癌癥的組合物,其中所述痘病毒還包含缺陷性J2R基因。
3.根據權利要求1或2的用于治療癌癥的組合物,其中所述痘病毒是牛痘病毒哥本哈根株。
4.根據權利要求1至3中任一項的用于治療癌癥的組合物,其中所述組合物和所述一種或多種物質經由全身路徑給藥或者給藥至腫瘤中,優選靜脈內給藥。
5.根據權利要求1至4中任一項的用于治療癌癥的組合物,其中伊力替康的劑量包括從5至100mg/kg/天,并且痘病毒的劑量包括從1x106至1x109pfu。
6.根據權利要求5的用于治療癌癥的組合物,其中靜脈注射所述痘病毒1至3次,并且在所述痘病毒的首次給藥之后3至10天注射伊力替康。
7.根據權利要求1至4中任一項的用于治療癌癥的組合物,其中草酸鉑靜脈內或腹膜內給藥,并且痘病毒靜脈內給藥。
8.根據權利要求7的用于治療癌癥的組合物,其中草酸鉑的劑量包括從0.5至10mg/kg/天,并且痘病毒的劑量包括從1x106至1x109pfu。
9.根據權利要求7或8的用于治療癌癥的組合物,其中所述痘病毒靜脈內注射1至3次,并且草酸鉑每2周對于1個或多個循環。
10.根據權利要求9的用于治療癌癥的組合物,其中在所述痘病毒組合物的首次給藥之后3至10天給藥所述草酸鉑。
11.根據權利要求1至10中任一項的用于治療癌癥的組合物,其中所述自殺基因編碼蛋白質,所述蛋白質具有至少一種胞嘧啶脫氨酶和一種尿嘧啶磷酸核糖轉移酶活性。
12.根據權利要求1至10中任一項的用于治療癌癥的組合物,其中自殺基因編碼包含基本上如序列標識符SEQ ID NO:1或SEQ ID NO:3中的序列所表示的氨基酸序列的多肽。
13.根據權利要求11或12的用于治療癌癥的組合物,其中所述使用還包括可藥用量的前藥。
14.根據權利要求13的用于治療癌癥的組合物,其中所述前藥是5-氟胞嘧啶。
15.根據權利要求14的用于治療癌癥的組合物,其中在所述痘病毒組合物給藥之后優選至少3天,更優選至少4天,和再更優選至少5天給藥所述前藥。
16.根據權利要求1至15中任一項的用于治療癌癥的組合物,其中所述癌癥選自乳腺癌、子宮癌、前列腺癌、肺癌、膀胱癌、肝癌、結腸癌、胰腺癌、胃癌、食道癌、喉癌、中樞神經系統癌癥(例如成膠質細胞瘤)和血癌,優選胰腺癌和結腸直腸癌。
- 還沒有人留言評論。精彩留言會獲得點贊!