用于消融手術的計劃系統和導航系統的制作方法
技術領域:
本發明涉及一種用于消融組織的外科手術。更加具體的,本發明涉及使用計劃系統以確定治療計劃,以及使用導航系統以實現消融手術的治療計劃。
背景技術:
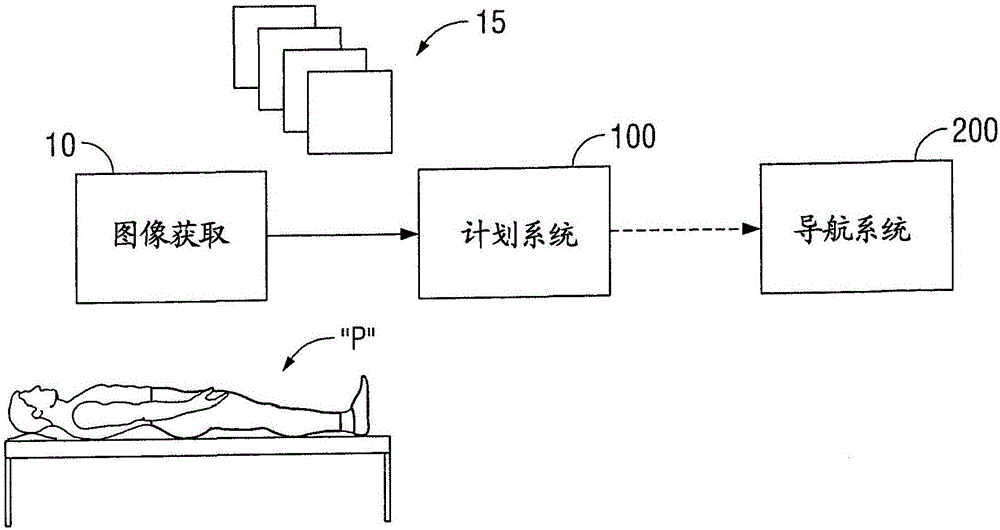
:電外科設備已經廣泛的使用。電外科手術包括在外科手術期間利用熱能和/或電能來切割、解剖、消融、凝結、燒灼、密封或其他處理生物組織。電外科手術通常使用的手持件進行,所述手持件包括適于在電外科手術期間傳輸能量至組織部位的外科設備(例如,端部執行器或消融探頭)、可操作地輸出能量的遠程電外科發生器、以及可操作的連接所述外科設備至遠程發生器的電纜組件。某些疾病的治療需要破壞惡性組織生長,例如腫瘤。在諸如癌癥的疾病的治療中,已經發現某些類型的腫瘤細胞在相比通常會對健康細胞有害的溫度稍低的高溫下變性。已知的治療方法,諸如高溫療法,通常包括將患病細胞加熱至高于41℃的溫度而保持鄰近健康細胞低于不可逆的細胞破壞發生的溫度。這些方法可包括施加電磁輻射以加熱、消融和/或凝結組織。有多種不同類型的電外科設備能夠用于執行消融手術。可以使用二維(2D)術前計算斷層掃描(CT)圖像和“消融區圖”來執行癌性腫瘤或良性腫瘤的腫瘤微創消融手術,所述“消融區圖”通常描述消融針在實驗的、離體組織中在一個范圍的輸入參數(功率、時間)上的特征。能量劑量(功率、時間)能夠與消融組織效應(體積、形狀)關聯以進行具體設計。能夠通過微波天線設計控制輸送至組織的能量劑量,例如,可利用天線電抗線圈來提供從設備至組織的已知位置的微波傳輸。在另一實例中,電介質緩沖使得能夠從設備至組織的相對恒定能量輸送,其獨立于不同的或變化的組織特性。在用戶確定應該使用哪個消融針來實現目標的處理后,用戶通過超聲引導來進行處理。通常,需要高水平技能來將外科設備置于由超聲識別的目標中。其中最重要的是選擇所需的角度和進入點來引導設備朝向超聲圖像面(例如,正在成像的目標處)。超聲引導介入包括使用實時超聲成像(經腹、術中等)來精確的引導外科設備至它們的指定目標。這能夠通過經皮應用和/或術中應用來進行。在每種情形中,超聲系統將包括換能器,其對患者組織成像并用于識別目標以及預期和/或遵循朝向目標的器械的路徑。超聲引導介入在目前廣泛的用于針吸活檢程序來確定已經探測的可疑病變的惡化(乳房、肝臟、腎臟、以及其他軟組織)。另外,中心線布置通常用來獲得頸靜脈通路以及允許輸送藥物。最后,新興用途包括腫瘤消融和器官(肝臟、肺、腎臟,等)的手術切除。在腫瘤消融的情形中,在實現超聲引導目標定位后,可利用活檢類針來輸送能量(RF、微波、低溫,等)以殺死腫瘤。在器官切除的情形中,解剖期間表層下解剖結構的直接知識、以及外科設備關于該解剖結構的顯示對于獲得成功的手術切緣而避開關鍵結構來說是關鍵的。在這些情形中的每個中,超聲引導通常提供二維圖像表面,其從患者所施加換能器的遠端獲取。對于用戶成功設備定位最重要的是能夠可視化和表征目標、選擇器械角度和進入點以到達目標、以及觀察外科設備及其朝向目標的運動。目前,用戶對目標成像并使用高水平技能來選擇器械角度和進入點。用戶則必須移動超聲換能器來觀察器械路徑(因此損失目標部位)或假定路徑是準確的直至設備到達圖像面。最重要的是能夠選擇所需的角度和進入點以引導設備朝向超聲圖像面(例如,正在成像目標處)。技術實現要素:本發明可使用短語“在一個實施方式中”、“在多個實施方式中”、“在一些實施方式中”、或“在其他實施方式中”,其中每個指代根據本發明的一個或多個相同或不同的實施方式。出于描述目的,以形式“A/B”的短語意指A或B。出于描述目的,以形式“A和/或B”的短語意指(A)、(B)或(A和B)。出于描述目的,以形式“A、B、或C中的至少一個”的短語意指“(A)、(B)、(C)、(A和B)、(A和C)、(B和C)、或(A、B和C)”。如附圖所示的以及整個下文說明書所描述的,在指代外科設備上的相對定位時與傳統一樣,術語“近側”指代設備更接近用戶或發生器的端,而術語“遠側”指代設備遠離用戶或發生器的端。術語“用戶”指代任何醫務人員(即,醫生、護士,等),其執行包括使用本文所述的本發明各個方面的醫療程序。如說明書中所使用的,術語“外科設備”通常指代外科手術工具,其施加電外科能量以治療組織。外科設備可包括但不限于針、探頭、導管、內窺鏡器械、腹腔鏡器械、血管閉合設備、外科縫合器等。術語“電外科能量”通常指代任何形式的電磁、光、或聲能。電磁(EM)能通常通過頻率的增加或波長的降低分類為無線電波、微波、紅外線、可見光、紫外線、X射線和伽馬射線。如本文所使用的,術語“微波”通常指代處于300兆赫(MHz)(3*108循環/秒)至300千兆赫(GHz)(3*1011循環/秒)的頻率范圍的電磁波。如本文所使用的,術語“RF”通常指代具有比微波更低頻率的電磁波。如本文所使用的,術語“超聲”通常指代具有大于人類聽力上限的頻率的循環聲壓。如本說明書中所使用的,術語“消融手術”通常指代任何消融手術,諸如微波消融、射頻(RF)消融或微波消融-輔助切除。如本說明書所使用的,“能量施加器”通常指代能夠用于從能量發生源如微波或RF電外科發生器傳輸能量至組織的任何設備。如本說明書中所使用的,術語“能量源”和“電源”指代以適于運轉電子線路形式的任何電能量源(例如,電池)。如本說明書中所使用的,“傳輸線路”通常指代能夠用于信號從一點至另一點傳播的任何傳輸介質。如本說明書所使用的,術語“開關”或“多個開關”通常指代任意電動致動器、機械致動器、電機械致動器(可旋轉致動器、可樞轉致動器、觸發器類致動器、按鈕等)、光學致動器、或任何合適設備,其通常實現電子設備、或其組件、器械、設備、輸送線路或連接線及其上附件、或軟件的連接和斷開連接目的。如本說明書所使用的,“電子設備”通常指代利用電子或離子在真空、氣體、或半導體中運動特性的設備或對象。如本文所使用的,“電子電路”通常指代電子或離子運動的路徑、以及由設備或對象為電子或離子提供的方向。如本文所使用的,“電氣線路”或簡單來說“電路”通常指代多個電氣設備和導體的組合,它們在彼此連接時形成導電路徑以實現期望功能。除了互連,電路的任何組成部件可以稱為“電路元件”,它們可包括模擬和/或數字組件。術語“發生器”可指代能夠提供能量的設備。該設備可包括能量源以及電路,所述電路能夠將能量源輸出的能量變更為具有期望強度、頻率、和/或波形的輸出能量。如本說明書中所使用的,“用戶接口”通常指代任何視覺、圖形、觸覺、聽覺、感官、或其他機構以提供信息至用戶或其他實體和/或從用戶或其他實體接收信息。本文所使用的術語“用戶接口”可指代人類用戶(或操作者)和一個或多個設備之間的接口,以使得能夠在用戶和設備之間通信。本發明中各個實施方式中可利用的用戶接口的實例包括但不限于開關、電位計、按鈕、撥號盤、滑動器、鼠標、定點設備、鍵盤、鍵區、操縱桿、軌跡球、顯示屏、各種類型的圖形用戶接口(GUIs)、觸屏、麥克風、以及其他類型的傳感器或設備,它們可接收人類發出的一些形式的激勵并產生響應其的信號。如本文所使用的,“計算機”通常指代以有目的方式傳輸信息的任何東西。本文所述的系統還可以利用一個或多個控制器來接收各種信息并轉換所接收的信息以產生輸出。控制器可包括任何類型的計算設備、計算電路、或任何類型的處理器或處理電路,其能夠執行存儲在存儲器中的一系列指令。控制器可包括多個處理器和/或多芯中央處理單元(CPUs),并可包括任何類型的處理器,諸如微處理器、數字信號處理器、微控制器、等。控制器還可包括存儲器以存儲數據和/或算法從而來執行一系列指令。本文所述的任何方法、程序、算法、或代碼可以轉化為編程語言或計算機語言、或以編程語言或計算機語言來表達。“編程語言”和“計算機程序”是用于把指令載入計算機的任何語言,并包括(但不限于)這些語言和它們的派生:匯編語言、Basic語言、批處理文件、BCPL、C、C+、C++、Delphi、Fortran、Java、JavaScript、機器代碼、操作系統命令語言、Pascal、Perl、PL1、腳本語言、VisualBasic、自身指定程序的元語言、以及所有的第一、第二、第三、第四及第五代計算機語言。還包括數據庫和其他數據模式、以及任意其他元語言。出于限定目的,在解譯、編譯、或使用編譯和解譯方法的語言之間沒有區別。出于限定目的,在程序的編譯版和源版本之間沒有區別。因此,參考程序,其中編程語言能夠以多于一種狀態(諸如源、編譯、對象、或鏈接語言)存在,可以指代任何的狀態以及所有狀態。該限定還包括有效指令和這些指令的含義。本文所述的任何方法、程序、算法或代碼可以包含在一個或多個機器可讀介質或存儲器中。術語“存儲器”可包括提供(例如,存儲和/或傳輸)諸如處理器、計算機、或數字處理設備的機器可讀形式的信息的機構。例如,存儲器可包括只讀存儲器(ROM)、隨機存取存儲器(RAM)、磁盤存儲介質、光存儲介質、閃存設備、或其他任意易失性或非易失性存儲器存儲設備。包含在它們上的代碼或指令可通過載波信號、紅外信號、數字信號、和其他類似信號來表達。本說明書中所使用的,短語“治療計劃”指代選定的消融針、能量水平、和/或治療持續時間以實現目標治療。術語“目標”指代預定治療的組織區域,或可包括且不限于腫瘤、纖維瘤、和待消融的其他組織。短語“消融區”指代將消融的組織區域和/或組織容積。如本說明書中所使用的,短語“計算斷層掃描”(CT)或“計算軸向斷層掃描”(CAT)指代利用計算機處理產生的斷層掃描的醫療成像方法。數字幾何處理用于從單個軸向旋轉采集的大系列二維X射線圖像來生成對象內部的三維圖像。如本說明書中所使用的,術語磁共振成像(MRI)、核磁共振成像(NMRI)、或磁共振斷層掃描(MRT)指代在X射線學中使用的以可視化內部細節結構的醫療成像技術。MRI利用核磁共振(NMR)特性來對體內原子核成像。MRI機器使用強力磁場來將體內的原子核磁性對準,而使用射頻場來系統的改變該磁性的對準。這引起核產生旋轉磁場,其由掃描器可探測,以及記錄該信息以構建所掃描身體區域的圖像。如本說明書中所使用的,術語“三維超聲”或“3D超聲”指代提供三維圖像的醫療超聲成像技術。如本說明書所使用的,術語“醫學數字成像和通信標準”(DICOM)指代用于處理、存儲、打印、和傳輸涉及醫療成像信息的標準。它包括文件格式定義和網絡通信協議。通信協議是應用協議,其使用TCP/IP以在各系統間通信。DICOM文件能夠在能接收DICOM格式的圖像和患者數據的兩個實體之間交換。本文所述的任意系統和方法可在有線網絡、無線網絡、點對點通信協議、DICOM通信協議、傳輸線路、可移動存儲介質等上傳輸數據。本文所述系統可利用一個或多個傳感器,其配置以探測組織和/或周圍環境的一個或多個屬性。所述屬性包括但不限于:組織阻抗、組織類型、組織透明度、組織順應性、組織或鉗口構件的溫度、組織中的水含量、鉗開口角度、組織中的水形態、能量輸送、以及鉗閉合壓。在本發明的一個方面,提供了一種消融計劃和導航系統。該計劃系統包括存儲器,其配置以存儲多個圖像;以及包括第一控制器,其配置以三維方式渲染多個圖像、自動分割多個圖像以對目標區域劃界、以及基于目標區域自動確定治療計劃。導航系統包括超聲設備,具有布置于其上的基準圖案并配置以獲得掃描平面中的超聲圖像;以及包括消融針,其具有圖像獲取設備,配置以獲取基準圖案的基準圖像;以及包括第二控制器,其配置以接收超聲圖像和基準圖像,其中所述控制器基于基準圖像確定消融針關于掃描平面的位置。消融計劃和導航系統還包括第三控制器,其配置以接收所渲染的多個圖像、目標區域、治療計劃、超聲圖像、以及消融針關于掃描平面的位置;以及包括顯示器,其配置以顯示第一顯示,其具有所渲染的多個圖像、目標區域、以及治療計劃;以及配置以顯示第二顯示,其具有超聲圖像、基于消融針關于掃描平面的位置的消融針虛擬圖像、以及治療計劃。在消融計劃和導航系統中,第一顯示和第二顯示顯示于單個屏幕上,以及可同時顯示或用戶能夠在第一顯示和第二顯示之間切換。可替代的,顯示器可具有兩個屏幕,以及第一顯示在第一屏幕上顯示和第二顯示在第二屏幕上顯示。顯示器還提供了圖形用戶接口。第一控制器執行容量分析以確定治療計劃,以及可調節治療計劃的輸入方式。第一控制器還可分割至少一根血管并基于血管與目標的接近度調節治療計劃,或第一控制器可分割至少一個器官并基于目標關于器官的位置調節治療計劃。在消融計劃和導航系統中,基準圖案固定至超聲設備上的已知位置,以及圖像獲取設備固定至消融針的已知位置。基準圖案具有多個已知特征和相對位置標記,它們保持在已知拓撲結構中。第二控制器將基準圖像對應至模型圖像,評估攝影機的位姿、以及將消融針轉換至模型坐標系。第二控制器還校準基準圖像的透鏡畸變。另外,第二控制器能夠識別基準標記中的拓撲結構,其中拓撲結構參照位于標記上的單個圖案上的已知位置中的兩個或更多個獨立唯一標識符。附圖說明本發明的上述和其他方面、特征、和優勢將在結合附圖時根據下面詳細描述而變得更加明顯,其中:圖1是根據本發明實施方式的計劃和導航系統的系統模塊圖;圖2A和2B是根據本發明實施方式的消融針的示意圖;圖3是圖2A和2B的消融針的輻射圖的示意圖;圖4是根據本發明實施方式的計劃系統的示意圖;圖5是描繪根據本發明實施方式的計劃系統的全部操作的流程圖;圖6和7是用于根據本發明實施方式的計劃系統中的圖形用戶接口的示意圖;圖8是描繪根據本發明實施方式的圖像分割和逆向計劃的算法的流程圖;圖9是描繪根據本發明實施方式的用于分割結節的算法的流程圖;圖10A-10B是消融區和能量輸送之間關系的圖形表示;圖11A是根據本發明另一實施方式的血管和目標之間關系的示意圖;圖11B是根據本發明另一實施方式的替代劑量曲線的圖形表示;圖12A-12C是根據本發明另一實施方式的計劃方法的示意圖;圖13是根據本發明實施方式的導航系統的示意圖;圖14A和14B是用于圖13的導航系統的圖形用戶接口的示意圖;圖15是描繪根據本發明實施方式的基準跟蹤算法的流程圖;圖16A和16B分別描繪了由攝影機獲得的圖像以及該圖像的校準版本;圖17是描繪根據本發明實施方式的用于找到白色圓圈的算法的流程圖;圖18A-18C描繪了圖17所描繪算法的中間圖像結果;圖19是描繪根據本發明實施方式的用于找到黑色圓圈和黑色區域的算法的流程圖;圖20A-20D描繪了圖19所描繪算法的中間圖像結果;圖21A是描繪根據本發明實施方式的匹配算法的流程圖;圖21B是描繪根據本發明實施方式的用于施加拓撲限制的算法的流程圖;圖22A-22D是用于圖21A算法的基準模型的示意圖;圖23是根據本發明另一實施方式的完整計劃和導航系統的示意圖;圖24是根據本發明又一實施方式的完整計劃和導航系統的示意圖;圖25A和25B是適于與圖24的系統一起使用的導航系統的示意圖;以及圖26-29是根據本發明各個實施方式的用于圖24的系統的圖形用戶接口的示意圖。具體實施方式本發明的特定實施方式將在下文中參照附圖進行描述;然而,應該理解的是,所公開實施方式僅是本發明的實例且可以各種形式體現。沒有描述公知的功能或構造以避免以不必要細節晦澀本發明。因此,本文所述的具體結構和功能細節不能解釋為限制,而僅僅作為權利要求書的基礎,以及作為教導本領域技術人員以實際上任何合適的細節結構來不同地利用本發明的代表性基礎。在整個附圖描述中相似參考數字指代相似或相同元件。轉向附圖,圖1描繪了根據本發明各實施方式的計劃和導航系統的整體視圖。如圖1所示,患者“P”的術前圖像15通過圖像獲取設備10獲取。圖像獲取設備10可包括但不限于獲得二維(2D)或三維(3D)圖像的MRI設備、CAT設備、或超聲設備。圖像獲取設備10存儲傳輸至計劃系統100的術前圖像15。術前圖像15可以通過將圖像15上傳到網絡上來傳輸至計劃系統100、通過無線傳輸裝置發射圖像15至計劃系統100、和/或將圖像15存儲在插入計劃系統100的可移動存儲器中。在本發明的實施方式中,術前圖像15以DICOM格式保存。在一些實施方式中,圖像獲取設備10和計劃系統100可結合為獨立單元。計劃系統100,其將在下文更加詳細描述,接收術前圖像15并確定目標尺寸。基于目標尺寸和選定的外科設備,計劃系統100確定設置,其包括實現目標治療的能量水平和治療持續時間。導航系統200,其在下文將更加詳細描述,利用布置于醫療成像設備(例如,超聲成像設備)上的基準圖案來確定外科設備的體內位置。外科設備的體內位置在顯示設備上以關于由醫療成像設備獲得的圖像來顯示。一旦外科設備定位在目標附近,則用戶基于由計劃系統確定的治療區設置來實現目標的治療。在一些實施方式中,用于使用計劃系統100來確定治療區設置,以及使用導航系統200來利用治療區設置實現治療。在其他實施方式中,在外科設備處于目標附近時,計劃系統100傳輸治療區設置至導航系統200以自動的實現目標的治療。另外,在一些實施方式中,計劃系統100和導航系統200結合為單個獨立系統。例如,單個處理器和單個用戶接口可用于計劃系統100和導航系統200,單個處理器或多個用戶接口可用于計劃系統100和導航系統200,或者多個處理器和單個用戶接口可用于計劃系統100和導航系統200。圖2A示出了根據本發明實施方式的外科設備的實例。具體而言,圖2A示出了具有電抗線圈72的消融針60的變體的側視圖,以及圖2B示出了沿圖2A的2B-2B的剖面圖。消融針60示出了輻射部62,其通過饋線(或軸桿)64電連接至近側定位的耦合器66。輻射部62示出以具有涂覆在節段62上的密封層68。電抗線圈72示出以部分地布置在饋線64的遠側節段上以形成電抗線圈部70,其靠近輻射部62定位。為了改善消融針60的能量聚焦,電抗線圈72用于將場傳播或輻射模式包含至消融針60的遠端。通常,電抗線圈72布置在消融針60上靠近輻射段。電抗線圈72置于介電材料上,所述介電材料布置在消融針60上。電抗線圈72是導電層,其可以通過管路或涂層覆蓋以迫使該導電層與下面的消融針60相符,進而在更遠端更接近輻射部62形成電連接(或短路)。電抗線圈72和下面的消融針60之間的電連接還可以通過其他連接方法實現,諸如軟焊、焊接、銅焊、壓接、使用導電粘合劑等。消融針60電耦接至發生器,其為消融針60提供電外科能量。圖3是根據本發明的消融針60的實施方式的剖面圖,其示出以發射的輻射圖的圖形表示。圖4至12C描述了根據本發明各個實施方式的計劃系統100的操作。轉向圖4,計劃系統100包括接收器102、存儲器104、控制器106、輸入設備108(例如,鼠標、鍵盤、觸摸板、觸屏,等)、以及顯示器110。在計劃系統100的操作中,接收器102接收以DICOM格式的術前圖像15并將這些圖像存儲在存儲器104中。控制器106然后處理圖像15,這將在下文詳述,并將已處理圖像顯示在顯示器110上。使用輸入設備108,用戶可以瀏覽圖像15,從圖像15中選擇一幅圖像,在所選擇圖像上選擇種子點,選擇消融針,調節能量水平,以及調節治療持續時間。由輸入設備108提供的輸入顯示在顯示器110上。圖5描繪了由計劃系統100使用的算法以確定治療計劃的概圖。如圖5所示,在步驟120中,通過無線連接、網絡,或通過從可移動存儲介質下載圖像并存儲在存儲器104中,來獲取以DICOM格式的圖像。控制器106則執行圖像15的自動的三維(3D)渲染,以及在步驟122中顯示3D渲染的圖像(如圖6所示)。在步驟124,執行圖像分割以對特定感興趣區域劃界以及計算感興趣區域的容積。如下所述,分割可以是用戶驅動或自動的。在步驟126,控制器執行逆向計劃操作,其還將在下文詳述,從而確定治療感興趣區域的治療算法。該治療算法可包括外科設備、能量水平、和/或治療持續時間的選擇。可替代的,用戶能夠選擇外科設備、能量水平、和/或治療持續時間以滿足治療醫生的目的,其將包括用于治療目標的“邊際值”以及周圍組織的限度。圖6和7描繪了可在顯示器110上顯示的圖形用戶接口(GUIs)。如圖6和7所示,每個GUI分割為多個區域(例如,區域132、134和136)用于顯示渲染的DICOM圖像。例如,區域132顯示了患者“P”沿橫剖面的圖像,以及區域134顯示患者“P”沿冠狀面的圖像。區域136描繪了患者“P”的3D渲染。在其他實施方式中,矢狀面也可顯示在GUI上。GUI允許用戶在下拉菜單131中選擇不同的消融針。GUI還允許用戶分別在區域133和135中調節功率和時間設置。另外的,GUI在區域137中具有多個其他工具,其包括但不限于啟動種子點選擇的計劃工具、對比工具、縮放工具、拖動工具、用于滾動瀏覽DICOM圖像的滾動條、以及用于顯示DICOM數據集渲染容積的3D渲染工具。圖8的流程圖描繪了用于執行圖像分割步驟124和逆向計劃步驟126的基本算法。如圖8所示,用戶在步驟140中選擇種子點(參見圖6,其中表現在區域132和134中目標“T”的中心)。在手動選擇種子點后,計劃系統100在步驟142中分割結節以對感興趣容積劃界。在其他實施方式中,可基于像素的強度值自動探測種子點。圖9描繪了用于分割結節的算法的流程圖。如圖9所示,一旦在步驟151中確定了種子點,該算法在步驟152中產生感興趣區域(ROI)。例如,ROI可包括4cm3的容積。在步驟153中,連接閾值濾波器施加閾值并在存儲于存儲器104中的DICOM圖像中找到連接至種子點的所有像素。例如,在分割肺結節時,閾值可在-400Hounsfield單位(HU)處開始并在100HU處終止。在步驟154,控制器106利用幾何過濾器來計算對象的尺寸和形狀。幾何過濾器使得能夠測量標簽容積中所有對象的幾何特征。該標簽容積能夠例如表示分割為不同解剖結構的醫療圖像。這些對象的各個幾何特征的測量能夠提供圖像中另外的洞察。該算法在步驟155中確定是否探測到預定形狀。如果未探測到預定形狀,則該算法行進至步驟156,其中閾值增加預定值。該算法重復步驟153至155直至探測到預定的對象。一旦探測到預定對象,該算法在步驟157處終止,以及計劃系統100行進至步驟144以執行容量分析。在容量分析期間,可通過控制器106計算球形對象的下述屬性:最小直徑、最大直徑、平均直徑、體積、球形度、最小密度、最大密度、以及平均密度。所計算的屬性可以在顯示器110上顯示,其在圖7的區域139中示出。容量分析可使用幾何過濾器來確定最小直徑、最大直徑、體積、延伸率、表面積、和/或球形度。在步驟144,圖像強度統計濾波器還可與幾何濾波器結合使用。圖像強度統計濾波器計算最小密度、最大密度以及平均密度。在步驟146中,針對劃界目標計算功率和時間設置。圖10描繪了給定時間段堆積至組織中的能量和所產生的消融區域之間的關系的各個曲線圖。該關系通過考慮目標組織(即,腫瘤、纖維瘤等)的尺寸和特征以及指定消融針的能量劑量/天線設計而允許逆向計劃。下表1示出了消融容積、功率、和消融針時間的關系圖的示例。表1消融容積(cm3)功率(W)時間(s)6140122140341140531110523805使用表1的數值,能夠從該表中導出線性等式,從而計算最佳功率和時間設置。例如,使用線性回歸分析,表1提供了下面等式:容積=0.292381*功率+8.685714*時間-44.0762(1)其能夠寫成功率=(容積-8.685714*時間+44.0762)/0.292381(2)能夠如下的使用來自容積分析的最大直徑加上1厘米邊際計算期望的容積:期望容積=4/3*pi*期望半徑^3(3)其中期望半徑可如下的計算:期望半徑=最大結節直徑/2+邊際(4)將期望容積代入等式(1)或(2)留下兩個未知數,功率和時間。使用等式(2),控制器106能夠通過代入時間值得出功率。控制器106選擇將功率保持低于70W或一些其他預定值的時間最小值,從而用戶能夠盡可能快的執行該過程而保持功率處于安全范圍。一旦146計算了功率和時間,功率和時間顯示在顯示器110上,如圖7所示(參見133和135)。用戶能夠分別使用控件133和135調節計算功率和/或時間,從而調節治療區138a和/或邊際138b。存儲器104和/或控制器106可存儲對應不同外科設備的多個公式。在用戶在下拉菜單131中選擇了不同的外科設備時,控制器106能夠執行上面所述的相同分析來確定保持功率低于70W或一些其他預定值的最小時間值。雖然上面所述過程描述了使用單個種子點來確定預定對象,一些目標會具有不規則形狀,其不能夠通過預定治療區來治療而不對其他組織造成損傷。在該情形中,可使用多個種子點來產生不規則形狀的治療計劃,其使用以多個位置重定位的單個外科設備或可同時使用的多個外科設備來治療不規則形狀的區域。在其他實施方式中,存儲器104和/或控制器106可存儲外科設備和治療區性能的目錄,其包括功率、時間、器械數量、以及實現體外或體內治療區所需的器械間隔。基于圖像分割和容積分析的結果,控制器可自動的選擇設備類型、設備數量、多個設備的間隔、和/或針對每個設備治療ROI的功率及時間設置。可替代的,用戶能夠使用GUI手動選擇設備類型、設備數量、多個設備的間隔、和/或針對每個設備治療ROI的功率及時間設置,從而產生治療計劃。在根據本發明的另一實施方式中,計劃系統100還可對除了目標之外的器官和其他重要結構分割。器官和其他結構如血管的分割用于提供更加先進的治療計劃。如上關于圖10所述的,治療區與能量輸送以規則方式相關聯。此外,公知的是大于三(3)毫米的血管會消極地影響治療區形成。血管的分割將允許血管和待評估目標之間的交互,包括血管直徑(D1)以及血管與提出的目標之間的距離D2(參見圖11A)。該交互可通過用戶手動的或通過控制器106自動的評估。使用血管直徑D1和距離D2,計劃系統100可自動的建議用于治療目的的交替劑量曲線,如圖11B所示。可替代的,控制器106可通過顯示器110為用戶提供建議以移動治療區。另外,不同的治療區投影將顯示在顯示器110上。此外,在圖8的計算功率和時間設置步驟146中,控制器將基于血管直徑和至目標區域的距離來利用不同的曲線。圖12A-12C描繪了使用器官分割的先進治療計劃。器官分割允許在計劃治療進程中具有至少兩個優勢。第一個情形,通常選擇微創治療以避免傷害器官。通過分割器官,控制器106能夠計算器官體積160以及減去確定的消融區162以確定剩下的器官164的體積,如圖12A所示。在控制器106確定剩下的器官體積太低時,則控制器106會提醒用戶需要替換治療計劃或會建議替代治療計劃。圖12B和12C描繪了定位在器官表面上目標“T”的治療計劃。傳統上,經常避免靠近器官表面的治療或需要另外的技術來在執行治療前將該器官與其他器官隔離。在根據本發明的另一實施方式中,在分割器官后,還能夠確定目標“T”的位置。在治療計劃中的治療區162凸出于器官表面外以及目標“T”位于表面上時,控制器106會提醒用戶治療區162影響到目標“T”附近的其他器官和/或結構以及該治療計劃需要變更。在其他實施方式中,控制器106可自動的為用戶提出指示外科設備、能量水平、治療持續時間的建議。控制器106還可建議如圖12B中示出的較小的治療區162或它可建議如圖12C所示的移動治療區162。在其他實施方式中,在分割目標、組織、器官、和其他結構后,已知的組織性質能夠歸于這些結構。這些組織性質包括但不限于:交叉頻率上的導電性和介電常數、導熱性、熱對流系數,等。圖8的計劃算法可使用歸因于分割腫瘤、組織、器官、和其他結構的組織性質來求解Pennes生物傳熱方程,從而計算出消融選定目標所需的劑量。針對使用生物傳熱方程的更全面求解實施的關鍵包括利用處于穩態的已知組織性質來預測初始空間溫度分布,利用隨著溫度上升的組織性質來調節根據溫度上升的空間性質,以及利用處于液-氣相變的組織性質。現在轉向圖13,根據本發明實施方式的導航系統通常示為200。一般而言,導航系統200結合固定至超聲換能器202的參照貼或基準貼204。基準貼204可印制在超聲換能器202上、通過粘結劑附接至超聲換能器202、或可移除的耦接至超聲換能器202。在一些實施方式中,基準貼布置在支撐結構上,所述支撐結構配置以可拆卸的固定如“夾到”超聲換能器的外殼上。超聲換能器202耦接至生成聲波的超聲發生器210。超聲換能器202和超聲發生器210可組合為獨立單元。超聲換能器202朝患者“P”發射聲波。所述聲波從患者“P”內的各種結構反射離開并由超聲換能器202接收。超聲換能器202將所反射的聲波傳輸至超聲發生器210,其將所反射聲波轉換為實時的二維(2D)圖像。所述2D圖像傳輸至控制器212。控制器212處理2D圖像并在顯示器214上顯示該2D圖像作為包括目標220的圖像218。圖像218是包括目標“T”的掃描平面“S”的實時表示。導航系統還結合攝影機208,其固定至外科設備206。攝影機208實時地獲取基準貼204的圖像以確定外科設備206關于掃描平面“S”的位置。特別的,基準貼204具有針對掃描平面“S”的預定空間關系。該限定空間關系存儲在控制器212中。攝影機208還具有針對外科設備206的已知空間關系,其存儲在控制器212中。為了確定外科設備206和掃描平面“S”之間的空間關系,攝影機208獲取基準貼204的圖像并將該圖像傳輸至控制器212。通過使用基準貼204的圖像,控制器212能夠計算外科設備206和掃描平面“S”之間的空間關系。在控制器212確定了外科設備206和掃描平面“S”之間的空間關系后,控制器212在顯示器214上顯示該關系。如圖13所示,顯示器214包括掃描平面“S”的圖像218,其包括目標“T”的目標圖像220。另外,控制器212關于圖像218疊加外科設備206虛擬圖像206a以指示外科設備206關于掃描平面“S”的位置。基于消融針206的角度和位置,控制器212能夠計算外科設備206的軌跡,并將所計算的軌跡顯示,通常示為216。在一些實施方式中,十字線或目標可疊加在圖像218上以指示外科設備206將與掃描平面“S”相交的位置。在其他實施方式中,所計算的軌跡216可以紅色或綠色示出以指示導航狀態。例如,在外科設備206處于將與目標“T”相交的路徑上時,所計算的軌跡216將以綠色示出。在外科設備206不處于與交叉目標“T”相交的路徑上時,所計算的軌跡216將以紅色示出。控制器212還能夠通過用戶輸入外科設備類型、能量水平、以及治療持續時間來控制。外科設備類型、能量水平、以及治療持續時間能夠在顯示器214上顯示,如圖14A所示。在外科設備206與目標“T”相交時,虛擬消融區222投影在圖像218上,如圖14B所示。能量水平和治療持續時間則能夠由用戶調節,以及控制器212將調節虛擬消融區222以反映能量水平和治療持續時間的變化。下面將參照圖15-22描述基準跟蹤系統。在基準跟蹤系統中,控制器212從攝影機208接收基準圖像。控制器212還包括先前存儲于其上的攝影機208的攝影機校準和畸變系數、基準系統模型、以及攝影機-天線校準數據。在其他實施方式中,攝影機208的攝影機校準和畸變系數、基準系統模型、以及攝影機-天線校準數據能夠在導航過程期間輸入至控制器212中。基于基準圖像、攝影機208的攝影機校準和畸變系數、基準系統模型、以及攝影機-天線校準數據,控制器212能夠輸出消融針206的位置以及診斷幀速率、殘留誤差、和跟蹤狀態至顯示器214。在一些實施方式中,攝影機208和基準貼204之間的距離能夠在約5厘米至約20厘米的范圍內。在一些實施方式中,攝影機208和基準貼204之間的距離能夠在約1厘米至約100厘米的范圍內。圖15示出了控制器212所利用的基準追蹤算法的基本流程圖。如圖15所示,在步驟230中獲取圖像幀。在步驟231,控制器212通過使用攝影機校準和畸變系數校正透鏡畸變。由攝影機208獲取的圖像可呈現透鏡畸變,如圖16A所示。因此,在圖像能夠用于進一步計算前,圖像需要校正畸變。在導航過程中使用攝影機208前,攝影機208用于采集不同角度上棋盤狀圖案的多幅圖像。該多幅圖像和多個角度用于產生攝影機矩陣和畸變系數。控制器212然后使用攝影機矩陣和畸變系數來校正透鏡畸變。在步驟232中,控制器212在圖像幀中使用圖17的算法找到白色圓圈。如圖17所示,步驟241(圖18A)中所接收到的圖像幀在步驟243中使用動態閾值(參見圖18B)閾值化。在使用動態閾值時,在每個有效幀后,動態閾值算法針對下一幀使用在有效幀中發現的圓圈來計算新的閾值。使用在有效幀中發現的圓圈,控制器212基于下面公式(5)來計算新的閾值:閾值=(黑圓圈強度平均+白圓圈強度平均)/2(5)可使用預定閾值來獲取初始有效幀,其然后用于計算新的閾值。可替代的,控制器212可通過測試閾值區間來直至發現某閾值產生有效幀,從而掃描到初始閾值。一旦發現了初始閾值,控制器212將基于有效幀使用公式(5)以得到動態閾值。在其他實施方式中,可使用固定閾值。固定閾值可以是存儲在控制器212中的預定數字或它可以通過測試閾值區間直至發現導致有效幀的閾值來確定。在閾值和自動增益控制施加至圖像后,在步驟244中執行連接域分析以發現閾值化圖像中的所有對象。在步驟245,將幾何過濾器應用至連接域分析的結果以及圖像幀。幾何過濾器計算對象的尺寸和形狀,并僅保持圓形及差不多合適尺寸的對象,如圖18C中所示。計算并存儲所有圓形對象的加權形心。返回圖15,除了在步驟232中找到白色圓圈外,控制器212還在步驟233中使用圖19描繪的算法來找到黑色圓圈。用于找到黑色圓圈的算法類似于圖17所示的用于找到白色圓圈的算法。為了找到黑色圓圈,在步驟241中接收到圖像幀后(參見圖20A),控制器212在步驟242中反轉圖像幀的亮度,如圖20B所示。然后,如上面關于圖17所述的,圖像如圖20C所示的閾值化,以及執行連通域分析,并利用幾何過濾器以獲得圖20D所示的圖像。在步驟248計算并存儲所有黑色圓圈的加權形心。此外,在步驟245,控制器212利用幾何過濾器來確定除圖像幀內黑色圓圈之外的黑色區域。控制器212在步驟249存儲已確定的黑色區域。在圖15的步驟234,控制器212使用圖21A所示的算法找到基準圖像和基準模型之間的對應關系。在圖21A所示的步驟251,控制器212使用拓撲限制來選擇四個白色圓圈,如圖21B所示。如圖21B所示,在步驟261,控制器212獲得圖19的步驟249中存儲的黑色區域并獲得圖17的步驟246中存儲的白色圓圈。控制器212則在步驟263中選擇第一黑色區域以及在步驟264中計算第一黑色區域中的白色圓圈數量。在步驟265,控制器212確定這些位于選定黑色區域中的圓圈是否匹配預定數量的圓圈。如果圓圈數量不匹配預定數量的圓圈,則算法行進至步驟266,其中選擇下一黑色區域,以及下一黑色區域的圓圈將在步驟264中再次計數。該過程重復直至步驟264中的圓圈數目匹配圓圈的預定數目。一旦步驟264中計數的圓圈數目匹配圓圈的預定數目,則算法行進至步驟267,在該處完成拓撲限制算法。在其他實施方式中,控制器212通過選擇四個最圓的圓圈來選定四個白色圓圈。在選擇了四個圓圈后,它們使用步驟252中凸殼算法以順時針順序布置。針對實向量空間V中點集X的凸殼或凸包絡是含有X的最小凸集。在所有點位于一條直線上時,凸殼是連接最外側兩點的線段。在平面情形中,凸殼是凸多邊形,除非所有點位于相同直線上。類似的,三維中,凸殼通常是最小凸多面體,其含有該集中的所有點。另外,模型中四個匹配基準點也以順時針順序布置。在步驟253,計算平面單應矩陣。在計算了平面單應矩陣后,使用該單應矩陣來將基準模型轉換為圖像坐標,其使用圖22所示的四個對應基準模型以找到最近的匹配圖像基準點(步驟254和255)。控制器212還在步驟256中計算殘留誤差。該算法使用產生的3D變換來將3D基準模型轉換為2D圖像。它然后將映射在2D圖像中的基準點之間的距離與2D圖像中探測的基準點對比。該殘留誤差是像素平均距離。該誤差用于檢驗精度以及部分地確定紅色/綠色導航狀態。控制器212則選擇最匹配和最小殘留誤差的模型。為了更加精確的結果,需要最小數量的黑色基準點匹配(例如,三個)。在圖15的步驟235中,執行攝影機的位姿評估。攝影機位姿評估包括計算攝影機和選定模型之間的3D變換,其通過迭代地將模型基準變形至基準圖像平面上以及最小化像素殘留誤差。目標是找到誤差函數的全局最小值。會發生的一個問題是誤差函數中出現的顯著的局部極小值(例如,從左側成像的天線看上去類似于從右側成像的天線),這需要避免。控制器212通過從多個起始點執行最小化以及選擇具有最小誤差的結果來避免局部極小值。一旦計算了3D變換,控制器能夠使用該3D變換來將外科設備206的坐標轉換至模型空間,并將外科設備206顯示為顯示器214中的虛擬外科設備206a。由于對象邊界在不同照明條件下擴展和收縮,傳統的方角基準點會基于照明條件變化。基準貼204使用黑色和白色圓圈,以及因此不會被該問題牽制,因為圓圈的中心始終保持一樣并持續良好的工作以計算加權形心。其他對比圖像或顏色也是能預料的。在本發明的另一實施方式中,以及如圖23所示,提供了計劃和導航系統300。系統300包括計劃系統302和導航系統304,它們連接至控制器306。控制器306連接至顯示器308,其可包括單個顯示屏或多個顯示屏(例如,兩個顯示屏)。計劃系統302類似于計劃系統100,以及導航系統304類似于導航系統200。在系統300中,顯示器308顯示上面所描述的計劃操作和導航操作。計劃操作和導航操作可以作為屏幕分割布置顯示在單個顯示屏上,計劃操作和導航操作可顯示在獨立屏幕上,或計劃操作和導航操作可顯示在相同屏幕上以及用戶可在各視圖之間切換。控制器306可從計劃系統引入劑量設置,并在導航操作期間使用該劑量設置來顯示消融區維度。在本發明的其他實施方式中,CT導航和軟件可以集成于計劃系統100。轉向圖24、25A和25B,計劃和導航系統通常以400示出。系統400包括圖像獲取設備402,其獲取患者“P”的CT圖像,具有電磁基準428和/或光學基準438。CT圖像以DICOM格式提供至計劃系統404,其類似于計劃系統100。計劃系統400用于確定如上所述的治療計劃,以及該治療計劃提供至控制器408并在顯示器410上作為計劃屏412顯示,如圖26所示。導航系統406可利用圖25A所示的電磁跟蹤系統、紅外線跟蹤系統、或圖25B所示的光學跟蹤系統。轉向圖25A,導航系統420包括電磁場發生器422、具有電磁換能器426的外科設備424、以及布置在患者上的電磁基準428。場發生器422發射電磁波,其由外科設備424和電磁基準428上的電磁傳感器(未明確示出)探測,以及然后用于計算外科設備424和電磁基準428之間的空間關系。該空間關系可由場發生器422計算,或場發生器422可提供數據至控制器408以計算消融針424和電磁基準428之間的空間關系。圖25B描繪了可替代的導航系統430,其類似于上面圖13所述的導航系統。在圖25B中,光學基準或基準點438置于患者上。附接至外科設備424的攝影機436采集基準點438的圖像并傳輸該圖像至控制器408以確定消融針關于基準點438的位置。在從導航系統406接收數據后,控制器408可將外科設備424的位置與CT圖像關聯,從而將外科設備424導航至目標“T”,如下文所述。在該情形中,患者基準(任意類型)上可具有不透射線的標記,以及允許CT期間可視化。這允許控制器將患者CT圖像坐標系關聯至器械跟蹤坐標系。控制器408和顯示器410彼此協作以將CT圖像顯示在導航屏440上,如圖27所示。如圖27所示,顯示屏440包括橫向視圖442、冠狀圖444、以及矢狀圖446。每個視圖包括目標“T”和消融區452(包括邊際)的視圖。橫向視圖442、冠狀圖444、以及矢狀圖446,消融區452全部從計劃系統404引入。另外,所有計劃元件(例如,設備選擇、能量水平、以及治療持續時間)自動的傳輸至導航屏440。導航屏440也是圖形用戶接口,其允許用戶調節設備選擇、能量水平、以及治療持續時間。導航引導屏448設置在顯示屏440上以輔助將消融針導航至目標“T”。基于從導航系統406接收的數據,控制器能夠確定外科設備424是否與目標“T”對準。如果外科設備424沒與目標“T”對準,則圓圈454將偏離外圓圈453的中心。用戶然后將調節外科設備424的進入角直至圓形454的中心與外圓圈453的中心對準。在一些實施方式中,在圓圈454的中心與外圓圈453的中心不對準時,圓圈454可顯示為紅色圓圈,或者在圓圈454的中心與外圓圈453的中心對準時,圓圈454可顯示為綠色圓圈。另外,控制器408可計算目標“T”和外科設備424之間的距離。在圖28描述的另一實施方式中,控制器408將虛擬外科設備424a疊加在3D渲染圖像上,并在屏幕462上顯示該組合圖像。類似于上面所述的方法,用戶能夠將圓圈453的中心與圓圈454的中心對準以將外科設備424導航至目標“T”。可替代的,用戶能夠通過觀察屏幕462上虛擬外科設備424a來確定外科設備424關于目標“T”的位置,從而將外科設備424導航至目標“T”。圖29描繪了本發明的另一實施方式,類似于上面的屏幕462,在圖29的實施方式中,屏幕472描繪與先前采集并渲染的CT圖像成空間關系的虛擬外科設備424a。CT圖像已經容積渲染以劃界目標“T”及另外的結構、血管、和器官。通過對目標“T”及另外的結構、血管、和器官容積渲染,用戶能夠將外科設備424導航進入患者,而同時避開了另外的結構、血管、和器官以阻止不必要的傷害。應該理解的是,前面描述僅是本發明的示意性描述。本領域技術人員能夠做出各種替代和修改而不偏離本發明的范圍。因此,本發明旨在包含所有這些替代、修改和變體。參照附圖所述的實施方式僅呈現以示范本發明的某些實例。與上面所述的那些和/或權利要求書中基本不同的其他元件、步驟、方法和技術也旨在包括在本發明的范圍內。當前第1頁1 2 3
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1