一種卟啉脂質體放射性藥物99mTc?TexaphyrinNPs及其制備方法與流程
本發明涉及腫瘤診斷放射性藥物,特別涉及一種卟啉脂質體放射性藥物99mtc-texaphyrinnps及其制備方法。
背景技術:
分子探針是分子影像技術的核心研究內容之一。近年來,用放射性核素、熒光染料、順磁和超順磁材料等標記的用于不同顯像模態的分子探針的研究成幾何量級增長。與傳統小分子探針相比,納米分子探針具有整合多元化功能與設計、藥物包裹于運載、體內循環時間長及能夠通過epr(enhancedpermeabilityandretentioneffect)效應被動靶向腫瘤等特點,從而可以增加藥物的抗癌功效并減小毒副作用。基于納米分子探針的多功能特性可以為臨床醫學提供一個集早期診斷、實時監測、定位診斷與個性化干預于一體的診治系統。納米探針的研究已經成為現代醫學發展的重要方向之一,但是過去的納米材料絕大多數是無機的,不僅難以降解,而且對人體會有微量毒性。脂質分子作為生物體組成的主要成分具有無可比擬的生物相容性,其自組裝形成的納米結構無論從均一性、穩定性,以及重復性方面,都有很大的優勢。在美國食品與藥物管理局(fda)現已批準使用和投入市場的若干種類的納米材料中,脂質體是目前應用最為普及的納米藥物制劑形式。
2011年,加拿大多倫多大學的鄭崗教授研究組構建了一種全新的、無毒的、可生物降解、具有高度靈敏度、由卟啉雙分子層自組裝形成的新型脂質體-卟啉納米囊泡(命名為porphysome)。porphysome的內層和外層都是由磷脂類物質構成,具有極好的酶生物降解性;而中間夾層中起作用的是天然卟啉衍生物,無毒可降解,對人體無害。porphysome的多功能特征體現在:一方面它本身是一種光敏劑,可用于pdt治療(光動力治療),當這種有機納米藥物到達腫瘤部位后,用激光照射腫瘤部位,這種藥物可以讓腫瘤組織中存在的基態氧轉為殺傷力極強的激發態氧,對腫瘤產生殺傷。另一方面,這種納米顆粒由8萬多個分子組成,密度很高,本身又具有光熱性功能,能用于光熱治療。此外,porphysome還可以用于癌癥的早期診斷。其組成成分之一的卟啉分子(此處為四氮環卟啉),一方面有熒光特征,能進行熒光成像。另一方面它也是優良的金屬螯合劑,其中心的四個氮原子可以與許多二價金屬離子結合生成非常穩定的有機絡合物。鄭崗課題組將porphysome標記了放射性核素64tc,并在原位前列腺腫瘤小鼠模型成功進行了pet顯像(positronemissioncomputedtomography,正電子發射計算機斷層顯像)。porphysome有非常良好的生物安全性及理化性質,在開發診治結合的多功能分子探針方面有極大的應用前景。但是目前所用的porphyrin(四氮環卟啉)不能與核磁增強劑gd及放射性核素177lu等3價金屬離子形成穩定的絡合物,限制了它在核磁成像以及核醫學顯像和治療等領域的進一步開發。
1988年美國德克薩斯大學(奧斯汀)的j.l.sessler教授領導的研究小組合成出一種稱為texaphyrin(原意為德克薩斯卟啉)的擴展卟啉。texaphyrin是一類三吡咯五氮雜環的卟啉衍生物(也可簡稱為5n卟啉),它能與三價金屬gd3+螯合獲得一種螯合有gd的卟啉衍生物gadoliniumtexaphyrin(gd-tex)。gd-tex可以選擇性地在腫瘤組織聚集,能用于磁共振成像(mri,magneticresonanceimaging)進行體內組織定位。相對之前提到的4n卟啉,texaphyrin具有五氮雜環,能夠與超過28種金屬離子形成穩定的1:1化合物,其中不但包括許多二價過渡金屬,也包括許多特別是三價的鑭系金屬離子。最近,一種新型錳(ii)-5n卟啉-磷脂脂質體被用于mri的成像研究,同時5n卟啉磷脂也被證實可以與多種金屬離子形成穩定的化合物。目前,尚沒有5n卟啉-磷脂脂質體使用單光子發射核素直接標記方法,也沒有5n卟啉-磷脂脂質體放射性標記物在單光子斷層成像(single-photonemissioncomputedtomography,spect)領域中的的體內應用。
技術實現要素:
本發明的目的是提供一種卟啉脂質體放射性藥物99mtc-texaphyrinnps及其制備方法,所述放射性藥物以德克薩斯卟啉-磷脂化合物、膽固醇、大豆氫化磷脂和磷脂-聚乙二醇2000為原料,且該藥物的制備過程中不需要連接在常規標記中所需要的任何雙功能螯合劑,如dtpa(二乙基三胺五乙酸)、hynic(6-叔丁氧羰肼基煙酸)等,放射性核素99mtc標記在不需要連接任何小分子多功能螯合劑的情況下實現自身標記形成99mtc-texaphyrinnps。該藥物能夠以被動靶向的方式濃聚到具有epr效應的腫瘤部位中,利用核醫學的spect顯像技術,可對腫瘤或其他具有epr效應的疾病進行顯像診斷和檢測。
本發明的目的是通過以下技術方案實現的:
一種卟啉脂質體放射性藥物99mtc-texaphyrinnps,包括納米材料和放射性核素99mtc,所述納米材料是由texaphyrin-lipid組成的脂質體納米脂質體,即texahyrinnps,所述放射性核素99mtc標記在不需要連接任何小分子多功能螯合劑的情況下實現自身標記形成99mtc-texaphyrinnps,所述texaphyrinnps放射性藥物為淡黃色透明注射針劑。
所述的卟啉脂質體放射性藥物99mtc-texaphyrinnps的制備方法,包括以下步驟:
1)texaphyrinnps納米材料的制備
將德克薩斯卟啉-溶血磷脂(texaphyrin-lipid)、膽固醇、氫化大豆磷脂和二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000(dspe-peg2000)充分溶于三氯甲烷中,通過減壓旋轉蒸發儀緩慢蒸干溶劑并在茄型瓶內壁上均勻形成磷脂薄膜,在真空干燥器中過夜除去任何有機溶劑,在瓶中加入ph為5.5的醋酸銨緩沖溶液,水化在55攝氏度的水浴超聲中進行,直至脂膜溶解,制備粗制的脂質體溶液,將所述粗制的脂質體溶液通過裝有雙層100nm孔徑聚碳酸酯膜的morgecle-15脂質體擠出器進行多次擠出,擠出溫度為55攝氏度,擠出液用ph為5.5的醋酸銨緩沖溶液配置成濃度為0.4mg/ml的texaphyrinnps溶液,最后經過pvdf濾膜過濾進行無菌分裝,即得到所述texaphyrinnps納米材料;
2)99mtc-texaphyrinnps的制備
將步驟1)制備得到的texaphyrinnps納米材料置于1.5ml的小管中,加入tppts和na[99mtco4],將反應液置于60℃的空氣浴或金屬浴加熱器中反應15-20分鐘,反應結束后室溫冷卻10分鐘,加入1ml磷酸鹽緩沖液,制成所述的卟啉脂質體放射性藥物99mtc-texaphyrinnps,通過超濾方法進行純化,經過放射性薄層層析或放射性高效液相色譜鑒定標記物的放射化學純度。
進一步的,步驟1)中所述德克薩斯卟啉-溶血磷脂(texaphyrin-lipid)、膽固醇、氫化大豆磷脂和二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000,各組分的摩爾比例分別為30%:30%:35%:5%。
進一步的,步驟2)中所述放射性薄層層析的方法為:展開紙選用長10cm、寬1.5cm的agilentitlc-sg硅膠玻璃纖維快速展開紙,樣品點于1cm處,用生理鹽水溶液進行展開,展開至9cm處將紙條取出自然晾干,展開后的紙條用bioscanar-2000進行檢測,其中,原點為99mtc的標記物,前沿為游離的99mtc離子。
進一步的,步驟2)中所述放射性高效液相色譜檢測方法為:使用安捷倫1260infinityhplc系統配備superose-12排阻柱,流動相為1ml/min的0.01m,ph為7.0的醋酸銨緩沖液,淋洗時間為30min,99mtc標記的納米標記物的保留時間為7分鐘,游離的99mtc的保留時間為15分鐘。
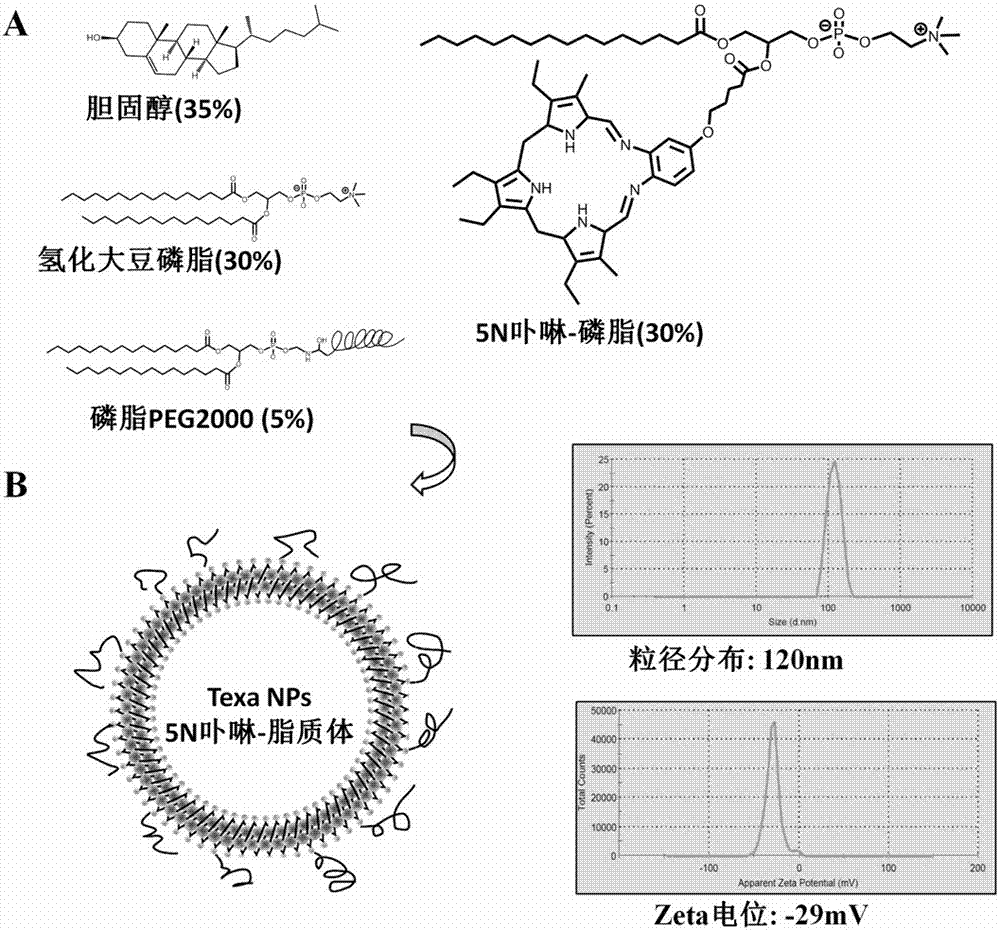
這里報道的5n卟啉-磷脂(texaphyrin-lipid)結構及5n卟啉脂質體的組成為(圖1a),在本發明中設計的5n卟啉具有親脂性,溶血磷脂上的羥基與5n卟啉上的羧基共價連接,形成一頭親水一頭親脂的雙親結構。5n卟啉磷脂具有類似一般磷脂的特點,可以形成類似脂質體的自組裝結構并且也可以作為脂質體的原料之一形成不同的脂質體。5n卟啉脂質體的結構示意圖及粒徑和電位為(圖1b)。5n卟啉具有多種金屬核素螯合的潛力并在制備成texaphyrinnps納米探針后可實現99mtc的固有直接標記并用于體內研究。
本發明相比現有技術的有益效果為:
1、本發明所述的卟啉脂質體放射性藥物,在制備過程中不需要連接在常規標記中所需要的任何雙功能螯合劑(如dota、hynic等),放射性核素99mtc標記在不需要連接任何小分子多功能螯合劑的情況下實現自身標記形成99mtc-texaphyrinnps;
2、本發明所述的卟啉脂質體放射性藥物用于具有epr效應的疾病中spect顯像,實現該新型納米材料診治一體化中“診”的目的;
3、本發明所述的卟啉脂質體放射性藥物可藥盒化,在德克薩斯卟啉脂質體中加入還原劑三苯基膦三間磺酸鈉鹽(3,3′,3″-phosphanetriyltris(benzenesulfonicacid)trisodiumsalt,tppts)和放射性核素99mtc后進行加熱即可實現固有標記;
4、本發明所述的卟啉脂質體放射性藥物能夠以被動靶向的方式濃聚到具有epr效應的腫瘤部位中,利用核醫學的spect顯像技術,可對腫瘤或其他具有epr效應的疾病進行顯像診斷和檢測。
以下結合附圖及實施例對本發明作進一步說明。
附圖說明
圖1為texaphyrinnps納米材料的組成成分、化學結構及摩爾占比(a)及texaphyrinnps納米探針的自組裝示意圖和該探針的粒徑表征和電位表征(b);
圖2為純化后的texaphyrinnps納米材料與普通脂質體為對照品的放射性hplc和itlc結果圖(a),99mtc-texaphyrinnps與對照實驗組標記情況對比(b);
圖3為99mtc-texaphyrinnps在c57b/l6小鼠路易斯肺癌皮下模型中于注射后4h和12h的生物分布;
圖4為99mtc-texaphyrinnps在c57b/l6小鼠路易斯肺癌皮下模型中注射后2、4、6和8h后的nanospect/ct的3d-mip顯像圖(虛線圈與箭頭指示腫瘤位置)。
具體實施方式
實施例1
1材料:
氫化大豆磷脂(hspc)和膽固醇(cholesterol)購自上海艾韋特醫藥科技有限公司(avt)。德克薩斯卟啉磷脂由多倫多大學醫學生物物理學系提供。二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000購自美國avantipolarlipids公司。醋酸和醋酸銨購自美國sigma-aldrich。tris(3-sulfonatophenyl)phosphinesodiumsalt(tppts)購自中國j&k百靈威科技有限公司。na99mtco4購自中國原子高科股份有限公司。
2方法與結果
2.1放射化學純度方法
itlc方法:選用agilentitlc-sg硅膠玻璃纖維紙,裁剪為長為10厘米,寬為1.5厘米的長方形紙條。將樣品點于1cm處,用生理鹽水溶液進行展開,展開至9cm處將紙條取出自然晾干。展開后的紙條用bioscanar-2000進行檢測。
hplc檢測方法:使用安捷倫1260infinityhplc系統配備superose-12排阻柱,流動相為1ml/min的0.01m,ph為7.0的醋酸銨緩沖液。淋洗時間為30min,99mtc標記的納米標記物的保留時間為7分鐘,游離的99mtc的保留實際那為15分鐘。
2.2texaphyrinnps納米材料的制備
將2mg德克薩斯卟啉-溶血磷脂(texaphyrin-lipid),0.86mg膽固醇,1.5mg大豆氫化卵磷脂(hspc)和二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000(dspe-peg2000)充分溶于5ml三氯甲烷,各組分的摩爾比例分別為30%:30%:35%:5%。圖1-a為texaphyrinnps脂質體納米材料的組成成分、化學結構及摩爾比例(a)。通過減壓旋轉蒸發儀緩慢蒸干溶劑并在茄型瓶內壁上均勻形成磷脂薄膜,在真空干燥器中過夜除去任何有機溶劑。在瓶中加入4mlph為5.5的醋酸銨緩沖溶液(0.1m,經過chelex100樹脂除離子)。水化在55攝氏度的水浴超聲中10分鐘,直至脂膜溶解,制備粗制的脂質體溶液。將脂質體溶液通過裝有雙層100nm孔徑聚碳酸酯膜的morgecle-15脂質體擠出器進行多次擠出,擠出溫度為55攝氏度。擠出液用ph為5.5的醋酸銨緩沖溶液(0.1m)配置成濃度為0.4mg/ml的texaphyrinnps溶液,經過0.22μm的pvdf濾膜過濾進行無菌分裝,即得到所述的texaphyrinnps納米材料。產物用nanozs90動態光散射儀進行粒徑和電位的表征。圖1-b為texaphyrinnps脂質體納米材料的自組裝示意圖和該探針的粒徑表征和電位表征,其粒徑為100nm,其點位為-29mv。
2.399mtc-texaphyrinnps的制備
將含有100μg的所述texaphyrinnps納米材料置于1.5ml的小管中,加入2.5mg的tppts和1.1gbq的na[99mtco4],置于60攝氏度的空氣浴加熱器中加熱20分鐘。制備的99mtc-texaphyrinnps使用超濾的方法進行純化,超濾裝置為15ml的millipore(mwco=100k)的超濾管。樣品用生理鹽水稀釋至2ml后進行超濾除游離99mtc,相對離心力為3000g,時間為15min。超濾純化共進行2次。對照樣品為使用同樣方法制備并標記的普通脂質體(65%氫化大豆軟磷脂,30%膽固醇和5%dspe-peg2000)。樣品通過itlc方法進行分析并用hplc方法進行驗證。圖2-a為99mtc-texaphyrinnps和陰性對照標記的普通脂質體liposomes的放射性hplc結果圖和放射性itlc結果圖。在放射性hplc檢測中,99mtc-texaphyrinnps的保留時間為7min,對照陰性標記物的保留時間為15min。在放射性itlc檢測中,99mtc-texaphyrinnps的相對遷移率(rf)為0,對照陰性標記物的相對遷移率為0.8。圖2-b為陰性對照標記的liposomes,99mtc-texaphyrinnps及兩種原料(texaphyrinnps,tppts)的單獨標記對照。結合對照實驗標記結果表明,99mtc-texaphyrinnps標記效率較高,并且texaphyrinnps是在tppts作為99mtc還原劑時才能有效標記,說明該標記結果不是通過對高锝酸分子99mtco4-的包裹造成的。
2.499mtc-texaphyrinnps在荷瘤鼠生物分布
將c57b/l6荷lewis小鼠肺癌皮下模型小鼠隨機分成若兩組,每組2只。各組實驗小鼠分別經尾靜脈注射100ml(740kbq)的99mtc-texaphyrinnps,于注射后4小時和12小時分別處死實驗小鼠,取血及主要臟器,稱重并測量放射性計數,經衰變校正后計算每克組織百分注射劑量率(%id/g)。在小鼠體內,肝和脾id%/g最高,符合納米材料的肝脾攝取。在注射后12小時,血液的%id/g仍然保持較高的水平,符合peg2000修飾表面后的隱形脂質體的血液長循環性。在所觀察的時間內,腫瘤攝取明顯高于肌肉等正常組織。
2.599mtc-texaphyrinnps在荷瘤鼠中的spet/ct成像
將將c57b/l6荷lewis小鼠肺癌皮下模型小鼠隨經尾靜脈注射100ml(~37mbq)99mtc-texaphyrinnps,于注射后于注射后2,4,8和12小時在medisonanospect/ct顯像系統中進行spect/ct顯像。圖4顯示了99mtc-texaphyrinnps在c57b/l6小鼠路易斯肺癌皮下模型中注射后2、4、8和12小時的3d-mip全身顯像圖。在注射后2小時的顯像圖中,我們可以看到小鼠心臟部位和頸部血管的血池,說明了藥物在體內的長循環性。在小鼠全身3d顯像中,可以看到標記物在腫瘤與肝、脾組織有明顯攝取。在全部顯像時間點中,均能清晰看到標記物在腫瘤部位有明顯濃聚,能清晰分辨腫瘤位置。
綜上所述,基于新型卟啉納米texaphyrinnps的卟啉脂質體放射性藥物99mtc-texaphyrinnps有用于全身spet/ct檢測腫瘤的應用潛力。
- 還沒有人留言評論。精彩留言會獲得點贊!