一種化學反應氣體的實驗裝置的制作方法
本發(fā)明涉及一種實驗裝置,尤其是一種化學反應氣體的實驗裝置,屬于化學試驗技術(shù)領(lǐng)域。
背景技術(shù):
在中學化學反應試驗中,濃、稀硝酸分別與銅反應的演示試驗視覺不理想,兩個反應的產(chǎn)物分別為紅棕色二氧化氮氣體與無色一氧化氮氣體。但是在傳統(tǒng)試驗中兩個反應都會出現(xiàn)紅棕色的氣體,這直接影響學生感性認識,使得學生易產(chǎn)生誤解,時常會有“濃硝酸與銅反應生成二氧化氮氣體,還是稀硝酸與銅反應生成二氧化氮氣體”這樣的問題產(chǎn)生。而事實上,應是稀硝酸與銅反應生成無色的一氧化氮氣體,濃硝酸與銅反應生成紅棕色的二氧化氮氣體,無色一氧化氮、紅棕色的二氧化氮涇渭分明,教科書上傳統(tǒng)的試驗操作存在弊端,造成稀硝酸與銅反應生成無色一氧化氮氣體有顏色的罪魁禍首是反應器中的空氣,所以微熱后生成的一氧化氮氣體會很快變?yōu)槎趸獨怏w,干擾了試驗觀察效果,這直接影響學生感性認識,達不到教學的預期效果。此外,化學反應放出的二氧化氮氣體以及一氧化氮氣體對環(huán)境污染嚴重,且反應不能控制,同時,在演示的過程中,在試管31口不易觀察到紅棕色氣體,為了更加直觀,不影響學生感性認識,就要使用大量的化學試劑,而這樣就造成浪費,污染嚴重,不利于形成環(huán)保意識,長期進行試驗,操作員很可能會出現(xiàn)呼吸道感染等病癥,影響身心健康。
專利號為cn201620227003的專利公開了一種濃、稀硝酸與銅反應的對比實驗裝置,解決了現(xiàn)有的實驗裝置存在的缺點,但其也存在一些不足之處,實驗裝置中沒有將氧氣或空氣排盡,生成的一氧化氮氣體會很快變?yōu)槎趸獨怏w,干擾了實驗觀察效果,也不能確保濃硝酸與銅反應只生成二氧化氮,稀硝酸與銅反應只生成一氧化氮,實驗準確度不高,不能更加直觀上區(qū)分兩者反應及反應物理化性質(zhì)的不同,該實驗中僅限于金屬銅,沒有其他金屬,不能使得學生了解和掌握其他金屬與稀、濃硝酸發(fā)生反應生氣何種氣體。
技術(shù)實現(xiàn)要素:
本發(fā)明正是針對現(xiàn)有技術(shù)存在的不足,提供一種化學反應氣體的實驗裝置。
為解決上述問題,本發(fā)明所采取的技術(shù)方案如下:
一種化學反應氣體的實驗裝置,包括氣體發(fā)生裝置和氣體驗證裝置;
所述氣體發(fā)生裝置包括第一容器,所述第一容器上端口安裝有第一密封塞,所述第一密封塞插裝有第一連接管和第一棒桿,所述第一棒桿的下端插入第一容器內(nèi),所述第一連接管的一端伸入第一容器上端口、另一端連接有透明無色氣球,所述第一連接管與透明無色氣球之間設置有控制氣體流通的第一鐵夾,所述第一棒桿的下端部固裝有第一金屬絲;
所述氣體驗證裝置包括第三容器,所述第三容器上端口安裝有第三密封塞,所述第三密封塞插裝有第三連接管和試管,所述第三連接管連接推進容器,所述第三連接管與推進容器之間設置有控制氣體流通的第三鐵夾;
所述透明無色氣球連接氣體驗證裝置的第三連接管,所述透明無色氣球與第三連接管之間設置有控制氣體流通的第四鐵夾。
作為上述技術(shù)方案的改進,所述實驗裝置還包括預處理裝置,所述預處理裝置包括第二容器,所述第二容器上端口安裝有第二密封塞,第二密封塞插裝有第二連接管和第二棒桿,所述第二棒桿的下端部固裝有第二金屬絲,所述第二連接管上設置有控制氣體流通的第二鐵夾;所述第二連接管連接氣體發(fā)生裝置中的第一密封塞。
作為上述技術(shù)方案的改進,所述第一金屬絲為不活潑金屬絲,所述第一容器內(nèi)盛裝有稀硝酸溶液,所述第一容器的下方設置有第一酒精燈。
作為上述技術(shù)方案的改進,所述第一金屬絲為銅絲。
作為上述技術(shù)方案的改進,所述第一金屬絲為活潑金屬絲,所述第一容器內(nèi)盛裝有稀硝酸溶液。
作為上述技術(shù)方案的改進,所述第一金屬絲為鐵絲。
作為上述技術(shù)方案的改進,所述第一金屬絲為不活潑金屬絲,所述第一容器內(nèi)盛裝有濃硝酸溶液。
作為上述技術(shù)方案的改進,所述第一金屬絲為銅絲。
作為上述技術(shù)方案的改進,所述第一金屬絲為活潑金屬絲,所述第一容器內(nèi)盛裝有濃硝酸溶液,所述第一容器的下方設置有第二酒精燈。
作為上述技術(shù)方案的改進,所述第一金屬絲為鐵絲。
作為上述技術(shù)方案的改進,所述第三容器為彈性容器。
作為上述技術(shù)方案的改進,所述第三容器內(nèi)盛裝有硫酸銅溶液。
作為上述技術(shù)方案的改進,所述第三連接管為t字形連接管。
作為上述技術(shù)方案的改進,所述試管為l形通孔狀,試管兩端分別放置有濕潤的脫脂棉和活性炭。
作為上述技術(shù)方案的改進,所第三容器的下方設置有振蕩器。
本發(fā)明與現(xiàn)有技術(shù)相比較,本發(fā)明的實施效果如下:
本發(fā)明所述一種化學反應氣體的實驗裝置,使得學生更加清晰直觀地觀察金屬與濃、稀硝酸反應過程和反應物,并且反應物能夠集中到透明無色氣球內(nèi),能更加清楚的觀察到無色的一氧化氮和紅棕色的二氧化氮,不易將兩者反應物混淆。
附圖說明
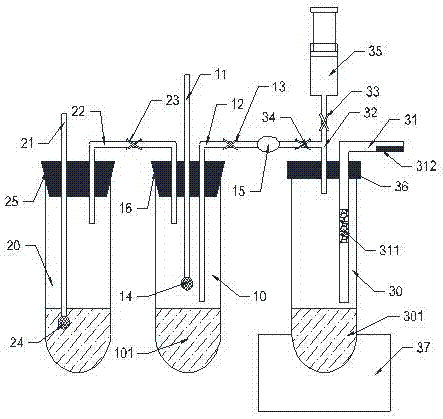
圖1為本發(fā)明一種化學反應氣體的實驗裝置的結(jié)構(gòu)示意圖;
圖2為本發(fā)明所述實驗裝置中一氧化氮實驗過程的結(jié)構(gòu)圖;
圖3為本發(fā)明所述實驗裝置中二氧化氮實驗過程的結(jié)構(gòu)圖;
圖4為本發(fā)明實施例一的化學反應實驗裝置結(jié)構(gòu)圖;
圖5為本發(fā)明實施例二的化學反應實驗裝置結(jié)構(gòu)圖;
圖6為本發(fā)明實施例三的化學反應實驗裝置結(jié)構(gòu)圖;
圖7為本發(fā)明實施例四的化學反應實驗裝置結(jié)構(gòu)圖。
具體實施方式
下面將結(jié)合具體的實施例來說明本發(fā)明的內(nèi)容。
如圖1所示,為本發(fā)明所述一種化學反應氣體的實驗裝置的結(jié)構(gòu)示意圖,包括預處理裝置、氣體發(fā)生裝置和氣體驗證裝置,所述預處理裝置包括第二容器20,所述第二容器20的上端口安裝有第二密封塞25,第二密封塞25插裝有第二棒桿21和第二連接管22,第二棒桿21的下端部固裝有第二金屬絲24,第二連接管22上設置有控制氣體流通的第二鐵夾23;所述氣體發(fā)生裝置包括第一容器10,所述第一容器10的上端口安裝有第一密封塞16,第一密封塞16插裝有第一棒桿11和第一連接管12,第一棒桿11的下端插入第一容器10內(nèi),第一連接管12的一端伸入第一容器10上端口、另一端連接有透明無色氣球15,第一連接管12與透明無色氣球15之間設置有控制氣體流通的第一鐵夾13,第一棒桿11的下端部固裝有第一金屬絲14;所述氣體驗證裝置包括第三容器30,所述第三容器30的上端口安裝有第三密封塞36,第三密封塞36插裝有第三連接管32和試管31,第三連接管32連接推進容器35,第三連接管32與推進容器35之間設置有控制氣體流通的第三鐵夾33;所述第二連接管22連接氣體發(fā)生裝置中的第一密封塞16,所述透明無色氣球15連接氣體驗證裝置的第三連接管32,所述透明無色氣球15與第三連接管32之間設置有控制氣體流通的第四鐵夾34。
所述第一容器10的上端口安裝有第一密封塞16,便于取放容器內(nèi)的液體,及清洗容器。
所述第二容器20的上端口安裝有第二密封塞25,便于取放容器內(nèi)的液體,及清洗容器。
所述第三容器30的上端口安裝有第三密封塞36,便于取放容器內(nèi)的液體,及清洗容器。
所述第三容器30為彈性容器,能夠?qū)ζ溥M行擠壓處理,氣體進入其內(nèi)部后還可復原,更利于直觀性的觀察。
所述第三容器30內(nèi)盛裝有硫酸銅溶液301,用于觀察及利于驗證所發(fā)生反應生成的氣體,強化對反應物性質(zhì)的認識,易于學生理解掌握要點。
所述第三連接管32為t字形連接管,縮短氧氣行走路徑,加快反應時間。
所述試管31為l形通孔狀,氫氣、氧氣等氣體能夠排出容器,而氧氣不會進入,試管31兩端分別放置有濕潤的脫脂棉311和活性炭312,用于檢測及吸附二氧化氮,避免進入外界,造成環(huán)境污染,脫脂棉為白色,利于觀察,活性炭312用于吸附,主要用于吸附試管31內(nèi)的少量有害氣體,防止污染環(huán)境以及對實驗者造成傷害。
所述第三容器30的下方設置有振蕩器37,便于觀察反應現(xiàn)象,了解反應過程,學生能夠更加直觀認識,以及強化對反應物性質(zhì)的認識。
推進容器35內(nèi)充滿氧氣,用于驗證實驗,氧氣與一氧化氮氣體發(fā)生反應生成紅棕色的二氧化氮,而氧氣與二氧化氮不發(fā)生反應,便于觀察反應現(xiàn)象及反應過程,學生能夠更加直觀認識,以及強化對反應物性質(zhì)的認識。
所述第二容器20內(nèi)盛裝有稀鹽酸溶液或稀硫酸溶液,第二棒桿21的下端部固裝有第二金屬絲24,第二金屬絲24為活潑金屬絲,如鐵、鋁等,能夠保證鐵、鋁等這些與稀鹽酸溶液或稀硫酸溶液反應只生成相對應的金屬鹽溶液和氫氣,且反應過程較為溫和,不易出現(xiàn)意外,第二金屬絲24為不活潑金屬絲,如銅等,銅與稀鹽酸溶液或稀硫酸溶液反應只生成相對應的金屬鹽溶液和氫氣,且反應過程較為溫和,不易出現(xiàn)意外,以上實驗試劑較為常用,容易購買,價格低。
【實施例一】,如圖4所示,所述第一金屬絲14為不活潑金屬絲,如銅絲141等,第一容器10內(nèi)盛裝有稀硝酸溶液101,所述氣體發(fā)生裝置還包括酒精燈,且第一酒精燈102位于第一容器10的下方,用于加熱,因為反應速率太低而需要加熱,來加快反應過來,銅與稀硝酸的化學反應方程式為:3cu+8hno3?3cu(no3)2+2no↑+4h2o,以上化學反應方程式中可知,銅與稀硝酸加熱反應生成一氧化氮。
【實施例二】,如圖5所示,所述第一金屬絲14為活潑金屬絲,如鐵絲142等,第一容器10內(nèi)盛裝有稀硝酸溶液101,反應時不需要加熱,即可發(fā)生化學反應,鐵與過量的稀硝酸的化學反應方程式為:fe+4hno3=fe(no3)3+no↑+2h2o,過量的鐵與稀硝酸的化學反應方程式為:3fe+8hno3=3fe(no3)2+2no↑+4h2o,以上化學反應方程式中可知,鐵與稀硝酸反應生成一氧化氮,且該反應過程不需要加熱,生成的一氧化氮與鐵的多少無關(guān),與稀硝酸的多少也無關(guān)。
【實施例三】,如圖6所示,所述第一金屬絲14為不活潑金屬絲,如銅絲141等,第一容器10內(nèi)盛裝有濃硝酸溶液103,反應時不需要加熱,即可發(fā)生化學反應,銅與濃硝酸的化學反應方程式為:cu+4hno3==cu(no3)2+2no2↑+2h2o,以上化學反應方程式中可知,銅與濃硝酸加熱反應生成二氧化氮。
【實施例四】,如圖7所示,所述第一金屬絲14為活潑金屬絲,如鐵絲142等,第一容器10內(nèi)盛裝有濃硝酸溶液103,反應時需要加熱,第一容器10的下方設置有第二酒精燈104,活潑金屬,如鐵在濃硝酸中會發(fā)生鈍化,生成一層致密而堅固的氧化物薄膜,從而阻止了內(nèi)部金屬的繼續(xù)反應,加熱后,氧化膜會被破壞,反應可以繼續(xù)進行,鐵與過量的濃硝酸的化學反應方程式為:fe+6hno3?fe(no3)3+3no2↑+3h2o,過量的鐵與稀硝酸的化學反應方程式為:fe+4hno3?fe(no3)2+2no2↑+2h2o,以上化學反應方程式中可知,鐵與濃硝酸反應生成二氧化氮,且該反應過程需要加熱,生成的二氧化氮與鐵量的多少無關(guān),與濃硝酸量的多少也無關(guān)。
本發(fā)明所述實驗裝置,其工作過程如下:
(1)一氧化氮實驗過程
首先進行預處理試驗,目的是除去容器中的氧氣,避免影響學生直觀認識,如圖2所示,第一容器10內(nèi)盛裝有稀硝酸溶液101,第一棒桿11下端部的第一金屬絲14位于第一容器10內(nèi)液面的上方,關(guān)閉第三鐵夾33,防止推進容器35內(nèi)的氧氣進入容器中,并對第三容器30進行擠壓處理,使其處于壓縮狀態(tài),打開第二鐵夾23、第一鐵夾13、第四鐵夾34,下移第二棒桿21,使其下端部的第二金屬絲24浸沒在第二容器20內(nèi)的稀鹽酸或稀硫酸溶液中,這時發(fā)生反應生成氫氣,最終氫氣會充滿第三容器30,且第三容器30鼓起,這樣能將各個容器中空氣盡數(shù)排出,以此達到除氧的目的,上移第二棒桿21,使其下端部的第二金屬絲24位于第二容器20內(nèi)液面的上方,停止發(fā)生化學反應,關(guān)閉第二鐵夾23、第四鐵夾34,擠壓第三容器30,使其處于壓縮狀態(tài),再打開第四鐵夾34,避免透明無色氣球15內(nèi)充滿氣體而鼓起,防止影響后續(xù)操作及判斷。
其次,關(guān)閉第四鐵夾34,下移第一棒桿11,使其下端部的第一金屬絲14浸沒在第一容器10內(nèi)的溶液中,兩者發(fā)生化學反應,透明無色氣球15變大,無顏色,即有無色氣體產(chǎn)生,得出該無色氣體不是二氧化氮,然后上移第一棒桿11,關(guān)閉第一鐵夾13,打開第四鐵夾34,無色氣體進入第三容器30,只能夠觀察到第三容器30慢慢鼓起,振蕩器37震蕩第三容器30,溶液顏色無變化,關(guān)閉第四鐵夾34,打開第三鐵夾33,第三容器30內(nèi)逐漸有紅棕色氣體生成,得出無色氣體在第三容器30內(nèi)與空氣中氧氣作用變成紅棕色氣體二氧化氮,隨著紅棕色氣體的生成,能夠觀察到第三容器30溶液逐漸變?yōu)榫G色,濕潤的脫脂棉311變成黃色,振蕩器37再次震蕩第三容器30,第三容器30溶液顏色變?yōu)樗{色,第三容器30雖有鼓起的現(xiàn)象,但仍處于擠壓狀態(tài),而銅離子呈藍色,二氧化氮溶解在水中呈黃色,兩者混合色為綠色,因此振蕩器37震蕩第三容器30后,溶液中的二氧化氮很快消失,能夠得出該紅棕色氣體為二氧化氮,再根據(jù)化合價守恒,得出第三容器30中的二氧化氮遇水生成硝酸和一氧化氮,從而再次驗證了金屬與稀硝酸反應生成無色的一氧化氮,而不是二氧化氮,并且一氧化氮遇到氧氣反應生成二氧化氮。
(2)二氧化氮實驗過程
首先進行預處理試驗,目的是除去容器中的氧氣,避免影響學生直觀認識,如圖3所示,第一容器10內(nèi)盛裝有濃硝酸溶液103,第一棒桿11下端部的第一金屬絲14位于第一容器10內(nèi)液面的上方,關(guān)閉第三鐵夾33,防止推進容器35內(nèi)的氧氣進入容器中,并對第三容器30進行擠壓處理,使其處于壓縮狀態(tài),打開第二鐵夾23、第一鐵夾13、第四鐵夾34,下移第二棒桿21,使其下端部的第二金屬絲24浸沒在第二容器20內(nèi)的稀鹽酸或稀硫酸溶液中,這時發(fā)生反應生成氫氣,最終氫氣會充滿第三容器30,且第三容器30鼓起,這樣能將各個容器中空氣盡數(shù)排出,以此達到除氧的目的,上移第二棒桿21,使其下端部的第二金屬絲24位于第二容器20內(nèi)液面的上方,停止發(fā)生化學反應,關(guān)閉第二鐵夾23、第四鐵夾34,擠壓第三容器30,使其處于壓縮狀態(tài),再打開第四鐵夾34,避免透明無色氣球15內(nèi)充滿氣體而鼓起,防止影響后續(xù)操作及判斷。
其次,關(guān)閉第四鐵夾34,下移第一棒桿11,使其下端部的第一金屬絲14浸沒在第一容器10內(nèi)的溶液中,兩者發(fā)生化學反應,透明無色氣球15變大,同時能夠觀察到變成紅棕色,即有紅棕色氣體產(chǎn)生,然后,上移第一棒桿11,關(guān)閉第一鐵夾13,打開第四鐵夾34,紅棕色氣體進入第三容器30,第三容器30鼓起,第三容器30內(nèi)的溶液變?yōu)榫G色,濕潤的脫脂棉311變成黃色,關(guān)閉第四鐵夾34,打開第三鐵夾33,第三容器30內(nèi)前后無明顯現(xiàn)象,第三容器30的壓縮狀態(tài)也無明顯變化,說明第三容器30內(nèi)無一氧化氮,即得出上述反應中不產(chǎn)生一氧化氮,而是二氧化氮,關(guān)閉第三鐵夾33,振蕩器37震蕩第三容器30,第三容器30中的溶液變藍,紅棕色氣體逐漸消失,再次打開第三鐵夾33,第三容器30中逐漸出現(xiàn)紅棕色氣體,再次驗證上述反應中不產(chǎn)生一氧化氮,而是二氧化氮,同時得出二氧化氮遇水生成硝酸和一氧化氮,最后得出金屬與濃硝酸反應生成紅棕色二氧化氮,而不是無色的一氧化氮。
以上可知,金屬材質(zhì)與稀硝酸反應生成一氧化氮,而不是二氧化氮,同時,金屬材質(zhì)與濃硝酸反應生成二氧化氮,而不是一氧化氮,使得學生更加清晰直觀地觀察反應過程及反應物,以及反應物的性質(zhì),不易將兩者混淆,易于學生理解掌握要點,所述發(fā)生裝置結(jié)構(gòu)簡單,易于操作,便于區(qū)分,能夠合理處理上述反應中所產(chǎn)生的有害氣體一氧化氮和二氧化氮,不會進入外界環(huán)境,避免造成環(huán)境污染,而且實驗人員也不會吸入一氧化氮和二氧化氮有害氣體,不會危害其身體健康,安全性好,可放心進行試驗,還能控制實驗反應過程,獲得更多的觀察時間,節(jié)省試劑,
本發(fā)明所述一種化學反應氣體的發(fā)生裝置,使得學生更加清晰直觀地觀察金屬與濃、稀硝酸反應過程及反應物,并且反應物能夠集中到透明無色氣球內(nèi),能更加清楚的觀察到無色的一氧化氮和紅棕色的二氧化氮,不易將兩者反應物混淆,以及強化了對反應物性質(zhì)的認識,易于學生理解掌握要點,而且本發(fā)明結(jié)構(gòu)簡單,易于操作,無環(huán)境污染,安全性好,成本低,節(jié)省試劑,易于控制實驗反應過程,增強了實驗的趣味性和直觀性,有效激發(fā)學生的學習興趣。
顯然,本領(lǐng)域的技術(shù)人員可以對本發(fā)明進行各種改動和變型而不脫離本發(fā)明的精神和范圍。這樣,倘若本發(fā)明的這些修改和變型屬于本發(fā)明權(quán)利要求及其等同技術(shù)的范圍之內(nèi),則本發(fā)明也意圖包含這些改動和變型在內(nèi)。
- 還沒有人留言評論。精彩留言會獲得點贊!