利用糖基轉移酶的糖類化合物衍生物的制造方法與流程
本發明涉及一種利用糖基轉移酶的糖類化合物衍生物的制造方法。
本發明還涉及由此方法而制得的衍生物。
背景技術:
氨基酚類一般是制造糖類化合物衍生物的重要中間產物,同時也在制造染料及其他藥物的中間化學體時使用。此外,4-氨基苯酚在代謝過程中的容易氧化成細胞毒性物質,會引起腎臟鄰近血管的多種疾病。(Lock etc., Studies on the mechanism of 4-aminophenol-induced toxicity to renal proximal tubules. Hum. Exp.Toxicol. 12(5), 383-388, 1993.)
現有技術中已對4-氨基苯酚衍生物的有機合成方法進行了一定的研究。例如,4-[2-(5-甲基)]-氨基噻唑-2,3-D-tert-丁基酚(日本專利,專利號:67023/1987)和3-甲基-4-羥基-5-n-丙烯-7-氟苯并呋喃(日本專利,專利號:53980/1987)是以2-乙氧甲酰或者2-甲酸芐酯作為誘導前體合成的。而且,上述兩種化合物是制備治療哮喘等過敏性疾病藥物的有效成分。同時,2,6-二氯-4-氨基苯酚衍生物和2,6-二氯-4-(3,4,5-三甲氧基苯甲酰)氨基苯酚衍生物被認為是具有免疫活性的優良物質,并且能有效抵抗PCA(過敏反應)(日本專利 專利號:271268/1986)。另外,4-(十二烷基氨基苯酚)-2-乙二醇-6-tert-丁基酚,4-(十八烷基氨基苯酚)-2,6-D-tert-丁基酚被認為是具有良好的防止酸化的活性,同時也是有顯著效果的穩定劑(日本專利 專利號:24782/1971)。
氨基酚類物質在食品、化妝品、醫藥品行業中有廣泛的應用,然而這類物質往往具有水溶解性低,易被光或熱分解或氧化生成有毒化合物質等缺點。因此,為了提高這類化合物的功能性,改善并增強其穩定性成為研究的熱點。
此外,已知對苯二酚和熊果苷具有良好的美白效果,通過抑制細胞內酪氨酸酶的活性來抑制黑色素的生成,因而可改善雀斑和皮膚老化等問題。然而,這類活性物質對細胞的功能性存在一定損傷,會產生副作用。因此,本發明的目的是尋求新的合成方法制備酪氨酸酶抑制劑對苯二酚和熊果苷的衍生物,使其在細胞內能夠穩定地發揮作用而避免副作用的產生。嘗試的方法包括化學方法(Wang etc. A new synthesis of α-arbutin via Lewis acid catalyzed selective glycosylation of tetra-O-benzyl-α-D-glucopyranosyl trichloroacetimidate with hydroquinone, 341, 1945-1947, 2006)和酶合成方法(Sugimoto etc. Enzymatic Synthesis of α-arbutin by α-anomer-selective glucosylation of hydroquinone using lyophilized cells of xanthomonas campestris WU-9701, 93, 328-330, 2002; Sugimoto etc. Synthesis of α-arbutin-α-glycosides and their inhibitory effects on human tyrosinase, 99, 272-276, 2005)。但是,由于制備合成α-1~4結構物質的淀粉酶價格過于昂貴。
因此,需要提供一種新的技術方案來解決上述問題。
技術實現要素:
本發明要解決的技術問題是提供一種利用糖基轉移酶的糖類化合物衍生物的制造方法。
本發明還要解決的技術問題是提供一種由此方法而制得的衍生物。
為解決上述技術問題,本發明的利用糖基轉移酶的糖類化合物衍生物的制造方法,包括以下步驟:在含糖濃度為0.1-1M的溶液中添加糖基轉移酶,使反應釜的最終活性濃度達到0.1-3.0 U/mL后,然后在15-50℃的反應釜里添加由2-氨基酸,3-氨基酸,4-氨基酸,對苯二酚及熊果苷構成的組中所選擇的至少一種的糖基受體,使最終活性濃度達到質量百分含量0.01-3%并使其反應,反應是在28-37℃下經過1-18小時而形成的,糖的葡萄糖或果糖基轉移到上述的受體中最后經醋酸酸化可得到糖類化合物衍生物。注意,上述反應中糖會在15-50℃的條件下進行分解,而處于28-37℃的條件下時,在1-18小時內是不完全分解的。
進一步的,所述糖基轉移酶是由葡聚糖蔗糖酶及果聚糖蔗糖酶形成族群中選擇出來的。
進一步的,所述葡聚糖蔗糖酶是從腸系膜明串珠菌菌株或銀耳菌絲體中獲取的;將其接種到含有K2HPO4和糖的培養基上進行培養,經人工發酵培養后得到菌液,將上述菌液進行分離純化,采用離子交換色譜的方式得到葡聚糖蔗糖酶。上述方法也是目前獲得該酶的通用方法。
葡聚糖蔗糖酶可從腸系膜明串珠菌NRRL B-1299, NRRL B-742, NRRL B-1355, NRRL B-512, NRRL B-1149, NRRL B-1142等系列菌株中獲得,但本發明選用的是腸系膜明串珠菌(Leuconostoc mensenteroides) NRRL B-1299菌株。
所述果聚糖蔗糖酶是從腸系膜明串珠菌菌株中獲取的。將該菌株其接種到含有K2HPO4和糖的培養基上進行培養,經人工發酵培養后得到菌液,將上述菌液進行分離純化,采用離子交換色譜的方式得到果聚糖蔗糖酶。上述方法也是目前獲得該酶的通用方法。
果聚糖蔗糖酶可從腸系膜明串珠菌NRRL B-512(ATCC 10830), NRRL B-1299, NRRL B-742, NRRL B-1355, NRRL B-1149, NRRL B-1142等系列菌株中獲得,但本發明選用的是腸系膜明串珠菌NRRL B-512(ATCC 10830)菌株。
進一步的,糖基轉移酶是果聚糖蔗糖酶時,糖的果糖基轉移到上述糖的受體中;糖基轉移酶是葡聚糖蔗糖酶時,糖的葡萄糖轉移到上述糖的受體中。
進一步的,添加的糖基轉移酶使反應釜的最終活性濃度達到0.5-2.0 U/mL。
利用糖基轉移酶的糖類化合物衍生物的制造方法制得的衍生物,糖的受體是N-氨基酸時,生成N-氨基酸衍生物,N的取值2-4。
進一步的,糖基轉移酶是葡聚糖蔗糖酶,上述的糖的受體是對苯二酚時,生成下述化學式Ⅳ的對苯二酚衍生物。
進一步的,糖基轉移酶是果聚糖蔗糖酶,上述的糖的受體是對苯二酚時,生成下述化學式Ⅴ的對苯二酚衍生物。
進一步的,糖基轉移酶是葡聚糖蔗糖酶,糖的受體是熊果苷時,生成下述化學式Ⅵ的熊果苷衍生物。
進一步的,生成的熊果苷衍生物經醋酸酸化以后可生成下述化學式Ⅹ的五乙酰熊果苷。
本發明的有益效果:本發明中選取2-氨基苯酚、3-氨基苯酚、4-氨基苯酚、對苯二酚及熊果苷等物質作為糖受體,在葡聚糖蔗糖酶以及果聚糖蔗糖酶的催化作用下,利用反應基質中擴散分布的糖,使得選取的受糖體與糖發生反應,形成新的化合物。反應所得到的衍生物,其水溶解性以及光、熱穩定性均得以加強,功能性質得到改善,在食品添加劑、化妝品、醫藥品以及老年癡呆的治療等方面體現了巨大的應用潛力。
附圖說明
圖1為蔗糖溶液中,不同種類的氨基苯酚誘導物在葡聚糖這趟作用下反應所得產物的TLC分析的物質分布結果圖。
其中,S為蔗糖;F為果糖。
條帶1,0.3M蔗糖+ 2-aminophenol + L. mesenteroides NRRL 1299 葡聚糖蔗糖酶;條帶2,0.3M蔗糖+ 3-aminophenol + L. mesenteroides NRRL 1299 葡聚糖蔗糖酶;條帶3,0.3M 蔗糖+ 4-aminophenol +L. mesenteroides NRRL 1299 葡聚糖蔗糖酶。
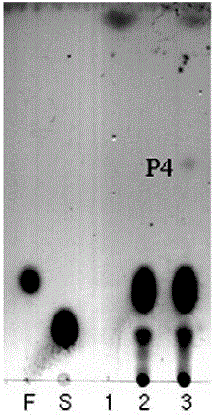
圖2 對苯二酚在葡聚糖蔗糖酶作用下生成物質的TLC分析結果圖。
其中,S為蔗糖;F為果糖。
條帶1,對苯二酚;
條帶2,0.3M蔗糖+緩沖液+ L. mesenteroides NRRL 1299 葡聚糖蔗糖酶;
條帶3,0.3M蔗糖+對苯二酚+ L. mesenteroides NRRL 1299 葡聚糖蔗糖酶。
圖3 對苯二酚在果聚糖蔗糖酶作用下生成物質的TLC分析結果圖。
其中,S為蔗糖;F為果糖。
條帶1,對苯二酚;條帶2, 0.3M蔗糖+緩沖液+L. mesenteroides NRRL 512 果聚糖蔗糖酶;條帶3, 0.3M蔗糖+對苯二酚+L. mesenteroides NRRL 512 果聚糖蔗糖酶。
圖4 熊果苷在葡聚糖蔗糖酶的作用下得到產物的TLC分析結果圖。
其中,S為蔗糖;F為果糖。
條帶1,0.3M 蔗糖+ 緩沖溶液+ L. mesenteroides NRRL 1299葡聚糖蔗糖酶;條帶2,0.3M 蔗糖 +熊果苷 + L. mesenteroides NRRL 1299 葡聚糖蔗糖酶。
圖5 本反應中的熊果苷與糖類物質反應產物結果分析圖。
條帶1,果糖;條帶2,酶反應物(無熊果苷);條帶3,酶反應物(有熊果苷);條帶4,熊果苷標準品;上述色譜分析結果用箭頭標明物質。
圖6a這個發明實例中得到的經提純后的分離物質熊果苷-G1的HPLC色譜分析圖譜圖。
圖6b這個發明實例中得到的經提純后的分離物質熊果苷-G2的HPLC色譜分析圖譜圖。
具體實施方式
為了加深對本發明的理解,下面對本發明作進一步詳述,該實施例僅用于解釋本發明,并不構成對本發明的保護范圍的限定。
下面實施例1-4是方法的實施例。
實施例1
本發明的利用糖基轉移酶的糖類化合物衍生物的制造方法,包括以下步驟:在含糖濃度為0.1M的溶液中添加糖基轉移酶,使反應釜的最終活性濃度達到0.1U/mL后,然后在15℃的反應釜里添加2-氨基酸,3-氨基酸,4-氨基酸,對苯二酚及熊果苷構成的組中所選擇的至少一種的糖基受體,使最終活性濃度達到質量百分含量0.01-3%并使其反應,反應是在28℃下經過1小時而形成的,糖的葡萄糖或果糖基轉移到上述的受體中最后經醋酸酸化可得到糖類化合物衍生物。
實施例2
利用糖基轉移酶的糖類化合物衍生物的制造方法,包括以下步驟:在含糖濃度為0.3M的溶液中添加糖基轉移酶,使反應釜的最終活性濃度達到0.5 U/mL后,然后在20℃的反應釜里添加由2-氨基酸,3-氨基酸,4-氨基酸,對苯二酚及熊果苷構成的組中所選擇的至少一種的糖基受體,使最終活性濃度達到質量百分含量0.01-3%并使其反應,反應是在32℃下經過8小時而形成的,糖的葡萄糖或果糖基轉移到上述受體中最后經醋酸酸化可得到糖類化合物衍生物。
實施例3
本發明的利用糖基轉移酶的糖類化合物衍生物的制造方法,包括以下步驟:在含糖濃度為0.5M的溶液中添加糖基轉移酶,使反應釜的最終活性濃度達到2.0 U/mL后,然后在25℃的反應釜里添加由2-氨基酸,3-氨基酸,4-氨基酸,對苯二酚及熊果苷構成的組中所選擇的至少一種的糖基受體,使最終活性濃度達到質量百分含量0.01-3%并使其反應,反應是在34℃下經過10小時而形成的,糖的葡萄糖或果糖基轉移到上述的受體中最后經醋酸酸化可得到糖類化合物衍生物。
實施例4
本發明的利用糖基轉移酶的糖類化合物衍生物的制造方法,包括以下步驟:在含糖濃度為1M的溶液中添加糖基轉移酶,使反應釜的最終活性濃度達到3.0 U/mL后,然后在50℃的反應釜里添加由2-氨基酸,3-氨基酸,4-氨基酸,對苯二酚及熊果苷構成的組中所選擇的至少一種的糖基受體,使最終活性濃度達到質量百分含量0.01-3%并使其反應,反應是在37℃下經過18小時而形成的,糖的葡萄糖或果糖基轉移到上述的受體中最后經醋酸酸化可得到糖類化合物衍生物。
糖基轉移酶是由葡聚糖蔗糖酶及果聚糖蔗糖酶形成族群中選擇出來的。
糖基轉移酶是果聚糖蔗糖酶時,糖的果糖基轉移到上述糖的受體中;糖基轉移酶是葡聚糖蔗糖酶時,糖的葡萄糖轉移到上述糖的受體中。
上述受糖體反應結束后所生成衍生物混合物經由凝膠滲透色譜層析柱(Gel permeation chromatography)進行初步分離,再用專用于右旋糖苷的P-2以及LH-20色度分析柱進行凝膠滲透色譜層析。然后,利用高效液相色譜(High performance Liquid Chromatography)將各受糖體的衍生物單獨分離出來。接著,利用核磁共振(NMR)和間串聯質譜(MALDI-TOP)等技術對各精制的糖類化合物衍生物進行結構分析。
下面實施例5-10是衍生物的實施例。
本發明的利用糖基轉移酶的糖類化合物衍生物的制造方法制得的衍生物,糖的受體是N-氨基酸時,生成N-氨基酸衍生物,N的取值2-4。
葡聚糖蔗糖酶的酶反應液中,除了糖類物質以外,還添加了其它化合物。溶液中添加的蔗糖作為底物在酶的作用下,產生帶羥基的葡萄糖游離分子。此時,再向反應液中添加選取的受糖體,受糖體在糖基轉移酶的作用下發生糖基轉移反應。在這個反應中,酶的種類不同,轉移到受糖體上的糖基種類也不同,與此同時,酶和受糖體的物質濃度配比不同也會影響反應產物的種類。
實施例5
糖的受體是2-氨基酸時,生成化學式Ⅰ的2-氨基酸衍生物。
[化學式Ⅰ]
2-氨基苯酚-O-α-D-低聚異麥芽糖
(2-Aminophenol-O-α-D-isomaltooligosaccharide)
(上式 n取0-5)
實施例6
糖的受體是3-氨基酸時,生成化學式Ⅱ的3-氨基酸衍生物。
[化學式Ⅱ]
3-氨基苯酚-O-α-D-低聚異麥芽糖
(3-Aminophenol-O-α-D-isomaltooligosaccharide)
(上式 n取0-5)
實施例7
糖的受體是4-氨基酸時,生成化學式Ⅲ的4-氨基酸衍生物。[化學式Ⅲ]
4-氨基苯酚-O-α-D-低聚異麥芽糖
(4-Aminophenol-O-α-D-isomaltooligosaccharide)
(上式 n取0-5)
實施例8
糖基轉移酶是葡聚糖蔗糖酶,上述的糖的受體是對苯二酚時,生成下述化學式Ⅳ的對苯二酚衍生物。
[化學式Ⅳ]
對苯二酚-O-α-D-低聚異麥芽糖
(Hydroquinone-O-α-D-isomaltooligosaccharide)
(上式 n取0-5)
實施例9
糖基轉移酶是果聚糖蔗糖酶,上述的糖的受體是對苯二酚時,生成下述化學式Ⅴ的對苯二酚衍生物。
[化學式Ⅴ]
對苯二酚-O-α-D-低果聚糖
(Hydroquinone-O-α-D-fructooligosaccharide)
(上式 n取0-5)
實施例10
糖基轉移酶是葡聚糖蔗糖酶,糖的受體是熊果苷時,生成下述化學式Ⅵ的熊果苷衍生物。
[化學式Ⅵ]
熊果苷-O-α-D-低聚異麥芽糖
(Arbutin-O-α-D-isomaltooligosaccharide)
(上式 n取0-5)
即當受糖體為2-氨基苯酚,則2-氨基苯酚在葡聚糖蔗糖酶的作用下,結合多個葡萄糖,生成2-氨基苯酚-O-α-D-低聚異麥芽糖(化學式Ⅰ);當受糖體為3-氨基苯酚,則3-氨基苯酚(m-aminophenol)在葡聚糖蔗糖酶的作用下,結合多個葡萄糖,生成3-氨基苯酚-O-α-D-低聚異麥芽糖(化學式Ⅱ);當受糖體為4-氨基苯酚,則4-氨基苯酚在葡聚糖蔗糖酶的作用下,結合多個葡萄糖,生成4-氨基苯酚-O-α-D-低聚異麥芽糖(化學式Ⅲ)。另外,對苯二酚在葡聚糖蔗糖酶的作用下,結合多個葡萄糖,生成對苯二酚-O-α-D-低聚異麥芽糖(化學式Ⅳ);而對苯二酚在果聚糖蔗糖酶的作用下,結合多個果糖,生成對苯二酚-O-α-D-低果聚糖(化學式Ⅴ)。當受糖體為熊果苷,則熊果苷會在葡聚糖蔗糖酶的作用下生成熊果苷-O-α-D-低聚異麥芽糖(化學式Ⅵ)。
區別在于,當選取的受糖體生成如化學式Ⅰ~Ⅵ中的糖類化合物衍生物,根據n值在2~5的取值不同,認為產生的糖類化合物衍生物的種類也不同。
這些經轉糖基作用生成的氨基酚類衍生物,其水溶解性得以提高,且具有耐光、耐熱分解的作用,能夠有效地防止光分解和熱分解。例如,就氨基苯酚而言,當其在光照或受熱條件下容易發生分解或出現褐變現象。本發明所得到的氨基苯酚衍生物的溶解性好,對光、對熱穩定性好。故可用于食品添加劑、化妝品、醫藥品以及老年癡呆癥藥物研究。此外,用上述糖類化合物衍生物所制備的功能性物質有助于改善生物的代謝途徑。本發明所得到的糖基化合物衍生物在食品、化妝品、醫藥品及老年癡呆型藥物中的使用含量限定在總重的0.001~10%之間。
葡聚糖蔗糖酶是從腸系膜明串珠菌菌株或銀耳菌絲體中獲取的;將其接種到含有K2HPO4和糖的培養基上進行培養,經人工發酵培養后得到菌液,將上述菌液進行分離純化,采用離子交換色譜的方式得到葡聚糖蔗糖酶。上述方法也是目前獲得該酶的通用方法。
葡聚糖蔗糖酶可從腸系膜明串珠菌NRRL B-1299, NRRL B-742, NRRL B-1355, NRRL B-512, NRRL B-1149, NRRL B-1142等系列菌株中獲得,但本發明選用的是腸系膜明串珠菌(Leuconostoc mensenteroides) NRRL B-1299菌株。
(一)酶液的制備:
例如1:將L.mesenteroides NRRL B-1299接種到1L含有5g酵母提取物、5g胨、20gK2HPO4、20g蔗糖的LB培養基,并在28℃下進行發酵培養。從上述培養液中分理出含有葡聚糖蔗糖酶的酶液,提純后備用。酶的純化采用DEAE瓊脂糖凝膠(DEAE-Sepharose)進行,用濃度為20mM的緩沖液(pH 6.8)提前沖洗濾柱,使柱內壓力平衡。然后將用約3倍的緩沖溶液作為流動相,帶動酶液進入液相裝置中,除去不需要的蛋白質雜質。類似的操作,用準備好的相同緩沖液配置的0~1M濃度的NaCl溶液吸附需要分離得到的酶。用緩沖液反復洗滌粗提取的葡聚糖蔗糖酶液三次,得到精制的葡聚糖蔗糖酶。
果聚糖蔗糖酶是從腸系膜明串珠菌菌株中獲取的。將該菌株其接種到含有K2HPO4和糖的培養基上進行培養,經人工發酵培養后得到菌液,將上述菌液進行分離純化,采用離子交換色譜的方式得到果聚糖蔗糖酶。上述方法也是目前獲得該酶的通用方法。
果聚糖蔗糖酶可從腸系膜明串珠菌NRRL B-512(ATCC 10830), NRRL B-1299, NRRL B-742, NRRL B-1355, NRRL B-1149, NRRL B-1142等系列菌株中獲得,但本發明選用的是腸系膜明串珠菌NRRL B-512(ATCC 10830)菌株。
例如2:將L.mesenteroides NRRL B-512 LWG型葡聚糖蔗糖酶按照0.3%(w/v)的固液比接種到液體培養基里,培養基中還含有胨、0.3%(w/v)K2HPO4和礦物質溶液(2% MgSO4·7H2O、0.1%NaCl、 0.1%Fe SO4·7H2O、0.1% MnSO4·H2O,、0.13% CaCl2·2H2O、2% (w/v)葡萄糖)培養12-16小時,OD600值為3.0。培養結束后,用DEAE瓊脂糖凝膠柱(DEAE-Sepharose)(規格為2.5×35cm)或CM-Sepharose(2.5×35cm)來分離提純果聚糖蔗糖酶。
(二)酶的反應過程
例1中的葡聚糖蔗糖酶是在濃度為0.3M的糖溶液中合成新的糖類化合物衍生物的。
當氨基苯酚類物質的反應在葡聚糖蔗糖酶的作用下進行,其中葡聚糖蔗糖酶、濃度為0.3M的蔗糖溶液以及0.5%的氨基苯酚物質以1:1:1(v/v/v)的比例添加,且在反應器中充分混勻后于28℃下進行反應。反應要保證28℃的條件下,在糖完全消耗之前(約3個小時)進行。
對苯二酚的反應條件是,葡聚糖蔗糖酶/果聚糖蔗糖酶、濃度為0.3M的蔗糖溶液以及1%對苯二酚按照1:1:1(v/v/v)的比例進行,將反應物充分混勻后在28℃條件下進行反應。反應務必保證在糖完全消耗之前(約3小時)進行。熊果苷的反應條件是葡聚糖蔗糖酶、濃度為0.3M的蔗糖溶液以及0.5%的受糖體以1:1:1(v/v/v)的比例添加,充分混勻后于28℃下進行反應。反應務必保證在糖完全消耗之前(約3小時)進行。熊果苷的合成反應條件是在20mM濃度的醋酸鈉緩沖液(pH 5.2 60ml)、12.25mM濃度的熊果苷、100mM濃度的糖溶液,還有2U/ml B-1299葡聚糖蔗糖酶,最終反應在28℃下進行到糖被耗盡之前,對反應液煮沸8分鐘,以滅酶活。
當反應物氨基苯酚在葡聚糖蔗糖酶作用下反應結束時,葡聚糖蔗糖酶的活性為1U/ml。1U是指酶在1min內分解1ml果糖溶液的μmol數。運用下述方法鑒別酶作用生成糖類化合物衍生物的反應是否結束。取1μl生成物,用Merck K6F TLC薄層色譜法進行分析鑒定:取硝基甲烷:丙醇:水=2:5:1.5(v/v/v)的混合溶液或者乙腈:水=85:15(v/v)的混合液與1μl生成物在點滴板中混合,然后展開實驗,觀察反應情況。反應一會后,采用HPTLC(High pressure thin layer chromatograph)薄層色譜法鑒定分離物質,此鑒定方法中所用的顯色劑含有0.5%(w/v)的α-萘酚和5%(v/v)的H2SO4。
(三)反應產物的結構確定
利用HPLC、NMR以及MALDI-TOP等分析方法來確定上述過程生成的產品的分子結構。反應產物用Bio Gel P-2柱來進行精制,將樣品溶液注入柱中,通過TLC來確認流出的分離物。分離得到的目標物質經真空濃縮后,再次用TLC來確認成分。總之,合成產品的成分組成由TLC、NMR、MALDI-TOF MS (Matrix-Assisted LaserDesorption Ionization-Time of Flight Mass Spectrometer)等來加以確定鑒別,反應的結果如圖1~4所顯示的。
從Leuconostoc mesenteroides NRRL B-1299菌株中得到的葡聚糖蔗糖酶作用于不同氨基苯酚受糖體分別得到以下氨基苯酚衍生物:2-氨基苯酚-O-α-D-低聚異麥芽糖(圖1-P1)、3-氨基苯酚-O-α-D-低聚異麥芽糖(圖1-P2)以及4-氨基苯酚-O-α-D-低聚異麥芽糖(圖1-P3)。對苯二酚經葡聚糖蔗糖酶作用得到產物如圖2所示,所得衍生物對苯二酚-O-α-D-低聚異麥芽糖 (圖2-P4),對苯二酚經果聚蔗糖酶作用得到產物如圖3所示,所得衍生物對苯二酚-O-α-D-低果聚糖(圖3-P5)。另外,熊果苷在葡聚糖蔗糖酶的作用下得到產物如圖4所示,產物為熊果苷的衍生物熊果苷-O-α-D-低聚異麥芽糖(圖4-P6、P7)。
另一方面,各分離樣品在47℃下經蒸發器濃縮,再利用HPLC進行各成分的純度確定。此時使用的分析柱為hypersil APS-2 NH2型(4.6×250mm Bio-Rad),流動相是體積比為4:1或3:1的乙腈/甲醇溶液,流動速率為0.5ml/min。在室溫條件下,利用RI檢波器對HPLC純化得到的樣品進行色譜圖分析,如圖5所示。經生物凝膠P-2色度分離得到的熊果苷經HPLC分析后確認含有G1物質和G2物質,且兩種物質分別占原樣品的23.8%和3.3%。 精制后的各樣品的分子量由MALDI-TOF-MS進行分析。將制備得到的熊果苷衍生物(3mg/ml)用去離子水稀釋,然后與2,5-二羥-苯甲酸(1mg/ml)混合,將混合好的溶液按1:1的比例溶入有機試劑乙腈中,取最終的混合液1μl滴入不銹鋼容器中,在室溫下緩慢干燥。利用MALDI-TOF-MS(Voyager DE-STR; Appled Bio Systems, USA)進行正像模式的質譜分析,此時附加65KV的電壓加快分析速度。取精制的熊果苷衍生物2~3mg,溶解于250μl的重水(D2O)中,通入NMR(直徑 3mm)管中,使用Unity Inova 500 spectrometer(Varian Inc., USA)進行分析。在500 MHz的電壓用1H核磁共振,在125 MHz下用13C核磁共振進行分析。結果如下表1所示。
[表1]
熊果苷及熊果苷衍生物的13C和1H核磁共振成像數據(單位:ppm)
熊果苷-G1物質
熊果苷-G1分子的m/z(質荷比)是457。從表1中我們可以看到,在4.89ppm(J=7.0Hz)觀察到熊果苷芳香族物質中的以β結合方式結合的葡萄糖的異頭構型信號。用HMBC(異核多鍵相關譜)確定了4.83ppm(J=3.5Hz)信號處的以α方式結合的葡萄糖分子。熊果苷衍生物的熊果苷信號是利用熊果苷分子結構上的碳來確定的(化學式Ⅶ)。和其他位置的碳相比,除了65.55ppm處的C-6’以外,其它的δ1-δ的值都為負的。上述差異是因為2.15ppm處的C-6’與葡萄糖分子發生結合,從而帶來了變化。利用HMBC也確認了,在65.55ppm處的葡萄糖的H-1’’與熊果苷C-6’之間發生耦合作用,以此確認熊果苷-G1結構含有4-羥基苯酰和β-異麥芽糖結構(化學式Ⅷ)。
[化學式Ⅶ]
[化學式Ⅷ]
熊果苷-G2物質
熊果苷-G2分子的m/z(質荷比)是610。從表1可以看出,在4.94ppm(J=7.0Hz)觀察到熊果苷芳香族物質中的以β結合方式結合的葡萄糖的異頭構型信號,同樣,用HMBC也可以得到相同的結論。在4.86ppm(J=3.5Hz)處和4.81ppm(J=3.5Hz)處可看到有兩個葡萄糖分子結合在熊果苷上。表1中66.83ppm處的C-6’和64.29ppm處的C-6”分別對應2.43ppm和4.97ppm。葡萄糖基與熊果苷中的C-6’相結合,而葡萄糖與熊果苷中的C-6”相結合。利用HMBC也確認了,在65.83ppm處的葡萄糖的H-1”與熊果苷C-6’之間發生耦合作用,而在65.20ppm處熊果苷的C-6”與葡萄糖H-1”’發生結合。以此確認熊果苷-G1結構含有4-羥基苯酰和β-低聚葡萄糖結構。
[化學式Ⅸ]
最后生成的熊果苷衍生物經醋酸酸化以后可生成下述化學式Ⅹ的五乙酰熊果苷。
[化學式Ⅹ]
五乙酰熊果苷。
- 還沒有人留言評論。精彩留言會獲得點贊!