一種雞毒支原體熒光定量檢測試劑盒及其檢測方法與流程
本發明屬于動物檢疫技術領域,具體涉及一種雞毒支原體熒光定量檢測試劑盒及其檢測方法。
背景技術:
雞毒支原體(Mycoplasma gallisepticum,MG)感染是雞慢性呼吸道病的一種,感染MG的雞臨床癥狀包括咳嗽、打噴嚏、鼻炎、結膜炎,呼吸時伴有鼻分泌物,也有可能患上單側或者雙側鼻竇炎。感染后會引起蛋雞產蛋率下降,肉雞體重減輕。雞毒支原體不同菌株的感染性和致病性不同,有時感染性并不明顯。傳播方式主要為垂直傳播和水平傳播,1943年,Delaplane等首次從感染雞群中分離出該病原體,此病流行范圍遍布世界,我國支原體感染陽性率已達50%~80%,成為威脅我國養禽業的重要疾病之一。
雞毒支原體感染,主要表現為慢性呼吸道癥狀,無其他特征性的臨床癥狀,同時易與其他細菌或病毒繼發和混合感染,給臨床診斷帶來困難。支原體培養營養要求高,體外培養生長緩慢,耗時較長,所以傳統的分離培養法不能滿足臨床診斷的需要,目前分子生物學方法在臨床診斷中因快速、靈敏的特點,應用越來越廣泛。
技術實現要素:
本發明針對現有技術中存在的不足,目的在于提供一種雞毒支原體熒光定量檢測試劑盒及其檢測方法。
為實現上述發明目的,本發明所采用的技術方案為:
一種雞毒支原體熒光定量檢測試劑盒,包括:熒光定量PCR反應液、陽性對照和陰性對照,所述熒光定量PCR反應液中包含上游引物和下游引物。
上述方案中,所述上游引物的序列為:5’-GAGCTAATCTGTAAAGTTGGTC-3’;所述下游引物的序列為:5’-GCTTCCTTGCGGTTAGCAAC-3’。
上述方案中,所述熒光定量PCR反應液中還包含SYBR Premix Ex Taq(Tli RNaseH Plus)。
上述方案中,所述熒光定量PCR反應液的組成為:10μmol/L上游引物0.25μL,10μmol/L下游引物0.25μL,SYBR Premix Ex Taq(Tli RNaseH Plus)5μL。
上述方案中,所述陰性對照為DEPC處理水。
上述方案中,所述陽性對照為:滅活的雞毒支原體活疫苗按1:1000倍稀釋的稀釋液。
利用上述試劑盒進行雞毒支原體熒光定量PCR的檢測方法,包括如下步驟:
(1)將待測樣品溶于DEPC水,煮沸、冰浴、離心后取上清作為待測樣品檢測模板DNA;
(2)取步驟(1)所得樣品檢測模板DNA與熒光定量PCR反應液配成反應體系進行熒光定量PCR反應;同時配制陽性對照反應體系、陰性對照反應體系同步進行熒光定量PCR反應;
(3)讀取樣品檢測通道、陽性對照檢測通道和陰性對照檢測通道的熒光數據,進行結果判定:陰性對照檢測通道應均無Ct值并且無擴增曲線;陽性對照檢測通道應均有特征性“S”型擴增曲線,且Ct值小于32,Tm值為84.7℃±1.5℃,則表明實驗成功,可進行樣品的陰性/陽性結果判斷,否則實驗視為無效;
樣品陰性結果判斷:樣品檢測通道無特征性擴增曲線、或Ct值≥32但Tm值不在84.1℃±1.5℃范圍內,則表明樣品中不含雞毒支原體;
樣品陽性結果判斷:樣品檢測通道出現“S”型擴增曲線,且Ct值小于32,且Tm值為84.1℃±1.5℃,則表明樣品中含有雞毒支原體。
上述方案中,所述熒光定量PCR反應為:第一階段,預變性,95℃3min;第二階段,95℃15s,59℃40s,40個循環,每次循環的59℃退火延伸時收集熒光信號;第三階段,生成融解曲線。
本發明所述雞毒支原體熒光定量PCR檢測方法中,若檢測樣品出現典型的擴增曲線,Ct值大于或等于32,且Tm值在84.1℃±1.5℃范圍內,應將樣品進行10倍稀釋后復檢;若仍出現典型擴增曲線,Ct值大于或等于32,且Tm值為84.1℃±1.5℃,則判為陽性,否則判為陰性。
本發明分別選擇雞毒支原體(MG)的16s rRNA基因的保守序列設計引物。引物長度為22個堿基左右,引物內無二級結構和重復性,引物間和引物內無互補序列,引物間的融解溫度(Tm值)相差小于5℃。
本發明的有益效果:
(1)采用本發明所述試劑盒對樣品進行雞毒支原體熒光定量PCR檢測,樣品的預處理過程非常簡單,即不需要對樣品進行支原體培養,也不需要對樣品中進行支原體基因提取,只需將樣品直接煮沸后冷卻即可,本發明所述檢測方式簡化了常規熒光定量PCR檢測方法中樣品的預處理過程,具有省時、省操作、節約成本等優點;同時全封閉反應,無需PCR后處理,操作安全;并且通過PCR產物進行實時熒光監控,PCR結束即可獲得結果,具有快速檢測的優勢;
(2)本發明所述雞毒支原體熒光定量檢測試劑盒具有檢測靈敏度高、特異性好、重復穩定性好等優點:試劑盒的靈敏度可達100拷貝/反應;使用試劑盒檢測大腸桿菌、沙門氏菌、巴氏桿菌、副雞嗜血桿菌、葡萄球菌等細菌,均顯示無交叉反應,使用試劑盒檢測雞毒支原體顯示出良好的特異性;使用試劑盒多次對含有不同濃度模板DNA的樣品進行重復檢測,均能檢測出來,說明可重復度高;
(3)本發明所述試劑盒及其檢測方法非常適用于雞咽喉拭子中雞毒支原體(MG)的檢測,適用于隱性感染或帶毒雞群的快速篩查。
附圖說明
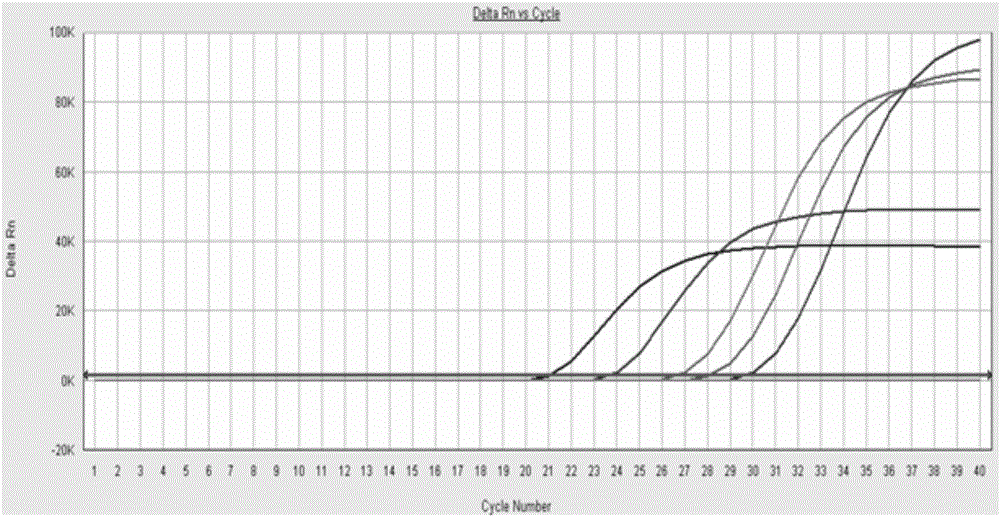
圖1為以滅活的雞毒支原體活疫苗(F36株)為樣品的檢測結果,曲線從左到右依次為樣本進行10-2、10-3、10-4、10-5、10-6稀釋后的擴增曲線。
圖2為以滅活的雞毒支原體活疫苗(F36株)為樣本的檢測結果,峰高從高到低的曲線依次為樣本進行10-2、10-3、10-4、10-5、10-6稀釋、擴增后融解曲線。
圖3為以大腸桿菌、沙門氏菌、巴氏桿菌、副雞嗜血桿菌、葡萄球菌為樣本,以滅活的雞毒支原體活疫苗為陽性對照的檢測結果,其中“S”型曲線為陽性對照的擴增曲線,其他樣本的均為起線。
圖4為以大腸桿菌、沙門氏菌、巴氏桿菌、副雞嗜血桿菌、葡萄球菌為樣本,以滅活的雞毒支原體活疫苗為陽性對照的檢測結果,其中,有融解峰的曲線為陽性對照融解曲線,其他樣本均沒有出現融解峰。
具體實施方式
為了更好地理解本發明,下面結合實施例進一步闡明本發明的內容,但本發明的內容不僅僅局限于下面的實施例。
實施例1
(1)引物的設計
根據Genbank登錄的已發表的雞毒支原體(MG)16S rRNA基因序列(Genbank登錄號KC995374.1)設計引物。通過分析實驗,得到以下引物:
雞毒支原體-上游引物:5’-GAGCTAATCTGTAAAGTTGGTC-3’
雞毒支原體-上游引物:5’-GCTTCCTTGCGGTTAGCAAC-3’。
(2)待檢樣品處理
a.取滅菌的1.5mL離心管,加入400μL無菌的PBS,將采集的咽喉拭子于PBS中旋轉洗滌,保留洗滌液;
b.將上述洗滌液12000r/min離心10min,棄上清,保留沉淀物;
c.將沉淀物加入400μL DEPC水混勻,于100℃水浴鍋中煮沸10min,煮沸后冰浴10min,2000r/min離心3min,上清作為樣品檢測模板DNA;
d.同時取陽性對照10μl加入400μLDEPC水混勻,重復步驟c的操作,上清作為陽性對照檢測模板DNA。
(3)PCR擴增反應體系配制
5μL SYBR Premix Ex Taq(Tli RNaseH Plus)分別加入0.25μL、10μmol/L上游引物、0.25μL、10μmol/L下游引物,充分混合均勻后,即得到熒光PCR反應液(見表1),再在熒光PCR反應液中加入4.5μL樣品檢測模板DNA/陽性對照檢測模板DNA/陰性對照檢測模板DNA,最終配成10μL的PCR擴增反應體系(1羽份)。
表1熒光PCR反應液(1羽份,5.5μl)
其中,SYBR Premix Ex Taq(Tli RNaseH Plus)購于大連寶生物生物工程有限公司,引物由生工生物工程(上海)股份有限公司合成。
實施例2雞毒支原體熒光定量PCR檢測
(1)將上述PCR擴增反應體系進行熒光定量PCR檢測,熒光定量PCR反應的參數設計如下:第一階段:預變性,95℃3min;第二階段:95℃15s,59℃40s,40個循環,在第二階段每次循環的59℃退火延伸時收集熒光;第三階段,生成融解曲線。
(2)分別讀取樣品檢測通道、陽性對照檢測通道和陰性對照檢測通道的熒光數據,進行結果判定:陰性對照檢測通道應均無Ct值并且無擴增曲線,陽性對照檢測通道應均有特征性“S”型擴增曲線,且Ct值小于32,Tm值為84.7℃±1.5℃,則表明實驗成功,可進行樣品的陰性/陽性結果判斷,否則實驗視為無效;
樣品陰性結果判斷:樣品檢測通道無特征性擴增曲線、或Ct值≥32但Tm值不在84.1℃±1.5℃范圍內,則表明樣品中不含雞毒支原體;
樣品陽性結果判斷:樣品檢測通道出現“S”型擴增曲線,且Ct值小于32,且Tm值為84.1℃±1.5℃,則表面樣品中含有雞毒支原體。
同時,若檢測樣品出現典型的擴增曲線,Ct值大于或等于32,且Tm值在84.1℃±1.5℃范圍內,應將樣品進行10倍稀釋后復檢;若仍出現典型擴增曲線,Ct值大于或等于32,且Tm值為84.1℃±1.5℃,則判為陽性,否則判為陰性。
實施例3可行性實驗
以滅活的雞毒支原體活疫苗為樣品,采用實施例1、實施例2的方法進行雞毒支原體熒光定量PCR檢測,檢測結果顯示:樣品出現典型的擴增曲線,Ct值小于32,Tm值為84.1℃。說明本發明所述試劑盒及其檢測方法具有確定的可行性。
實施例4靈敏性實驗
以滅活的雞毒支原體活疫苗為樣品,將其用DEPC水進行10-2、10-3、10-4、10-5、10-6稀釋后,采用實施例1、實施例2的方法進行雞毒支原體熒光定量PCR檢測,檢測結果如圖1、圖2所示,圖1從左到右的曲線分別代表稀釋了10-2、10-3、10-4、10-5、10-6的雞毒支原體活疫苗樣品,圖2中峰高從高到低的曲線分別代表稀釋了10-2、10-3、10-4、10-5、10-6的雞毒支原體活疫苗樣品,從圖1和圖2可以看出:雞毒支原體稀釋10-6倍數后仍然能被本發明所述試劑盒及其檢測方法檢出,說明本發明所述試劑盒具有非常好的特異性和非常高的靈敏性。通過對雞毒支原體活疫苗樣品進行拷貝數測定后,再采用本發明所述試劑盒進行檢測,結果顯示,本發明所述試劑盒的靈敏度能達到100拷貝/反應;同時使用本發明所述試劑盒多次對含有不同濃度模板DNA的樣品進行重復檢測,均能檢測出來,說明可重復度高。
實施例5特異性實驗
分別以大腸桿菌、沙門氏菌、巴氏桿菌、副雞嗜血桿菌、葡萄球菌為樣品,以雞毒支體為陽性對照,采用實施例1、2的方法進行熒光定量PCR,結果如圖3、圖4所示,從圖3和圖4可以看出:大腸桿菌、沙門氏菌、巴氏桿菌、副雞嗜血桿菌、葡萄球菌樣品均無特征性擴增曲線,無特異性融解峰,而陽性對照(雞毒支原體樣品)出現“S”型曲線擴增曲線和特異性融解峰,表明本發明所述試劑盒具有非常好的特異性。
顯然,上述實施例僅僅是為清楚地說明所作的實例,而并非對實施方式的限制。對于所屬領域的普通技術人員來說,在上述說明的基礎上還可以做出其它不同形式的變化或變動。這里無需也無法對所有的實施方式予以窮舉。而因此所引申的顯而易見的變化或變動仍處于本發明創造的保護范圍之內。
- 還沒有人留言評論。精彩留言會獲得點贊!