一種全自動循環腫瘤細胞陰性富集裝置的制作方法
本發明涉及循環腫瘤細胞全自動檢測設備領域,尤其涉及一種全自動循環腫瘤細胞陰性富集裝置。
背景技術:
循環腫瘤細胞(Circulating Tumor Cell,CTC)是存在于外周血中的各類腫瘤細胞的統稱,其可自發或通過診療操作從實體腫瘤病灶(原發灶或轉移灶)脫落,進入體循環系統(如外周血)。大部分CTC進入外周血后會發生凋亡或被吞噬,少數能夠逃逸并錨著病灶以外的組織或器官上,進而發展成為轉移灶,增加惡性腫瘤患者死亡風險。因此,CTC檢測可有效地應用于體外早期診斷、預后評價、個體化治療(包括快速臨床化療藥物篩選和耐藥性的檢測)、腫瘤復發監測及新的腫瘤藥物開發等。
目前,市場上已出現的CTC富集和檢測的產品或服務,唯一獲得FDA批準的CTC檢測設備是CellSearch系統,該系統是基于免疫磁珠分離技術而開發出的檢測設備,它利用標記有針對上皮細胞黏著分子(Epithelial Cell Adhesion Molecule,EpCAM)抗體的磁性顆粒進行CTC的捕獲,該方法具有特異性強的優點,但是其無法識別未表達目標標記的未知細胞,且其捕獲效率還是較低,白細胞的干擾較大。另外,目前的一些CTC檢測設備和技術尚沒有實現檢測過程的全自動化控制,即沒有實現血液檢測樣品和試劑的自動化進樣,細胞的自動化捕獲及鑒定分析,因此CTC的檢測存在過多的人為干預,使得CTC的檢測準確性低,檢測成本過高。
鑒于循環腫瘤細胞也就是CTC總共有15個分型,而CellSearch只能檢測到其中一個型別,漏檢率很高,因此,本領域技術人員致力于開發一種以排除法原理篩選并富集CTC的全自動裝置。
技術實現要素:
本發明旨在基于密度梯度離心法提供一種從全血中陰性富集循環腫瘤細胞的方法及其全自動設備,該方法利用不同種類細胞的密度差異將其分層,并用沉淀法棄去主要的干擾細胞,從而獲得符合一定密度標準的循環腫瘤細胞。
為實現上述目的,本發明提供了一種全自動循環腫瘤細胞陰性富集裝置,包括離心單元、轉移單元、儲料單元和收集分析單元;所述離心單元用于液體的離心以及細胞的染色、清洗和孵育,所述轉移單元用于樣本、試劑和材料的轉移,所述儲料單元用于試劑和材料的儲存,所述收集分析單元用于收集富集獲得的循環腫瘤細胞進行計數或分析。
進一步,所述離心單元以離心機為核心,所述儲料單元設置于所述離心單元的周圍,所述轉移單元被設置于所述裝置操作面的上方,其可在所述離心單元和所述儲料單元之間轉運樣本、試劑和材料。
優選地,本發明處理的樣本為血液樣本。
進一步,所述儲料單元包括試劑儲料倉、耗材儲料倉和廢棄物儲料倉;優選地,還可包括攪拌棒儲料倉。
進一步,所述試劑儲料倉中至少儲存有密度梯度離心液、多聯抗體試劑、細胞染色試劑和緩沖液。
優選地,所述試劑包括密度梯度離心液、多聯抗體試劑、免疫熒光染色試劑、細胞固定試劑、緩沖液;其中,所述多聯抗體試劑可結合至少兩種干擾細胞,優選為可結合血液中的白細胞和紅細胞;所述細胞染色劑優選為可特異性識別和結合循環腫瘤細胞表面抗原的熒光抗體。進一步,所述試劑還可以包括核酸染色劑、捕獲增強試劑、通透試劑中的一種或多種。
陰性富集法中最大的干擾是白細胞和紅細胞,上述方法采用多聯抗體將白細胞與紅細胞結合起來;在本發明的一種優選實施方式中,所述結合體的密度較大,經密度梯度離心而沉淀,而作為目標的CTC位于中間層,該層中除了目標CTC以外,還可能有與其密度相類似的其它細胞,這些其它細胞可能也是CTC,或是值得進一步分析研究的非CTC細胞。
優選地,所述耗材包括一次性移液槍頭。
進一步,所述離心單元還包括視覺識別系統,用于對離心液體分層的成像、各層吸取液體量和高度的計算。
優選地,所述視覺識別系統的計算方法分為兩部分,均是根據視覺識別照片(上下層以光電傳感器對顏色加以區分)來計算的:
1)計算需抽掉的上層液體高度值:根據樣本所在高度減去照片中上層與下層相接處的高度的差,加上調整的高度(防止抽液過多對下層造成擾動);
2)計算需添加的液體高度值:用設定的最終高度減去現有液面的高度,必要時還要減去添加目標液體之前所需添加的小劑量試劑的高度。
進一步,所述離心單元采用的離心機為步進式離心機,可根據需要任意移動樣本的通道位置;進一步,所述步進式移動樣本通道位置即:在操作者上機時在離心機上放置離心管或轉移單元添加和吸取液體時,離心機可以緩慢順時針或逆時針旋轉移動,將已操作通道移走,并將相鄰通道轉至操作位。采用所述步進式移動樣品通道位置,便于上機放置樣品管,同時可以便于配合轉移單元工作,使轉移單元與樣本品通道通過最短路徑配合,能夠節約轉移單元反復移動位置所消耗的時間,加快整個流程的進度。
優選地,所述離心單元能夠實時記憶和記錄每個樣本通道的位置,便于將樣本初始編號和提取物/分析物樣本編號的對應,并且每一個生物樣本在離心過程中的任意位置是有路徑記憶以及動態與靜態位置可設定和控制的。
更優選地,所述離心機為數字化離心機,在離心過程中,操作者可根據樣本的離心要求設定加速與減速曲線,采用的減速曲線是智能可控的有剎車減速,在不擾動樣本分層的基礎上,能夠快速剎車,節省了時間,而現有的離心機減速,為了避免樣本的分層擾動,都是采取無剎車減速,減速時間非常長。
進一步,本發明所述離心單元還具有混勻機構,所述混勻機構被設置在離心機的每個樣本通道底部,該機構可帶動離心試管進行自旋和/或搖晃運動。
進一步,所述轉移單元由一個或多個機械臂組成,所述機械臂能夠進行上下、左右和/或轉軸運動;優選地,所述機械臂可兼容hamilton的移動系統;在本發明的一種優選實施方式中,所述多個機械臂分別用于轉移樣品、廢棄液、試劑和固體材料;在本發明的另一種優選實施例中,所述機械臂具有“一臂多用”的特點,可用于移取液體或固體材料。
在本發明的一種優選實施方式中,所述全自動循環腫瘤細胞陰性富集裝置還包括攪拌棒。優選地,所述攪拌棒通過電磁場被所述機械臂抓取而實現轉移。
進一步優選地,所述攪拌棒為螺旋槳狀。
優選地,所述機械臂能帶動所述攪拌棒進行自轉運動,從而實現攪拌和混勻的動作。
進一步,所述收集分析單元具有觀察窗,可供操作者觀察或機器自動拍照。
此外,本發明還提供一種全自動循環腫瘤細胞陰性富集方法,包括以下步驟:
1)在離心單元中,交錯放置裝有全血樣本的試管A和裝有密度梯度離心液的試管B,在離心單元外的試管架中放置干凈的試管C;
2)向全血樣本試管A中加入緩沖液和交聯抗體試劑,進行混勻和孵育;
3)將孵育后的全血樣本輕輕加入旁邊預裝了密度梯度離心液的試管B中,經離心后進行視覺識別與計算,然后吸取循環腫瘤細胞層;
4)將吸取的循環腫瘤細胞層移入離心單元外的試管C中,并用轉移單元將試管B從離心單元中移出;
5)用轉移單元將試管C移入離心單元中,加入緩沖液后離心,棄去上清;
6)向試管C中加入免疫熒光染色試劑,經染色孵育后,加入緩沖液,再經離心棄上清后,加入固定試劑并混勻;
7)將用固定試劑重懸后的循環腫瘤細胞轉移至收集分析單元內進行進一步的分析。
本發明具有以下有益效果:
(1)本發明的陰性富集裝置是首次實現陰性富集循環腫瘤細胞的自動化設備,結構緊湊,循環腫瘤細胞的富集和染色步驟均可在離心單元內完成,不需要專設染色平臺;
(2)本發明的離心單元采用步進式移動樣本通道位置,便于配合機械臂工作,使機械臂與樣本通道通過最短路徑配合,能夠節約機械臂反復移動所需時間,加快整個流程的進度;所述離心平臺所用離心機的減速曲線采用智能可控的有剎車減速,與傳統的離心機自由停車相比,即避免了離心停車對液體的擾動,又節約了離心時間。
(3)本發明每個通道的樣本和試劑操作是獨立的,樣本和試劑沒有交叉污染,本發明的孵育過程是動態的,有攪拌和外磁強化,且本發明需要對生物樣本進行預處理的過程是全自動的。
附圖說明
圖1是本發明的一個較佳實施例的結構示意圖;
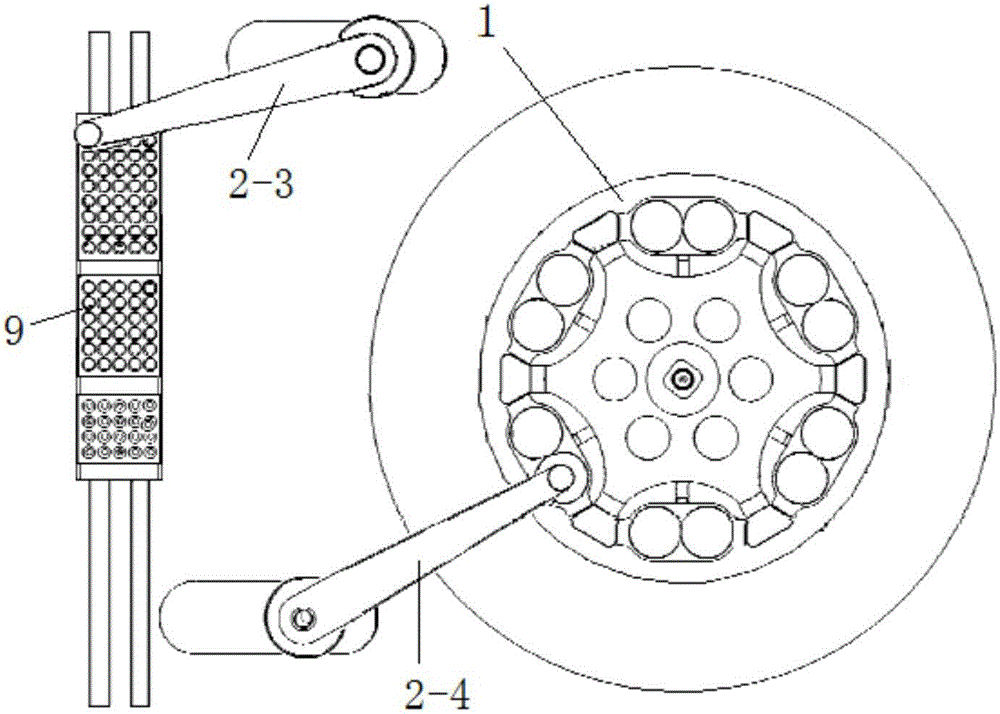
圖2是本發明中機械臂的另一個較佳實施例的結構示意圖。
具體實施方式
下面結合附圖與實施例對本發明作進一步詳細描述,但本領域技術人員根據以下實施例中具體方案的替換、轉用或組合均包含于本發明的保護范圍之內。采用與本發明裝置類似設計流程樣本處理的液體工作站形式,或者采用與本發明方法類似的富集方法,均在本發明的構思范圍之內。
實施例1
本實施例提供了一種全自動循環腫瘤細胞陰性富集裝置(圖1),包括離心單元、轉移單元、儲料單元和收集分析單元;其中,離心單元的核心部件為具有12個樣本通道的數字化離心機1,所述離心單元用于液體的離心以及細胞的染色、清洗和孵育;轉移單元由具有橫向(X)和縱向(Y)軌道的兩個轉移機械頭2-1、2-2組成,該兩個轉移機械頭還可在垂直操作面的方向上(Z,圖中未示出)移動;儲料單元包括試劑儲料倉3、移液槍頭儲料倉4、攪拌棒儲料倉5、試管儲料倉6和廢液儲料倉7,所述試劑儲料倉3中至少儲存有密度梯度離心液、多聯抗體試劑、免疫熒光染色試劑、細胞固定試劑和緩沖液,多聯抗體試劑可結合白細胞與紅細胞;收集分析單元,該收集分析單元包括多個讀數盒8,用于收集富集獲得的循環腫瘤細胞進行計數或分析。
進一步,離心平臺的離心機1為步進式離心機,可根據需要任意移動樣本的通道位置,在一種優選的實施方式中,如圖1所示的a和b位為機械臂的操作位,每次需要移液操作時,將樣本離心管轉至a和b位,兩個轉移機械頭2-1、2-2同時移動至此位進行添加或吸取液體,固定操作位后,由于機械臂的移動路徑被縮短,且機械臂和離心機同時參與位移,使總的運行流程縮短。此外該數字化離心機可根據樣本的離心要求設定加速與減速曲線,采用的減速曲線是智能可控的有剎車減速,在不擾動樣本分層的基礎上,能夠快速剎車,可進一步節省時間。該離心機還能夠實時記憶和記錄每個樣本通道的位置,便于將樣本初始編號和提取物/分析物樣品編號的對應,并且每一個生物樣本在離心過程中的任意位置是有路徑記憶,以及動態與靜態位置可設定和控制。
本實施例的離心單元還包括視覺識別系統,能夠對離心液體分層的成像、各層吸取液體量和高度進行計算;此外離心機的通道底部還設置有混勻機構,可通過自旋和/或搖晃使樣品中的液體混勻。
所述轉移單元的機械臂連有兩個轉移機械頭2-1和2-2,可以插取和釋放移液槍頭,吸取和吹出液體,此外還可以通過電磁場抓取、轉移攪拌棒,所述攪拌棒的上端設置有鐵磁性物質,可被轉移機械頭抓取,此處抓取方式不唯一,能滿足要求的抓取方式都是可行的。
在本發明的另一種實施方式中,機械臂除了可以設置直線軌道外,還可以設置成繞軸旋轉的形式,如圖2所示,該離心單元有兩個旋轉式機械臂2-3和2-4,它們從左側可沿軌道滑動的儲料倉9中移取槍頭、試劑等,為離心機1提供液體轉移。
如圖1中所示,本實施例中的離心機內樣本通道為兩個一組,共6組,機器運行之前在每組通道中的a位置放置全血樣本,b位置放置密度梯度離心液,轉移單元則可在離心機a通道和b通道之間轉移液體,以及在離心機和試管架之間轉移液體和離心試管。
在本發明的一種優選實施例中,樣本的稀釋步驟和密度梯度離心步驟分別在離心機的a和b位置進行,收集獲得的CTC細胞被轉移至試管儲料倉6上的干凈試管中,然后將該試管轉移至離心機中進行后續的染色步驟,在此實施例中轉移單元可轉移試管,轉移試管的方式可以是夾取式、磁抓取式等;在本發明的另一種優選實施例中,樣本的稀釋步驟在試管儲料倉6上的試管中進行,用攪拌棒進行攪拌混勻,混勻后的液體樣本轉移至離心機中的a位置,密度梯度離心步驟在b位置進行,此實施例中無需轉移試管。
本實施例中的裝置可同批富集和檢測6個樣本,且兼容了樣本前處理過程,運行時間短、效率高。
實施例2
本發明所述的視覺識別系統的一種優選實施例的具體計算方法包括兩部分,分別是吸取液體高度的計算和需要添加液體高度的計算,都是根據視覺識別系統所拍攝的照片進行計算。
計算需抽掉的上層液體高度值:根據樣本所在高度減去照片中上層與下層相接處的高度的差,加上調整的高度(防止抽液過多對下層造成擾動);
計算需添加的液體高度值:用設定的最終高度減去現有液面的高度,必要時還要減去添加目標液體之前所需添加的小劑量試劑的高度。
例如,默認全血樣本體積為10mL,離心后樣本分為上層血漿和下層血細胞,吸取上層血漿后,需添加0.2mL的試劑,然后添加稀釋緩沖液至5mL,其中調整的高度為0.8mL液體對應的高度,則其計算的總步驟為兩步:
1)計算需抽掉的上層血漿的高度值:10mL樣本所在高度減去照片中上層血漿與下層血細胞相接處的高度的差,加上7mm的高度(0.8mL液體對應的高度);
2)計算需添加的稀釋緩沖液高度值:所需稀釋緩沖液為5mL所在高度值減去抽取血漿后的液面高度與需在稀釋緩沖液之前添加的0.2mL的小劑量試劑之和;
例:10mL樣本中共有7mL的上層血漿,則抽取值為6.2mL(7-0.8),需添加的稀釋緩沖液為1mL(5-3.8-0.2)。
實施例3
一種全自動循環腫瘤細胞的陰性富集方法,主要包括以下步驟:
1)在離心單元中,交錯放置裝有全血樣本的試管A和裝有密度梯度離心液的試管B,在離心單元外的試管架中放置干凈的試管C;
2)向全血樣本試管A中加入緩沖液和交聯抗體試劑,進行混勻和孵育;
3)將孵育后的全血樣本輕輕加入旁邊預裝了密度梯度離心液的試管B中,經離心后進行視覺識別與計算,然后吸取循環腫瘤細胞層;
4)將吸取的循環腫瘤細胞層移入離心單元外的試管C中,并用轉移單元將試管B從離心單元中移出;
5)用轉移單元將試管C移入離心單元中,加入緩沖液后離心,棄去上清;
6)向試管C中加入免疫熒光染色試劑,經染色孵育后,加入緩沖液,再經離心棄上清后,加入固定試劑并混勻;
7)將用固定試劑重懸后的循環腫瘤細胞轉移至收集分析單元內進行進一步的分析。
具體地,所述陰性富集方法的自動化操作步驟可參見表1。
表1 CTC陰性富集自動化操作步驟
以上詳細描述了本發明的較佳具體實施例。應當理解,本領域的普通技術人員無需創造性勞動就可以根據本發明的構思作出諸多修改和變化。因此,凡本技術領域中技術人員依本發明的構思在現有技術的基礎上通過邏輯分析、推理或者有限的實驗可以得到的技術方案,皆應在由權利要求書所確定的保護范圍內。
- 還沒有人留言評論。精彩留言會獲得點贊!