用于引導和靶向按需物質遞送的納米結構的載體的制作方法
本專利文件要求2014年6月13日提交的美國臨時專利申請號US62/012,136和發明名稱為“用于磁引導的治療劑的納米級(nanoscale)結構(NANOSCALE STRUCTURES FOR MAGNETICALLY-GUIDED THERANOSTICS)”以及2014年7月25日提交的美國臨時專利申請號US62/029,373和發明名稱為"用于靶向和按需(on-demand)遞送分子物質的納米結構的載體(NANOSTRUCTURED CARRIERS FOR TARGETED AND ON-DEMAND DELIVERY OF MOLECULAR SUBSTANCES)"的優先權和利益。將上述專利申請的全部內容作為本專利文件的公開內容的組成部分參考。
有關聯邦資助研究或研發的聲明
本發明由政府資助在國立衛生研究院(National Institutes of Health)(NIH)資助的資助金R01DA024871與國立藥物濫用研究所(National Institute on Drug Abuse)(NIDA)資助的資助金R01DA025296下進行。政府在本發明中擁有一定權利。
技術領域
本專利文件涉及使用納米級材料技術的系統、裝置和方法。
背景技術:
納米技術提供用于制造具有以分子或原子等級為特征的結構、裝置和系統的方法,例如,在一些應用中,一至數百的納米范圍的結構。例如,可以將納米級裝置配置成與一些較大分子例如生物分子、例如酶類似的大小。用于生成納米結構、納米裝置或納米系統的納米大小的材料可以展示出不同的獨特特性,例如,包括光學特性,這些特性在較大尺寸的相同材料中不存在,且這類獨特的特性可以被開發于廣泛的應用。
技術實現要素:
公開了用于制造和實現設計(engineered)的納米級結構的技術、系統和裝置,所述設計的納米級結構用于攜帶物質和提供該物質在生物系統中的定向、靶向和受控遞送。
在一個方面,用于攜帶有效負荷的納米結構裝置包括:內部微粒結構,其包括內部微粒結構的內腔的開口;至少部分在內部微粒結構的外表面上形成的外殼結構;外殼結構內的多個磁性納米微粒;和能夠使分子有效負荷以化學方式連接內部微粒結構的內腔表面上的官能化層,其中磁性納米微粒被構造成與外磁場發生相互作用,以便磁引導(steer)納米結構裝置。
在一個方面,生產納米結構的方法包括在芯微粒上形成內部微粒結構,其中所述芯微粒部分被內部微粒結構的結構包裹(encase);使納米微粒與內部微粒結構的結構的外表面連接;在覆蓋至少連接的納米微粒的一些的內部微粒結構的結構外表面上形成涂層;和從內部微粒結構中除去芯微粒,其中除去的芯微粒在內部微粒結構的結構的外表面內形成內腔和形成從內部微粒結構的結構的外表面的開口。
在一個方面,制造載體結構的方法包括通過在芯微粒上連接多個掩蔽(mask)微粒形成模板,所述掩蔽微粒在所連接的芯微粒的外表面上形成掩蔽區;使納米微粒連接模板的未掩蔽表面,其中掩蔽微粒防止納米微粒連接外表面的掩蔽區;通過連接的納米微粒的材料生長形成未掩蔽表面上的涂層產生模板的未掩蔽表面上的殼結構;和通過從模板中除去掩蔽微粒產生多孔的載體結構,其中除去的掩蔽微粒在殼結構的外表面與芯微粒外表面之間形成開口。
在一個方面,制造載體結構的方法包括通過使多個掩蔽微粒連接的芯微粒上形成模板,所述掩蔽微粒在所連接的芯微粒的外表面上形成掩蔽區;使納米微粒連接模板的未掩蔽表面,其中掩蔽微粒防止納米微粒連接外表面的掩蔽區;通過使未掩蔽表面上連接的納米微粒材料生長成島狀結構,在模板的未掩蔽表面上生成不連續的島狀結構(island structure);通過在模板的未掩蔽表面上和不連續的島狀結構上形成外層產生殼結構,其中所產生的殼結構包括具有包埋在外層的內表面上的島狀結構的外層;和通過從模板中除去掩蔽微粒產生載體結構,其中除去的掩蔽微粒形成在殼結構的外表面和芯微粒的外表面之間延伸的開口。
在一個方面,納米微粒包括構造的殼以便包括中空內部和在中空內部與殼外表面之間延伸的一個或多個開口;連接至殼的中空內部或外表面之一或兩者的磁性納米微粒,其中磁性納米微粒被構造成與外磁場發生相互作用,以便磁引導納米微粒;和通過能夠使分子有效負荷連接至殼表面的連接分子使分子有效負荷連接至殼。
在一個方面,制造微粒的方法包括在芯微粒上形成第一官能化層,以便產生官能化的芯微粒,其中所形成的第一官能化層在芯微粒表面產生相對于芯微粒表面上電荷相反的電荷;在官能化的芯微粒上形成第二官能化層,以便產生雙官能化的芯微粒,其中所形成的第二官能化層在官能化的芯微粒表面上生成不同于第二官能化層形成之前的帶相反電荷的表面;通過在雙官能化的芯微粒上連接多個掩蔽微粒形成模板,其中掩蔽微粒在其表面上包括相對于雙官能化的芯微粒相反的電荷,且其中掩蔽微粒在其所連接的雙官能化的芯微粒外表面上形成掩蔽區;通過在雙官能化的芯微粒的未掩蔽表面上形成涂層產生雙官能化的芯微粒的未掩蔽表面上的殼結構,其中掩蔽微粒防止涂層連接至外表面的掩蔽區;和通過除去掩蔽微粒和雙官能化的芯微粒產生官能化中空的多孔微粒,其中除去的掩蔽微粒形成在殼結構的中空內部與外表面之間延伸的開口。在所述方法的一些實施方式(implementations)中,例如,所述方法還可以包括,在除去掩蔽微粒和雙官能化的芯微粒之前,通過使用具有與殼結構相反電荷的材料涂敷層,在殼結構表面上形成層;和通過除去掩蔽微粒和雙官能化的芯微粒產生雙官能化中空的多孔微粒,其中除去的掩蔽微粒形成在殼結構的中空內部與層的外表面之間延伸的開口。
本專利文件中所述的主題可以按照提供如下特征的一種或多種的特定方式實施。所公開的技術包括可以用于和生物體體內和體外的各種診斷和治療應用的多官能(multi-functional)納米微粒平臺。在一些實施方案中,例如,所公開的納米微粒可以被生產為納米級碗樣(bowl-like)結構(例如納米碗),其具有能夠攜帶和遞送有效負荷物質的中空內部和官能化內部和/或外部表面,并且可以任選地被賦予可以在需要時打開和關閉以釋放有效負荷的封蓋(cap)結構。在一些實施方式中,例如,所公開的納米結構技術可以作為遞藥膠囊、受保護的酶載體實施,用于在檢測試驗中隔離檢測反應種類;和/或作為隔離和受限的化學催化劑實施。在一些實施方案中,例如,所公開的納米結構可以被生產為納米/微米級載體結構,例如納米級威浮球樣(wiffle ball-like)結構和納米級高爾夫球樣結構,其具有中空或實心內部和多孔殼,所述殼具有官能化的內和/或外表面,并且能夠磁性引導,從而確保控制釋放有效負荷、改善細胞攝取和其它特征。例如,可以應用實施所公開的技術,所述應用包括、但不限于靶向/按需遞送分子和材料,以便診斷和/或治療(治療診斷學)人和動物的疾病。
附圖簡述
圖1顯示用于合成所公開技術的納米碗載體結構的示例性制造方法的說明性示意圖。
圖2顯示在內部加載有效負荷和選擇性官能化以在外部包括靶向分子的示例性納米微粒載體的說明性示意圖。
圖3顯示使用包含巰基的硅烷官能化的馬來酰亞胺用于與二氧化硅面接(interfacing)的實例的示意圖。
圖4A和4B顯示描述使用激光輔助的或RF加熱納米碗結構的氧化鐵納米微粒釋放或打開/關閉示例性納米碗載體的封蓋結構以控制釋放有效負荷的示例性方法的說明性示意圖。
圖4C顯示關閉、打開和分離狀態的示例性納米碗結構的可切換和可拆卸的閂鎖結構的實例的示意圖。
圖5顯示所公開的納米載體的示例性實施方式的說明,其中強磁體可以優先將示例性磁響應納米碗拉出血流和進入所關注的組織。
圖6顯示示例性修飾的二氧化硅納米微粒的FTIR光譜圖。
圖7顯示所公開技術的制造方法的示例性實施方式的示例性結果的圖像。
圖8顯示所公開的使用模板定向法生產示例性納米碗結構的技術的示例性制造方法的圖示。
圖9A和9B顯示描述由聚苯乙烯芯和二氧化硅模板制成的示例性模板的掃描電子顯微鏡檢查(SEM)圖像。
圖10顯示具有增加厚度的聚苯乙烯模板的衛星微粒(satellite particle)上形成的納米碗的二氧化硅外部的示例性制造的結構的SEM圖像。
圖11A顯示使用表明官能化的芯和衛星微粒模板生產納米碗結構的示例性制造方法的說明性示意圖。
圖11B-11D顯示在示例性納米碗制造方法實施過程中得到的微粒的示意圖和相關SEM圖像。
圖12顯示用于生產二氧化硅橄欖-樣納米結構的示例性制造方法的圖示。
圖13A-13D顯示在不同反應時間內使用60mM TEOS生產的示例性偏心二氧化硅/聚苯乙烯微粒的SEM圖像。
圖14A-14E顯示使用不同TEOS濃度形成的示例性納米級橄欖結構的SEM圖像。
圖15A-15E顯示使用60mM TEOS濃度、應用不同大小的模板合成的示例性納米級橄欖結構的SEM圖像和數據圖。
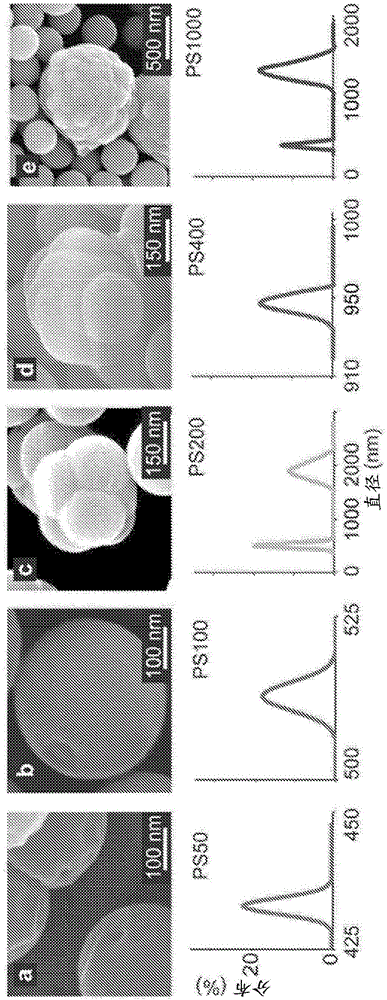
圖16A-16C顯示用于使用胺類、羥基和硫酸酯官能化的示例性聚苯乙烯納米球的分析的SEM圖像和附帶數據圖。
圖17顯示描述合成用于形成所述結構的不同反應的多孔和中空/多孔的載體結構的示例性制造方法的說明性示意圖。
圖18A顯示金殼上包括二氧化硅殼的示例性載體結構的說明性示意圖。
圖18B顯示包埋在二氧化硅殼內部的金島上包括二氧化硅殼的示例性載體結構的說明性示意圖。
圖19顯示包括加入圖18A的示例性金/二氧化硅殼內部的氧化鐵納米微粒的示例性載體結構的說明性示意圖。
圖20顯示包括內部具有分子和外部具有靶向分子的圖18B的示例性二氧化硅殼/金島的選擇性官能化的示例性載體結構的說明性示意圖。
圖21A-21F顯示示例性多孔和中空/多孔納米載體結構的SEM圖像。
圖22A和22B顯示可以用于在雙-官能化模板結構上制造所公開的技術的多孔中空納米-/微米-微粒的示例性合成方法的說明性示意圖。
圖23A和23B顯示圖22A和22B的示例性中空的多孔的納米合成方法的實施過程中得到的微粒實例的SEM圖像。
圖24顯示用于制造多孔納米-/微米-級高爾夫球和中空的多孔納米-/微米-級威浮球的示例性合成方法的說明性示意圖。
圖25A-25F顯示使用不同甲醛濃度和金離子濃度制備的示例性鍍金模板微粒的SEM圖像。
圖26A和26B顯示來自使用200nm芯的示例性金高爾夫球合成方法階段的SEM圖像。
圖27顯示描述所公開的用于生產示例性復合磁性納米級碗-樣結構(‘納米碗’)的技術的示例性制造方法的說明性示意圖。
圖28A-28F顯示包括使用示例性制造方法生產的示例性微粒的電子顯微鏡檢查圖像的圖像。
圖29顯示胺-修飾的詹納斯(Janus)模板的FTIR數據圖。
圖30A和30B顯示示例性納米碗的殼的磁性滯后和UV/Vis數據圖。
圖31A-31C顯示除去聚苯乙烯之前和之后示例性官能化磁金-二氧化硅的寬視野圖像和數據圖。
圖32A-32F顯示通過水凝膠介質引導的示例官能化磁性納米碗的縮時(time lapse)圖像和數據圖。
圖33顯示有和沒有示例性金/二氧化硅納米碗的Rho B的拉曼光譜數據圖。
圖34顯示當羧化聚苯乙烯微粒被加入到二氧化硅溶液-凝膠反應中時形成的示例性cPS-二氧化硅詹納斯微粒的說明性示意圖和附帶圖像。
圖35A顯示使用具有不同直徑cPS芯的小二氧化硅制造方法生產的示例性微粒的圖像。
圖35B包括DLS直方圖數據圖。
圖36顯示使用具有不同直徑cPS芯的大的二氧化硅制造方法生產的示例性微粒的電子顯微照片和附帶DLS直方圖。
圖37顯示通過經改變TEOS/PS之比生成的示例性小的二氧化硅方法生產的示例性PS/二氧化硅復合物的圖像。
圖38顯示通過經改變TEOS/PS之比生成的示例性大的二氧化硅方法生產的示例性PS/二氧化硅復合物的圖像。
圖39顯示詹納斯微粒形成過程中芯的作用的示例性模型的說明性示意圖。
圖40顯示示例性合成方法的說明性示意圖。
圖41顯示示例性官能化微粒的SEM圖像。
圖42顯示俘獲金膠體微粒的示例性二氧化硅高爾夫球的說明性示意圖。
圖43顯示具有俘獲金納米微粒的季銨官能化凹孔(pits)的合成的二氧化硅高爾夫球的SEM圖像。
發明詳述
公開了用于制造和實現設計的納米級結構的技術、系統和裝置,所述設計的納米級結構用于攜帶物質并且提供在生物系統中定向、靶向和受控遞送以及釋放所述物質。所公開的技術包括多官能納米微粒平臺,其可以用于體內和體外的活生物體的各種診斷和治療應用。所公開的多官能納米微粒平臺提供可控定向和引導設計的納米微粒至納米微粒所施用的生物系統中的特定區域(例如組織、器官或區)的能力。例如,所公開的納米微粒可以被構造成作為對磁場響應而運動,使得當施用于人體受試者血流或通過人體受試者的消化系統攝入時,所述納米微粒被外部施加的磁場引導至所關注的組織或器官(例如胰腺、乳腺、前列腺、腦、淋巴結等),所述外部施加的磁場可以將施用的微粒聚集在靶向區域中。所公開的多官能納米微粒平臺提供特異性地靶向和結合選擇細胞的能力。例如,所公開的納米微粒可以被構造成包括靶向配體,其可以與其中引導納米微粒的區域中的選定細胞上的相應受體發生相互作用。所公開的多官能納米微粒平臺提供封閉和保護一種或多種物質(例如有效負荷)的能力,并且允許有效負荷通過外部刺激例如在通過選定細胞攝取納米微粒(例如胞吞)時按需主動或控制釋放。在所公開技術的一些實施方式中,可以生產多官能納米微粒以便在微粒的內部提供一種化學官能團,例如用于吸引和/或連接有效負荷,并且在微粒的外部上提供獨特的不同化學基團,例如其可以用于封蓋或密封微粒。例如,所公開的納米微粒可以被構造成包括固定密封納米微粒體上的開口(例如所有開口)的封蓋,其通向其中包含有效負荷的中空內部區。所述封蓋可以連接至納米微粒體,使得它可以通過外部刺激可控地例如按需打開和關閉。
在納米級結構(納米結構)的一些實施方式中,例如,納米結構可以下述形式合成:納米級碗-樣結構(‘納米碗’),所述納米級碗-樣結構(‘納米碗’)被賦予一個或多個可以按需被打開和關閉的可啟動的封蓋。納米碗的示例性應用可以包括該納米碗內攜帶的分子和其它小物質的區域靶向/按需遞送和控制釋放,用于診斷和/或治療(治療診斷學)人和動物疾病。在設計物質結構的一些實施方式中,例如,可以合成具有中空內部和多孔殼(具有官能化內和/或外表面的)納米級和/或微米級載體結構,用于物質有效負荷的磁性引導遞送和控制釋放,這可以促進在期望區域通過靶細胞的所述物質的細胞攝取,同時將非靶向攝取和免疫應答最小化。
所公開的納米碗的示例性實施方案
在本申請技術的一些方面,可以使用易溶于水的化學物質使所公開的納米級結構化載體形成作為圍繞包含羧化物(carboxylate)的芯微粒的不對稱碗。另外,對于這種示例性不對稱納米級碗結構,可以進行適應性改變,從而允許被添加到殼內部和外部的不同修飾。在一些實施方式中,例如,這類修飾可以包括例如通過添加納米碗載體的氧化鐵/金殼產生對磁響應性的納米-載體。
用于生產示例性納米碗載體的制造方法可以包括如下技術的一種或多種:(i)通過圍繞羧化物修飾的芯形成的二氧化硅納米碗的不對稱生長合成納米-載體;(ii)對納米碗載體結構進行修飾,包括,例如,通過對納米碗的內和外表面的差別官能化進行;對二氧化硅表面進行修飾,包括,通過烷氧基硅烷和/或通過除去芯進行;(iii)產生納米級封蓋結構,其連接至納米碗載體的主體(例如殼)并且其可以打開/關閉用于從納米碗內部控制釋放示例性載荷(例如分子和材料),其中可以通過使用物理和/或化學能(例如來自生物系統外部的外部來源,例如外部施加的磁場或通過在靶細胞或組織處或其內部的內部來源,例如pH條件或與胞內核苷酸、酶或細胞器的相互作用)啟動納米-載體的封蓋打開/關閉;(iv)將示例性分子有效負荷(例如藥物、圖像造影劑等)載入納米碗;(v)從納米碗中控制釋放分子有效負荷;(vi)使用二氧化硅頂部上的金或其它金屬殼對納米碗外表面進行外表面修飾,使用惰性或生物相容性材料(例如聚乙二醇或類似惰性聚合物)鈍化和/或添加靶向部分以便改善細胞更新(例如靶向配體,包括肽類、寡核苷酸、蛋白質或其它,以便與整聯蛋白或其它細胞受體發生相互作用);和/或(vii)將氧化鐵納米微粒加入到示例性二氧化硅納米碗結構的外部或內部,其可以用于在外部磁場下引導納米-載體至生物系統(例如活生物體)中的特定位置。
圖1-5顯示用于生產和實現所公開的納米級結構化載體的示例性納米結構和制造技術的說明性示意圖。圖1顯示用于合成示例性納米碗載體的制造方法的說明性示意圖,其描述用于生產納米碗結構的不同反應。圖2顯示內部加載有效負荷(例如藥物)并且選擇性官能化以便外部包括靶向分子的示例性納米微粒載體的說明性示意圖。圖3顯示馬來酰亞胺被用于與二氧化硅面接的包含巰基的硅烷官能化的實例的示意圖。圖4A和4B顯示描述示例性方法的說明性示意圖,所述示例性方法使用激光輔助的或RF加熱納米碗結構的氧化鐵納米微粒和/或金殼釋放或打開/關閉示例性納米碗載體的封蓋結構,用于控制釋放有效負荷,例如,在一些實施方案中,這可以導致保持就位的封蓋結構通過DNA釋放。圖5顯示所公開的納米-載體的示例性實施方式的說明,其中強磁體可以優先將示例性磁響應納米碗從血流中拉出并且使其進入所關注的組織。
圖1顯示用于合成示例性納米碗載體主體的所公開的技術的示例性制造方法100。在該實例中,合成方法100使用二氧化硅納米碗微粒111在官能化的芯微粒112、例如羧化物官能化的芯微粒(例如聚苯乙烯芯微粒)上不對稱形成,正如方法101中所示。在一些實施方式中,合成方法100可以包括,使二氧化硅納米碗微粒111表面官能化的過程102,例如使用包含胺的烷氧基硅烷使表面胺官能化,其被描述為過程102中所示的表面或層111A。在二氧化硅納米碗微粒111表面修飾后,示例性合成方法100可以包括將氧化鐵納米微粒113和金納米微粒種子114添加到示例性二氧化硅納米碗微粒111外部,這可以使其以靜電方式連接至表面,正如過程103和104中所示。例如,氧化鐵和金納米微粒種子可以被配置成大約5-15nm。示例性合成方法100可以包括形成涂層115,例如通過在示例性接種的納米碗微粒111的外表面上的金納米種子114之間產生填充材料來進行,正如過程105中所示。例如,生產填充材料涂層115可以包括將示例性接種的二氧化硅納米碗111/聚苯乙烯芯112復合物置于離子金溶液中并且添加填充金納米種子114之間空間的還原劑。在一些實施方式中,例如,涂層115可以在二氧化硅納米碗微粒111上作為外殼生長。在圖1中所示的實例中,金納米微粒種子114促進生長位置,從而在二氧化硅納米碗微粒111上產生外部金殼。最終,示例性合成方法100可以包括除去示例性芯微粒112,正如過程106中所示。在一些實施方式中,例如,正如過程107中所示,示例性合成方法100可以包括例如使用不同的適合的溶劑和酸進一步向下浸蝕納米碗微粒111的示例性二氧化硅材料,以便擴展二氧化硅納米碗載體主體120的中空內部區。
圖2顯示使用不同分子修飾示例性納米碗載體的外和/或內表面的示例性官能化方法,例如,得到內部加載有效負荷230和選擇性官能化以便外部包括靶向分子225的納米碗載體主體220。例如,正如圖2中所示,對于示例性二氧化硅納米碗主體120的內表面,烷氧基硅烷化學物質可以用于各種分子載荷或有效負荷例如包括藥物或造影劑在內的分子形成界面(interface)。圖3顯示使用用于與二氧化硅發生面接的包含巰基的硅烷的馬來酰亞胺官能化的實例的示意圖。涉及圖2,例如,對于示例性二氧化硅納米碗主體120的外表面,帶有游離巰基或胺的任意分子可以用于自發地連接至示例性金涂層的表面。這可以用于例如連接鈍化劑,如聚乙二醇或靶向部分。正如圖2的實例所示,納米碗載體主體220可以包括納米碗載體主體220的外表面(例如示例性金涂層115的外表面)上的官能化層211以便連接靶向劑225或鈍化劑。
所公開的納米碗可以被構造成包括包含分子載荷或有效負荷的蓋(例如封蓋),其可以在需要使用外部刺激時被可控地打開。在一些實施方案中,例如,可以使用DNA origami、完全包囊和包裹微粒的脂質體或聚合物生成所述封蓋。在一些實施方案中,例如,可以將所述封蓋選擇性地置于納米碗腔上,以密封具有內部俘獲的示例性載荷(例如任意藥物、造影劑等)的納米-載體。圖4A和4B說明示例性激光輔助的或RF-輔助的加熱技術以便可控地打開和關閉所述封蓋。納米碗載體可以在其鄰近位置釋放有效負荷。在一些實施方式中,這可以牽涉使所述封蓋上(例如覆蓋微粒)與DNA束縛。例如,DNA的熔點基于核苷酸組成和長度可高度調節的。使用~50nm大小的示例性封蓋微粒并且使用連接至封蓋微粒和載體的納米碗結構的DNA的互補鏈,可以生成熱敏感性墊或密封物。或者,例如,脂質體也可以用于密封微粒。
實例如圖3、4A和4B中所示,示例性納米碗表面(圖3)和示例性載體封蓋結構和與納米碗結構的連接機制(圖4A和4B),用于可控地打開/關閉載體以便加載和釋放載荷至納米碗內部和從其中離開。例如,載荷或有效負荷230(例如藥物、造影劑或其它類型載荷)如圖3中所示被官能化至納米碗載體主體220內部區,例如官能化至示例性二氧化硅納米碗微粒111的內表面。為了差別官能化,可以使用藥物或造影劑修飾納米碗載體主體220內部。一種用于連接的這樣的實例是使用烷氧基硅烷修飾藥物(一甲基奧瑞他汀E(monomethylauristatin E),MMAE),如圖3中所示。此外,例如,封蓋的納米碗載體可以用于將藥物封閉在內部并且可控地打開封蓋結構以便能夠釋放藥物。可以將有效負荷/載荷加載入示例性納米碗載體主體220的內腔并且用可以通過外部刺激連接并且可控地啟動以便打開和關閉的示例性封蓋微粒密封。在一些實例中,可以將有效負荷(例如藥物)加載入納米碗載體主體(例如將納米碗與高濃度的期望的有效負荷一起溫育),且封蓋微粒可以通過自組裝的單層(SAM)或其它類型的封蓋微粒與納米碗的官能化層的自組裝連接至納米碗并且密封開口(例如將有效負荷封閉在內部區域內)。在另外的實例中,封蓋微粒可以通過DNA開關連接至納米碗并且密封開口(例如將有效量有效負荷封閉在內部區域內),其中將DNA的切換開關“ON”切換至打開(OPEN)位置,以便使有效負荷擴散入腔,且其中將DNA切換開關“OFF”切換至關閉(CLOSED)位置,以便將有效負荷密封在納米碗內部。
有效負荷從納米碗載體中的可控制釋放放
在實施方式中,例如,可以使用多種機制的任意種操作所公開的納米碗載體,以便使載荷/有效負荷(例如分子)連接至納米-載體并且從該納米-載體中釋放所述載荷/有效負荷(例如分子)。在納米碗載體的示例性實施方案中,包括內部官能化的載荷/有效負荷分子(例如藥物、造影劑等),化學連接基可以使活性分子與納米碗結構(例如二氧化硅等)的內部區域形成界面。在MMAE的實例情況中,它通過胞內發現的酶敏感性二肽連接基(纈氨酸-瓜氨酸)保持連接至示例性二氧化硅內部。可以使用另外的化學連接基,它們對細胞外部的酶敏感,使得它也可以在那里釋放其有效負荷。還可以使用對光、pH和敏感的另外的化學連接基,使得該化學連接基按需釋放有效負荷。
在納米-載體的示例性實施方案中,包括封蓋或蓋結構,納米-載體可以被構造成在功能上對外部刺激有響應,例如磁性納米微粒的RF加熱或金殼的近紅外(NIR)加熱,例如,以便將封蓋熔化掉(正如圖4A中所示例的)或啟動DNA開關/閂鎖打開(正如圖4B中所示例的)。當除去加熱時,例如,DNA開關關閉,并且切斷膠囊外部的治療劑擴散。用于啟動開關的可選方法可以包括使用另一條DNA鏈進行DNA置換或與另外的化學部分發生相互作用。
圖4A顯示納米碗載體主體220內部區域中加載有效負荷230的示例性納米碗載體400A的說明性示意圖,其中封蓋微粒420(例如金納米微粒)對開口密封,使得有效負荷230被封閉在納米碗載體400A內,并且不能滲漏出納米碗載體400A。在納米碗載體的該示例性實施方案中,封蓋微粒420包括在封蓋微粒420外表面上的官能化層411,例如具有特定核苷酸序列的核酸,所述官能化層411被配置成例如通過烷氧基硅烷鍵連接互補鏈415、例如具有官能化至納米碗載體主體220內部區域的互補核苷酸序列的DNA鏈。包括納米碗載體400A的核苷酸序列和互補鏈415的官能化層411可以形成分子鉸鏈(例如核酸,例如DNA),其連接至納米碗載體主體220的二氧化硅內部區域和封蓋微粒420,以使封蓋微粒420結合納米碗載體主體220,其可以基于外部刺激可控地被打開。正如圖4A的示意圖中所示,當將外部刺激(例如光刺激(例如激光)、RF刺激等)施加于納米碗載體400A以導致納米微粒113和/或金涂層115(產熱)激發時,使得所述分子鉸鏈415熔化,由此釋放封蓋微粒420并且能夠釋放有效負荷230’。
圖4B顯示納米碗載體主體220內部區域中加載有效負荷230的示例性納米碗載體400B的說明性示意圖,其中使用可切換的閂鎖結構440使封蓋微粒420(例如金納米微粒)對開口密封,使得有效負荷230被封閉在納米碗載體400B內,并且不能滲漏出納米碗載體400B。在納米碗載體的該示例性實施方案中,封蓋微粒420包括連接至納米碗載體主體220的二氧化硅內部區域中的封蓋微粒420的可切換閂鎖結構440。在一些實施方式中,例如,可切換的閂鎖結構440包括分子拉鏈和彈簧裝置,例如DNA拉鏈彈簧傳動裝置。分子拉鏈和彈簧裝置的實例描述在美國專利公開號US 2014/0080198A1中,將該文獻的全部內容作為本專利文件公開內容的組成部分引入參考。例如,可以通過偶聯至封蓋微粒420的示例性分子拉鏈/彈簧傳動裝置440可控地阻塞開口,得到納米微粒閘門機制,當特定刺激(例如互補核苷酸序列)被納米碗載體400B識別時,其可以打開和分離或關閉開口。可切換閂鎖結構440能夠拉開拉鏈,使得其部分延伸以便從開口中開啟封蓋微粒420,由此使得有效負荷230’從納米碗載體400B中釋放。在另外的實施方式中,例如,可以通過施加外輻射(例如近紅外加熱金殼115、RF加熱氧化鐵納米微粒113和/或金殼115)打開納米碗載體400B的封蓋微粒420。這類加熱可以通過施加的輻射產生,使得示例性分子拉鏈/彈簧傳動裝置440可以打開,且除去加熱可以關閉拉鏈并且重新密封微粒。
示例性分子拉鏈/彈簧傳動裝置440在一條臂上共價連接至納米微粒(即封蓋微粒420),其足夠大以阻塞納米碗載體主體220開口。另一方面,示例性分子拉鏈/彈簧傳動裝置440共價連接至納米碗載體主體220內部(例如在內部區域底部)。傳動裝置440的拉鏈結構的分子序列可以被設計成與核苷酸或病毒的RNA或DNA的某一序列互補。在該特異性鏈的識別時,拉鏈可以解開和開啟膠囊中的開口。在一種應用中,例如,有效負荷230可以包括可以被載入納米碗載體主體220的抗病毒藥,且由此可以被釋放入細胞,以便在納米碗載體400B遇到具有與分子拉鏈/彈簧傳動裝置440互補序列的病毒時,治療病毒感染。
圖4C顯示在配置為關閉、打開和分離狀態的分子拉鏈/彈簧傳動裝置時可切換閂鎖結構440的實例的示意圖。關閉狀態491的實例納米碗載體包括通過一條臂連接至封蓋微粒420并且通過另一條臂連接至納米碗載體主體220內部的示例性分子拉鏈/彈簧傳動裝置,其中納米碗載體主體220偶聯有拉鏈結構的互補序列,使得內部區域的開口被封蓋微粒420完全阻塞和密封。在如打開狀態492中所示的互補核苷酸序列(例如病毒或其它寡核苷酸)識別時,拉鏈展開且納米微粒開啟膠囊開口,使得內部有效負荷被釋放。作為再次纏繞和導致納米碗載體成為關閉狀態的可替代選擇,例如,分子拉鏈/彈簧傳動裝置可以被配置成在與互補核苷酸雜交時使偶聯臂與封蓋微粒420分離,正如分離針頭493中所示,使得封蓋微粒420與納米碗載體完全分離且釋放有效負荷。
在圖4A和4B的說明性示意圖中所示的實施方案實例中,納米碗載體400A和400B被構造成包括具有單一封蓋微粒420的單一開口,以便對開口密封并且將有效負荷230封閉在載體內部區域內部。在另外的示例性實施方案中,例如,納米碗載體400A和400B可以包括通過在制造過程中例如使用方法100使用多個芯微粒112形成的納米碗載體主體120上的多個開口;且納米碗載體400A和400B可以包括多個封蓋微粒420和可傳動釋放機制(例如分子鉸鏈結構415或可切換閂鎖結構440),以便對相應的開口密封并且將有效負荷230封閉在載體內部區域內部。
納米碗載體至特定細胞的靶向
納米-載體可以通過使靶向分子連接至微粒外部靶向至特定細胞。在使用金涂層的一些實例中(例如示例性納米碗結構的金填充劑和/或鍍層),可以通過使用帶有游離巰基或胺基團的靶向分子實現這一目的。巰基和胺基團自發地與金表面形成強鍵。外表面還可以被鈍化配體如聚乙二醇修飾,以便改善血流中的循環時間。
納米碗載體的磁性引導
在一些實施方式中,例如,可以將強外部磁體置于所關注的身體區域,且通過靜脈內注射的納米碗載體優先在接近磁體的局部組織內收集。例如,這在難以接近例如腦或深部癌瘤區域中是特別有用的。圖5顯示示例性納米碗載體(例如納米碗載體400A或400B)的示例性實施方式的說明,其中強磁體可以優先將示例性磁響應納米碗拉出血流并且使其進入所關注的組織。
納米碗合成的示例性制造方法和官能化
在一些實施方式中,所公開的制造方法可以包括使用基于溶液的方法生產磁敏感性金納米碗結構的合成技術,實施所述基于溶液的方法可以生成具有兩個可以被官能化的化學不同表面的微粒,如圖1中所示。進行示例性制造方法的示例性實施方式,且一些示例性結構如圖6和7中所示。圖6顯示示例性(N-(2-氨基乙基)-3-氨基丙基)三甲氧基硅烷(AEAPTMS)修飾的二氧化硅納米微粒的FTIR光譜圖。圖7顯示描述實施示例性制造方法和表征這類方法各自產物的結果的圖像(例如圖7的標度條(scale bar)表示50nm)。
制造方法的示例性實施方式包括使用二氧化硅/聚苯乙烯模板以便合成納米碗結構。例如,在帶有磁攪棒的玻璃小瓶中,制備去離子(DI)水、無水異丙醇和氫氧化銨的溶液。同時向所述溶液中,加入在劇烈攪拌的溶液形式的羧化聚苯乙烯(PS,100nm)和原硅酸四乙酯(TEOS)。將所述溶液攪拌2hrs。然后通過以1000g離心7min洗滌所述溶液,將沉淀重新懸浮于異丙醇2次和DI水2次。最終在2mL水中進行分散。
制造方法的示例性實施方式包括二氧化硅胺表面官能化技術。例如,將(N-(2-氨基乙基)-3-氨基丙基)三甲氧基硅烷(AEAPTMS)加入到無水乙醇中,形成1%(v/v)溶液。將一定量的SiO2/PS模板加入到所述溶液中,使官能化進行2hrs。此后,用無水乙醇和DI水將微粒洗滌2次。最終的洗滌后,將微粒重新懸浮于2mL DI水。
制造方法的示例性實施方式包括使氧化鐵納米微粒連接至載體。例如,氧化鐵合成包括使FeCl3·6H2O和FeCl2·4H2O的混合物與氫氧化銨在氮氣氣氛中在80℃下反應,然后在添加油酸后使所述溶液反應1.5小時。用去離子水將制成的磁石納米微粒洗滌至中性pH。例如,氧化鐵穩定(使用檸檬酸鹽)包括使油酸涂敷的納米微粒在水中旋轉,潷析水。然后將微粒懸浮于檸檬酸、氯仿和N,N-二甲基甲酰胺(DMF)的混合物中。然后將所述混合物在90℃在油浴中攪拌12小時。從油浴中拉出微粒,使其冷卻至室溫。隨后使用磁體,通過添加分離的乙醇沉淀微粒。將微粒分散于丙酮中,再通過磁體分離3-4次,以除去所有痕量的游離檸檬酸。將檸檬酸鹽修飾的微粒再懸浮于DI水。例如,氧化鐵納米微粒接種于模板微粒結構包括包括在45℃將胺修飾的模板微粒溶液和檸檬酸鹽修飾的氧化鐵溶液共同攪拌至少30min。為了從所述混合物中除去過量的游離氧化鐵納米微粒,將所述溶液重復離心至少2次。顯示氧化鐵連接在帶正電荷的200nm SiO2上的示例性結果的圖像如圖7的D組中所示。
制造方法的示例性實施方式包括將金接種至載體。例如,制備金種溶液的方法包括如下步驟。在攪拌的同時用四(羥甲基)磷鎓氯化物(THPC)的濃溶液還原氫氧化鈉(NaOH)和氯金酸(HAuCl4)。將所述溶液在4℃在冷藏箱中放置24小時,然后用于生成5nm大小金種。例如,金接種納米碗模板包括使金納米微粒連接至模板微粒,其中將胺-修飾的模板微粒溶液和膠體金溶液在45℃攪拌至少30min。為了除去過量的游離物,離心所述溶液,洗滌至少4次。當成功時,例如,典型地形成深紅色沉淀,將其再分散于DI水。
制造方法的示例性實施方式包括通過鍍金使在載體上形成外部涂層。例如,通過混合K2CO3、HAuCl4、DI水和在4℃下暗處過夜制備鍍金溶液。該步驟將氯金酸轉化成氫氧化金溶液。將一定量的金接種的模板微粒加入到相似量的相當的氯金酸中。將甲醛加入到鍍金溶液中以啟動鍍層。使鍍層進行30分鐘;在此過程中,溶液從澄清變成深紫色。然后用DI水將微粒洗滌4次,以除去過量的金離子,再分散于2mL DI水中。
制造方法的示例性實施方式包括從載體結構中除去芯微粒。例如,在室溫(RT)下將模板微粒放入過量的四氫呋喃(THF)2天。然后用水洗滌微粒以便除去痕量的THF。
制造方法的示例性實施方式包括除去部分載體結構。例如,通過浸蝕形成載體內腔。在聚苯乙烯溶解后,通過NaOH浸蝕載體,形成納米碗結構,其中將官能化的二氧化硅納米碗結構放入1M NaOH溶液1小時,隨后使用HCl中和NaOH。
圖7的圖像顯示所用示例性制造方法的不同方法實施方式的示例性結果。示例性二氧化硅/聚苯乙烯(SiO2/PS)模板微粒合成及其隨后使用胺的修飾(例如,其中示例性表征結果如圖6中所示)易于再現。示例性SiO2/PS模板微粒被生產為180-200nm直徑,如圖7的A組中所示。正如圖6中所述FTIR光譜所顯示的,模板上的二氧化硅成功地被二氧化硅和胺的標記修飾。正如圖7B組中所示,用DMF處理微粒,在其后面遺留其中使用過聚苯乙烯微粒的腔。可以使用NaOH進一步浸蝕打開內腔,正如圖7的C組圖像中所示。首先使用胺修飾的商購可得到的200nm SiO2測試氧化鐵和金的連接,以便觀察它們是否可以被共同接種。然后將預先接種氧化鐵的微粒(圖7,D組)與金種一起溫育。圖7的E組顯示這種雙重接種。在一些實施方式中,鍍金的二氧化硅微粒可以被配置成均勻的,而在另外的情況中,如圖7的F組中所示,其可以被配置成零散的(patchy)。
表面官能化部分從示例性納米碗中的示例性釋放
一旦納米碗載體被合成,則可以給它們加載任意各種分子有效負荷,例如藥物,并且在納米結構的化學上不同的表面上被靶向部分官能化。在靶向分子CPE和藥物MMAE的示例性情況中,這些分子易于被修飾。例如,所述過程可以使用可以在胞內被酶裂解的纈氨酸瓜氨酸(VC)二肽連接基進行。或者,例如,對胞外肽類敏感的連接基也可以用于釋放藥物。
表面連接:為了二氧化硅表面的內部官能化,本文還通過用巰基丙基三甲氧基硅烷(MPTS)取代包含巰基的硅烷使用用于示例性Mal-vc-MMAE–CPE連接的馬來酰亞胺-硫化學,如圖3中所示。可以加入過量的MPTS,以確保MPTS完全連接至vcMMAE。這類硅烷官能化策略可以用于使熒光團官能化,然后連接至二氧化硅。為了外部官能化,示例性靶向劑CPE290-319可以在肽的C-末端上使用半胱氨酸定制合成。這種巰基易于在水性條件下連接至金。官能化首先可以使用CPE290-319在過量的最大數量的CPE肽類中開始,所述肽類可以被壓縮在微粒表面上。在離心和洗滌后,隨即可以將微粒與MPTS-Mal-vc-MMAE一起溫育。這種連接可以在乙醇中進行。
細胞靶向:可以使用抗-CPE抗體對處理細胞進行免疫組織化學來證實綴合物的胞吞作用。攝入的CPE290-319會在熒光顯微鏡上顯示處于細胞的胞質溶膠中。為了測試細胞毒性,例如,人卵巢癌細胞系2008和OVCAR-3超表達密蛋白(claudin)-3和-4蛋白,且不同量的綴合物可以用于測試治療效能。2008細胞中的密蛋白-3和密蛋白-4的敲低(knockdown)可以作為陰性對照。此外,可以將綴合物與游離MMAE和游離CPE290-319比較。在直至96小時的多個時間點,CPE290-319-vc-MMAE綴合物、游離MMAE和游離CPE290-319對培養物中腫瘤細胞的作用可以使用細胞計數試劑盒-8(Cell Counting Kit)試驗評價。例如,為了敲低生成,可以實施如下操作。可以用慢病毒構建體遞送的shRNAi處理2008細胞以敲低密蛋白-3或-4。同時敲低兩種蛋白質可以導致細胞死亡。通過mRNA表達和蛋白質表達驗證敲低可以使用逆轉錄酶PCR和蛋白質印跡進行。例如,為了綴合物的穩定性,可以實施如下操作。綴合物的穩定性可以通過在PBS中溫育該綴合物并且在不同時間間隔檢查降解產物來測試。此外,可以通過將連接基與組織蛋白酶-B一起溫育并且使用LC/MS檢查分離的MMAE測試連接基官能度。細胞死亡機制可以包括如下。例如,MMAE是高度有效的微管蛋白連接劑。蛋白質印跡可以檢查CPE290-319-vc-MMAE處理的細胞與未處理細胞中游離微管蛋白與微管之比,以便證實MMAE靶向預期的蛋白質,從而誘導細胞凋亡。在一些實施方式中,例如,可以使用磁體定位微粒進行。例如,強磁體可以用于在培養皿中將微粒定位于確定的位置。
示例性納米碗結構的示例性封蓋
使用任意多種策略封蓋示例性納米碗主體。例如,這類封蓋可以包括納米碗的不可逆打開和納米碗的可逆打開以及使用脂質體。
示例性DNA連接的金微粒作為封蓋微粒的:納米碗-封蓋微粒可以包括被DNA官能化的金微粒,從而生成致密官能化的DNA微粒。在一些實例中,它牽涉使用~20個核苷酸的巰基基修飾的DNA用于起始官能化。然后因DNA上的磷酸鹽,可以使鹽的濃度升至較低靜電排斥。可以進行第二輪的官能化以便生成致密的DNA官能化金微粒。為了使DNA連接至二氧化硅,可以使用胺官能化的互補DNA。可以使用羧乙基-硅烷三醇一鈉溶液使二氧化硅被羧基官能化。該分子與二氧化硅表面上的無機羥基基團反應,得到用于胺官能化的DNA的連接點。然后EDC/NHS交聯劑可以用于使羧基基團連接在胺上。在這些微粒被DNA官能化后,可以共同溫育封蓋微粒和納米碗并且形成一種微粒。
封蓋微粒與納米碗主體的示例性連接不限于DNA或金微粒。其它不可逆連接可以對化學或酶降解有響應。此外,還可以包括應用可重復使用的、可切換的分子連接或打開和關閉的傳動結構即閥門。
制造方法可以包括幾點,此時,可以進行表征。一個實例包括,在完成DNA連接后,DNA連接染料如Sybr Green可以用于證實封蓋微粒或納米碗中存在DNA。另一個實例包括在封蓋微粒退火后至納米碗。這可以通過使用凝膠電泳比較退火的封蓋和納米碗各自與納米碗和封蓋微粒比較證實。另外,可以使用TEM使各微粒成像,以便顯示成功組合。
為了示例性有效負荷(例如藥物)加載,可以實施如下操作。例如,在納米碗和封蓋被退火前,可以加入高度過量的藥物,并且在納米碗和封蓋退火時,藥物在物理上應當保持被俘獲在納米碗的容積內。通過RF脈沖或NIR激光加熱微粒應當將考慮加熱至足以熔化互補DNA,且由此釋放微粒。釋放還可以通過化學方式進行,例如與互補DNA鏈的相互作用,使用添加其它肽類、離子或小分子的構型轉化。
所公開的納米碗的示例性實施方案
在所公開的技術的一些示例性實施方案中,所公開的納米結構載體可以包括帶有磁官能團的不對稱金和二氧化硅納米碗結構,其中用于制造這些示例性納米結構載體的方法可以包括如下過程。示例性制造方法可以包括使用芯-衛星模板的過程,生成為包括單一較大的帶負電荷的芯和許多較小的與之連接的帶正電荷的衛星微粒而構造的納米碗。模板微粒可以用于合成多孔金殼。示例性制造方法可以包括使用正電荷芯和負電荷衛星的過程,生成納米碗結構,即芯-衛星模板,可以由它合成納米碗結構。在示例性過程中,可以使用靜電吸引其它材料例如包括金、二氧化硅和/或氧化鐵圍繞衛星微粒特定地合成納米碗結構。示例性過程可以包括溶解芯-衛星模板以便從該模板中釋放多個納米碗。
可以將所公開的納米結構載體作為具有可以儲存特定載荷的確定封閉結構(例如納米級碗-樣結構)的遞送系統應用。可以將所公開的納米結構載體作為具有防止載荷被動滲漏(例如被動擴散)的孔的遞送系統應用。可以將所公開的納米結構載體作為具有可以按需打開和關閉的封蓋的遞送系統應用。可以使用本技術的模板輔助的方法將所公開的納米結構載體制成不對稱碗納米結構的形式,其中示例性納米碗結構選擇性地圍繞芯-衛星模板的衛星形成,例如使用靜電吸引。
圖8顯示描述所公開的技術的示例性制造方法800的示意圖說明,所公開的技術的示例性制造方法800使用芯-衛星模板定向的方法生產示例性納米碗結構。各種材料可以用于使用示例性芯-衛星模板微粒-輔助的方法800生成不同的納米碗結構,如圖8中所示。使用方法800生產的納米碗結構的實例可以包括二氧化硅納米碗、金納米碗和磁響應金納米碗。方法800包括用于生產芯-衛星模板微粒810的過程801,所述芯-衛星模板微粒810被構造成包括較大的帶負電荷的芯微粒811和較小的帶正電荷的衛星微粒812。在一些實施方式中,例如,過程801可以包括以預定比例共同混合帶負電荷的芯微粒和帶正電荷的衛星微粒,例如小于1:100的芯與衛星微粒。例如,1:100芯與衛星微粒之比得到足夠的衛星以便飽和全部芯微粒。帶正電荷的衛星812可以選擇性地被修飾以便吸引帶負電荷的分子或納米微粒。
方法800包括基于所生產的芯-衛星模板微粒810生產二氧化硅納米碗結構822的過程802。例如,過程802可以包括無機二氧化硅圍繞帶正電荷的衛星微粒812生長和模板微粒、即芯微粒811和衛星微粒812溶解,得到多個合成的二氧化硅納米碗結構822。所合成的二氧化硅納米碗結構822包括外部二氧化硅殼結構和中空內部,包括中空內部的開口。
方法800包括基于所生產的芯-衛星模板微粒810生產金納米碗結構832的過程803。例如,過程803可以包括形成金納米微粒種子831,其被吸引至衛星微粒812,使金殼832通過金納米微粒種子831在衛星微粒812上生長;和模板微粒、即芯微粒811和衛星微粒812溶解,以便釋放金納米碗結構833。所合成的金納米碗結構833包括外部金殼和中空內部,包括中空內部的開口。
方法800包括基于所生產的芯-衛星模板微粒810生產磁響應金納米碗結構844的過程804。過程804可以包括吸引氧化鐵納米微粒種子841和金納米微粒種子831至帶正電荷的衛星微粒812。過程804可以包括使金殼832通過內部包埋氧化鐵納米微粒841的金納米微粒種子831在衛星微粒812上生長。過程804可以包括溶解模板微粒、即芯微粒811和衛星微粒812,導致形成磁響應金納米碗結構844。所合成的磁響應金納米碗結構844包括金殼內包埋氧化鐵納米微粒的外部金殼和中空內部,包括中空內部的開口。值得注意的是,可以使用圖8中所示的示例性制造方法800使另外的材料生長和形成,以便成形并且產生所公開的技術的納米碗結構。
圖9A和9B顯示掃描電子顯微鏡檢查(SEM)圖像,其顯示出使用所公開的模板合成制造方法由帶負電荷的1000nm聚苯乙烯芯(圖9A中)和帶正電荷的100nm(陽離子聚電解質官能化的)聚苯乙烯衛星(圖9B)中生產的材料。例如,也可以由純二氧化硅或二氧化硅和聚苯乙烯混合物制成模板。圖10顯示例如根據圖8中所示方法在聚苯乙烯模板的衛星微粒上形成的納米碗的二氧化硅外部的具有遞增厚度(例如左至右)的示例性制造的結構的SEM圖像。圖10的SEM圖像顯示通過控制二氧化硅形成條件能夠控制在衛星微粒上生長的示例性納米碗的二氧化硅外部的厚度,所控制的條件例如,TEOS的量,包括中值量的TEOS(中間圖像)和大量的TEOS(右側圖像)。
在一些實施方式中,例如,示例性的制造方法可以包括使用陽離子聚電解質(例如聚(二烯丙基二甲基氯化銨)或聚(烯丙基胺鹽酸鹽))涂敷羧化物-修飾的聚苯乙烯球(例如100nm直徑)。示例性的制造方法可以包括靜電吸引帶負電荷的芯(例如1000nm直徑),例如其中芯可以由羧化物-修飾的聚苯乙烯和二氧化硅制成。然后,可接種衛星微粒并且鍍金和/或涂敷二氧化硅或涂敷氧化鐵。
在所公開的技術的一些示例性實施方案中,可以使用芯-衛星模板合成所公開的納米碗結構,所述芯-衛星模板包括大的帶正電荷的芯和許多較小的與之連接的帶負電荷的衛星微粒。圖11A顯示使用表面官能化的芯和衛星微粒模板生產納米碗結構(例如二氧化硅納米碗)的一個實例的說明性示意圖,其包括如下過程。正如圖11A中所示,所述方法包括使帶負電荷的芯微粒(例如1μm聚苯乙烯)使用涂層(例如聚合物涂層,例如聚二烯丙基二甲基氯化銨(PDDA))官能化的過程1101,以便形成帶正電荷的芯微粒表面。所述方法包括連接衛星微粒(例如100nm帶負電荷的聚苯乙烯微粒(例如聚苯乙烯-COOH))的過程1102。所述方法包括過程1103,其使帶正電荷的官能化的芯和帶負電荷的衛星模板與帶正電荷的硅烷反應,形成殼結構(例如二氧化硅殼結構),例如QuATPmS或ATPmS等,視期望的表面修飾而定。所述方法包括過程1104,其通過除去官能化的芯–衛星模板、例如使用有機溶劑浸蝕掉聚苯乙烯和涂敷芯的聚合物(PDDA)生產納米碗結構。圖11B-11D顯示示例性制造方法實施過程中得到的微粒的說明性示意圖和相關的SEM圖像。圖11B中所示的SEM圖像(A)顯示100nm PS-COOH衛星,其通過電荷相互作用被連接至PDDA-涂敷的聚苯乙烯芯。圖11C中所示的SEM圖像(B)顯示使用QuATPmS涂敷后的結構或花粉樣團(polle),例如,每個衛星的尺寸增加了20-30nm。圖11D中所示的SEM圖像(C)顯示使用DMF的浸蝕過程后產生的納米碗結構。圖11B-11D中的示例性刻度條表示500nm。
示例性方法包括形成聚合物涂敷的模板的過程。例如,用DI水稀釋特定量的1μm羧化物-修飾的聚苯乙烯;向所述溶液中分別加入劇烈攪拌溶液形式的NH4OH(29%)和聚二烯丙基二甲基氯化銨(PDDA)。聚合物涂敷的模板形成過程可以包括使反應進行,例如20分鐘。例如,可以用4.5mL DI水稀釋500μL 1μm PS-COOH(2.7%vol/vol)水溶液;然后可以加入320μL NH4OH(29%),攪拌;在攪拌的同時,可以加入2.5mL 1%PDDA,保持攪拌20分鐘。聚合物涂敷的模板形成過程可以包括洗滌溶液,例如通過以3200g離心15min和將沉淀再懸浮于DI水中3次和乙醇中2次來進行。聚合物涂敷的模板形成過程可以包括最終分散于80%乙醇的DI水溶液。
示例性方法包括使衛星微粒連接至聚合物涂敷的模板微粒的過程。例如,可以將1μm在80%乙醇中的PDDA涂敷的羧化物-修飾的聚苯乙烯與特定量的100nm羧化物-修飾的聚苯乙烯一起溫育30分鐘。然后可以通過以1000g離心5min將所述溶液洗滌3次。衛星微粒連接方法可以包括在乙醇中進行最終分散。
示例性方法包括通過胺表面官能化使二氧化硅官能化的過程。例如,可以將乙醇添加到產生的溶液中。官能化過程可以包括劇烈攪拌所述溶液。官能化過程可以包括向攪拌的溶液中添加少量N-(三甲氧基甲硅烷基丙基)-N,N,N-三甲基氯化銨,即在甲醇中50%(QuATPmS)。官能化過程可以包括使攪拌的反應進行例如2小時,然后將其加熱至60℃,例如,同時再攪拌2小時。官能化過程可以包括通過離心、例如以3200g離心15min 3次用DI水洗滌反應溶液。
示例性方法包括過程形成聚電解質涂層或TMOS涂層。示例性方法包括除去示例性聚苯乙烯的過程。例如,模板除去過程可以包括將模板微粒置于過量的DMF中,同時攪拌和在100℃加熱過夜。模板除去過程可以包括離心樣品和再懸浮于DMF,例如重復3次。模板除去過程可以包括用水洗滌微粒以除去痕量的DMF。
所公開的詹納斯納米微粒的示例性實施方案
兩種或更多種不同表面特性的膠體微粒(詹納斯微粒)在催化、生物成像和遞藥中具有意義。偏心式納米微粒是詹納斯微粒的類型,其包括封閉大部分模板微粒的殼,從而使得部分模板表面暴露。公開了本技術所公開的納米結構和制造方法的示例性實施方案,包括圍繞詹納斯模板(例如羧化物-修飾的聚苯乙烯芯)的二氧化硅殼構成的偏心式詹納斯納米微粒的溶液-凝膠合成。在用有機溶劑除去聚苯乙烯芯后合成納米級碗-樣結構。示例性詹納斯模板(例如偏心式二氧化硅/聚苯乙烯微粒)和納米碗結構可以用作用于位點專一的官能化或治療診斷學的通用平臺。
具有兩種或更多種獨特表面化學的膠體微粒可以稱作詹納斯微粒,例如在Roman神話的兩面神像之后命名的。多表面化學的組合可以生成具有其自身獨特特性的材料。詹納斯微粒可以在催化、生物醫學成像和藥物遞送中具有寬泛的應用。
所公開的技術包括溶液-凝膠、非-微乳化方法,其用于具有包囊詹納斯模板(例如羧化物-修飾的聚苯乙烯芯)的二氧化硅殼(例如稱作納米級橄欖微粒或‘橄欖;)的偏心式二氧化硅微粒的受控合成。所公開的方法包括制造二氧化硅納米微粒(溶液-凝膠)且可以包括添加羧基修飾的聚苯乙烯。描述了所公開的制造方法的示例性實施,其顯示聚苯乙烯模板大小、表面官能化和原硅酸四乙酯(TEOS)濃度對詹納斯模板-樣微粒形態的作用,并且顯示了用有機溶劑除去聚苯乙烯芯后示例性合成的納米碗結構。納米碗可以被設計成具有腔或中空內部區域,其可以用于儲存有效負荷(例如治療劑)并且在實施過程中可以被生物相容性材料結構封蓋,用于治療劑(例如造影劑分子和治療劑)的有效和受控遞送和釋放。
用于實例實施的示例性方法和材料如下。例如,材料包括如下。得到羧化物(PS-COOH)修飾表面的球形膠體聚苯乙烯,其具有:50nm(實際45±6.2nm)直徑,在水中2.6%;100nm(實際:85±6.7nm)直徑,在水中2.62%;和200nm(實際:190±6.5nm)直徑,在水中2.65%。得到具有胺(PS-NH2)修飾表面的聚苯乙烯,其具有:200nm(實際:230nm±16.1)直徑,在水中2.5%;硫酸鹽(PS-SO4)修飾表面的聚苯乙烯,在水中2.65%,200nm(實際194±9nm)直徑和羥基(PS-OH)修飾表面,200nm直徑(實際190±16.1nm),在水中2.6%。得到氫氧化銨(NH4OH,29.79%)、二甲基甲酰胺(DMF)、TEOS(98%)和無水異丙醇(IPA)。在全部示例性實施方式中使用的去離子水使用具有18.2MΩ電阻的Millipore Advantage A10系統生產。
例如,實例微粒形成過程如下。在具有700μL H2O、4mL IPA和1.3mL NH4OH的20mL玻璃閃爍瓶中合成二氧化硅橄欖。向所述混合物中同時加入100μL聚苯乙烯球和83μL TEOS(60mM),同時攪拌(另有描述的除外)。使所述溶液反應2小時,然后通過離心終止反應(另有描述的除外)。將反應混合物以500g離心5min;將上清液轉(沉淀棄去)至新鮮15mL離心管并且以或大于3000g離心5min(例如3221g 5min)。將得到的沉淀分散于~15mL IPA。通過在IPA中(例如以3221g)離心2次洗滌微粒,然后再分散并且用H2O洗滌2次(例如通過以3221g離心)。
例如,微粒直徑和成像技術的確定如下。使用動態光散射(DLS)或通過來自SEM圖像的100個測量值的平均值測量微粒直徑。例如,Brookhaven ZetaPlus DLS儀器用于測量溶液中的微粒尺寸。將每個樣品測量5次,得到信號平均值。報告最大峰。直方圖得自DLS或SEM測量值并且使用OriginPro 7.0繪圖。為了成像,例如,使用鈀噴涂樣品以便改善成像,例如使用Emitech K575X噴涂器。SEM圖像使用配備FEI Sirion柱的FEI XL30得到,以便能夠超高分辨。
實例實施的示例性結果如下。圖12顯示在反應開始時使用羧化聚苯乙烯納米微粒(PS-COOH)并且使用氫氧化銨溶液、IPA、DI水制造的示例性偏心式二氧化硅/聚苯乙烯微粒(例如二氧化硅納米級橄欖)的示意圖說明,其中添加TEOS和PS-COOH、以偏心方式圍繞PS-COOH集中的二氧化硅。過量的PS-COOH產生具有在二氧化硅中包埋一個或多個模板的橄欖。使用有機溶劑(例如DMF)除去模板,生成二氧化硅納米碗結構(例如無聚苯乙烯模板的橄欖)。在示例性的實施方式中,例如,橄欖的實際形成相當快速地發生,例如在前15-20分鐘內,且反應從半透明溶液變換成不透明的白色溶液。另外的處理時間不影響橄欖的形態;它僅允許使微粒固化的時間,但不包裹暴露的聚苯乙烯。只要反應期限為18hr,則在SEM中觀察到橄欖。反應通常在2hr后終止,例如,這確保不形成聚集物。圖13A-13D顯示反應溶液中1hr(圖13A)、2hr(圖13B)、3hr(圖13C)和18hr(圖13D)后使用60mM TEOS生產的示例性偏心式二氧化硅/聚苯乙烯微粒的SEM圖像。聚苯乙烯模板始終保持部分暴露。
圖14A-14E顯示使用不同TEOS濃度形成的示例性納米級橄欖結構的SEM圖像,例如保持所有另外的反應劑恒定。示例性圖像顯示從遞增TEOS濃度出現的兩種趨勢,例如(i)橄欖直徑遞增;和(ii)被二氧化硅覆蓋的聚苯乙烯遞增。使用如下TEOS濃度以便形成橄欖。每個示例性制造條件的平均橄欖直徑和變異系數包括:(a)20mM(222nm,0.15),如圖14A中所示;(b)40mM(206nm,0.08),如圖14B中所示;(c)60mM(244nm,0.15),如圖14C中所示;(d)80mM(298nm,0.18),如圖14D中所示;和(e)100mM(539nm,0.34),如圖14E中所示。例如,調整TEOS濃度、同時保持每種另外的條件相同改變至二氧化硅封閉PS-COOH的程度。當TEOS濃度和聚苯乙烯的二氧化硅覆蓋增加時,所以微粒大小正如DLS所測定的,如圖14A中所示。在低TEOS濃度(例如20mM,40mM)下,半數至四分之三的聚苯乙烯表面被二氧化硅封閉。在較高濃度(例如80mM、100mM)下,二氧化硅幾乎吞沒聚苯乙烯。
例如,3種不同大小的PS-COOH用于研究模板大小對偏心式微粒形成的作用。使用60mM TEOS與標準反應條件、無PS、50nm、100nm和200nm直徑PS-COOH模板合成微粒。圖15A-15E顯示使用60mM TEOS濃度、應用不同大小的模板、即不同直徑的PS-COOH模板合成的示例性納米級橄欖結構的SEM圖像和數據圖:(a)50nm,如圖15A中所示;(b)100nm,如圖15B中所示;(c)200nm直徑,如圖15C中所示;和(d)無模板,如圖15D中所示。圖15E顯示描述使用50nm和100nm模板制成的橄欖的數據圖,其顯示當與無模板制成的二氧化硅樣品比較時較小的平均直徑。例如,未報告使用200nm模板進行橄欖合成的大小分布,因為二氧化硅難以圍繞眾多200nm模板包裹(例如它們聚集,遺留其中聚苯乙烯球曾經存在的凹印(imprint))。正如圖15A和15B中SEM圖像所示例的,50nm和100nm PS-COOH模板成功地制成偏心式納米微粒。這些橄欖平均小于純的二氧化硅微粒。然而,60mM TEOS混合物中包括的200nm PS-COOH顯然難以形成或完全不形成。例如,從SEM圖像中可以看出,二氧化硅試圖圍繞PS-COOH包裹,但并不成功,遺留圓形凹槽(indent)和大量聚集的微粒。比較具有200nm PS-COOH大小的純二氧化硅微粒(例如350nm),示例性結果啟示,存在二氧化硅可以吞沒PS-COOH的大小的上限。可以啟示形成過程中二氧化硅與PS-COOH的相互作用歸因于多個弱鍵。偏心式微粒的成功形成由此可以在生長時鉸鏈連接,足以使二氧化硅通過物理方式俘獲PS-COOH。
在示例性實施方式的示例性結果中,例如,模板微粒的表面官能度顯然在橄欖形態上起重要作用。將200nm PS-NH2、PS-OH或PS-SO4加入60mM TEOS反應溶液得到完全被二氧化硅包囊的微粒。圖16A-16C顯示表征使用胺類(圖16A)、羥基(圖16B)和硫酸酯/鹽(圖16C)官能化的示例性200nm聚苯乙烯球的SEM圖像和附帶數據圖,例如將它們加入到60mM TEOS溶液中。例如,這些聚苯乙烯球被二氧化硅均勻地涂敷,正如SEM和DLS分析數據圖所證實的。例如,通過得到的微粒直徑隨聚苯乙烯模板大小增加和顯示具有平滑形態的球形微粒的SEM圖像觀察到這一結果。因此,TEOS與PS-COOH之間的一些不確定的相互作用能夠使示例性橄欖納米結構形成,其不與包含另外的表面官能團的聚苯乙烯模板一起出現。
例如,示例性實施方式的示例性結果可以啟示,二氧化硅與PS-COOH在形成過程中與多個弱鍵發生相互作用之間相互作用。例如,比較具有200nm PS-COOH大小的純的二氧化硅微粒(350nm),啟示芯的大小與表面官能度在詹納斯模板形成過程中起重要作用。詹納斯模板的成功形成由此可以在生長時鉸鏈,足以使二氧化硅通過物理方式俘獲芯。
可以使用方法使二氧化硅圍繞不同表面官能度的聚苯乙烯生長。在一些實施方式中,均勻的殼圍繞胺-終止的聚苯乙烯生長,而二氧化硅島圍繞硫酸鹽/酯終止的聚苯乙烯生長。那些實施方式與所述示例性實施方式之間的差異可能歸因于所用水和氫氧化銨的相對量。上述那些實施方式使用3.5mL DI水和0.5mL氫氧化銨;水的體積高于氫氧化銨6倍。在所公開方法的示例性實施方式中,所用的水的體積約為所用氫氧化銨體積的一半。二氧化硅納米微粒的直徑(例如使用方法形成的那些)對于反應條件中的較小改變都高度敏感并且對于殼的形成可能亦是如此。
例如,因為示例性納米級橄欖結構在同一微粒上包含二氧化硅和羧基基團,所以化學部分如靶向部分和治療劑可以以空間確定的方式獨立地連接。所述橄欖可以具有作為多功能遞送平臺的應用,因為它可以在納米級上以空間方式構成不同的化學部分,這是在現存遞藥系統如納米脂質體或二氧化硅中不常見的特征。或者,例如,通過除去聚苯乙烯,所述橄欖變成具有用于治療劑或診斷劑的內部載體空間的納米碗。然后所公開的納米碗可以被生物相容性材料封蓋,包括PLGA、脂質體和脫乙酰殼多糖。
對于治療劑從納米碗結構中的有條件釋放和控制釋放,例如封蓋(例如封蓋微粒),有效負荷可以通過與DNA的特異性相互作用、酶加工或環境觸發器如溫度和pH而被釋放。現存的遞送系統提出具有孔或開放表面,其能夠被動和/或連續釋放其載荷(造影劑分子或治療劑)。所公開的納米碗結構可以用于控制釋放造影劑分子或治療(治療診斷)劑。
所公開的納米/微米球結構的示例性實施方案
在本技術的一些方面中,公開了技術、系統和裝置,其用于制造和實現納米/微米級載體結構,其具有中空的和多孔殼官能化的內和/或外表面并且能夠磁性引導,它們能夠控制釋放有效負荷、改善細胞攝取和其它特征。在一些實施方式中,所公開的技術的納米/微米級載體結構可以用于靶向和按需遞送用于人和動物中異常病理學情況和疾病的診斷和/或治療的分子和小分子(例如重組治療診斷劑)。
具有100nm至100μm直徑的中空的、多孔微米-和納米-粒在催化、光電子學、生物傳感、治療劑和診斷劑的納米遞送、細胞培養和毒素清除方面具有特別的意義。這類微粒結構用于包囊和儲存。在一些情況中,納米微粒被另外的元素、例如金或允許任務定向的官能化的自組裝的有機分子表面修飾。這種額外的官能化可以包括對光、溫度、pH和其它環境線索的反應性。例如,金通常具有許多非常具有吸引力的光物理學特性,這些特性能夠被利用于成像和熱操作。金可以用于設計不同結構,包括實心球和桿體、中空結構例如納米籠和芯/殼結構。
在一些實施方案中,例如,所公開的技術可以包括用于生產納米/微米載體結構的制造方法,通過制造包括芯微粒的模板微粒來進行,所述芯微粒被用于制造可以因期望應用被官能化的選擇材料形成的多孔和/或中空/多孔殼結構的掩蔽微粒覆蓋。在一些實施方案中,例如,可以將殼結構制成金納米級或微米級高爾夫球,其具有實體二氧化硅芯,所述芯具有帶有連通芯的凹孔或孔的外部金殼表面。在一些實施方案中,例如,可以將殼結構制成具有帶有連通中空內部的孔的金殼表面的中空的和多孔的金納米級或微米級威浮球。這些實施方案可以進一步被修飾允許容納二氧化硅殼內的金層或島,由此促進使外的實體(例如氧化鐵微粒、分子、鈍化劑)連接至載體結構內部。
在一些實施方案中,例如,用于生產所公開的納米/微米級載體結構的制造方法可以包括如下過程的一個或多個。示例性制造方法可以包括:(i)合成花粉-樣模板微粒,其具有與之連接的較大中心微粒和較小衛星微粒,例如所述微粒可以由二氧化硅、聚苯乙烯或兩者的組合制成;其中該合成可以包括(i.a.)將小的金納米微粒(例如~5nm)添加至花粉-樣模板外部;(i.b.)使用金納米微粒使較大的金島或金殼生長;和/或(i.c)通過在分步溶解二氧化硅中溶解模板生成多孔高爾夫球-樣殼或中空的和多孔的威浮球-樣殼。示例性的制造方法可以包括(ii)對模板進行修飾,其可以包括使示例性二氧化硅層圍繞金島或金殼生長和/或將氧化鐵納米微粒添加至示例性二氧化硅高爾夫/威浮球-樣殼的外和/或內表面。示例性的制造方法可以包括(iii)使結構(例如球/微粒)的內和外表面差別官能化;用烷氧基硅烷修飾示例性二氧化硅表面并且除去芯。示例性的制造方法可以包括(iv)將分子有效負荷(例如例如藥物、圖像造影劑等)載入殼。例如,可以載入殼的分子有效負荷可以包括藥物、造影劑、酶、蛋白質、激素、糖蛋白、糖脂、核酸、適體、脂質和/或者金屬的、聚合的或陶瓷的納米微粒。示例性的制造方法可以包括(v)從示例性威浮球中控制釋放分子有效負荷。示例性的制造方法可以包括(vi)使用鈍化層、例如包括聚乙二醇或類似的惰性聚合物對表面進行外表面修飾,并且添加靶向部分以便改善細胞攝取。示例性的制造方法可以包括(vii)在外部磁場作用下將示例性磁加載的高爾夫/威浮球載體結構導入特定位置。
可以將所公開的納米/微米載體結構配置成能夠是內表面雙向官能化的微粒,例如,這歸因于存在金和二氧化硅。磁性引導所公開的納米/微米載體結構通過包含磁材料是可能的。所公開的制造方法可以使用基于同一模板的合成方法生產多種類型的微粒,例如兩種示例性多孔高爾夫球-樣載體結構和中空/多孔威浮球-樣載體結構。所公開的制造方法可以生產這些多種微粒類型,其具有不同的大小,例如具有200nm或1μm直徑。
圖17-21顯示用于生產和實現所公開的納米/微米載體結構的制造技術的說明性示意圖。
殼結構的示例性合成
圖17顯示描述生產用于形成結構的不同反應的多孔和中空/多孔的載體結構的示例性制造方法的說明性示意圖,所形成的結構例如為多孔高爾夫球-樣載體結構(納米高爾夫球)和中空的和多孔的威浮球-樣載體結構(納米威浮球)。所述制造方法包括用于合成模板微粒的過程1701,所述模板微粒包括使掩蔽微粒連接至芯微粒,例如,可以通過靜電相互作用連接。在過程1701的一些實施方式中,例如,帶負電荷的衛星膠體聚苯乙烯球(例如~100nm)可以用作掩蔽微粒并且連接至較大陽離子二氧化硅芯微粒(例如~1μm)。所述制造方法包括使納米微粒連接至芯微粒的未覆蓋部分的過程1702。在過程1702的一些實施方式中,例如,膠體金連接至示例性二氧化硅芯微粒,其中示例性聚苯乙烯掩蔽微粒防止這類金連接在其中掩蔽微粒連接至芯微粒的區域上。例如,可以通過將小的金納米微粒(例如~5nm)添加至花粉樣模板的外部形成金層。所述制造方法包括通過使連接的納米微粒在芯微粒的未覆蓋部分上的材料生長形成層的過程1703,由此在模板上形成殼結構。在過程1703的一些實施方式中,例如,使用生產金殼的金納米微粒使較大的金島或區域在模板上生長。例如,可以將模板浸入氫氧化金溶液并且處理以便導致金種成核進入圍繞模板的金殼。所述制造方法包括從模板中除去掩蔽微粒形成多孔的載體結構的過程1704。在過程1704的一些實施方式中,例如,在二氧化硅芯微粒上形成的具有外部金多孔殼的多孔高爾夫球結構可以通過溶解示例性聚苯乙烯掩蔽微粒形成。另外或可選地,所述制造方法包括通過除去微粒和芯微粒(或至少部分芯微粒)除去模板以形成中空的多孔的載體結構的掩蔽過程1705。在過程1705的一些實施方式中,例如,可以通過在分步溶解過程中溶解示例性聚苯乙烯掩蔽微粒和示例性二氧化硅芯、例如首先溶解掩蔽微粒且然后溶解芯微粒形成金多孔殼的中空的和多孔的威浮球結構。
模板和/或殼的示例性修飾
所述制造方法還可以包括對模板進行能夠使殼差別官能化的表面修飾過程。在一些實施方式中,例如,所述制造方法可以包括使二氧化硅層圍繞金殼生長的過程。圖18A顯示金殼1812上示例性載體結構包括二氧化硅殼1811的說明性示意圖。在一些實施方式中,例如,所述制造方法可以包括形成金島的過程。圖18B顯示包埋在二氧化硅殼1821內部的金島1822上包括二氧化硅殼1821的示例性載體結構的說明性示意圖。在一些實施方式中,例如,氧化鐵納米微粒可以被連接入殼的外部和/或內部。圖19顯示加入到圖18A的示例性二氧化硅/金殼內部的包括氧化鐵納米微粒1933的示例性載體結構的說明性示意圖。在一些實施方式中,例如,也可以將氧化鐵納米微粒1933置于殼的外部。
所述制造方法還可以包括對形成的殼結構進行能夠使用不同分子使殼外部和/或內部官能化的表面修飾過程。圖20顯示示例性載體結構的說明性示意圖,包括使用分子和/或小分子2040(例如,包括有效負荷,例如藥物)在內部和使用靶向分子2050在外部使示例性二氧化硅殼1821/金島1822的選擇性官能化。所述制造方法可以包括使用二氧化硅表面,烷氧基硅烷化學使各種分子形成界面的過程。所述制造方法可以包括例如使用游離巰基或胺在金表面上連接分子的過程,所述游離巰基或胺自發地連接至金表面。例如,這可以用于連接鈍化劑,如聚乙二醇或靶向部分。
具有有效負荷的示例性載體加載
為了差別官能化,例如,可以使用藥物或造影劑修飾內部。一種這類用于連接的實例是使用連接至殼結構的烷氧基硅烷或基于材料連接至殼結構的連接分子修飾藥物(一甲基奧瑞他汀E,MMAE)。
有效負荷從載體中的示例性釋放
在一些實施方式中,化學連接基使活性分子與二氧化硅形成界面。可以使用的化學連接基可以選自對細胞內部或外部的酶敏感的那些,例如導致有效負荷在靶標處從載體中控制釋放。另外的示例性化學連接基可以選自對光、pH和溫度或其它刺激物敏感的那些,以便控制有效負荷遞送。
載體結構可以靶向至特定細胞。例如,在使用威浮球結構(例如中空的和多孔的載體結構)的實施方式中,載體可以通過使靶向分子連接在殼的外部靶向至特定細胞。例如,對于外部金殼,這可以通過使用帶有游離巰基或胺基團的靶向分子實現。巰基和胺基團與金表面自發地形成強鍵。外表面還可以被鈍化配體如聚乙二醇修飾,以改善血流中的循環時間。
載體的示例性磁性引導
在使用制造的納米/微米載體結構的一些實施方式中,例如,納米高爾夫球和納米威浮球,可以將強外部磁體置于所關注的身體區域上,且可以將載體經靜脈內注入體內(例如在生物相容性溶液中),以便優先集中于接近磁體的局部組織。例如,這對于難以接近的區域特別有用,例如腦或深部癌瘤。正如上述圖5中所示,可以將納米/微米載體結構(例如納米高爾夫球或納米威浮球)注入受試者(例如人或動物受試者)血流,且強磁體可以用于引導和定向(例如優先拉出)示例性磁響應載體(例如納米球)離開血液并且進入所關注的組織。
用于納米球載體合成和官能化的制造方法的示例性實施方式
在一些實施方式中,所公開的制造方法可以包括如下示例性合成技術,以便使用基于溶液的方法生產磁敏感性金/二氧化硅納米球結構,如圖17-20中所示。進行示例性制造方法的示例性實施方式,其中示例性結果如圖21中所示。
PDDA對示例性二氧化硅微粒的表面官能化
膠體二氧化硅在高于~2.2的pH值下具有凈負表面電荷。可以使用陽離子聚電解質例如聚(二烯丙基二甲基氯化銨)(PDDA)逆轉膠體二氧化硅表面上的凈電荷。PDDA以靜電方式連接至表面并且逆轉膠體二氧化硅表面上的凈電荷。聚合物中的季銨離子與膠體的脫質子化的硅烷醇基之間形成化學計算的鹽鍵。這通過向5mL 2%膠體二氧化硅的分散體(pH≥11)中添加320μL氫氧化銨來進行。隨后,在4℃下將所述溶液放入超聲冰浴,且然后向所述混合物中加入5mL 1w%t PDDA水溶液。將得到的溶液保持在超聲浴中20min。然后將包含所述溶液的試管以3200g離心10min,以除去未吸附的聚合物。將離心和再分散重復4次,在兩者之間進行清潔容器的轉換。將白色沉淀重新分散于5mL水。
示例性模板的合成
帶負電荷的衛星膠體聚苯乙烯球連接至較大的陽離子二氧化硅芯。~100nm直徑的羧基-官能化的聚苯乙烯球以靜電方式被吸引至1000nm PDDA-官能化的二氧化硅。在2mL離心管中,將1mL PDDA-官能化的二氧化硅以3200g離心并且再分散于1mL EtOH中。在4℃下將包含PDDA-官能化的二氧化硅溶液的試管放入超聲冰浴10min。然后向PDDA-官能化的二氧化硅中加入25μL羧基-官能化膠體聚苯乙烯水溶液,保持在超聲冰浴中另外5min。然后將所述混合物以1000g離心5min,潷析,并且將淀重新分散于1mL水。
金種與模板的連接
具有1-3nm直徑的膠體金納米微粒用作鍍金過程的金種。將54mL水和50μL 10M氫氧化鈉彼此混合。在單獨的容器中,用1mL水稀釋12μL 80%四(羥甲基)磷鎓氯化物(THPC),加入到原始溶液中,攪拌5min。向所述溶液中加入15mL 1%氯金酸,再持續攪拌30min。將金種溶液在4℃下靜置24小時,然后使用。THPC同時還原氯金酸和穩定水溶液中的金納米微粒,得到帶有負電荷的金納米微粒。推定金的堆積密度且完全轉化成3nm金種,金種濃度為1.0×1016金種/mL。
通過共同添加100μL模板溶液和5mL金種溶液、同時劇烈攪拌使示例性金種連接至模板。將所述溶液在45℃攪拌至少30min。為從所述混合物中除去過量的游離金種,將所述溶液以1000g離心10min。將該離心步驟重復至少2次。最終,形成淡粉白色沉淀,將其重新分散于1mL水中。
示例性金殼的生長
使用氫氧化金溶液使金殼在帶有連接的聚苯乙烯衛星的示例性金-接種的膠體二氧化硅模板上生長。在100mL瓶子中,通過將70mL5.37mM K2CO3攪拌10min、然后向所述溶液中添加3.15mL 1%氯金酸制備氫氧化金溶液。最初氫氧化金溶液為亮黃色,在冷藏前攪拌1小時后變澄清。將所述溶液在4℃下置于黑暗中24小時。然后用于電鍍(plating)。然后將500μL金-接種的模板加入到15mL氫氧化金中并且劇烈混合5min,然后添加50μL 37%甲醛。甲醛添加通過將氫氧化金還原成金屬金啟動電鍍過程。該步驟進行后快速添加5μL NH4OH。這導致金種圍繞模板成核為殼。使用大玻璃杯將得到的溶液混合約3小時。然后將所述混合物以1000g離心5min以除去溶液。將該步驟重復至少4次。將沉淀重新分散于2mL水中。
示例性模板的溶解
當除去100nm聚苯乙烯衛星時,生成示例性金高爾夫球。離心后將鍍金的模板重新分散于5mL二甲基甲酰胺(DMF)中。將包含所述溶液的試管在60℃下放入超聲水浴中20min,然后以3200g離心10min并且重新分散于DMF中。將離心和使用DMF沖洗重復2次以上,然后再分散于水中。
通過經金高爾夫球分散于10%氫氟酸(HF),同時在2mL離心管中除去二氧化硅芯制成中空金高爾夫球。將得到的混合物保持靜置24小時。將該步驟再次重復。通過與水一起離心將中空金高爾夫球沖洗6次且然后再分散于2mL水中。
圖21A-21F顯示使用上述示例性合成技術的示例性多孔和中空/多孔納米載體結構(例如金高爾夫球)的掃描電子顯微照片(SEM)圖像。圖21A的圖像(A)顯示示例性1000nm聚苯乙烯/SiO2模板。圖21B的圖像(B)顯示模板的示例性金種。圖21C的圖像(C)顯示金殼生長。圖21D的圖像(D)顯示較小聚苯乙烯的溶解(例如形成金高爾夫球)。圖21E的圖像(E)顯示SiO2芯微粒的溶解(例如形成中空金威浮球)。圖21F的圖像(F)顯示示例性1000nm金殼模板的廣角視圖。圖21A-21E的圖像中所示的標度條表示200nm。圖21F的圖像中所示的標度條表示2μm。
雙官能化的中空的多孔納米微粒的示例性實施方案
在所公開的技術的一些示例性實施方案中,中空的多孔納米微粒(例如中空的多孔二氧化硅納米球)、包括雙向-官能化的中空的多孔納米微粒可以在示例性分步靜電組裝過程中合成。圖22A和22B顯示可以用于在雙向-官能化模板結構上制造所公開的技術的多孔中空納米-/微米-微粒(例如二氧化硅納米球)的示例性合成方法的說明性示意圖,其中可以將所生產的多孔中空納米微粒制成在微粒內部上具有一個化學官能團,而在微粒外部上具有另一個化學官能團。正如圖22A中所示,所述方法包括使帶負電荷的芯微粒官能化的過程2201,例如形成涂層,從而在芯微粒上提供帶正電荷的表面。例如,在過程2201的一些實施方式中,通過第一涂層(例如PDDA)來涂敷1μm修飾的羧化聚苯乙烯微粒以形成帶正電荷的芯微粒。所述方法包括再修飾官能化微粒的過程2202,從而形成第二涂層,以便在帶負電荷的芯上的帶正電荷的第一官能化層上得到帶負電荷的官能化表面,例如,由此產生雙-官能化的芯微粒。例如,在過程2202的一些實施方式中,第二涂層(例如聚(丙烯酸)(PAA))可以在芯微粒上形成,以便形成雙-官能化的芯微粒的帶負電荷的表面。所述方法包括使帶正電荷的衛星微粒連接至多層涂敷的帶負電荷的芯微粒的過程2203。例如,在過程2203的一些實施方式中,雙-官能化聚合物涂敷的芯(例如PAA-PDDA-PS)可以連接至100nm胺修飾的聚苯乙烯微粒。所述方法包括在芯-衛星模板上形成殼(例如二氧化硅殼)的過程2204。例如,在過程2204的一些實施方式中,帶正電荷的硅烷(例如QuATPmS)可以生長在帶負電荷的PAA-PDDA-PS芯上,同時避免生長在帶正電荷的衛星上,從而在芯微粒上產生二氧化硅殼。在所述方法的一些實施方式中,如圖22A中所示,例如,所述方法包括除去芯-衛星模板和產生中空的多孔納米微粒(例如中空的多孔二氧化硅納米球)的過程2205。例如,在過程2205的一些實施方式中,用有機溶劑浸蝕芯和衛星微粒。而在所述方法的一些實施方式中,如圖22B中所示,例如,所述方法可以包括過程2205前在殼上形成外部官能化表面(例如涂層)的過程2206,其中所述涂層包括與殼帶相反的電荷。例如,在過程2206的一些實施方式中,原硅酸四乙酯(TEOS)可以用于在雙-官能化的芯模板上的二氧化硅殼上形成最終的薄層。
在圖22A和22B中所述方法的一些實施方案中,例如,方法可以使用過程2201中起始帶正電荷的芯微粒實施,以便形成具有帶負電荷的表面的官能化的芯微粒。過程2202可以包括在芯微粒上形成帶正電荷的第二涂層,以便形成雙-官能化的芯微粒,使得過程2203包括使帶負電荷的衛星微粒連接至雙-官能化的芯微粒的帶正電荷的外表面。過程2204可以包括使用帶負電荷的涂層材料形成殼(例如帶負電荷的硅烷形成二氧化硅殼),使得過程2206可以包括在殼上形成帶正電荷的外部官能化的表面。
圖23A和23B顯示示例性中空的多孔納米球合成方法的實施過程中得到的實例微粒的SEM圖像。圖23A和23B中的示例性標度條表示200nm。
示例性方法包括形成聚合物涂敷的模板的過程。例如,用DI水稀釋特定量的1μm羧化物-修飾的聚苯乙烯;向所述溶液中以劇烈攪拌溶液的形式分別加入NH4OH(29%)和聚二烯丙基二甲基氯化銨(PDDA)。聚合物涂敷的模板形成過程可以包括使反應進行,例如20分鐘。聚合物涂敷的模板形成過程可以包括,例如通過以3200g離心15min和將沉淀再懸浮于DI水3次洗滌溶液。然后,將沉淀在懸浮于DI水中。聚合物涂覆的模板形成過程可以包括添加一定量的聚(丙烯酸)(PAA),同時溶液攪拌,例如其中所述過程允許相反電荷的聚電解質(PAA)在PDDA上組裝。允許反應20分鐘。然后,聚合物涂覆的模板形成過程可以包括,例如通過以3200g離心15min和將沉淀再懸浮于DI水3次洗滌溶液。最終分散可以在80%乙醇的DI水溶液中進行。
示例性方法包括使衛星微粒連接至聚合物涂敷的模板微粒的過程。例如,將1μm PAA/PDDA涂敷的羧化物-修飾的在80%乙醇中的聚苯乙烯微粒與特定量的100nm氨基-修飾的聚苯乙烯一起溫育30分鐘。然后通過以1000g離心5min將所述溶液洗滌3次。最終分散在乙醇中進行。衛星微粒連接過程可以包括在乙醇中進行最終分散。
示例性方法包括通過胺表面官能化使二氧化硅官能化的過程。例如,可以將乙醇加入到產生的溶液中。官能化過程可以包括劇烈攪拌所述溶液。官能化過程可以包括向攪拌的溶液中加入少量N-(三甲氧基甲硅烷基丙基)-N,N,N-三甲基氯化銨的50%甲醇溶液(QuATPmS)。官能化過程可以包括允許攪拌的反應進行,例如2小時,然后加熱至60℃,例如,同時再攪拌2小時。官能化過程然后可以包括通過離心、例如以3200g離心15min 3次用DI水洗滌反應溶液。
示例性方法包括除去示例性聚苯乙烯的過程。例如,模板除去過程可以包括將模板微粒置于過量的DMF中,同時攪拌和在100℃加熱過夜。模板除去過程可以包括離心樣品和再懸浮于DMF,例如重復3次。模板除去過程可以包括用水洗滌微粒以除去痕量的DMF。
中空納米金高爾夫球和威浮球的示例性實施方案
中空的、多孔納米微粒例如納米-載體、納米脂質體、納米殼、中間多孔天然有機材料具有催化、光電子學和生物傳感的廣泛應用,以便遞送治療劑和診斷劑。眾多這些中空納米結構由基于硅的材料或有機聚合物制成且通常被金屬和用于任務定向的官能化的自組裝的有機分子涂敷。描述了這類多孔和中空的多孔納米結構及其使用模板合成方案的制造方法的示例性實施方案。例如,在另外的載體結構設計中,如下所述的示例性制造方法能夠生產:(i)具有帶有凹孔的實心二氧化硅芯和金表面的納米級球(例如納米高爾夫球);和(ii)表面上帶有中空金殼和孔的納米級球,例如無二氧化硅(例如納米威浮球)。在一些實施方式中,例如,通過將帶負電荷的100nm直徑聚苯乙烯珠接觸帶正電荷的1微米直徑二氧化硅芯生成模板。隨后鍍金和溶解聚苯乙烯珠產生具有等距離直徑(例如100nm)的凹孔的金殼,類似于高爾夫球。此外,通過溶解二氧化硅芯,生成具有孔的中空高爾夫球。示例性制造方法的所公開的模板策略可以適用于另外的金屬和氧化物。
所公開的技術的示例性中空的、多孔微米-和納米-微粒可以用于各種應用,包括催化、光電子學、生物傳感、治療劑和診斷劑的納米遞送、細胞培養和毒素清除。這類結構因存在孔也用于包囊和儲存。納米微粒可以被另外的元素表面修飾,例如金或能夠工作定向的官能化的自組裝的有機分子。這種額外的官能化可以包括對光、溫度、pH和其它環境線索的反應性。
金通常具有許多非常具有吸引力的光物理學特性,其能夠被利用于成像以及熱操作,例如,包括表面等離子共振(SPR)、表面增強的拉曼光譜法(SERS)和光熱加熱。在生物學應用中,金是生物相容性的且可被包含巰基的配體和靶向分子修飾。
生成中空的、多孔金納米結構因其光學響應表面及其儲存或催化的能力而也是富有吸引力的。在先在制備這類納米結構時的嘗試限于大尺寸(數十個微米大小范圍)。使用所公開的技術,例如,可以設計和生成可控大小的金殼高爾夫球和中空金威浮球(例如200nm和1μm直徑,如本文所述示例性實施方式中所示),其具有可控大小的特征,例如凹孔大小和孔徑,這表明本納米結構制造技術的可伸縮性。
進行示例性實施方式以便制造和表征示例性納米級和微米級金高爾夫球和金威浮球。使用下列示例性材料。得到具有羧化物修飾的表面(PS-COOH,2.73wt%水溶液)與100nm直徑的膠體聚苯乙烯球、具有200nm或1000nm直徑(2wt%的水溶液)的球形膠體二氧化硅(SiO2)和聚(二烯丙基二甲基氯化銨)(PDDA)Mw~8,500(28wt%的水溶液)。得到四(羥甲基)磷鎓氯化物(THPC)(80%的水溶液)和氫氧化鈉(NaOH,10M)。得到碳酸鉀(K2CO3)、甲醛(37%)、氫氧化銨(NH4OH)(29.79%)、氫氟酸(HF,48%)和二甲基甲酰胺(DMF)和無水乙醇(EtOH)。得到為粉末和制備成1wt%水溶液的氯金酸(HAuCl4)。在全部實施方式中使用的水使用具有18.2MΩ電阻的Millipore Advantage A10系統生產。
示例性的制造方法可以包括用PDDA使二氧化硅微粒表面官能化的過程。膠體二氧化硅在高于~2.2的pH值下具有凈負表面電荷。可以使用陽離子聚電解質例如PDDA逆轉膠體二氧化硅表面上的凈電荷。PDDA以靜電方式連接至表面并且逆轉膠體二氧化硅表面上的凈電荷。聚合物中的季銨離子與膠體的脫質子化的硅烷醇基之間形成化學計算的鹽鍵。這通過向5mL 2%膠體二氧化硅的分散體(pH≥11)中添加320μL氫氧化銨來進行。隨后,在4℃下將所述溶液放入超聲冰浴,且然后向所述混合物中加入5mL 1w%t PDDA水溶液。將得到的溶液保持在超聲浴中20min。然后將包含所述溶液的試管以3200g離心10min,以除去未吸附的聚合物。將離心和再分散重復4次,在兩者之間進行清潔容器的轉換。最終沖洗時,將二氧化硅沉淀重新分散于5mL水中。
示例性的制造方法可以包括合成模板的過程。例如,使帶負電荷的衛星膠體聚苯乙烯球連接至較大的陽離子二氧化硅芯。~100nm直徑的羧基-官能化聚苯乙烯球以靜電方式被吸引至1000nm PDDA-官能化的二氧化硅。例如,在2mL離心管中,以3200g離心1mL PDDA-官能化的二氧化硅并且再分散于1mL EtOH中。在4℃下將包含PDDA-官能化的二氧化硅溶液的試管放入超聲冰浴10min。然后將25μL羧基-官能化膠體聚苯乙烯水溶液加入到PDDA-官能化的二氧化硅中,并且保持在超聲冰浴中另外的5min。然后將所述混合物以1000g離心5min,潷析并且將沉淀重新分散于1mL水中。
示例性的制造方法可以包括使金種連接至模板的過程。例如,將具有1-3nm直徑的膠體金納米微粒用作鍍金過程的金種。在這些示例性實施方式中,膠體金接種溶液的用途依賴于在其合成過程中混合反應物的次序和方法。例如,可以通過共同混合54mL水和50μL 10M氫氧化鈉制備它們。在單獨的容器中,用1mL水稀釋12μL 80%THPC,靜置5min,然后加入到氫氧化鈉水溶液中。然后將所述混合物再攪拌5min,然后添加2mL 1wt%HAuCl4。所述溶液變成棕紅色,攪拌30min,然后儲存在4℃下(例如24小時,然后所用)。將金種溶液在4℃下靜置24小時,然后使用。THPC同時還原氯金酸和穩定在水溶液中的金納米微粒,得到帶有負電荷的金納米微粒。例如,推定金的堆積密度和完全轉化成3nm金種,金種濃度為1.0×1016金種/mL。
通過共同添加100μL模板溶液和5mL金種溶液、同時劇烈攪拌使金種連接至模板。將所述溶液在45℃攪拌至少30min。為了從所述混合物中除去過量的游離金種,將所述溶液以1000g離心10min。將該離心過程重復至少2次。最終,淡紅白色沉淀形成,重新分散于1mL水中。
示例性的制造方法可以包括使金殼生長的過程。例如,通過示例性無電鍍過程使金種生長成互聯的金殼結構(例如在金-接種的帶有連接的聚苯乙烯衛星的膠體二氧化硅模板上)。例如,通過將70mL 5.37mM K2CO3水溶液攪拌10min、然后添加3.15mL 1wt%HAuCl4制備氫氧化金(Au(OH)3)儲備溶液(例如183μM)。氫氧化金溶液最初為亮黃色的,在冷藏前攪拌1小時后變澄清。將所述溶液置于4℃下黑暗中老化24小時,然后用于電鍍。然后將500μL金-接種的模板加入到15mL氫氧化金溶液中,劇烈攪拌5min,然后添加50μL 37%甲醛。例如,添加甲醛通過將氫氧化金還原成金屬金啟動電鍍過程。該工藝步驟后快速添加5μL 29%NH4OH。例如,所述過程導致金種成核進入圍繞模板的殼。使用大玻璃杯(例如電轉烤肉架)混合得到的溶液和翻滾約3小時。然后將所述混合物以1000g離心5min,潷析以除去廢物并且再分散于水中。將該工藝過程重復至少4次。將沉淀再分散于2mL水中。
示例性的制造方法可以包括除去模板(例如通過溶解)和形成金高爾夫球結構的過程。例如,當除去100nm聚苯乙烯衛星時,生成金高爾夫球,例如通過經離心后再分散于5mL DMF用溶劑溶解聚苯乙烯。離心后將鍍金的模板再分散于5mL DMF。將包含所述溶液的試管在60℃下放入超聲水浴20min,然后以3200g離心10min并且再分散于DMF中。將離心和使用DMF沖洗重復2次以上,然后再分散于水中。
在所述方法的一些實施方式中,例如,示例性的制造方法可以包括除去二氧化硅芯和形成中空金威浮球結構的過程。例如,通過經將金高爾夫球分散于10%HF中、例如同時在2mL離心管中除去二氧化硅芯制成中空金高爾夫球,其中將得到的混合物保持靜置24小時。離心高爾夫球并且用HF浸蝕1次以上。再通過與水一起離心沖洗中空金球(例如威浮球)(例如6次),然后再分散于2mL水中。
例如,使用FEI XL30SFEG UHR顯微鏡在5kV加速電壓下得到掃描電子顯微鏡檢查(SEM)圖像。
圖24顯示用于制造多孔納米-/微米-級高爾夫球和中空的多孔納米-/微米-級威浮球的示例性合成方法的說明性示意圖。圖24中所示的實例產生金納米高爾夫球和金納米威浮球。正如該示意圖中所示,在金接種過程2401中,被帶有以靜電方式連接的較小聚苯乙烯(PS)衛星球的陽離子聚電解質(PDDA)官能化的二氧化硅芯微粒用于選擇性地連接其PDDA-官能化的二氧化硅芯上的納米大小的膠體金。顯示無電鍍過程2402,其描述使納米大小的金種生長為互聯的金殼。通過溶解聚苯乙烯衛星合成金高爾夫球微粒,如過程2403中所示。在所述方法的一些實施方式中,如過程2404中所示,隨后溶解二氧化硅芯完成中空的多孔金威浮球微粒的合成。
示例性合成方法的示例性實施方式產生如下實例結果。通過使100nm羧基-修飾的聚苯乙烯連接至1000nm PDDA-官能化的二氧化硅芯合成模板。通過在合成過程中改變聚苯乙烯球的濃度,可以將連接至二氧化硅芯的聚苯乙烯球的量控制到飽和,其中實例如圖21A的SEM圖像中所示。這可以歸因于靜電排斥,其限制可以連接至表面的聚苯乙烯微粒數量。金殼形成包括小金種連接至模板和填充種子之間的間隙的無電鍍過程。例如,金種具有負表面電荷并且被THPC單層穩定。這將金種吸引至模板上帶正電荷的PDDA-官能化的二氧化硅的表面。由于類似原因,所以種子的負表面電荷防止連接至模板上的聚苯乙烯。這些種子由此用作接下來的部分金殼形成的成核部位,其中實例如圖21B的SEM圖像中所示。金殼生長通過將金離子還原成金屬金來完成。生長優先發生在預先形成的金表面即金接種的模板上。當種子生長時,它們彼此接觸并且最終圍繞接種的部分模板形成完整的金殼,其中實例如圖21C中的SEM圖像所示。在金殼形成后,模板微粒溶解可以生成金高爾夫球微粒(例如圖21D的SEM圖像中所示的實例)或中空的多孔微粒(例如圖21E的SEM圖像中所示的實例)。例如,通過溶解聚苯乙烯珠,生成金高爾夫球。此外,例如,將二氧化硅溶于HF稀溶液產生內部中空的多孔殼。金高爾夫球形成的進一步檢驗顯示聚集未隨目前的反應條件發生,其中實例如圖21F的SEM圖像所示。
金殼的厚度和完整性根據種子在模板上的表面覆蓋度、金還原動力學和金離子/模板比決定。例如,模板上較為致密的金接種意味著金種不必生長為較大,以便接觸相鄰種子。經測定,二氧化硅上金種的飽和極限約為30%表面覆蓋度,無鹽。可以預計模板芯上金接種密度接近飽和極限。
通過改變甲醛濃度和金離子濃度控制模板微粒上的金殼生長。圖25A-25C顯示使用遞增甲醛濃度例如7μL(圖25A)、50μL(圖25B)和100μL(圖25C)制備的15mL 183μM氫氧化金電鍍溶液的鍍金模板微粒的SEM圖像;示例性標度條表示100nm。圖25D-25F顯示使用50μL 37%甲醛與不同量的氫氧化金溶液例如2.5mL(圖25D)、5mL(圖25E)和15mL(圖25F)的鍍金模板微粒的SEM圖像;示例性標度條表示500nm。例如,推定充分接種的模板,厚度和完整性還受限于甲醛/金反應動力學。由于反應自由能是高度有利的,所以模板上的金沉積率是殼形成的決定性因素。在添加甲醛時,金生長不足以使金種彼此接觸。這導致金殼不完整。為了形成完整的金殼,如圖25A-25C中所示需要較高濃度的甲醛。金覆蓋度也可能受限,只要不存在足量的覆蓋模板的金離子存在于溶液中。這顯然基于圖25D-25F中所示的示例性結果,其中增加具有相同量的甲醛的金溶液體積得到更完整和較厚的金殼。例如,使用較少的金,模板具有尚未消失的不同金島。例如,使用更多的鍍金屬溶液,金殼從斑點生長成粗殼且最終生長成更為平滑的殼。如果足夠厚的殼生長,則金封閉聚苯乙烯。
示例性實施方式包括生產較小的模板,其使用帶正電荷的200nm PDDA二氧化硅芯和帶負電荷的100nm羧基-修飾的聚苯乙烯生成。圖26A和26B顯示來自使用示例性200nm芯的示例性金高爾夫球合成過程階段的SEM圖像。圖26A的SEM圖像顯示包含PDDA-官能化200nm二氧化硅芯和100nm羧化物-修飾的聚苯乙烯衛星的膠體分層模板微粒。圖26B中的SEM圖像顯示完成無電鍍金過程后和除去聚苯乙烯衛星前的微粒。
使用兩種不同材料構成的所公開的分層模板結構,可以生產具有潛在極為不同的應用的相同微粒的兩種變化形式(例如納米/微米高爾夫球和納米/微米威浮球)。例如,金高爾夫球的孔具有二氧化硅底且允許它們選擇性地被官能化。中空金威浮球的空白中心提供不能被金高爾夫球利用的儲存容量并且可以用于儲存和釋放治療診斷劑。
所公開的磁定向的納米碗的示例性實施方案
在本技術的一些方面,公開了用于制造和實現復合納米-/微米-級載體的技術、系統和裝置,所述復合納米-/微米-級載體將不同特性合并在同一載體上,其可以用于各種應用,包括遞藥、催化和生物學成像。例如,使用所公開的技術的模板合成方法,可以使用二氧化硅/聚苯乙烯詹納斯模板生產示例性磁金/二氧化硅納米碗。示例性納米碗可以被制造成包括3層結構,包括被金殼涂敷的二氧化硅芯和夾心在其中的小氧化鐵納米微粒。例如,在該示例性制造方法的實施方式中,僅在詹納斯模板的二氧化硅上選擇性鍍金可以確保當模板中的聚苯乙烯被溶解掉且遺留在二氧化硅內部時,僅所述碗的外部被金涂敷。例如,這允許得到具有金外部和二氧化硅內部的磁響應納米碗。
圖27顯示描述用于生產示例性復合磁性納米級碗-樣結構(‘納米碗’)的所公開的技術的示例性制造方法的說明性示意圖。所述方法包括用于合成二氧化硅/聚苯乙烯詹納斯模板的過程2701,例如在圖12中。在所述方法的一些實施方式中,例如,所述方法可以包括修飾表面(例如在二氧化硅/聚苯乙烯詹納斯模板上形成胺-官能化表面)以便促進隨后連接納米微粒的過程2702。所述方法包括使納米微粒連接至詹納斯模板、例如氧化鐵和金納米微粒的過程2703。所述方法包括使殼在詹納斯模板上生長的過程2704。在過程2704的一些實施方式中,例如,過程2704包括使用內部分散的接種的模板(例如金和/或氧化鐵納米微粒)還原氯化金溶液。在所述方法的一些實施方式中,例如,殼的外表面可以進一步被修飾。例如,在金殼復合納米碗的情況中,金表面被聚乙二醇修飾以保持微粒充分分散。所述方法包括形成進入橄欖內部的開口以形成納米碗結構的過程2705。例如,金覆蓋的模板通過將暴露的聚苯乙烯溶于有機溶劑變成磁碗。
示例性制造方法表示具有金外殼的復合磁性納米碗和二氧化硅碗的自下而上的合成方法。描述了示例性制造方法和得到的復合磁性納米碗微粒的示例性實施方式。例如,在包括圍繞部分暴露的聚苯乙烯芯的二氧化硅殼的不對稱二氧化硅/聚苯乙烯詹納斯模板樣模板上構建微粒。示例性實施方式顯示使用電子顯微鏡檢查、UV/vis&IR光譜法和磁力測定法的得到的微粒形成,并且顯示這些實例納米碗的磁響應轉運。此外,拉曼光譜法顯示這些微粒提供有效的SERS平臺。
圖28A-28F顯示包括使用示例性制造方法生產的示例性微粒的電子顯微鏡檢查圖像的圖像。圖28A顯示示例性詹納斯模板形成的電子顯微照片(例如二氧化硅/聚苯乙烯詹納斯模板)。圖28B顯示示例性金和氧化鐵納米微粒連接在二氧化硅上的電子顯微照片。圖28C顯示示例性金殼形成的電子顯微照片。圖28D顯示除去聚苯乙烯芯的電子顯微照片。圖28E顯示示例性鍍金的微粒在溶液中的圖像。圖28F顯示溶液中的示例性磁金/二氧化硅微粒吸引至容器外部磁體的圖像。
圖28A-28F中所示的示例性結果提供每一過程時形態改變的可視化顯影。例如,用胺-硅烷修飾詹納斯模板(AEAPTMS)產生正表面電荷,例如+20-30mV,正如根據ζ電位測定的。例如,依次連接帶負電荷的15nm氧化鐵(IONP)和3-5nm金(AuNP)納米微粒,其中IONP被強負電荷修飾,且AuNP由四(羥甲基)磷鎓氯化物(THPC)在堿性條件下還原氯金酸(HAuCl4)來合成。例如,充分洗滌的IONP/AuNP詹納斯模板的TEM圖像(未顯示)顯示較大的IONP和較小的AuNP的致密的表面覆蓋度。
組合接種和pH在模板的適當接種中起關鍵因素的作用。為了接種的模板保持在溶液中穩定,當使用靜電組裝方法時,需要電荷快速逆轉。胺修飾的模板在僅IONP存在下通常聚集。制造商提供的IONP為亞飽和濃度且由此中和表面電荷(例如ζ電位典型地為-10-+10mV)而不是完全逆轉它。例如,同時接種IONP和金,例如這歸因于金種濃度足夠高至逆轉表面電荷并且穩定接種的模板。通過調整IONP和詹納斯模板之比,例如,如果需要,殼上IONP的量可以進一步優化。此外,例如,pH是檢驗的因素,例如這歸因于在堿性條件下合成金種溶液并且保持高度堿性(例如pH>9)。在這類高pH值下,例如,胺化的模板因二氧化硅表面上的大部分胺類脫質子化而通常為中性。將IONP加入接種溶液不會顯著地降低pH,且在這些條件下接種的嘗試導致大量聚集。IONP/金種溶液中用少量10mM HCl將pH調整至7-8產生無聚集的模板和IONP和金的成功接種,如圖28B中的TEM觀察到的。
在示例性的實施方式中,例如,通過將IONP/AuNP詹納斯模板懸浮于HAuCl4電鍍溶液并且在模板上還原金形成完整殼,例如,如圖28C中所示。例如,恰在還原前將聚(乙烯吡咯烷酮)(40kDa)加入到所述溶液中,因為它在電鍍過程中改善金表面覆蓋度。在形成金殼后,將目前鍍金的詹納斯模板懸浮于DMF,并且溶解聚苯乙烯,例如,如圖28D中所示。示例性實施方式的示例性結果顯示,納米碗在懸浮于溶液中時展示出深藍綠色(teal)(圖28E),并且可以被磁吸引至容器側壁(圖28F)。
在示例性的實施方式中,例如,不同的表征方式用于證實不同過程的完成。例如,在詹納斯模板形成后,用(3-氨基乙基氨基)丙基-三甲氧基硅烷(AEAPTMS)修飾詹納斯模板表面,用FTIR證實。圖29顯示胺-修飾的詹納斯模板的FTIR數據圖。光譜顯示相當于在1500和3600cm-1處的伯胺類的峰。此外,分別在1100和2100cm-1處更顯著地觀察到硅氧烷和甲硅烷基氫化物鍵。這些測定結果證實目前金納米碗的吸光度測量值表明在840nm處形成吸光度峰,預示金殼圍繞二氧化硅芯。
圖30A和30B顯示示例性納米碗的殼的磁性滯后和UV/Vis數據圖。圖30A顯示微粒的磁性滯后,這表明,盡管使用15nm鐵磁微粒,但是復合微粒保持一定的鐵磁特征。圖30B顯示鍍金的納米碗的UV/Vis光譜,例如,其中840nm處的峰預示成功形成金殼。例如,使用振動樣品磁場計測定微粒的磁性滯后并且發現其為適度鐵磁的。磁金殼納米碗的飽和磁化強度為0.4-0.6emu/g。15nm IONPs在15nm大小時通常是超順磁性的,但在這種特定情況中,復合微粒顯然保持一定的具有顯著的滯后現象的鐵磁特征。
圖31A-31C顯示除去聚苯乙烯之前(圖31A)和之后示例性聚乙二醇化磁金-二氧化硅的寬視野圖像和數據圖(圖31B)。圖31C顯示除去聚苯乙烯之前(例如實心紅色,264nm)和之后(例如斑點綠色,282nm)的附帶DLS數據。例如,鍍金詹納斯模板和納米碗的寬視野圖像和DLS顯示納米碗的單分散性。聚乙二醇化鍍金詹納斯模板顯示與在外二氧化硅表面上完全形成金殼一起形成的各微粒。在樣品的264nm處的單峰揭示出的DLS數據顯示與SEM圖像中觀察到的良好的一致性。在用THF除去聚苯乙烯后,例如,證實磁金納米碗在SEM(圖31B)和DLS(圖31C中的實線)中為分散性的。例如,來自這些示例性實施方式的示例性數據顯示在平均直徑適度增加至282nm,而在兩條曲線上運行t-檢驗顯示兩個群體彼此具有顯著性差異。
圖32A-32F顯示通過水凝膠介質引導的示例性官能化磁性納米碗的縮時圖像和數據圖。例如,示例性聚乙二醇化磁性納米碗通過GelMA-co-A6ACA水凝膠被吸引至Nd-Fe-B磁體(圖32A中的左側所示)。圖32B-32E顯示引導的官能化磁性納米碗分別通過隨著0、9、27和52hr縮時的凝膠的示例性縮時圖。正如縮時圖像中所示,例如,凝膠右側變成明顯更藍綠色,因為納米碗浸潤凝膠并且在左側脫離。在更高的光學放大倍數下,例如,如圖32F-32H中所示,在9、27和52hr時的凝膠分別顯示在9小時右側圓形區域中藍綠色向前累積(圖32F),向左側移動并且在27hr時以大約通過該凝膠路徑三分之二的方式更多擴散(圖32G),且大部分微粒在52小時時通過凝膠(圖32H)。例如,圖32F-32H中的圓形曲線高亮顯示可以隨著時間進行在凝膠中觀察到的顯著性差異。圖32I顯示:描述每個圖像中點狀直線之間示例性線對比掃描的數據圖顯示在9小時右側的較大量的反襯度(contrast)。使用27和52hr的反襯度水平,例如,表明大部分微粒已經通過,后面僅遺留痕量的納米碗。對于圖32F-32H中所示的圖像,虛線之間的距離為2mm。
圖32A-32H中所示的示例性數據顯示納米碗通過具有縮時圖像的多孔材料的能力。在示例性的實施方式中,例如,明膠-甲基丙烯酸酯-共-N-丙烯酰基6-氨基己酸凝膠一側上放置在一處進入的強稀土磁體并且在52小時期間內成像。在時程內聚乙二醇化納米碗被吸引至磁體且微粒在凝膠中浸潤可以被顯影為預先澄清凝膠中的藍綠色。例如,所述凝膠隨時間的推移逐步變成更為藍綠色;且在靠近檢查中,微粒前部可以觀察到浸潤凝膠并且隨時間的進展遍及擴散。
此外,示例性金/二氧化硅納米碗可以用作SERS平臺,其合并了連接拉曼報道分子的靈敏度和特異性的優點。例如,使用羅丹明B(Rho B)作為探針分子測試示例性納米碗的SERS活性。當激發激光和拉曼散射聲子頻率接近局限性表面等離子共振頻率時,SERS效應可以被最大化。例如,示例性納米碗在840nm呈現最大吸收峰。基于此,示例性632和785nm激光用于這些示例性實施方式中的拉曼激發。圖33顯示使用和不使用金/二氧化硅納米碗的Rho B的示例性拉曼光譜。圖33顯示0.1M羅丹明B在水溶液中的拉曼光譜的數據圖(光譜(a));金/二氧化硅納米碗上的1×10-6M羅丹明的SERS光譜,150mW 632nm激發,30s獲取(光譜(b));和金/二氧化硅納米碗上的1×10-6M羅丹明的SERS光譜,150mW 785nm激發,30s獲取(光譜(c))。正如示例性數據中所示,存在拉曼強度的顯著增加,例如,其中使用785nm激光激發的金/二氧化硅納米碗上的SERS強度大于單一Rho B10-倍;且比使用632nm激光的相同樣品強7-倍。
所公開的磁金成殼的納米碗可以通過用生物相容性材料包括脂質體、脫乙酰殼多糖和PLGA密封碗用于各種應用,例如遞藥媒介物。例如,為了從所述碗中有條件的和控制釋放治療劑,可以通過與DNA的特異性相互作用、酶加工或環境觸發器如溫度和pH釋放這類封蓋。例如,所公開的納米碗可以用于磁性引導遞送和受控按需釋放造影劑分子(治療診斷)活性劑。
針對示例性詹納斯微粒的芯大小的示例性實施方式
描述了檢驗羧化聚苯乙烯(cPS)芯大小對cPS-二氧化硅詹納斯微粒形態(例如其大小和形狀)的作用的示例性實施方式和結果。例如,在這些示例性實施方式中研究2種不同的二氧化硅大小和5種不同的cPS芯大小。來自電子顯微鏡檢查(EM)和動態光散射(DLS)分析的示例性結果表明復合cPS-二氧化硅微粒獲得了2種不同形狀,例如(i)當cPS芯的大小遠小于非-cPS二氧化硅(b-SiO2)球時,形成部分包囊的詹納斯微粒;和(ii)當cPS芯大于或等于b-SiO2球時,例如,形成覆盆子-樣結構而非詹納斯微粒。例如,當cPS芯的大小遠小于非-cPS二氧化硅(b-SiO2)球時,得到~100nm-500nm大小的cPS-二氧化硅詹納斯微粒。示例性大小可變的納米級詹納斯微粒在多功能遞送治療診斷平臺和催化中具有廣泛應用。
例如,所述示例性實施方式檢驗cPS芯大小對cPS-二氧化硅形態的依賴性,例如,其中通過添加不同芯大小的(例如50-1000nm)cPS芯以形成小(例如~180nm)和大(例如380nm)b-SiO2納米微粒生成cPS-二氧化硅微粒。用于分別生產示例性小b-SiO2和大b-SiO2的反應條件在本文中稱作“小配方(recipe)”和“大配方”。使用b-SiO2納米微粒大小作為參比評價芯大小對cPS-二氧化硅微粒形態的依賴性;且使用TEM、SEM和DLS評價微粒形態。不使用任何cPS芯,上述舉出的配方生成小(例如~180nm)和大(例如~380nm)直徑b-SiO2納米微粒。
圖34顯示當將羧化聚苯乙烯微粒加入到二氧化硅溶液-凝膠反應中時形成的示例性cPS-二氧化硅詹納斯微粒的說明性示意圖和附帶圖像。在溶液-凝膠反應開始時添加cPS之后首先觀察到形成cPS-二氧化硅詹納斯微粒。正如圖34中所示,可以通過平滑二氧化硅殼和其中恰恰二氧化硅滿足cPS的表面上不同的凹陷來鑒定這些微粒。這些凹陷易于在SEM圖像中識別,這歸因于二氧化硅中的特征性圓形斑點。
首先通過保持反應體積恒定來研究大小依賴性。檢驗不同直徑(50nm-400nm)的4種cPS芯的較小配方,同時檢驗5種不同cPS芯(50-1000nm)的大配方。
圖35A顯示使用具有不同直徑cPS芯的小二氧化硅過程的示例性微粒的圖像,例如,圖像(a)中的50nm;圖像(b)中的100nm;圖像(c)中的200nm;圖像(d)中的和400nm。圖35A中的圖像各自包括寬視野圖像插入物,其顯示示例性cPS-二氧化硅微粒的更詳細的圖像。通過添加50nm芯大小的小二氧化硅過程生成均勻大小的詹納斯微粒。添加100nm芯生成具有嘗試覆蓋該芯的多個二氧化硅殼的微粒。當芯變大(例如200、400nm)時,二氧化硅圍繞多個成塊的(lumpy)殼中較大芯形成,且過量的二氧化硅合并成較小的微粒。對于較小的乙醇配方,小于小b-SiO2的芯(例如50nm)形成充分確定的詹納斯微粒,如圖35A的圖像(a)中所示。然而,當PS芯直徑類似地改變大小或遠大于b-SiO2微粒時,二氧化硅開始涂敷簇狀物(clumps)的cPS,如圖35A的圖像(b)中所示。簇狀物變成更大量,且確定的覆盆子-樣殼隨著芯大小增加形成,正如圖35A中的圖像(c)和(d)中所示。二氧化硅完全涂敷cPS,遺留過量TEOS,圍繞它形成純的二氧化硅微粒,覆盆子殼和詹納斯微粒形成也是相對均勻的,正如可以在寬視野圖像中觀察到的。圖35B包括顯示相應DLS分布的直方圖數據圖。
示例性實施方式顯示當使用大二氧化硅配方改變芯大小時出現的類似趨勢。圖36顯示使用應用不同直徑cPS芯的大二氧化硅制造過程生產的示例性微粒的電子顯微照片和附帶DLS直方圖。例如,圖像和相應的直方圖包括如下cPS芯大小:圖像(a)中的50nm;圖像(b)中的100nm;圖像(c)中的200nm;圖像(d)中的和400nm;和圖像(e)中的1000nm。50和100nm芯大小相當于圍繞新的部分包囊。中間大小的芯(例如200nm)顯示形成覆盆子-樣殼。非常大的芯(例如400、1000nm)顯示cPS芯被覆盆子-樣殼覆蓋,所述覆盆子-樣殼具有大于使用小二氧化硅過程形成的殼的二氧化硅簇狀物。DLS直方圖揭示出形成較大結構,并且證實較小的二氧化硅微粒。當使用50nm芯時,多個芯顯然幾乎完全被包囊在單一詹納斯微粒中,如圖36的(a)組中所示。當使用100nm芯時,二氧化硅對cPS的包囊明顯減少,如圖36的(b)組中所示。此外,形成具有較小cPS芯(例如50-100nm)的cPS-二氧化硅詹納斯微粒,而直徑大于相應的較小配方中的微粒。例如,使用接近大b-SiO2的微粒大小的中間大小的芯(例如200,400nm),完整的二氧化硅殼使用不同水平的隆起塊(bump)形成。例如,示例性200nm芯顯示具有圍繞殼的幾個確定隆起塊的完整二氧化硅殼,如圖36的(c)組中所示。例如,示例性400nm芯顯示這種趨勢的較大進展,因為可以觀察到在cPS芯外部上形成更多隆起塊,如圖36的(d)組中所示。例如,當芯(例如1000nm)遠大于b-SiO2時,隆起塊顯然在二氧化硅表面上極為顯著,如圖36的(e)組中所示。
覆盆子-樣殼(例如cPS芯>b-SiO2微粒)形成可能是不同TEOS/cPS之比而非芯大小的結果。為了解釋這種可能性,對于使用相同配方制成的不同芯大小,使TEOS與cPS之比保持恒定。圖37顯示通過經改變TEOS/PS之比在1010(圖像(a)、(b)和(c);和在109(圖像(d)、(e)和(f))生成的示例性小二氧化硅過程生產的示例性PS/二氧化硅復合物的圖像。例如,當芯大小從200nm(例如圖像(a)、(d))增加至400(例如圖像(b)、(e))和增加至1000nm(例如圖像(c)、(f))時,觀察到隆起塊更為顯著且數量大于較大二氧化硅過程。從示例性實施方式的示例性結果中,顯而易見,當芯大小增加時,二氧化硅殼開始變平滑(例如圖像(c))或融合(例如圖像(f)),例如,這取決于TEOS/PS之比。過量的二氧化硅融合成較小的二氧化硅微粒,且作為較小的球是顯著的。從這些SEM圖像中,覆盆子-樣二氧化硅殼涂敷全部cPS芯,且溶液中任意過量的TEOS形成二氧化硅納米微粒。改變TEOS/PS之比不會影響殼的總體形態。此外,以相同的TEOS/PS之比,當芯大小增加時,殼展示出多個顯著的隆起塊以及較大數量的隆起塊。
圖38顯示通過經改變TEOS/PS之比在1010(圖像(a)、(b)和(c);和在109(圖像(d)、(e)和(f))生成的示例性小二氧化硅過程生產的示例性PS/二氧化硅復合物的圖像。經證實二氧化硅-包囊的cPS區別于實心二氧化硅微粒的方面在于其較大的直徑和表面上的多個隆起塊。例如,當芯大小從200nm(例如圖像(a)、(d))增加至400(例如圖像(b)、(e))和增加至1000nm(例如圖像(c)、(f))時,隆起塊變得更為顯著且數量眾多,其達到其中它們不能不能完全覆蓋微粒表面的點。與圖37中的示例性結果類似,覆盆子-樣殼涂敷全部cPS芯,且過量的TEOS也形成二氧化硅納米微粒,如圖38的結果中所示。這些實例結果啟示,改變TEOS/PS之比通常不會顯著地影響覆盆子殼的總體形態。此外,當芯大小增加時,殼展示出更大量的隆起塊。然而,在具有相同TEOS/PS之比和cPS芯大小處于小(例如形成小b-SiO2微粒的條件)與大(例如形成大b-SiO2微粒的條件)配方(例如圖37的圖像(a)與圖38的圖像(a))之間的比較樣品中,使用小配方的二氧化硅殼上的各隆起塊與大配方相比減少。
圖39顯示在詹納斯微粒形成中芯的作用的示例性模型的說明性示意圖。例如,當芯大小遠小于b-SiO2粒徑時,詹納斯微粒形成。當芯和b-SiO2直徑彼此大小接近時,覆盆子-樣殼圍繞僅帶有幾個隆起塊的cPS形成。當芯遠大于b-SiO2時,TEOS形成覆盆子-樣殼,其具有圍繞PS芯的大量圓形突出。芯與b-SiO2之間的大小差異越大,則隆起塊越為明顯和數量越多。另外,未摻入覆盆子殼的任意過量的TEOS隨后形成與b-SiO2大小類似的二氧化硅納米微粒。如果cPS芯直徑保持相同且TEOS/PS之比增加,則逐步形成隆起塊狀二氧化硅殼,以便彼此融合,形成更為平滑的殼(圖39的(b)組)。
用示例性詹納斯二氧化硅納米微粒詹納斯微粒俘獲膠體金納米微粒的示例性實施方式
描述了示例性實施方式,其顯示基于示例性雙官能化的二氧化硅納米微粒的金納米微粒(GNPs)俘獲器平臺(二氧化硅高爾夫球),所述平臺能夠以物理方式將不同大小的GNPs吸附在pH受控的緩沖液中。例如,使用不均勻分層模板合成衍生的二氧化硅高爾夫球,同時使用分散于具有預定溶液離子強度的pH受控緩沖液中的二氧化硅高爾夫球俘獲一個或多個膠體GNPs。呈現實例獲取的掃描電子顯微鏡(SEM)圖像以便使GNPS定位于二氧化硅高爾夫球上。所公開的技術的這種示例性生物相容性俘獲器平臺模板確保較大的官能化的二氧化硅芯,其具有以物理方式吸附至二氧化硅芯表面的100nm直徑的聚苯乙烯微粒。在一個實例中,通過在官能化的二氧化硅芯上選擇性地涂敷二氧化硅、隨后用有機溶劑溶解聚苯乙烯微粒制造具有100nm凹孔的生物相容性俘獲器平臺。例如,俘獲器平臺在再循環醫療GNPs中是相當有用的,從而可以提供用于在人體醫療保健中GNPs的有經濟意義的持續應用的有價值的工具。俘獲器平臺還可以潛在地應用于從植物組織或細胞中非侵害性采集GNPs,從而促進金蓄積,提供用于采集GNPs作為天然產物的有價值的工具。
‘Greener’,更持續性的GNP合成和分選方法可以通過更依賴于生物合成方法、隨后是使用二氧化硅高爾夫球的非侵害性GNP俘獲和較少依賴于毒性化學合成方法來實現。使用示例性修飾的分層模板策略與不同芯(例如二氧化硅)和衛星(例如聚苯乙烯)材料,這些示例性實施方式的結果顯示,可以通過不均勻分層模板策略實現二氧化硅納米微粒的選擇性表面官能化目的。還證實,不均勻分層模板策略與其均勻復本同樣是大小可變的。例如,顯示二氧化硅高爾夫球能夠將膠體金納米微粒俘獲在pH受控緩沖液內部。
官能化NP的合成和二氧化硅高爾夫球的制備使用如下過程,例如:(1)PS連接的模板合成;(2)模板上TEOS電鍍;和(3)PS浸蝕。通過經FEI XL30SFEG UHR SEM的掃描電子顯微鏡檢查(SEM)從形態上評價胺和季銨官能化NP制造和二氧化硅高爾夫球制備的示例性結果。例如,通過預制的模板微粒上的TEOS自組裝合成二氧化硅高爾夫球。該反應由濃銨催化。通過使較小的100nm PS微粒以物理方式分別吸附在胺官能化1000nm二氧化硅微粒和季銨官能化1000nm二氧化硅微粒上制備模板微粒。隨后,例如,通過在水浴中將所述微粒溶于加熱至60℃的DMF,從二氧化硅高爾夫球表面浸蝕出100nm PS微粒。圖40顯示示例性合成方法的說明性示意圖。圖40顯示示例性應用于二氧化硅高爾夫球合成中的不均勻分層模板過程。(a)組顯示示例性二氧化硅芯(例如灰色);(b)組顯示被(3-氨基丙基)-三甲氧基硅烷(APTMS)或N-三甲氧基甲硅烷基丙基-N,N,N-三甲基氯化銨的殼官能化的示例性二氧化硅芯(例如綠色),所述(3-氨基丙基)-三甲氧基硅烷(APTMS)或N-三甲氧基甲硅烷基丙基-N,N,N-三甲基氯化銨的殼上以靜電方式連接了較小的聚苯乙烯(PS)衛星球(例如藍色),如(c)組中所示。(d)組顯示生長為官能化殼外部互聯二氧化硅殼的示例性TEOS殼。(e)組顯示聚苯乙烯衛星溶解完成了二氧化硅高爾夫球微粒的合成。
圖41顯示示例性官能化微粒、例如來自使用1000nm二氧化硅芯的二氧化硅高爾夫球合成過程階段的官能化微粒的SEM圖像。例如,(a)組顯示通過胺或季銨官能化1000nm二氧化硅球表面上100nm羧化物-修飾的聚苯乙烯自組裝生成的模擬花粉的結構。(b)組顯示TEOS在胺官能化殼上生長后,除去聚苯乙烯提供模擬多孔高爾夫球的結構(箭頭指示孔)。(c)組顯示TEOS在胺官能化殼上生長后,除去聚苯乙烯提供模擬多孔高爾夫球的結構(箭頭指示孔)。
APTMS量和N-三甲氧基甲硅烷基丙基-N,N,N-三甲基氯化銨的量在合成過程中可變,且最終,兩種化合物的量均被調節至飽和。二氧化硅NPs和羧化PS NPs的濃度和表面官能化化學物質的量均說明PS NPs在芯微粒表面上的密度。
在PS浸蝕過程中,例如,評價氯仿、甲苯和二甲基甲酰胺(DMF)浸蝕掉PS的能力。期望的溶劑溶解PS并且防止PS粘結至二氧化硅高爾夫球,而不是僅軟化PS。在這些示例性實施方式中,例如,DMF作用最佳。在這些示例性實施方式中,例如,氯仿的密度高至微粒難以從溶液中被離心出來。此外,氯仿僅從微粒表面浸蝕出大部分PS,而遺留在PS上的是粘性的,即高爾夫球凹孔可能被PS覆蓋。在這些示例性實施方式中,例如,甲苯也無法充分除去PS微粒。因此,DMF用于除去PS,例如用DMF 3次,同時保持水浴中溫度在60℃。
在這些示例性實施方式中,例如,用季銨官能化的二氧化硅高爾夫球俘獲GNPs僅在pH受控緩沖液中進行。通過在水或水-乙醇混合物中的俘獲反應無法觀察到用二氧化硅高爾夫球吸附GNPs。俘獲反應在5種不同種類的介質中進行,例如水、80%乙醇水溶液、20%乙醇水溶液、20%在鄰苯二甲酸氫鉀緩沖液中的乙醇和鄰苯二甲酸氫鉀緩沖液。通過在鄰苯二甲酸氫鉀緩沖液中的俘獲反應測試40nm和20nm GNPs。將離心后處理的比例謹慎地保持在500rcp以確保GNP俘獲不歸因于機械力,而是在緩沖液中的電吸附。在這些示例性實施方式中,例如,用二氧化硅高爾夫球俘獲40nm和20nm GNPs,如圖42和43中所示。在二氧化硅高爾夫球凹孔內部觀察到GNPs。例如,對于40nm GNPs,在凹孔中實現單一GNP俘獲。例如,對于20nm GNPs,2-3個GNPs可以優選被1個凹孔俘獲。
圖42顯示俘獲金膠體微粒的示例性二氧化硅高爾夫球的說明性示意圖。(a)組顯示帶有凹孔內部官能化季銨的示例性二氧化硅高爾夫球微粒(例如綠色)。(b)組顯示示例性二氧化硅高爾夫球微粒將具有單一GNP的40nm GNPs俘獲在每個凹孔中。(c)組顯示示例性二氧化硅高爾夫球微粒將具有多個GNPs的20nm GNPs俘獲在每個凹孔中。
圖43顯示具有俘獲GNPs的季銨官能化凹孔的合成的二氧化硅高爾夫球的SEM圖像。圖像(a)和(c)顯示示例性二氧化硅高爾夫球微粒將具有單一GNP的40nm GNPs俘獲在每個凹孔中(箭頭指示被控俘獲的GNPs)。圖像(b)和(d)顯示示例性二氧化硅高爾夫球微粒將例如具有多個GNPs的20nm GNPs俘獲在每個凹孔中(箭頭指示劑被控俘獲的GNPs)。
應用由2種不同材料制成的不均勻合成模板,制造具有能夠植物冶金(phytomining)或醫療應用的2種二氧化硅高爾夫球。二氧化硅高爾夫球的凹孔具有胺或季銨官能化的底,并且可以促進它們進一步被選擇性地官能化。季銨官能化的二氧化硅高爾夫球優先將<50nm的膠體金微粒俘獲在pH=4緩沖液中。單一俘獲和多次俘獲依賴于目標金膠體微粒的大小。
示例性實施方式包括電泳遷移率模型和ζ電位測量。例如,凹孔的吸引電場強度的評估如下所述。
當將膠體二氧化硅浸入水溶液時,它從微粒表面處的質子化/脫質子化變成帶電荷。局部靜表面電荷密度σ依賴于微粒大小。例如,具有2nm直徑的二氧化硅微粒的σ的值大于具有500nm直徑的二氧化硅微粒的σ的值4倍。當膠體二氧化硅微粒直徑增加時,微粒上的表面電荷密度下降。隨大小的增加,微粒的表面電荷密度接近平板的表面電荷密度。
平板附近的電荷和電位分布通過Poisson-Boltzmann方程控制,其中φ是流體內的電位;F是法拉第常數;Ci0和zi是體積摩爾濃度和ith離子種類的化合價。二氧化硅納米微粒的表面電荷密度可以通過完全多-粒子電荷管理模型模型化,并且顯示為通過給出,其中KA和KB是2種推定的質子化反應的平衡常數,為[H+]s,且Ntotal其為納米微粒的固/液界面上硅烷醇官能團的總數位置密度。Ntotal的值通過下式給出:在示例性模型中,估計值是使用理想化條件在球體表面上各凹孔的靜電場強度,且球體表面近似值為帶負電荷的無窮大板的近似值,且我們將凹孔近似為正點電荷。
靜電場強度表示為:
和
ET=Es-Ep=0
其中R0是距表面的距離,其中凈電場ET=0。此外,其中a是膠體微粒的半徑,且為1/κ,其為德拜長度。當a·k>>1時,微粒表面上的總電荷與ζ電位成正比(即QT∝ζ)。
實施例
下列實施例是本技術的幾個實施方案的示例。可以在如下列出的實施例之前或如下列出的實施例之后提供本技術另外的示例性實施方案。
在本技術的一個實施例中(實施例1),用于生產遞送有效負荷的納米結構的方法包括在芯微粒上形成殼結構,以便生成模板,其中芯微粒部分被殼結構封閉;使納米微粒連接至殼結構的外表面;在覆蓋至少一些連接的納米微粒的殼結構的外表面上形成涂層;從模板中除去芯微粒,其中除去的芯微粒形成具有來自外表面的開口的殼結構的內腔;和在殼結構的內腔中載入分子有效負荷。
實施例2包括如實施例1中的方法,其中殼結構包括二氧化硅。
實施例3包括如實施例1中的方法,其中芯微粒上形成不對稱形狀的殼結構。
實施例4包括如實施例1中的方法,其中殼結構包括實質上500nm或更小的大小。
實施例5包括如實施例1中的方法,其中芯微粒包括聚苯乙烯。
實施例6包括如實施例5中的方法,其中聚苯乙烯芯微粒被羧化物-末端涂層官能化。
實施例7包括如實施例5中的方法,其中聚苯乙烯芯微粒包括實質上150nm或更小的大小。
實施例8包括如實施例1中的方法,還包括在連接納米微粒前,以化學方式修飾殼結構的外表面。
實施例9包括如實施例1中的方法,其中納米微粒包括氧化鐵納米微粒和金納米微粒之一或兩者。
實施例10包括如實施例9中的方法,其中氧化鐵納米微粒包括5-15nm的大小。
實施例11包括如實施例9中的方法,其中形成涂層包括在殼結構的外表面上納米微粒的至少一些之間產生填充材料。
實施例12包括如實施例11中的方法,其中生產填充材料包括將模板放入離子金溶液和添加金的還原劑,由此在連接至外表面的金納米微粒之間形成金材料并且涂敷氧化鐵納米微粒。
實施例13包括如實施例1中的方法,其中納米微粒的靜電相互作用使納米微粒連接至殼結構的外表面。
實施例14包括如實施例1中的方法,還包括在加載前,浸蝕內腔內的至少部分殼結構以便從殼結構中除去材料。
實施例15包括如實施例1中的方法,其中所述加載包括用能夠使分子有效負荷連接至殼結構的連接分子使殼結構外表面或殼結構內腔的內表面的至少一種官能化。
實施例16包括如實施例15中的方法,還包括通過將刺激施加于殼結構以導致分子有效負荷從連接分子中化學分離來釋放所述分子有效負荷。
實施例17包括如實施例16中的方法,其中施加刺激包括提供化學物質、發光、改變pH環境或改變溫度的至少一種。
實施例18包括如實施例1中的方法,還包括使封蓋微粒連接至殼結構以便覆蓋開口和將分子有效負荷包含在內腔內,其中連接封蓋微粒以允許可控地運動,從而基于外部刺激暴露開口。
實施例19包括如實施例18中的方法,其中通過封蓋微粒表面上形成的自組裝單層(SAM)的分子自組裝使封蓋微粒連接至殼結構。
實施例20包括如實施例18中的方法,其中用具有核苷酸的互補序列的2條鏈的核酸使封蓋微粒連接至殼結構,第一條鏈連接至封蓋微粒,而互補的第二條鏈連接至殼結構的內腔。
實施例21包括如實施例18中的方法,還包括通過將外部刺激施加于殼結構以導致封蓋微粒的可控運動以暴露殼結構的開口來釋放分子有效負荷。
實施例22包括如實施例21中的方法,其中施加外部刺激包括是施加熱。
實施例23包括如實施例1中的方法,其中所述分子有效負荷包括造影劑、酶、蛋白質、激素、糖蛋白、糖脂、核酸、適體、脂質或者金屬的、聚合的或陶瓷的納米微粒的至少一種藥物。
在本技術的一個實施例中(實施例24),用于遞送有效負荷的裝置包括殼結構,其被構造成包括殼結構內腔的開口;至少在殼結構外表面上部分形成的涂層,且在涂層內包括多個磁性納米微粒;和能夠以化學方式使分子有效負荷連接至殼結構的內腔的表面上的官能化層。
實施例25包括如實施例24中的裝置,其中殼結構包括二氧化硅。
實施例26包括如實施例24中的裝置,其中殼結構包括實質上200nm或更小的大小。
實施例27包括如實施例24中的裝置,其中磁性納米微粒包括氧化鐵納米微粒。
實施例28包括如實施例24中的裝置,其中磁性納米微粒包括5-15nm的大小。
實施例29包括如實施例24中的裝置,其中磁性納米微粒能夠與外部磁場發生相互作用以便以磁性引導納米結構。
實施例30包括如實施例24中的裝置,其中所述涂層包括金。
實施例31包括如實施例24中的裝置,還包括與殼結構綴合的靶向配體分子,所述配體分子對目標結構上發現的報道分子具有親和力,以便將殼結構吸引和結合至目標結構。
實施例32包括如實施例24中的裝置,其中所述裝置是可操作的以便可控地釋放所述分子有效負荷,其通過將刺激施加于殼結構來進行,以便導致分子有效負荷從官能化層中化學分離。
實施例33包括如實施例32中的裝置,其中所述刺激包括化學物質、光、pH環境或溫度的至少一種。
實施例34包括如中實施例24的裝置,其中所述分子有效負荷包括藥物、造影劑、酶、蛋白質、激素、糖蛋白、糖脂、核酸、適體、脂質或者金屬的、聚合的或陶瓷的納米微粒的至少一種。
在本技術的一個實施例中(實施例35),用于遞送有效負荷的裝置包括殼結構,其被構造成包括殼結構內腔的開口;至少在殼結構外表面上部分形成的涂層,且在涂層內包括多個磁性納米微粒;和連接至殼結構以覆蓋開口并且在內腔內包含分子有效負荷的封蓋微粒,其中封蓋微粒連接至殼結構能夠使得封蓋微粒可控地運動,以便基于外部刺激暴露開口。
實施例36包括如實施例35中的裝置,其中通過封蓋微粒表面上形成的自組裝單層(SAM)的分子自組裝使封蓋微粒連接至殼結構。
實施例37包括如實施例35中的裝置,其中用具有核苷酸的互補序列的2條鏈的核酸使封蓋微粒連接至殼結構,第一條鏈連接至封蓋微粒,而互補的第二條鏈連接至殼結構的內腔。
實施例38包括如實施例35中的裝置,其中所述裝置是可操作的以便可控地釋放所述分子有效負荷,其通過將熱施加于殼結構來進行,以便導致封蓋微粒可控地運動,從而暴露殼結構的開口。
實施例39包括如中的裝置實施例21,其中施加熱包括射頻(RF)加熱或近紅外(NIR)加熱。
實施例40包括如實施例35中的裝置,其中殼結構包括二氧化硅。
實施例41包括如實施例35中的裝置,其中殼結構包括實質上200nm或更小的大小。
實施例42包括如實施例35中的裝置,其中磁性納米微粒包括氧化鐵納米微粒。
實施例43包括如實施例35中的裝置,其中磁性納米微粒包括5-15nm的大小。
實施例44包括如實施例35中的裝置,其中磁性納米微粒能夠與外部磁場發生相互作用,以便磁性引導納米結構。
實施例45包括如實施例35中的裝置,其中所述涂層包括金。
實施例46包括如實施例35中的裝置,還包括與殼結構綴合的靶向配體分子,所述配體分子對目標結構上發現的受體分子具有親和力,以便將殼結構吸引和連接至目標結構。
實施例47包括如中的裝置實施例35,其中所述分子有效負荷包括藥物、造影劑、酶、蛋白質、激素、糖蛋白、糖脂、核酸、適體、脂質或者金屬的、聚合的或陶瓷的納米微粒的至少一種。
在本技術的一個實施例中(實施例48),用于生產材料結構的方法包括通過在芯微粒上連接多個掩蔽微粒形成模板,所述掩蔽微粒在它們所連接的芯微粒的外表面上形成掩蔽區;使納米微粒連接至模板的未掩蔽表面,其中所述掩蔽微粒防止納米微粒連接至外表面的掩蔽區;通過連接的納米微粒的材料生長在未掩蔽的表面上形成涂層,以便在模板的未掩蔽表面上形成殼結構;和從模板中除去掩蔽微粒,其中除去的掩蔽微粒形成在殼結構的內部區和外表面之間延伸的開口以封閉芯微粒,由此產生多孔的載體結構。
實施例49包括實施例48的方法,其中掩蔽微粒通過靜電相互作用連接至芯微粒。
實施例50包括實施例49的方法,其中芯微粒包括陽離子二氧化硅且掩蔽微粒包括聚苯乙烯。
實施例51包括實施例48的方法,其中納米微粒包括金納米微粒。
實施例52包括實施例51的方法,其中金納米微粒包括5nm或更小的大小。
實施例53包括實施例48的方法,其中形成涂層包括將模板微粒浸入包含納米微粒的外部材料的溶液,導致成核和圍繞模板微粒生長。
實施例54包括實施例53的方法,其中納米微粒包括金納米微粒且所述溶液包括氫氧化金,形成包括產生成核進入金殼結構的金種。
實施例55包括實施例54的方法,其中多孔的載體結構包括在二氧化硅芯微粒上形成的外部金多孔殼。
實施例56包括實施例48的方法,其中除去包括溶解溶液中的掩蔽微粒。
實施例57包括實施例48的方法,還包括從模板中除去至少部分芯微粒以便產生中空的、多孔的載體結構。
實施例58包括實施例48的方法,還包括在從模板中除去掩蔽微粒之前形成圍繞多孔的載體結構的外層,其中多孔的載體結構包括具有外層內表面上包埋的涂層的外層;和從模板中除去至少部分芯微粒以便產生中空的、多孔的載體結構。
實施例59包括實施例58的方法,其中外層包括二氧化硅,且涂層包括金。
實施例60包括實施例48的方法,其中通過連接的納米微粒的材料生長在未掩蔽表面上形成涂層,在模板的未掩蔽表面上形成涂層的不連續的島狀結構;和進一步包括在從模板中除去掩蔽微粒之前形成圍繞殼結構的外層,其中多孔的載體結構包括具有在外層內表面上包埋的島狀結構的外層;和從模板中除去至少部分芯微粒以產生中空的、多孔的載體結構,其具有在外層內表面上包埋的島狀結構。
實施例61包括實施例60的方法,其中外層包括二氧化硅,且所述島狀結構包括金。
實施例62包括實施例58的方法,還包括將磁性納米微粒加入到內表面,產生中空的、多孔的載體結構;和/或將磁性納米微粒加入到外表面,產生中空的、多孔的載體結構。
實施例63包括實施例62的方法,其中磁性納米微粒包括氧化鐵納米微粒。
實施例64包括實施例48的方法,還包括向多孔的載體結構中加載分子有效負荷,其中所述加載包括用能夠連接分子有效負荷的連接分子使涂層官能化。
實施例65包括實施例58、60或62的方法,還包括向中空的、多孔的載體結構中加載有效負荷,其中所述加載包括用能夠連接分子有效負荷的連接分子使內表面或外表面的至少一種官能化。
實施例66包括實施例64或65的方法,還包括釋放分子有效負荷,其通過向載體結構上施加刺激,以導致分子有效負荷從連接分子中化學分離來進行。
實施例67包括實施例66的方法,其中施加刺激包括提供化學物質、發光、改變pH環境或改變溫度的至少一種。
在本技術的一個實施例中(實施例68),微粒裝置包括殼結構,其被構造成包括殼結構的內部區域與外表面之間延伸的一個或多個開口;連接至殼結構的內部區域或外部區域之一或兩者的磁性納米微粒;和用使分子有效負荷連接至殼結構表面的連接分子連接至殼結構的分子有效負荷。
實施例69包括實施例68的裝置,其中磁性納米微粒包括氧化鐵納米微粒。
實施例70包括實施例68的裝置,其中殼結構包括圍繞內層形成的外層。
實施例71包括實施例70的裝置,其中外層包括二氧化硅,且內層包括金。
實施例72包括實施例70的裝置,其中內層包含不連續的島狀結構。
實施例73包括實施例72的裝置,其中外層包括二氧化硅,且島狀結構包括金。
實施例74包括實施例68的裝置,其中所述分子有效負荷包括藥物、造影劑、酶、蛋白質、激素、糖蛋白、糖脂、核酸、適體、脂質和/或者金屬的、聚合的或陶瓷的納米微粒的至少一種。
盡管本專利文件包含許多特征,但是不應當將它們視為對任何發明或要求保護的范圍的限定,而被視為描述對特定發明的特定實施方案特定的特征。本專利文件中單獨實施方案上下文中描述的一些特征也可以以單一實施方案的組合形式實施。相反,單一實施方案上下文中所述的不同特征也可以以多個實施方案單獨或以任意適合的亞組合的方式實施。此外,盡管可以將上述特征描述為以一些組合的方式起作用,且甚至最初照此要求保護,但是來自要求保護的組合的一個或多個特征在一些情況中可以從該組合中排除,并且要求保護的組合可以涉及亞組合或亞組合的變化形式。
類似地,盡管稱作可以按照特定次序描述在附圖中,但是不應當將其理解為需要這類操作按照所示的特定次序或依次進行,或進行全部示例性的操作,以便達到期望的結果。此外,本專利文件中所述的實施方案中的各種系統構件的分離不應當被理解為在所有實施方案中都需要這類操作。
僅描述了幾種實施方式和實施例,而可以基于本專利文件中所述和示例的進行另外的實施、強化和改變。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 含叔胺藥物物質的靶向遞送的制造方法與工藝
- 一種磁靶向雙載藥遞釋系統及其制備方法與流程
- 用于引導和靶向按需物質遞送的納米結構的載體的制造方法與工藝
- 附載蟾毒靈的多肽修飾的聚甲基丙烯酸寡聚乙二醇酯-聚己內酯納米制劑的制作方法
- 附載蟾毒靈的多肽修飾的聚甲基丙烯酸寡聚乙二醇酯-聚己內酯納米制劑的制作方法
- 一種用于治療去勢抵抗性前列腺癌的靶向前藥及其納米制劑和制備方法
- 一種具有內涵體逃逸功能的腫瘤靶向前藥及其納米制劑和制備方法
- 具有腦腫瘤靶向和腫瘤組織穿透能力的d構型多肽及其基因遞釋系統的制作方法
- 聚乙二醇-聚乳酸羥基乙酸-聚賴氨酸納米遞送系統、制備方法及其應用的制作方法
- 載蟾蜍靈的環肽修飾的聚乙二醇-聚乳酸羥基乙醇酸-聚賴氨酸納米粒的制作方法
- 靶向PD-1的多肽及其應用的制造方法與工藝
- 靶向同位素生產系統的制造方法與工藝
- 在制備68GA?螯合物官能化的靶向劑中用作金屬抑制劑的單糖、二糖或多糖的制造方法與工藝
- 用于引導和靶向按需物質遞送的納米結構的載體的制造方法與工藝
- 通過PROSTRATIN靶向K?RAS介導的信號轉導通路和惡性腫瘤的制造方法與工藝
- 腫瘤靶向核磁共振/熒光雙模態成像造影劑及其制備和應用的制造方法與工藝
- pH氧化還原雙敏感的PAMAM靶向納米給藥載體及其制備方法與制造工藝
- 具有卵巢腫瘤靶向D構型多肽及其基因遞釋系統的制造方法與工藝
- 靶向survivin納米抗體及其制備方法和應用與制造工藝
- 用于PSMA靶向的成像和放射療法的金屬/放射性金屬標記的PSMA抑制物的制造方法與工藝
- 阻斷UBE2M介導Neddylation修飾在腎細胞癌治療中的應用的制造方法與工藝
- 無載體共組裝腫瘤靶向抗癌納米藥物及其制備方法與應用與流程
- 一種用于判斷靶向單克隆抗體治療腫瘤療效的預測分子的制造方法與工藝
- 一種靶向CD47的免疫檢查點抑制劑藥物組合物及其制備方法與流程
- 具有淋巴靶向功能的生物自組裝納米晶注射劑及制備方法與流程
- 用于檢測肝癌的基因標志物及其用途的制造方法與工藝
- 特異性shRNA篩選及其靶向Ang?2基因抑制肺癌細胞的驗證方法與流程
- 一種多功能自動化生物細胞提取分離控制系統及采用該系統實現的細胞提取分離方法與流程
- 一種融合蛋白及光敏劑復合物及其制備方法和應用與流程
- 具有可視化和顯示光斑邊界功能的光動力治療系統的制造方法與工藝
- 腫瘤靶向核磁共振/熒光雙模態成像造影劑及其制備和應用的制造方法與工藝
- pH氧化還原雙敏感的PAMAM靶向納米給藥載體及其制備方法與制造工藝
- 具有卵巢腫瘤靶向D構型多肽及其基因遞釋系統的制造方法與工藝
- 靶向survivin納米抗體及其制備方法和應用與制造工藝
- 用于PSMA靶向的成像和放射療法的金屬/放射性金屬標記的PSMA抑制物的制造方法與工藝
- 一種線粒體靶向的粘度熒光探針及其制備方法和應用與制造工藝
- 一種兼具熒光可視、磁靶向和pH敏多功能的復合空心微球藥物載體及其制備方法與制造工藝
- 一種用于修飾微泡的多肽以及靶向GBM的藥物制劑的制造方法與工藝
- 白果內酯作為腦靶向增效劑在制備防治腦腫瘤藥物的應用的制造方法與工藝
- 機器人輔助精確靶向穿刺軟組織目標柔性針夾緊固定裝置的制造方法
- 一種用于判斷靶向單克隆抗體治療腫瘤療效的預測分子的制造方法與工藝
- 一種檢測肺癌相關基因熱點突變的試劑盒及其應用的制造方法與工藝
- 一種為肺癌提供離體個體化藥物測試的方法及培養基與流程
- 一種谷胱甘肽/超聲雙重刺激響應納米聚合物囊泡、其制備方法及應用與流程
- 一種多重刺激響應交聯型聚合物納米水凝膠、其制備方法及應用與流程
- 一種靶向CD47的免疫檢查點抑制劑藥物組合物及其制備方法與流程
- 具有淋巴靶向功能的生物自組裝納米晶注射劑及制備方法與流程
- 用于檢測肝癌的基因標志物及其用途的制造方法與工藝
- 特異性shRNA篩選及其靶向Ang?2基因抑制肺癌細胞的驗證方法與流程
- 一種具有靶向功能仿病毒結構高分子囊泡及其制備與應用的制造方法與工藝