DJ?1在治療或診斷成體神經(jīng)干細胞損傷或異常分化所致疾病中的用途的制作方法
本發(fā)明涉及DJ-1的新的藥理用途,尤其涉及DJ-1在治療或診斷成體神經(jīng)干細胞損傷或異常分化所致疾病中的用途,屬于DJ-1的新醫(yī)藥用途領(lǐng)域。
背景技術(shù):
帕金森病(Parkinson′s disease,PD)是嚴重影響人類健康的第二大神經(jīng)退行性疾病,影響著全球數(shù)百萬人的健康。PD是以黑質(zhì)紋狀體多巴胺能通路神經(jīng)退行性病變?yōu)橹饕卣鳎殡S相應(yīng)的四大運動障礙,包括靜止性震顫、肌肉強直、運動遲緩和姿勢步態(tài)異常。長期以來,臨床上對PD的關(guān)注聚焦于它的運動癥狀,目前PD的治療方法和手段包括藥物治療、手術(shù)治療、運動療法、心理疏導(dǎo)及照料護理等,其中,藥物治療為首選,且是整個治療過程中的主要治療手段,其目的是增加腦內(nèi)多巴胺水平或提高多巴胺受體活性。手術(shù)治療則是藥物治療的一種有效補充。目前應(yīng)用的治療手段,無論是藥物或手術(shù)治療,只能改善其主要的運動癥狀,但不能阻止其病情的發(fā)展,更無法治愈。近年來,越來越多的證據(jù)顯示PD的臨床表現(xiàn)譜更為廣泛,除上述運動癥狀外還包括非運動癥狀(non-motor symptoms,NMS),如各種認知、精神、睡眠、自主和感覺功能障礙。一些NMS如嗅覺障礙、焦慮、抑郁以及學(xué)習(xí)記憶功能減退等會早發(fā)于經(jīng)典的運動癥狀幾年甚至十幾年并貫穿疾病始終,稱為先兆PD(prodromal PD)。其中嗅覺障礙是最早出現(xiàn)的NMS,被認為是PD運動癥狀期前的標(biāo)志,最終可影響90%的患者。目前,NMS已是公認的PD癥狀的重要組成部分,也是導(dǎo)致患者殘障和生活質(zhì)量下降的主要原因。
PD一旦發(fā)生將隨著時間的推移而漸進性加重,有證據(jù)顯示在疾病早期階段的病程進展較后期階段要快。因此,早期診斷、盡早開始治療、爭取掌握疾病的修飾時機,對今后帕金森病的整個治療成敗起關(guān)鍵性作用。由于上述NMS出現(xiàn)在PD發(fā)病的起始階段,所以對PD的早期診治有著重要的意義,但目前臨床上對此類癥狀的治療效果欠佳。已有研究表明,PD的這些早發(fā)的NMS與嗅球(Olfactory Bulb,OB)和海馬的功能密切相關(guān),而且這些癥狀的發(fā)生與存在于這兩個腦區(qū)的成體神經(jīng)干細胞微生境——側(cè)腦室室管膜下區(qū)(Subventricular Zone,SVZ)/OB和海馬齒狀回顆粒下層(Subgranular,SGZ)出現(xiàn)的成體神經(jīng)發(fā)生的異常變化相平行。正常的嗅覺以及認知和學(xué)習(xí)記憶功能依賴于OB和海馬內(nèi)的成體神經(jīng)干細胞的持續(xù)的增殖和分化成成熟的神經(jīng)元,以維持正常神經(jīng)元的數(shù)量。由此可見,PD的NMS發(fā)生與成體神經(jīng)發(fā)生有著緊密的聯(lián)系。可以通過有效調(diào)控這兩個腦區(qū)的內(nèi)源性成體神經(jīng)干細胞的增殖與分化,功能性修復(fù)受損變性神經(jīng)元,實現(xiàn)疾病的精準(zhǔn)個體化自身治愈過程。
成體神經(jīng)干細胞在大多數(shù)時間處于靜止?fàn)顟B(tài),保持著低代謝率。盡管在受損和病理狀態(tài)下,成體神經(jīng)干細胞反應(yīng)性增殖和分化,但只有很少一部分進入分化階段,大部分新生細胞死亡。而能進入神經(jīng)網(wǎng)絡(luò)的新生神經(jīng)元也只占很小的一部分,其他的則分化成為星形膠質(zhì)細胞和少突膠質(zhì)細胞。近年來,研究者采取多種干預(yù)手段調(diào)節(jié)不同腦實質(zhì)損傷情況下內(nèi)源性成體神經(jīng)干細胞的增殖及分化以期達到更好的治療效果。
DJ-1/PARK7基因最早是在1997年被發(fā)現(xiàn),被認為是一種絲裂原依賴性癌基因(Nagakubo D,Taira T,Kitaura H,Ikeda M,Tamai K,Iguchi Ariga S M,et al.DJ-1,a novel oncogene which transforms mouse NIH3T3cells in cooperation with ras[J].Biochem Biophys Res Commun,1997,231:509-513.)。它的表達產(chǎn)物DJ-1是一種多功能蛋白,涉及多種細胞過程,包括抗氧化應(yīng)激、蛋白酶活性、轉(zhuǎn)錄調(diào)節(jié)和信號通路調(diào)節(jié)、分子伴侶以及腫瘤生成和遷移,其功能性突變可導(dǎo)致常染色體隱性遺傳早發(fā)家族性PD的發(fā)生。DJ-1以同型二聚體的形式廣泛存在于哺乳動物的組織中。在腦內(nèi),DJ-1在基底節(jié)、丘腦、小腦、海馬、皮質(zhì)回路以及嗅球中表達較高。在亞細胞水平,DJ-1主要分布在細胞質(zhì),在線粒體和細胞核也有一定的分布。目前已報道的研究認為,DJ-1主要是通過保護線粒體功能和抑制氧化應(yīng)激損傷而發(fā)揮神經(jīng)保護作用。DJ-1基因發(fā)生突變(如L166P和M26I),遷移至線粒體的DJ-1蛋白即為無效的單體,或者其他原因引起DJ-1蛋白功能缺失時,可導(dǎo)致線粒體膜電位降低以及線粒體片段化等,也會使線粒體產(chǎn)生功能障礙或者引發(fā)氧化應(yīng)激;DJ-1蛋白可通過自身氧化、阻止細胞凋亡而發(fā)揮保護細胞免受氧化應(yīng)激損傷的作用。而迄今為止,尚未有文獻報道DJ-1能夠調(diào)節(jié)成體神經(jīng)干細胞的增殖和分化,以抵抗成體神經(jīng)干細胞損傷或分化異常,更未有報道DJ-1能夠應(yīng)用于治療或診斷成體神經(jīng)干細胞損傷或異常分化所致疾病。
技術(shù)實現(xiàn)要素:
本發(fā)明所要解決的主要技術(shù)問題是提供一種治療或診斷由成體神經(jīng)干細胞損傷或異常分化所致疾病的藥物或試劑。
為解決上述技術(shù)問題,本發(fā)明所采取的技術(shù)方案是:
本發(fā)明首先構(gòu)建了1-甲基-4-苯基-1,2,3,6-四氫吡啶(MPTP)誘導(dǎo)的PD小鼠模型,通過實驗觀察發(fā)現(xiàn),在MPTP誘導(dǎo)的PD小鼠模型大腦的海馬齒狀回顆粒下層(Subgranular Zone,SGZ)和側(cè)腦室的室腦膜下區(qū)(Subventricular Zone,SVZ)的增殖的細胞(BrdU+)中,細胞核內(nèi)DJ-1水平增加,而BrdU+的數(shù)量保持不變,這說明了DJ-1的核轉(zhuǎn)位維持了正常的神經(jīng)發(fā)生。在嗅球(Olfactory Bulb,OB)區(qū),BrdU+細胞中并沒有出現(xiàn)DJ-1的核轉(zhuǎn)位,提示了DJ-1的核轉(zhuǎn)位可能僅發(fā)生于神經(jīng)發(fā)生的早期,而隨著細胞的分化遷移將逐漸消失。
本發(fā)明的實驗中采用了MPTP誘導(dǎo)的動物模型。MPTP是一種神經(jīng)毒素,它穿過血腦屏障后會被星形膠質(zhì)細胞和5-羥色胺能神經(jīng)元內(nèi)的單胺氧化酶B作用,代謝成有毒性的1-甲基-4-苯基吡啶(MPP+),釋放到細胞外后不能穿越血腦屏障。MPP+與多巴胺轉(zhuǎn)運體高度親和,可由此進入多巴胺能神經(jīng)元,直接破壞大腦特別是黑質(zhì)中多巴胺能神經(jīng)元。該模型在神經(jīng)生化和運動行為學(xué)表現(xiàn)方面都與PD極其相似,是目前研究PD最理想的動物模型。
此外,本發(fā)明還發(fā)現(xiàn)遷移到嗅小球?qū)拥腂rdU+數(shù)量增多,而且在一些BrdU-的球旁細胞中發(fā)現(xiàn)了DJ-1的核轉(zhuǎn)位,這些實驗結(jié)果說明DJ-1通過核轉(zhuǎn)位也可能保護了嗅小球?qū)拥姆窃鲋臣毎墓δ堋?/p>
本發(fā)明發(fā)現(xiàn)MPTP并未影響小鼠大腦SGZ區(qū)BrdU+陽性細胞數(shù),進一步發(fā)現(xiàn)DJ-1轉(zhuǎn)移到了SGZ和SVZ的BrdU+細胞的細胞核,這表明DJ-1的核轉(zhuǎn)位保持了增殖細胞(即成體神經(jīng)干細胞)的數(shù)量以抵抗MPTP引起的神經(jīng)元損傷,是機體的一種自我修復(fù)機制。在成年的大腦中,SVZ的成體神經(jīng)干細胞可經(jīng)過早期的增殖分化生成神經(jīng)祖細胞,并沿吻側(cè)遷移流(rostral migratory stream,RMS)輸入OB的中心區(qū)域——顆粒細胞層,再進一步分化、成熟、遷移到OB的其他區(qū)域。正常嗅覺功能取決于新生神經(jīng)元的持續(xù)性輸入。本發(fā)明發(fā)現(xiàn)在MPTP組OB的顆粒細胞層和嗅小球?qū)覤rdU+細胞中并沒有發(fā)現(xiàn)DJ-1的核轉(zhuǎn)位,說明DJ-1的核轉(zhuǎn)位發(fā)生在了成體神經(jīng)干細胞增殖分化的早期。本發(fā)明還發(fā)現(xiàn),在OB的嗅小球?qū)硬糠諦rdU-細胞中出現(xiàn)DJ-1的核轉(zhuǎn)位,這可能與上述其他區(qū)域的核轉(zhuǎn)位的發(fā)生依賴于不同的機制。
本發(fā)明認為通過注射MPTP建立急性PD模型激活了DJ-1參與的自我修復(fù)機制,維持了正常的神經(jīng)發(fā)生,SGZ和SVZ/OB依靠不斷產(chǎn)生新生神經(jīng)元以維持正常生理功能,而這兩個腦區(qū)與PD非運動癥狀密切相關(guān)。
綜合本發(fā)明的上述實驗成果,DJ-1可具有以下幾方面的用途:
首先,DJ-1可制成治療或診斷成體神經(jīng)干細胞損傷或異常分化所致疾病的藥物或試劑;其中,所述的成體神經(jīng)干細胞損傷或異常分化所致疾病包括帕金森病;優(yōu)選的,所述的帕金森病是帕金森病的非運動癥狀。例如,可以將DJ-1構(gòu)建到腺病毒載體等基因治療載體中制備得到基因治療藥物,該基因治療藥物可以有效的治療成體神經(jīng)干細胞損傷或異常分化所導(dǎo)致的疾病,尤其是對于帕金森病的非運動癥狀具有非常好的療效。現(xiàn)有的治療帕金森病的藥物大多對于帕金森病的非運動癥狀療效不佳,本發(fā)明將對于帕金森病的非運動癥狀的臨床治療具有重要的意義。
另外,可以將DJ-1應(yīng)用于診斷成體神經(jīng)干細胞損傷或異常分化所致疾病,尤其是應(yīng)用診斷早期帕金森病。例如,可以將DJ-1蛋白制成抗體,通過免疫組織化學(xué)分析等手段,對早期帕金森病進行準(zhǔn)確的診斷。也可以DJ-1為靶基因設(shè)計引物,通過定量PCR方式對檢測樣品中的DJ-1的表達水平進行檢測,進而達到診斷早期帕金森病的目的,由此,本發(fā)明提供了以下各種檢測試劑盒:
一種用于診斷成體神經(jīng)干細胞損傷或異常分化所導(dǎo)致疾病的檢測試劑盒,該檢測試劑盒中含有DJ-1蛋白或用DJ-1蛋白所制備的抗體。
一種用于診斷成體神經(jīng)干細胞損傷或異常分化所致疾病的檢測試劑盒,該檢測試劑盒中含有DJ-1蛋白編碼基因或含有擴增DJ-1蛋白編碼基因的引物。
附圖說明
圖1本發(fā)明的實驗流程示意圖以及SGZ和SVZ區(qū)中BrdU+細胞數(shù)量統(tǒng)計結(jié)果;A:實驗流程示意圖;B:SGZ和SVZ區(qū)中BrdU+細胞數(shù)量統(tǒng)計結(jié)果,與生理鹽水組比較p>0.05(n=5)。
圖2 MPTP誘導(dǎo)了SGZ區(qū)和SVZ區(qū)BrdU+細胞及OB嗅小球?qū)覤rdU-細胞中DJ-1核轉(zhuǎn)位實驗結(jié)果;SGZ(A),SVZ(B),OB的顆粒細胞層(D)和OB的嗅小球?qū)?E)的免疫熒光染色成像;下方4張圖像為上方圖中白色方框區(qū)域的放大圖像;紅色熒光標(biāo)記BrdU,綠色熒光標(biāo)記DJ-1,藍色熒光標(biāo)記細胞核,第4列圖像為前3者的重疊,白色箭頭指示的DJ-1核轉(zhuǎn)位。C:OB的尼氏染色結(jié)果,右圖為左圖中方框區(qū)域的放大圖像,顯示OB的顆粒細胞層。
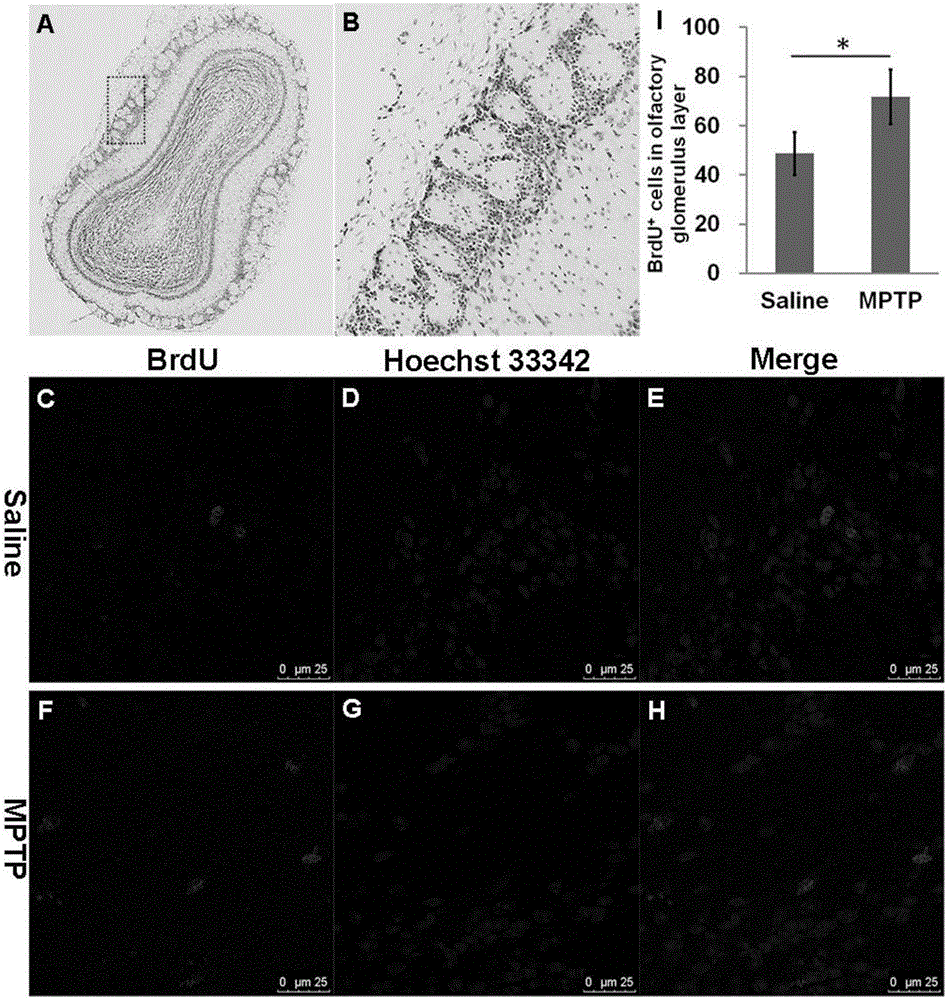
圖3 MPTP增加了BrdU+細胞向OB的嗅小球?qū)訁^(qū)域遷移;A:OB冠狀切片的尼氏染色;B:A圖中的黑框內(nèi)嗅小球?qū)訁^(qū)域放大圖像;C~H:腦組織切片進行免疫熒光染色;紅色熒光標(biāo)記BrdU,藍色熒光標(biāo)記細胞核,第3列圖像為前2者的重疊;I:嗅小球?qū)訁^(qū)BrdU+細胞數(shù)量的統(tǒng)計分析,*與生理鹽水組比較p<0.05(n=5)。
具體實施方式
下面結(jié)合具體實施例來進一步描述本發(fā)明,本發(fā)明的優(yōu)點和特點將會隨著描述而更為清楚。但是應(yīng)理解所述實施例僅是范例性的,不對本發(fā)明的范圍構(gòu)成任何限制。本領(lǐng)域技術(shù)人員應(yīng)該理解的是,在不偏離本發(fā)明的精神和范圍下可以對本發(fā)明技術(shù)方案的細節(jié)和形式進行修改或替換,但這些修改或替換均落入本發(fā)明的保護范圍。
1實驗方法
1.1動物分組及處理
20只10周齡的C57BL/6小鼠隨機分為生理鹽水對照組和MPTP處理組。MPTP處理組每次腹腔注射20mg/kg MPTP,共4次,間隔2小時,生理鹽水對照組腹腔注射等體積的生理鹽水。14天后處死取腦,處死前24小時腹腔注射150mg/kg 5-溴脫氧尿嘧啶核苷(BrdU)用于標(biāo)記增殖的成體神經(jīng)干細胞(圖1A)。
1.2腦冰凍切片的制備
腹腔注射60mg/kg戊巴比妥鈉麻醉小鼠。經(jīng)心臟灌流40ml PBS后再灌流40ml 4%多聚甲醛。取出小鼠大腦置于4%多聚甲醛中固定12小時,然后分別用20%和30%的梯度蔗糖溶液脫水,在干冰中快速冷凍后用OCT包埋制備連續(xù)冰凍冠狀切片,厚度為20μm。
1.3免疫熒光染色
每6張連續(xù)切片取1張進行免疫熒光染色,每只取8張,每組5只,觀察在SGZ、SVZ和OB區(qū)的BrdU+的數(shù)量以及DJ-1在BrdU+細胞中的分布情況。染色前先對腦組織切片進行DNA變性處理:1N HCl冰上孵育10min后再用2N HCl室溫孵育10min,然后置于37℃孵箱繼續(xù)孵育20min,隨后用0.1M的硼酸鹽緩沖液室溫孵育10min,最后用含0.1%Triton X-100的PBS清洗3次,每次10min。接下來進行免疫熒光染色。先用含10%的正常羊血清和0.3%Triton X-100的PBS在37℃封閉1小時,然后用抗BrdU抗體和抗DJ-1抗體(溶于含2%的正常羊血清和0.3%TritonX-100的PBS)4℃孵育過夜。用PBS清洗3遍后,用Alexa555標(biāo)記的羊抗大鼠lgG和Alexa488標(biāo)記的羊抗兔lgG(溶于含2%的正常羊血清和0.3%Triton X-100的PBS)37℃孵育1小時。用PBS清洗3遍后,Hoechst 33342(5μg/ml)室溫孵育5min標(biāo)記細胞核。最后用防熒光淬滅封片劑封片。染色完成后利用熒光共聚焦掃描顯微鏡SP8-Confocal-MP-FLIM進行觀察。
1.4統(tǒng)計分析
數(shù)據(jù)用mean±SD表示。利用統(tǒng)計軟件SPSS 22對組間差異進行單因素方差分析檢測,p<0.05被認為具有統(tǒng)計學(xué)差異。
2實驗結(jié)果
2.1MPTP處理組的小鼠大腦SGZ和SVZ區(qū)中BrdU+細胞數(shù)量保持不變
BrdU作為胸腺嘧啶脫氧核苷的類似物可以摻入到處于細胞周期S期的增殖細胞的DNA中,通過熒光標(biāo)記BrdU以識別增殖的細胞。實驗結(jié)果顯示,與生理鹽水對照組(SGZ:203±30.05;SVZ:80.00±7.00)相比MPTP處理組(SGZ:187.33±27.21;SVZ:74.00±8.89)的小鼠大腦SGZ區(qū)中BrdU+細胞數(shù)量沒有顯著差異(SGZ:p=0.54;SVZ:p=0.41,n=5)(圖1B)。
2.2MPTP處理后的DJ-1核轉(zhuǎn)位情況
本實驗觀察了在SGZ、SVZ和OB區(qū)BrdU+細胞中的DJ-1亞細胞分布。免疫熒光染色結(jié)果發(fā)現(xiàn),MPTP處理14天后在BrdU+細胞(紅色)中DJ-1(綠色)表達增加區(qū)域與核區(qū)(藍色)重疊,提示BrdU+細胞中DJ-1發(fā)生了核轉(zhuǎn)位(圖2A和B)。在OB顆粒細胞層(圖2C,尼氏染色指示顆粒細胞層位置)的BrdU+細胞中未發(fā)現(xiàn)DJ-1核轉(zhuǎn)位(圖2D)。但在OB的嗅小球?qū)影l(fā)現(xiàn),DJ-1在部分BrdU-細胞中發(fā)生了核轉(zhuǎn)位(圖2E)。
2.3MPTP增加了BrdU+細胞向OB的嗅小球?qū)訁^(qū)域遷移
免疫熒光染色結(jié)果發(fā)現(xiàn),與生理鹽水對照組(48.67±8.62)相比,MPTP處理組(71.67±11.15)中BrdU+細胞(紅色)向OB的嗅小球?qū)舆w移的數(shù)量顯著增加(p=0.048,n=5)(圖3)。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 一種維持小鼠上胚層干細胞自我更新狀態(tài)的培養(yǎng)方法與制造工藝
- 一種促進神經(jīng)干細胞增殖和分化的培養(yǎng)方法與制造工藝
- 一種誘導(dǎo)成纖維細胞轉(zhuǎn)分化為神經(jīng)細胞的方法與制造工藝
- 干細胞的分化狀態(tài)的判定方法以及該判定方法中使用的新的分化標(biāo)記與制造工藝
- 喹唑啉化合物在調(diào)控神經(jīng)干細胞增殖和分化中的應(yīng)用的制造方法與工藝
- 具有促進干細胞分化的支架材料及其制備方法和用途與制造工藝
- 一種阻斷帕金森患者淋巴細胞周期的藥物及制備方法與制造工藝
- 一種治療腦部損傷類疾病的神經(jīng)干細胞注射液的制造方法與工藝
- 間充質(zhì)干細胞培養(yǎng)試劑盒的制作方法
- 一種干細胞運輸箱的制作方法
- 一種神經(jīng)干細胞培養(yǎng)基及利用其進行的人神經(jīng)干細胞體外長期培養(yǎng)擴增方法
- 一種負載移植性神經(jīng)干細胞的PF-127-LV-NFcocktail復(fù)合物及其制備方法和應(yīng)用
- 一種用于制備神經(jīng)干細胞的試劑盒及制備神經(jīng)干細胞的方法
- 一種神經(jīng)干細胞的大規(guī)模制備方法
- 一種用于貼壁培養(yǎng)人神經(jīng)干細胞的臨床級無血清培養(yǎng)基的制作方法
- 膠質(zhì)細胞源生神經(jīng)營養(yǎng)因子基因修飾的胚胎神經(jīng)干細胞構(gòu)建的制作方法
- 與神經(jīng)干細胞分化相關(guān)基因dcf1的新用途的制作方法
- 誘導(dǎo)干細胞分化為神經(jīng)干細胞的阿魏酸及其鈉鹽的試劑和藥物用途的制作方法
- 由人類滋養(yǎng)層干細胞生成神經(jīng)干細胞的制作方法
- 一種能無限自我更新的神經(jīng)干細胞、其制備方法及其用途的制作方法
- 一種牙髓間充質(zhì)干細胞的復(fù)蘇培養(yǎng)基及其復(fù)蘇培養(yǎng)方法
- 培養(yǎng)多能干細胞的制作方法
- 一種培養(yǎng)神經(jīng)干細胞的試劑盒的制作方法
- 一種宮頸癌干細胞培養(yǎng)裝置的制造方法
- 多能干細胞的培養(yǎng)方法、該方法中所使用的多能干細胞的培養(yǎng)用試劑盒及培養(yǎng)基的制作方法
- 一種干細胞分化培養(yǎng)基及其應(yīng)用
- 一種用于培養(yǎng)人脂肪干細胞的培養(yǎng)基的制作方法
- 干細胞培養(yǎng)基及培養(yǎng)宮內(nèi)膜干細胞的方法
- 一種神經(jīng)干細胞添加劑的制作方法
- 神經(jīng)干細胞在介導(dǎo)影響p25和p35蛋白表達中的應(yīng)用
- 小鼠海馬神經(jīng)干細胞向軟骨細胞分化的方法
- 自罹患神經(jīng)管缺陷胎兒羊水分離人類神經(jīng)干細胞的制作方法
- 一種培養(yǎng)神經(jīng)干細胞的試劑盒的制作方法
- 一種豬生殖干細胞體外分化精子的建立方法
- 一種神經(jīng)干細胞添加劑的制作方法
- Sfrp2在促進牙源性間充質(zhì)干細胞成骨/成牙分化中的應(yīng)用
- 神經(jīng)干細胞在介導(dǎo)影響p25和p35蛋白表達中的應(yīng)用
- 分化培養(yǎng)基及其在制備神經(jīng)干細胞中的用圖
- 多能干細胞向多能腎前體分化的方法
- 一種誘導(dǎo)神經(jīng)干細胞分化為多巴胺能神經(jīng)元的方法