一種可載藥聚乙烯醇洗脫微球的制備方法與流程
本發明涉及一種可永久栓塞的藥物載體的制備方法,涉及生物醫藥領域,尤其涉及一種可載藥聚乙烯醇洗脫微球的制備方法。
背景技術:
原發性肝癌是一種常見的惡性腫瘤,其發病率和死亡率均較高,全球肝癌的發病率呈逐年上升的趨勢。我國是全球肝癌發病率最高和病死數最多的國家,肝癌的發病率成為死亡率僅次于胃癌、肺癌的第三大惡性腫瘤。該病嚴重威脅人們的身體健康,常見的治療腫瘤方案是采用手術切除法,但是對于中晚期的腫瘤患者來說,介入療法(ranscatheter arterial chemoembolization,TACE)是比較理想的治療方案。介入治療指的是經導管動脈化療栓塞術,即經導管將含藥微球輸入靶組織,阻斷腫瘤的供血動脈并緩慢釋放藥物,從而提高化療藥物的局部濃度,降低了全身的毒副作用。一系列臨床分析顯示TACE能有效地控制腫瘤生長,延長患者生存期。對于不能手術切除的中晚期肝癌患者,TACE是首選的非手術治療方法。
聚乙烯醇(PVA)是一種水溶性高分子聚合物,攜帶官能基團單一(只有羥基)又可以大量人工合成,被廣泛應用于生產生活中多個領域,是一種非常安全的大分子有機物。它對人體無毒、無副作用,且具有良好的生物相容性,在醫療領域有著廣泛的應用,例如PVA水凝膠應用在傷口敷料、人工關節和眼科;PVA薄膜應用在人工腎膜、藥用膜等方面;針對癌癥的治療,由PVA制備的血管栓塞劑已應用在醫學臨床上。目前,以PVA作為原料制備栓塞微球已有一些報道,但是PVA用來制備載藥微球尚有缺陷:一是傳統的PVA微球只能起著機械栓塞的作用,無法負載藥物;二是雖然近些年有人對PVA微球進行表面改性,試圖接枝上載藥基團,但接枝率低,使得微球的載藥率低,藥物易突釋。另外純PVA分子中氫鍵較多,鏈段之間相互作用強,形成的微球由于高結晶性而溶脹差,彈性不足,作為血管栓塞劑的材料柔軟性不夠。
技術實現要素:
針對上述缺陷,本文首先將2-丙烯酰胺-2-甲基丙磺酸(AMPS)加入到聚乙烯醇溶液中,在引發劑作用下,對聚乙烯醇進行改性,使其接枝上大量的磺酸基團,同時,以N,N-亞甲基雙丙烯酰胺(MBA)做交聯劑,在反相微懸浮條件下,制備出含有磺酸基團的聚乙烯微球。由于2-丙烯酰胺-2-甲基丙磺酸分子中的磺酸基是強電離基團,親水性極強,將該基團引入到聚乙烯醇分子上,可以大大提高聚乙烯醇糖微球對藥物阿霉素的負載率;另一方面聚乙烯醇進行改性后,鏈段結構規整性破壞,減弱了結晶性,可以改善聚乙烯醇微球的溶脹性和柔順性,更有利于微球在血管中的靶向栓塞。且含有磺酸基團的聚乙烯醇微球具有無細胞毒性、生物相容性好、原料來源廣泛等優點。
本發明提供制備一種可載藥聚乙烯醇洗脫微球作為藥物載體的技術方案,依次包括以下步驟:
1)配制聚乙烯醇混合液,將聚乙烯醇、2-丙烯酰胺-2-甲基丙磺酸按一定比例溶解在蒸餾水中,完全溶解后,加入N,N-亞甲基雙丙烯酰胺溶液,常溫下磁力攪拌,混合均勻;然后再加入計量的過硫酸鉀,攪拌數分鐘。
2)改性聚乙烯醇微球的制備,將上述聚乙烯醇混合液滴入到油相里,完成乳化后,加入計量的的亞硫酸氫鈉,采用反相微懸浮交聯方法,在40℃條件下攪拌反應8小時后,加入少量鹽酸和戊二醛,反應2小時,固化成球,最后用大量乙醇清洗數次、蒸餾水浸泡洗滌數次,真空干燥,得到粒徑在100~700um含有磺酸基團的改性聚乙烯醇微球,即可載藥聚乙烯醇洗脫微球。
具體的,所述步驟1)中,聚乙烯醇規格為1788型,聚乙烯醇混合液的質量分數為5%~15%,2-丙烯酰胺-2-甲基丙磺酸的用量占聚乙烯醇質量的1~2倍,N,N-亞甲基雙丙烯酰胺占聚乙烯醇質量的1%~10%,其方法是先將N,N-亞甲基雙丙烯酰胺溶解在其質量6倍的N,N-二甲基乙酰胺中形成溶液,再將此溶液加入到聚乙烯醇溶液中。
具體的,所述步驟1)中,引發劑為過硫酸鉀與亞硫酸氫鈉的氧化-還原引發體系,過硫酸鉀的用量占聚乙烯醇質量的1%,亞硫酸氫鈉的用量是過硫酸鉀質量的五分之一。
具體的,所述步驟2)中,油相為正庚烷、正辛烷、石蠟油或大豆油,油相與水相的體積比為4:1~8:1。
具體的,所述步驟2)中,乳化劑為司班80與吐溫60按重量比4:1的復配物,其總用量占油相質量的1%~5%。
具體的,所述步驟2)中,將上述聚乙烯醇混合液逐漸滴入到油相里,通氮氣保護,完成乳化后,加入計量的亞硫酸氫鈉水溶液,接著升溫至40℃,并控制攪拌速度為300~500rad/min,反應8h后,加入戊二醛,在濃度36%的鹽酸催化下,固化成球,鹽酸用量占聚乙烯醇質量的10%,戊二醛用量占聚乙烯醇質量的5%~20%。
本發明還提供一種可載藥聚乙烯醇洗脫微球在制備藥物載體中的應用方法,其特征是首先根據權利要求1所述的方法制備可載藥聚乙烯醇洗脫微球,選擇其中任何一微球品種0.5g,經過真空干燥,浸泡在飽和濃度的鹽酸阿霉素水溶液中,在8℃溫度下攪拌3小時,過濾出載藥微球,用去離子水沖洗微球表面殘留藥物,真空干燥微球后密封保存,可在pH 7.4的磷酸緩沖液介質中釋放藥物。
可載藥的洗脫微球在靶向導向腫瘤組織的動脈中,不僅阻斷對腫瘤組織的營養供給,還可以釋放抗腫瘤藥物,隨著腫瘤組織中抗癌藥物濃度的升高,對病變部位起到抑制的作用。
借由上述方案,本發明至少具有以下優點:
1.使用一種新的制備方法,先在聚乙烯醇分子接枝上磺酸基團,再形成微球,使得微球中含有大量的磺酸基團,從而提高微球的載藥率;
2.改善了微球的內部結構,提高了微球的溶脹性和柔軟性,更有利于微球在血管中的靶向栓塞;
3.由于該微球含有磺酸基團,通過電荷吸附藥物分子,大大消除了微球表面物理吸附而引起的突釋,起到了緩釋藥物的目的;
4.制備出的洗脫微球無毒、細胞相容性較好,符合人體使用的安全性標準;在人體內可永久栓塞;
5.通過反相微懸浮聚合方法合成的洗脫微球,方法簡單、條件溫和,無副產物產生,反應完全,產物純凈。
上述說明僅是本發明技術方案的概述,為了能夠更清楚了解本發明的技術手段,并可依照說明書的內容予以實施,以下是本發明的較佳實施例并配合附圖詳細說明如后。
附圖說明
圖1為可載藥聚乙烯醇洗脫微球的合成路線。
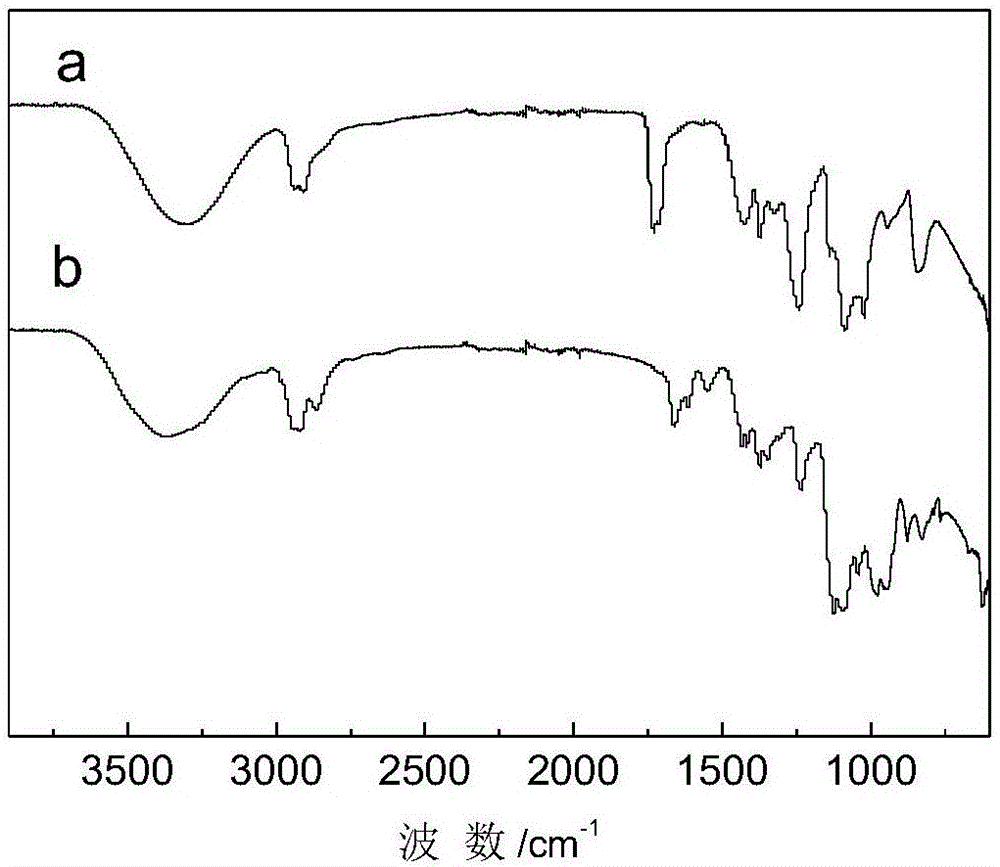
圖2為改性前后聚乙烯醇的紅外譜圖,其中a:未改性聚乙烯醇;b:改性后聚乙烯醇微球。
圖3為本發明中可載藥聚乙烯醇洗脫微球的超景深顯微鏡照片。
圖4為本發明中可載藥聚乙烯醇洗脫微球在pH 7.4的磷酸緩沖液中的累計釋放率曲線。
具體實施方式
下面結合附圖和實施例,對本發明的具體實施方式作進一步詳細描述。以下實施例用于說明本發明,但不用來限制本發明的范圍。
1)可載藥聚乙烯醇洗脫微球的制備:
實施例1.
將1.1g聚乙烯醇和2.2g,2-丙烯酰胺-2-甲基丙磺酸加入到8.9g蒸餾水中,常溫下,磁力攪拌至完全溶解,然后加入0.314g,14%MBA溶液,混合均勻后,再加入計量0.275g,4%過硫酸鉀溶液,攪拌數分鐘。量取50ml正庚烷,放入到250ml三口燒瓶中,加入0.68g(占油相質量的2%)乳化劑,其中司班80為0.544g,吐溫60為0.134g(司班80與吐溫60質量比為4:1),常溫下機械攪拌,轉速為350rad/min,通氮氣保護。完成乳化后,用微量注射器逐滴加入0.22g,1%亞硫酸氫鈉溶液,然后升溫至40℃,反應8h后,加入0.3ml鹽酸和0.5g,25%戊二醛溶液,2h后,用大量乙醇破乳、清洗微球,反復洗滌數次,最后將微球放入35℃真空干燥箱中干燥24小時,得到粒徑在100~700um的改性聚乙烯醇微球。
實施例2.
將1.1g聚乙烯醇和2.2g,2-丙烯酰胺-2-甲基丙磺酸加入到8.06g蒸餾水中,常溫下,磁力攪拌至完全溶解。其他合成過程和實施例1相同。
實施例3.
將1.1g聚乙烯醇和2.2g,2-丙烯酰胺-2-甲基丙磺酸加入到9.90g蒸餾水中,常溫下,磁力攪拌至完全溶解。其他合成過程和實施例1相同。
實施例4
將1.1g聚乙烯醇和2.2g,2-丙烯酰胺-2-甲基丙磺酸加入到11.12g蒸餾水中,常溫下,磁力攪拌至完全溶解。其他合成過程和實施例1相同。
表1不同濃度的聚乙烯醇濃度對制備微球的影響
實施例5
將1.1g聚乙烯醇和2.2g,2-丙烯酰胺-2-甲基丙磺酸加入到8.9g蒸餾水中,常溫下,磁力攪拌至完全溶解,然后加入0.314g,14%MBA溶液,混合均勻后,再加入計量0.275g,4%過硫酸鉀溶液,攪拌數分鐘。量取50ml石蠟油,放入到250ml三口燒瓶中,加入0.80g司班80(占油相質量2%),常溫下機械攪拌,轉速為400rad/min,通氮氣保護。完成乳化后,用微量注射器逐滴加入0.22g,1%亞硫酸氫鈉溶液,然后升溫至40℃,反應8h后,加入0.3ml鹽酸和0.5g,25%戊二醛溶液,2h后,用大量正己烷、異丙醇清洗微球,反復洗滌數次,最后將微球放入35℃真空干燥箱中干燥24小時,得到粒徑在100~700um的改性聚乙烯醇微球。
實施例6
稱取上述實施例1改性聚乙烯醇微球25mg,放入10ml,2mg/ml的阿霉素溶液中。室溫下,緩慢震蕩,通過使用紫外分光光度計,在不同時間段,檢測波長在483nm處阿霉素溶液的濃度,計算微球的載藥率,按照下列公式計算微球的載藥率(LR):
LR(%)=WD/WS×100
式中WD——微球中藥物的質量,mg
WS——投入微球的質量,mg
通過計算,改性后聚乙烯醇微球載藥率達到23.5%。
實施例7
表面功能化可載藥洗脫微球的合成路線圖。如圖1。
實施例8
分別取少量未改性聚乙烯醇和改性后的聚乙烯醇微球,使用全反射傅里葉紅外光譜儀,在4000~500cm-1的波數范圍內進行紅外吸收掃描,得到紅外譜圖。圖2為改性前后聚乙烯醇的紅外譜圖,其中a:未改性聚乙烯醇;b:改性后的聚乙烯醇微球。
實施例9
選取粒徑在400~500um的改性后聚乙烯醇微球,分別在超景深顯微鏡下觀察微球形貌。圖3為本發明中可載藥聚乙烯醇洗脫微球的超景深顯微鏡照片。
實施例10
選取粒徑均在400~500um的改性載藥微球和未改性載藥微球,各稱取25mg,放入PBS(pH 7.4)緩沖溶液中,然后將其置于恒溫水浴振蕩器中,溫度控制在37±0.5℃,定點量取5mL上清液,并及時補充相同體積的新鮮介質,通過紫外分光光度計檢測緩沖液中藥物含量,重復操作3次取平均值,計算不同時間段在PBS(pH 7.4)介質中的累計釋放率,并繪制相應曲線。
圖4為本發明中載藥微球在PBS(pH 7.4)介質中的累計釋放率曲線。
以上所述僅是本發明的優選實施方式,并不用于限制本發明,應當指出,對于本技術領域的普通技術人員來說,在不脫離本發明技術原理的前提下,還可以做出若干改進和變型,這些改進和變型也應視為本發明的保護范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!