丹酚酸A作為脂蛋白相關(guān)磷脂酶A2抑制劑的新用途的制作方法
本發(fā)明屬于醫(yī)藥技術(shù)領(lǐng)域,具體是丹酚酸a作為脂蛋白相關(guān)磷脂酶a2抑制劑的新用途。
背景技術(shù):
脂蛋白相關(guān)磷脂酶a2(lp-pla2)是一種ca2+不依賴型的分泌磷脂酶a2,血漿lp-pla2與脂蛋白顆粒結(jié)合,其中約80%與低密度脂蛋白(ldl)結(jié)合,尤其是小顆粒ldl,僅10%與高密度脂蛋白(hdl)結(jié)合。lp-pla2與分泌型磷脂酶a2(spla2)、胞漿型磷脂酶a2(cpla2)共同組成磷脂酶a2(phospholipasea2,pla2)家族。研究表明,cpla2、spla2和lp-pla2在促進(jìn)炎癥反應(yīng)和引起動脈粥樣硬化(as)中起著重要的作用,與心血管事件的發(fā)生有密切關(guān)系。其中,lp-pla2作為一種新的炎癥標(biāo)志物,是當(dāng)前研究的熱點。研究顯示,lp-pla2與as、腫瘤等嚴(yán)重威脅人類健康的重大疾病密切相關(guān)。lp-pla2能水解氧化ldl,產(chǎn)生溶血卵磷脂(lpc)和氧化非酯化脂肪酸(oxnefa)兩種前體炎性因子,促進(jìn)as發(fā)生。大量報道表明lp-pla2抑制劑具有抗as作用,可用于降低冠心病患者的心血管事件,明顯延緩as發(fā)展,減少損傷血管巨噬細(xì)胞含量和緩解動物模型的斑塊炎癥。但是已有的lp-pla2抑制劑未能降低心臟病發(fā)作和中風(fēng)的整體風(fēng)險,而且副作用多。這也促使人們尋求新的有效lp-pla2抑制劑。
丹酚酸a(saa)是唇形科植物丹參的干燥根及根莖中所含的一種水溶性酚酸類化合物。近年來研究表明,saa在心腦血管疾病保護(hù)、抗肝損傷、糖尿病及并發(fā)癥、抗腫瘤等方面有顯著活性。但是丹酚酸a作為脂蛋白相關(guān)磷脂酶a2抑制劑的研究未見報道。
技術(shù)實現(xiàn)要素:
為了解決上述技術(shù)問題,本發(fā)明提供了一種丹酚酸a作為脂蛋白相關(guān)磷脂酶a2抑制劑的新用途。
本發(fā)明的另一個目的是提供了丹酚酸a作為脂蛋白相關(guān)磷脂酶a2抑制劑在制備防治動脈粥樣硬化藥物中的用途。
本發(fā)明還提供了丹酚酸a作為脂蛋白相關(guān)磷脂酶a2抑制劑在制備防治心腦血管疾病藥物中的用途。
本發(fā)明還提供了丹酚酸a作為脂蛋白相關(guān)磷脂酶a2抑制劑在制備防治糖尿病及并發(fā)癥藥物中的用途。
本發(fā)明還提供了丹酚酸a作為脂蛋白相關(guān)磷脂酶a2抑制劑在制備抗腫瘤藥物中的用途。
所述的用途,其中丹酚酸a與藥學(xué)上可接受的載體組成臨床可以接受的制劑。
所述載體包括藥學(xué)領(lǐng)域的常規(guī)稀釋劑,賦形劑,填充劑,粘合劑,濕潤劑,崩解劑,吸收促進(jìn)劑,表面活性劑,吸附載體,潤滑劑等,必要時還可以加入香味劑,甜味劑等。本發(fā)明藥物可以制成片劑,粉劑,粒劑,膠囊,口服液及注射用藥等多種形式,上述各劑型的藥物均可以按照藥學(xué)領(lǐng)域的常規(guī)方法制備。
本發(fā)明通過高脂飼喂聯(lián)合vd3注射和球囊損傷術(shù)建立大鼠as模型,研究丹酚酸a對as大鼠血清lp-pla2含量和活性的影響,對as大鼠主動脈lp-pla2mrna和蛋白表達(dá)的影響。結(jié)果顯示,丹酚酸a可降低as大鼠血清lp-pla2含量及活性,下調(diào)主動脈lp-pla2蛋白的表達(dá),從而發(fā)揮抗as作用。通過建立人胰腺癌bxpc3裸鼠皮下移植瘤模型,通過瘤內(nèi)注射和靜脈注射兩種給藥途徑給予2mg/kgsaa,研究saa對荷瘤裸鼠lp-pla2、cpla2、spla2表達(dá)的影響,結(jié)果發(fā)現(xiàn),saa可顯著降低荷瘤裸鼠腫瘤組織、瘤旁組織及血清中l(wèi)p-pla2、cpla2、spla2的含量,可顯著減小腫瘤體積。通過建立zdf大鼠模型,結(jié)果顯示丹酚酸a可顯著降低zdf大鼠血清中l(wèi)p-pla2含量,由此可見,丹酚酸a在作為脂蛋白相關(guān)磷脂酶a2抑制劑以及防治動脈粥樣硬化、防治心腦血管疾病、抗腫瘤、防治糖尿病及并發(fā)癥中具有廣闊的應(yīng)用前景。
附圖說明
圖1為丹酚酸a對as大鼠血清中l(wèi)p-pla2含量的影響。
其中,與正常組比較,##p<0.01;與模型組比較,*p<0.05,**p<0.01。
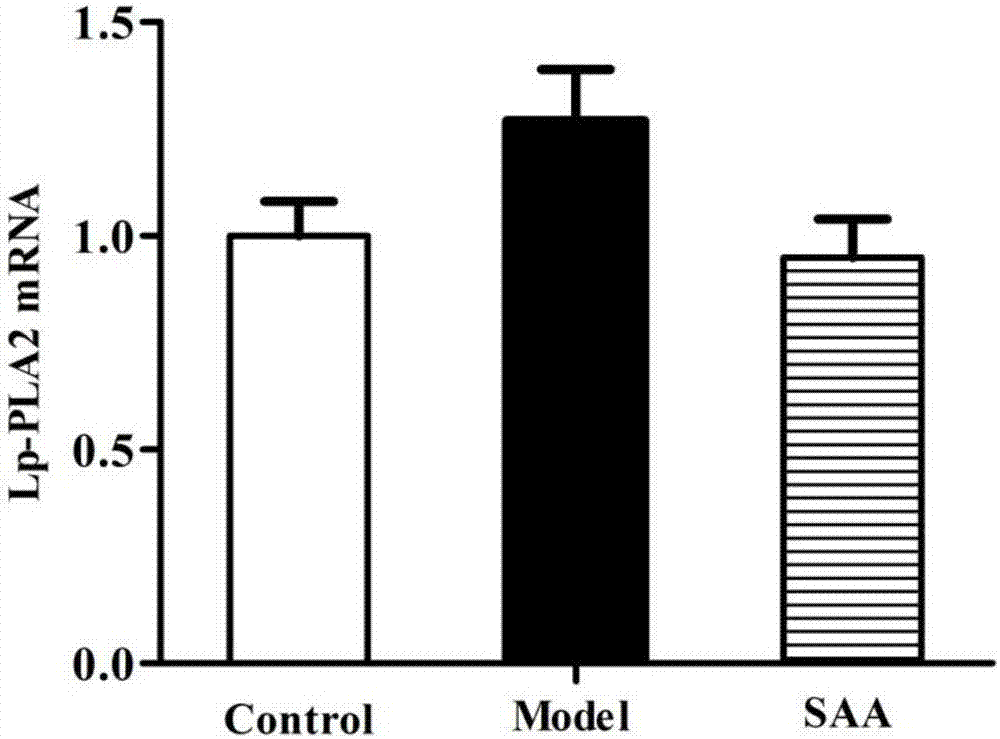
圖2為丹酚酸a對as大鼠主動脈lp-pla2mrna表達(dá)的影響。
圖3為丹酚酸a對as大鼠主動脈lp-pla2蛋白表達(dá)水平的影響。
其中,與正常組比較,##p<0.01;與模型組比較,*p<0.05。
圖4為丹酚酸a對人胰腺癌bxpc3移植瘤裸鼠lp-pla2、cpla2、spla2含量的影響。
其中,saa-1組為瘤內(nèi)注射2mg/kgsaa,saa-2組為尾靜脈注射給予2mg/kgsaa;與對照組比較,*p<0.05,**p<0.01。
圖5為丹酚酸a對人胰腺癌bxpc3裸鼠移植瘤生長的抑制作用。
圖6為丹酚酸a對zdf大鼠組織中l(wèi)p-pla2mrna表達(dá)的影響。
圖7為丹酚酸a對zdf大鼠組織中l(wèi)p-pla2蛋白表達(dá)的影響。
具體實施方式
實施例1:丹酚酸a對as大鼠血清中l(wèi)p-pla2含量的影響
材料:丹酚酸a、維生素d3注射液、戊巴比妥鈉、大鼠lp-pla2elisa檢測試劑盒、血小板活化因子乙酰水解酶分析試劑盒。
實驗動物:spf級雄性sd大鼠,6~8周齡,體重220~250g。
(1)實驗方法
1.模型建立和分組給藥
1.1模型建立
雄性sd大鼠適應(yīng)性飼養(yǎng)1周后,用于模型制備,高脂飼喂(膽固醇1%、豬油10%、蛋黃粉10%、3號膽鹽0.5%、基礎(chǔ)飼料78.5%),同時腹腔注射40萬iu/kg的vd3。vd3注射2周后,參照文獻(xiàn)行主動脈球囊損傷術(shù)。大鼠用3%戊巴比妥鈉(45mg/kg)腹腔麻醉,頸部剃毛,背部固定于鼠板。碘酒消毒頸部皮膚,無菌條件下作頸部正中開口,鈍性分離大鼠左側(cè)頸總動脈,結(jié)扎遠(yuǎn)心端,動脈夾夾閉近心端,暫時阻斷左側(cè)頸總動脈近心及遠(yuǎn)心端血流。在兩端之間的動脈壁上約呈45°顯微剪剪開一“v”形開口,向近心端仔細(xì)輕柔插入2.0×20mm直徑球囊導(dǎo)管,松開動脈夾,使球囊進(jìn)入近心端動脈,并向頸總動脈起始部推送8~10cm。手推式壓力泵注入生理鹽水,將球囊充盈,用4~6atm加壓球囊,然后,回抽球囊(以回來時有明顯阻力感,又可以拉動球囊為宜),當(dāng)球囊回撤至切口處時球囊完全減壓,然后再將球囊導(dǎo)管推送入主動脈,再次充盈球囊、回撤減壓,使之與動脈內(nèi)膜摩擦,造成內(nèi)膜機(jī)械損傷。如此來回摩擦5次后,釋放球囊氣體,退出導(dǎo)管,結(jié)扎近心端頸總動脈。生理鹽水沖洗傷口,并灑青霉素鈉防感染,縫合肌肉和皮膚,碘酒再次消毒皮膚,將動物放入保溫箱保暖護(hù)理待其蘇醒。
1.2分組給藥
次日,選擇手術(shù)成功的大鼠,按體重隨機(jī)分為2組,即模型組(model)、saa組(saa)、每組6只。另6只作為正常組(control),共3組,每籠3只飼養(yǎng)。正常組和模型對照組大鼠均尾靜脈注射5ml/kg生理鹽水,saa組每天尾靜脈注射saa1mg/kg,連續(xù)4周。試驗期間,除正常組飼喂普通飼料外,其余各組高脂飼喂,并于給藥前和給藥2周時分別注射10萬iu/kgvd3。
1.3血清lp-pla2含量及活性測定
1.3.1血清lp-pla2含量測定
采用elisa法測定大鼠血清中l(wèi)p-pla2含量。操作步驟按照試劑盒說明進(jìn)行。
1.3.2血清lp-pla2活性測定
按pafacetylhydrolaseassaykit試劑盒說明書進(jìn)行測定,根據(jù)說明書提供的公式計算各樣本的lp-pla2活性。結(jié)果以每分鐘每升血漿水解paf的微摩爾數(shù)表示lp-pla2活性(μmol/min/l)。
(2)實驗結(jié)果:與正常組比,as模型組大鼠血清lp-pla2含量和活性顯著升高(p<0.05)。與模型組比,saa給藥組lp-pla2含量和活性均明顯降低(p<0.05)。結(jié)果詳見圖1。
實施例2:丹酚酸a對as大鼠主動脈lp-pla2mrna表達(dá)的影響
材料:丹酚酸a、維生素d3注射液、戊巴比妥鈉、逆轉(zhuǎn)錄試劑盒、熒光定量試劑盒、總rna提取試劑盒。
實驗動物:spf級雄性sd大鼠,6~8周齡,體重220~250g。
(1)實驗方法
1.模型建立和分組給藥
1.1模型建立
雄性sd大鼠適應(yīng)性飼養(yǎng)1周后,用于模型制備,高脂飼喂(膽固醇1%、豬油10%、蛋黃粉10%、3號膽鹽0.5%、基礎(chǔ)飼料78.5%),同時腹腔注射40萬iu/kg的vd3。vd3注射2周后,參照文獻(xiàn)行主動脈球囊損傷術(shù)。大鼠用3%戊巴比妥鈉(45mg/kg)腹腔麻醉,頸部剃毛,背部固定于鼠板。碘酒消毒頸部皮膚,無菌條件下作頸部正中開口,鈍性分離大鼠左側(cè)頸總動脈,結(jié)扎遠(yuǎn)心端,動脈夾夾閉近心端,暫時阻斷左側(cè)頸總動脈近心及遠(yuǎn)心端血流。在兩端之間的動脈壁上約呈45°顯微剪剪開一“v”形開口,向近心端仔細(xì)輕柔插入2.0×20mm直徑球囊導(dǎo)管,松開動脈夾,使球囊進(jìn)入近心端動脈,并向頸總動脈起始部推送8~10cm。手推式壓力泵注入生理鹽水,將球囊充盈,用4~6atm加壓球囊,然后,回抽球囊(以回來時有明顯阻力感,又可以拉動球囊為宜),當(dāng)球囊回撤至切口處時球囊完全減壓,然后再將球囊導(dǎo)管推送入主動脈,再次充盈球囊、回撤減壓,使之與動脈內(nèi)膜摩擦,造成內(nèi)膜機(jī)械損傷。如此來回摩擦5次后,釋放球囊氣體,退出導(dǎo)管,結(jié)扎近心端頸總動脈。生理鹽水沖洗傷口,并灑青霉素鈉防感染,縫合肌肉和皮膚,碘酒再次消毒皮膚,將動物放入保溫箱保暖護(hù)理待其蘇醒。
1.2分組給藥
次日,選擇手術(shù)成功的大鼠,按體重隨機(jī)分為2組,即模型組(model)、saa組(saa)、每組6只。另6只作為正常組(control),共3組,每籠3只飼養(yǎng)。正常組和模型對照組大鼠均尾靜脈注射5ml/kg生理鹽水,saa組每天尾靜脈注射saa1mg/kg,連續(xù)4周。試驗期間,除正常組飼喂普通飼料外,其余各組高脂飼喂,并于給藥前和給藥2周時分別注射10萬iu/kgvd3。
1.3熒光定量pcr
用總rna提取試劑盒提取大鼠血管組織總rna,按產(chǎn)品說明書進(jìn)行操作。按逆轉(zhuǎn)錄試劑盒說明書操作步驟合成cdna,選取gapdh為內(nèi)參基因,大鼠gapdh和lp-pla2mrna引物序列如下表。按照熒光定量試劑盒操作步驟,將cdna用實時熒光定量pcr儀進(jìn)行擴(kuò)增,反應(yīng)操作在冰上進(jìn)行。
表1實時熒光定量pcr引物序列
(2)實驗結(jié)果
與正常組比較,as模型組血管lp-pla2mrna表達(dá)有升高趨勢,給予1mg/kgsaa能降低lp-pla2mrna的表達(dá)。結(jié)果詳見圖2。
實施例3:丹酚酸a對as大鼠主動脈lp-pla2蛋白表達(dá)的影響。
材料:丹酚酸a,維生素d3注射液、戊巴比妥鈉、lp-pla2抗體
實驗動物:spf級雄性sd大鼠,6~8周齡,體重220~250g。
(1)實驗方法
1.模型建立和分組給藥
1.1模型建立
雄性sd大鼠適應(yīng)性飼養(yǎng)1周后,用于模型制備,高脂飼喂(膽固醇1%、豬油10%、蛋黃粉10%、3號膽鹽0.5%、基礎(chǔ)飼料78.5%),同時腹腔注射40萬iu/kg的vd3。vd3注射2周后,參照文獻(xiàn)行主動脈球囊損傷術(shù)。大鼠用3%戊巴比妥鈉(45mg/kg)腹腔麻醉,頸部剃毛,背部固定于鼠板。碘酒消毒頸部皮膚,無菌條件下作頸部正中開口,鈍性分離大鼠左側(cè)頸總動脈,結(jié)扎遠(yuǎn)心端,動脈夾夾閉近心端,暫時阻斷左側(cè)頸總動脈近心及遠(yuǎn)心端血流。在兩端之間的動脈壁上約呈45°顯微剪剪開一“v”形開口,向近心端仔細(xì)輕柔插入2.0×20mm直徑球囊導(dǎo)管,松開動脈夾,使球囊進(jìn)入近心端動脈,并向頸總動脈起始部推送8~10cm。手推式壓力泵注入生理鹽水,將球囊充盈,用4~6atm加壓球囊,然后,回抽球囊(以回來時有明顯阻力感,又可以拉動球囊為宜),當(dāng)球囊回撤至切口處時球囊完全減壓,然后再將球囊導(dǎo)管推送入主動脈,再次充盈球囊、回撤減壓,使之與動脈內(nèi)膜摩擦,造成內(nèi)膜機(jī)械損傷。如此來回摩擦5次后,釋放球囊氣體,退出導(dǎo)管,結(jié)扎近心端頸總動脈。生理鹽水沖洗傷口,并灑青霉素鈉防感染,縫合肌肉和皮膚,碘酒再次消毒皮膚,將動物放入保溫箱保暖護(hù)理待其蘇醒。
1.2分組給藥
次日,選擇手術(shù)成功的大鼠,按體重隨機(jī)分為2組,即模型組(model)、saa組(saa)、每組6只。另6只作為正常組(control),共3組,每籠3只飼養(yǎng)。正常組和模型對照組大鼠均尾靜脈注射5ml/kg生理鹽水,saa組每天尾靜脈注射saa1mg/kg,連續(xù)4周。試驗期間,除正常組飼喂普通飼料外,其余各組高脂飼喂,并于給藥前和給藥2周時分別注射10萬iu/kgvd3。
1.3westernblot
按照蛋白提取試劑盒和定量試劑盒的操作說明提取主動脈總蛋白并進(jìn)行定量。將已定量的總蛋白樣品,電泳、轉(zhuǎn)膜和封閉,nc膜與合適稀釋度的一抗在37℃孵育1h后,4℃放置48h,tbs洗后與二抗37℃孵育1h,tbs洗后,將nc膜放至odyssey紅外熒光掃描儀上進(jìn)行掃描,分析蛋白條帶,計算灰度值。
(2)實驗結(jié)果:與正常組比較,模型組lp-pla2蛋白表達(dá)量顯著升高,有統(tǒng)計學(xué)差異(p<0.05)。與模型組相比,saa給藥組lp-pla2蛋白表達(dá)量顯著降低(p<0.05)。結(jié)果詳見圖3。
實施例4:丹酚酸a對人胰腺癌bxpc3移植瘤裸鼠lp-pla2、cpla2、spla2表達(dá)的影響。
材料:丹酚酸a,人胰腺癌bxpc3細(xì)胞,小鼠lp-pla2elisa檢測試劑盒,小鼠cpla2elisa檢測試劑盒,小鼠spla2elisa檢測試劑盒。
實驗動物:spf級balb/c-nu/nu裸鼠,雄性,4-5周齡。
(1)實驗方法
1.模型建立和分組給藥
1.1細(xì)胞培養(yǎng)
bxpc3細(xì)胞以rpmi1640完全培養(yǎng)液(含10%胎牛血清和100u/ml青霉素和100mg/ml鏈霉素)于37℃,5%co2培養(yǎng)箱傳代培養(yǎng)。收集對數(shù)生長期細(xì)胞接種。細(xì)胞以pbs清洗2-3次,生理鹽水重懸,臺盼蘭拒染法計數(shù)活細(xì)胞,調(diào)整細(xì)胞濃度至2.5×107/ml,細(xì)胞懸液放置于冰上,接種過程在細(xì)胞懸液制備后1小時內(nèi)完成。
1.2分組和處理
每只裸鼠頸背皮下接種上述腫瘤細(xì)胞懸液,以游標(biāo)卡尺每天測量裸小鼠的腫瘤直徑,待每只小鼠的腫瘤均長至100-150mm3后按體重和瘤體積進(jìn)行隨機(jī)分為3組,模型對照組、saa-1給藥組、saa-2給藥組,各5只。saa-1給藥組每天一次瘤內(nèi)注射給予2mg/kg的saa,saa-2給藥組每天一次尾靜脈注射給予2mg/kg的saa,連續(xù)給藥21天。
2.lp-pla2、cpla2、spla2含量測定
采用elisa法測定大鼠瘤組織、瘤旁組織和血清中l(wèi)p-pla2、cpla2、spla2含量。操作步驟按照試劑盒說明進(jìn)行。
實驗結(jié)果:與對照組比較,saa-1組和saa-2組大鼠瘤組織、瘤旁組織和血清中l(wèi)p-pla2、cpla2、spla2含量均顯著下降(p<0.01,p<0.05)。saa-1和saa-2組之間無顯著性差異(p>0.05)。結(jié)果詳見圖4。
實施例5:丹酚酸a對人胰腺癌bxpc3裸鼠移植瘤生長的抑制作用。
材料:丹酚酸a,人胰腺癌bxpc3細(xì)胞。
實驗動物:spf級balb/c-nu/nu裸鼠,雄性,4-5周齡。
(1)實驗方法
1.模型建立和分組給藥
1.1細(xì)胞培養(yǎng)
bxpc3細(xì)胞以rpmi1640完全培養(yǎng)液(含10%胎牛血清和100u/ml青霉素和100mg/ml鏈霉素)于37℃,5%co2培養(yǎng)箱傳代培養(yǎng)。收集對數(shù)生長期細(xì)胞接種。細(xì)胞以pbs清洗2-3次,生理鹽水重懸,臺盼蘭拒染法計數(shù)活細(xì)胞,調(diào)整細(xì)胞濃度至2.5×107/ml,細(xì)胞懸液放置于冰上,接種過程在細(xì)胞懸液制備后1小時內(nèi)完成。
1.2分組和處理
每只裸鼠頸背皮下接種上述腫瘤細(xì)胞懸液,以游標(biāo)卡尺每天測量裸小鼠的腫瘤直徑,待每只小鼠的腫瘤均長至100-150mm3后按體重和瘤體積進(jìn)行隨機(jī)分為2組,模型對照組和丹酚酸a(saa)組,各5只。saa組每天一次瘤內(nèi)注射給予2mg/kg的saa,連續(xù)給藥21天。
2.結(jié)果觀察
每3天各組裸鼠稱重,并用游標(biāo)卡尺測量每只裸鼠移植瘤的瘤結(jié)節(jié)最大直徑a和最小徑b,計算瘤體積(v),計算公式為:v=1/2×a×b2。根據(jù)瘤體積繪制移植瘤生長曲線。
實驗結(jié)果:給藥3~21d后,saa組裸鼠移植瘤體積均顯著或極顯著小于模型對照組(p<0.01,p<0.05)。結(jié)果詳見圖5。
實施例6:丹酚酸a對zdf大鼠血清中l(wèi)p-pla2含量的影響
材料:丹酚酸a、大鼠血小板活化因子乙酰水解酶分析試劑盒。
實驗動物:spf級zdf大鼠,7~8周齡,雄性;spf級瘦型zl大鼠,7~8周齡,雄性。
飼料:purina#5008營養(yǎng)組分:蛋白質(zhì)23.75%、總脂肪7.55%、粗纖維4.00%、消化能14.6兆焦/千克。
(1)實驗方法
1.模型建立和分組給藥
7-8周齡雄性zdf大鼠32只,飼喂purina#5008飼料,另取8只同周齡zl大鼠飼喂基礎(chǔ)飼料,作為正常對照組。4周后,將zdf大鼠根據(jù)glu、tc及體重,分為4組,即模型對照組、丹酚酸a(saa)低、中、高劑量組,每組8只。zdf大鼠2只一籠,zl大鼠4只一籠。saa低、中、高劑量組zdf大鼠每天分別尾靜脈注射saa0.25mg·kg-1、0.5mg·kg-1、1mg·kg-1,模型對照組和正常對照組每天給予5ml·kg-1生理鹽水,連續(xù)給藥12周。
2.血清中l(wèi)p-pla2活性測定
使用elisa試劑盒檢測給藥前與給藥4、8、12周時血清中l(wèi)p-pla2活性,具體方法按pafacetylhydrolaseassaykit試劑盒說明書進(jìn)行,根據(jù)說明書提供的公式計算各樣本的lp-pla2活性。結(jié)果以每分鐘每升血漿水解paf的微摩爾數(shù)表示lp-pla2活性(μmol/min/l)。
(2)實驗結(jié)果:與正常對照組相比,模型對照組lp-pla2活性均顯著升高(p<0.01);在給藥4、8、12周時saa高劑量組的lp-pla2活性均極顯著低于模型對照組(p<0.01),而給藥12周時saa中劑量組的lp-pla2活性也顯著低于模型對照組(p<0.05)。結(jié)果詳見表2。
表2saa對zdf大鼠lp-pla2活性的影響(
注:與正常組比較,**p<0.01;與模型組比較,#p<0.05,##p<0.01。
實施例7:丹酚酸a對zdf大鼠組織中l(wèi)p-pla2mrna表達(dá)的影響
材料:丹酚酸a、逆轉(zhuǎn)錄試劑盒、熒光定量試劑盒、總rna提取試劑盒。
實驗動物:spf級zdf大鼠,7~8周齡,雄性;spf級瘦型zl大鼠,7~8周齡,雄性。
飼料:purina#5008營養(yǎng)組分:蛋白質(zhì)23.75%、總脂肪7.55%、粗纖維4.00%、消化能14.6兆焦/千克。
(1)實驗方法
1.模型建立和分組給藥
7-8周齡雄性zdf大鼠24只,飼喂purina#5008飼料,另取8只同周齡zl大鼠飼喂基礎(chǔ)飼料,作為正常對照組。4周后,將zdf大鼠根據(jù)glu、tc及體重,分為3組,即模型對照組、丹酚酸a(saa)0.5mg·kg-1、saa1mg·kg-1給藥組,每組8只。zdf大鼠2只一籠,zl大鼠4只一籠。saa給藥組zdf大鼠每天分別尾靜脈注射saa0.5mg·kg-1、1mg·kg-1,模型對照組和正常對照組每天給予5ml·kg-1生理鹽水,連續(xù)給藥12周。
2.熒光定量pcr
用總rna提取試劑盒提取大鼠腎、肝組織總rna,按產(chǎn)品說明書進(jìn)行操作。按逆轉(zhuǎn)錄試劑盒說明書操作步驟合成cdna,選取gapdh為內(nèi)參基因,大鼠gapdh和lp-pla2mrna引物序列如下表。按照熒光定量試劑盒操作步驟,將cdna用實時熒光定量pcr儀進(jìn)行擴(kuò)增,反應(yīng)操作在冰上進(jìn)行。表3實時熒光定量pcr引物序列
(2)實驗結(jié)果:與正常對照組相比,模型對照組腎、肝組織lp-pla2mrna表達(dá)量均顯著升高(p<0.05);與模型對照組比,saa各組的腎組織中l(wèi)p-pla2mrna的表達(dá)顯著下降(p<0.05),肝組織中l(wèi)p-pla2mrna的表達(dá)有下降趨勢(p>0.05)。結(jié)果詳見圖6。
實施例8:丹酚酸a對zdf大鼠組織中l(wèi)p-pla2蛋白表達(dá)的影響
材料:丹酚酸a、lp-pla2抗體。
實驗動物:spf級zdf大鼠,7~8周齡,雄性;spf級瘦型zl大鼠,7~8周齡,雄性。
飼料:purina#5008營養(yǎng)組分:蛋白質(zhì)23.75%、總脂肪7.55%、粗纖維4.00%、消化能14.6兆焦/千克。
(1)實驗方法
1.模型建立和分組給藥
7-8周齡雄性zdf大鼠16只,飼喂purina#5008飼料,另取8只同周齡zl大鼠飼喂基礎(chǔ)飼料,作為正常對照組。4周后,將zdf大鼠根據(jù)glu、tc及體重,分為2組,即模型對照組、丹酚酸a(saa)1mg·kg-1給藥組,每組8只。zdf大鼠2只一籠,zl大鼠4只一籠。saa給藥組zdf大鼠每天分別尾靜脈注射saa1mg·kg-1,模型對照組和正常對照組每天給予5ml·kg-1生理鹽水,連續(xù)給藥12周。
2.westernblot
按照蛋白提取試劑盒和定量試劑盒的操作說明提取主動脈總蛋白并進(jìn)行定量。將已定量的總蛋白樣品,電泳、轉(zhuǎn)膜和封閉,nc膜與合適稀釋度的一抗在37℃孵育1h后,4℃放置48h,tbs洗后與二抗37℃孵育1h,tbs洗后,將nc膜放至odyssey紅外熒光掃描儀上進(jìn)行掃描,分析蛋白條帶,計算灰度值。
(2)實驗結(jié)果:與正常對照組相比,模型對照組腦、腎組織lp-pla2蛋白表達(dá)量均顯著升高(p<0.05);與模型對照組比,saa給藥組腦、腎組織中l(wèi)p-pla2蛋白的表達(dá)有下降趨勢(p>0.05)。結(jié)果詳見圖7。
以上所述僅為本發(fā)明的較佳實施例,并不用以限制本發(fā)明,凡在本發(fā)明的精神和原則之內(nèi)所作的任何修改、等同替換和改進(jìn)等,均包含在本發(fā)明的保護(hù)范圍之內(nèi)。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 人Lp-PLA2生物素-鏈霉親和素?zé)晒饷庖邔游鰴z測卡及其制備方法
- 一種硒蛋白磷脂保健品及其制備方法
- 一種脂蛋白磷脂酶a2測定試劑盒及其使用方法
- 一種重組華支睪吸蟲分泌型磷脂酶a2蛋白及其體外可溶性表達(dá)與純化制備方法
- 脂蛋白相關(guān)磷脂酶a2單克隆抗體、抗體對及制備方法、用圖
- 一種與咪唑乙煙酸抗性相關(guān)蛋白bm-1及其編碼基因與應(yīng)用
- 一種磷脂膠原蛋白豆?jié){粉的制作方法
- 油菜抗旱及ABA耐受相關(guān)的蛋白BnSIP1的基因及其應(yīng)用
- 玉米分泌型磷脂酶A2基因ZmsPLA2-2在改變植物抗旱性中的應(yīng)用
- 脂蛋白磷脂酶A2(Lp-PLA2)免疫熒光探針檢測試劑盒的制作方法
- 自然酶活性脂蛋白相關(guān)磷脂酶a2及制備過程的制作方法
- 脂蛋白磷脂酶a2免疫層析定量檢測試紙條的制作方法
- 一種檢測脂蛋白磷脂酶a2濃度的試劑盒及其制備方法
- 含脂蛋白相關(guān)性磷脂酶a2抑制劑的藥物組合物及應(yīng)用
- 一種定量檢測樣本中脂蛋白磷脂酶a2濃度的液態(tài)芯片試劑盒及其制備方法
- 用于檢測脂蛋白相關(guān)磷脂酶a2的試劑盒及其制備和應(yīng)用
- 同時測定血漿中脂蛋白磷脂酶a2和c反應(yīng)蛋白的層析法快速檢測卡及試劑盒的制作方法
- 血漿脂蛋白磷脂酶a2的時間分辨熒光免疫檢測方法及試劑盒的制作方法
- 一種同時測定血漿中脂蛋白磷脂酶a2與c反應(yīng)蛋白含量的檢測方法及試劑盒的制作方法
- 血漿脂蛋白磷脂酶a2活性檢測試劑盒及其檢測方法
- 含脂蛋白相關(guān)性磷脂酶a2抑制劑的藥物組合物及應(yīng)用
- 一種定量檢測樣本中脂蛋白磷脂酶a2濃度的液態(tài)芯片試劑盒及其制備方法
- 用于檢測脂蛋白相關(guān)磷脂酶a2的試劑盒及其制備和應(yīng)用
- 同時測定血漿中脂蛋白磷脂酶a2和c反應(yīng)蛋白的層析法快速檢測卡及試劑盒的制作方法
- 血漿脂蛋白磷脂酶a2的時間分辨熒光免疫檢測方法及試劑盒的制作方法
- 一種同時測定血漿中脂蛋白磷脂酶a2與c反應(yīng)蛋白含量的檢測方法及試劑盒的制作方法
- 血漿脂蛋白磷脂酶a2活性檢測試劑盒及其檢測方法
- 一種脂蛋白相關(guān)磷脂酶a2酶聯(lián)免疫檢測試劑盒及制備方法
- 一種人血漿脂蛋白磷脂酶免疫層析試紙條的制作方法
- 脂蛋白相關(guān)磷脂酶a2定量檢測試劑盒及制備、操作方法