CpG復合佐劑在MUC1融合蛋白抗腫瘤中的用途的制作方法
技術領域:
本發明提供一種cpg復合佐劑在muc1融合蛋白抗腫瘤中的用途,涉及cpg-odn2006與mf59聯合作為免疫佐劑在重組muc1-mbp融合蛋白抗腫瘤中的醫用用途,屬于免疫學治療領域。
背景技術:
:
cpg-odn是人工合成的含有非甲基化胞嘧啶鳥嘌呤二核苷酸(cpg)的寡脫氧核苷酸(odn),可模擬細菌dna刺激b細胞、樹突狀細胞活化,間接激活nk和t細胞等多種免疫效應細胞,增強抗原提呈細胞的加工和提呈,誘導th1型免疫應答,產生較強的體液免疫和細胞免疫應答,可用于腫瘤治療、過敏性疾病、感染性疾病、免疫功能低下者。目前公認的對人免疫刺激活性最強是cpg-odn2006。國外已經對cpg-odn2006進行了多項臨床試驗,包括對黑色素瘤、肺小細胞癌、皮膚t細胞淋巴瘤,證實是高效低毒的新型免疫佐劑。國內沃森生物將cpg-odn作為乙型肝炎疫苗佐劑,目前正在進行臨床iii期實驗,而國內目前尚未發現用于腫瘤疫苗佐劑的報道。
mf59是將span85(0.5%,v/v),tween80(0.5%,v/v),角鯊烯(4.3%,v/v)混和乳化制得的水包油乳劑,1997年作為流感疫苗佐劑在歐盟獲批上市。因其誘導體液免疫反應的效果更好,常被用于人類流感疫苗。但近年,已有研究者通過向疫苗制劑中添加病原相關分子模式(pamp)的模擬物來改變mf59的免疫特點,并證實mf59聯合其它佐劑確實可以通過某些機制向利于腫瘤免疫的th1方向發展。這為mf59在其他領域存在潛在應用價值提供了一定的理論基礎。
muc1是mucins粘蛋白家族的重要成員,存在于正常腺管上皮細胞及其來源的腫瘤細胞表面,由多肽核芯(核芯肽)和側枝糖鏈構成。由于正常組織muc1與腫瘤組織不同,使其成為免疫細胞攻擊的靶點。經反復動物實驗以及部分人體實驗研究證實,muc1是腫瘤疫苗研制的有效靶點。目前以muc1為靶點研制的腫瘤疫苗,49個處于臨床試驗階段,其中,tg4010和tecemotide也已經完成iii期臨床并取得良好的結果。本研究組長期以來以muc1為靶點,首次通過基因工程技術將muc1基因與大腸桿菌麥芽糖結合蛋白偶聯制成重組muc1-mbp融合蛋白。研究發現重組muc1-mbp融合蛋白單獨免疫小鼠,很難產生強烈的細胞免疫應答;而與cpg-odn2006聯合免疫,既能產生特異性體液免疫應答,又能產生的細胞免疫應答;尤其是當cpg-odn2006與mf59聯合后,能更加顯著協同增強重組muc1-mbp融合蛋白誘導的特異性細胞免疫應答,發揮更加顯著的抗腫瘤作用。
技術實現要素:
:
本發明提供了一種cpg復合佐劑在muc1融合蛋白抗腫瘤中的用途,用于人類治療或預防腫瘤。
所述的cpg復合佐劑為cpg-odn與mf59聯合復合佐劑,其中,cpg-odn2006,序列是:5'-tcgtcgttttgtcgttttgtcgtt-3',也稱cpg-odn7909,是一種非甲基化胞嘧啶鳥嘌呤二核苷酸為核心的序列。mf59是將span85(0.5%,v/v),tween80(0.5%,v/v),角鯊烯(4.3%,v/v)混和乳化制得的水包油乳劑。
本發明涉及cpg-odn2006與mf59以及muc1-mbp聯合適用于下述醫療用途:
1.cpg-odn2006與mf59作為重組muc1-mbp融合蛋白佐劑,三者聯合作為治療性疫苗,治療癌癥包括表達muc1的腺癌、肝癌、血液腫瘤等。
2.cpg-odn2006與mf59作為重組muc1-mbp融合蛋白佐劑,三者聯合作為預防性疫苗,應用于各種表達muc1的各種癌癥的預防,包括表達muc1的腺癌、肝癌、血液腫瘤等。
本發明所述的cpg-odn2006與mf59復合佐劑的制備工藝,包括以下步驟:
1、將span85、tween80、角鯊烯和10nm檸檬酸鈉分別按照體積比0.5%、0.5%、4.3%和94.7%進行混合,用乳化機乳化10min,變成乳白色勻質狀,制成mf59乳劑;
2、采用冷凍離心機離心,6000rpm離心5min不發生分層,即達到乳化標準.
3、經0.22μm濾膜過濾除菌,備用;
4、將cpg-odn2006按照2mg/ml溶于水中,與mf59乳劑按照1:2體積比進行混合制成復合佐劑。
通過研究實驗表明,本發明cpg-odn2006與mf59與muc1-mbp融合蛋白不僅協同刺激誘導muc1特異性體液免疫應答,而且能顯著協同誘導muc1特異性細胞免疫應答,并具有顯著的抗腫瘤作用。因此,cpg-odn2006與mf59與muc1-mbp三者聯用可作為癌癥疫苗開發應用于臨床免疫治療和預防領域。
本發明的積極效果在于:以cpg-odn2006與mf59作為聯合佐劑,利用它們的聯合協同增強重組muc1-mbp誘導muc1特異性抗體應答和t細胞免疫應答,協同誘導顯著地抑制腫瘤的效果,cpg-odn2006與mf59聯合重組muc1-mbp融合蛋白可作為疫苗用于表達muc1的腫瘤包括腺癌、血液腫瘤等治療或預防的用途;cpg-odn2006與mf59聯合可制成重組muc1-mbp疫苗的佐劑。
附圖說明
圖1為重組muc-mbp的sds-page分析電泳圖;
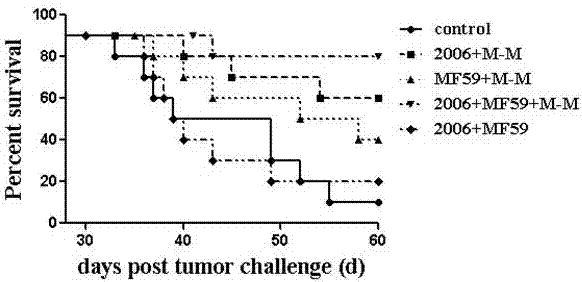
圖2為不同佐劑聯合對muc1-mbp誘導的荷瘤小鼠生存期的影響曲線圖。
具體實施方式
通過以下實施例進一步舉例描述本發明,并不以任何方式限制本發明,在不背離本發明的技術解決方案的前提下,對本發明所作的本領域普通技術人員容易實現的任何改動或改變都將落入本發明的權利要求范圍之內。
實施例1
cpg-odn2006與mf59復合佐劑的制備工藝,包括以下步驟:
將0.5mlspan85、0.5mltween80和4.3ml角鯊烯加入10nm檸檬酸鈉94.7ml中,用乳化機乳化10min,變成乳白色勻質狀,制成mf59乳劑。采用冷凍離心機離心,6000rpm離心5min不發生分層,即達到乳化標準。經0.22μm濾膜過濾除菌,備用。將cpg-odn2006按照2mg/ml溶于水中,與mf59乳劑按照1:2體積比進行混合制成復合佐劑。
實施例2
cpg-odn2006與mf59復合佐劑聯合muc1-mbp融合蛋白疫苗的制備工藝,包括以下步驟:
重組muc1-mbp融合蛋白(純度98%,內度素小于5eu/mg)參見重組人muc1-mbp融合蛋白抗腫瘤疫苗及生產工藝,(專利號zl03111045.2)制備;按照實施例1中的方法制備cpg-odn2006與mf59復合佐劑;將muc1-mbp融合蛋白與復合佐劑按照1:3體積的比例混合制成疫苗。
實驗例1
1.材料
重組muc1-mbp融合蛋白(純度98%,內度素小于5eu/mg)參見重組人muc1-mbp融合蛋白抗腫瘤疫苗及生產工藝,(專利號zl03111045.2)制備,丙烯酰胺和tris購自sigma公司,亞甲丙烯酰胺購自上海生物工程公司,bsa購自碧云天生物科技有限公司。
2.方法
2.1重組muc1-mbp純度分析
將重組muc1-mbp融合蛋白10μl加入10%分離膠和4%濃縮膠sds-page凝膠上樣孔中,并采用低分子量蛋白marker作為對照,在10-20ma下進行電泳,結束后采用考馬斯亮藍進行顏色分析。
2.2重組muc1-mbp含量分析
將重組muc1-mbp融合蛋白稀釋成6個稀釋度,按照bca試劑盒說明書進行操作,配制蛋白標準品,采用酶標儀檢測吸光光度值a490nm。
3.結果
3.1重組muc1-mbp的鑒定
將本研究組制備的重組muc-mbp通過sds-page分析,如圖1所示,在62kd處可見一條較純的條帶,通過分析結果表明,電泳純度為100%.結果與預期一致,可用于后續的實驗研究。
3.2重組muc1-mbp的含量分析
經bca試劑盒分析結果表明1.15mg/ml,與實際值1.2mg/ml相比較,結果基本一致,占實測值95.8%,在質量控制90-110%的范圍內,可用于后續的實驗。
實驗例2
1.材料
cpg-odn2006由上海生工合成(lot:9405454467);30個氨基酸muc1多肽(純度95%)由上海紫域生物,bcg購自成都生物制品所,抗igg1-hrp、抗igg2c-hrp和抗igg-hrp購自southernbiotech。span85和tween80購自genview,角鯊烯購自tci。
6~8周齡,18~20gc57bl/690只小鼠購自北京華阜康生物科技有限公司。
2.方法
2.1小鼠免疫
將小鼠稱重,隨機分為9組,每組10只鼠,雌雄各半,分別為生理鹽水組,cpg-odn2006(0.25mg/kg),cpg-odn2006(0.25mg/kg)+mf59組,muc1-mbp(0.25mg/kg)組,cpg-odn2006(0.25mg/kg)+muc1-mbp(0.25mg/kg)組,cpg-odn2006(0.5mg/kg)+mf59+muc1-mbp(0.25mg/kg)組,cpg-odn2006(0.25mg/kg)+al(oh)3+muc1-mbp(0.25mg/kg),cpg-odn2006(0.25mg/kg)+bcg(15mg/kg)+muc1-mbp(0.25mg/kg)組。皮下多點注射,每2周免疫一次,共免疫2次。
2.2elisa檢測muc1特異抗體及亞類
如上所述,小鼠第2次免疫后4-7天安樂死處死小鼠,眼球采血,常溫靜置4小時后,4℃離心,3000rpm,10min,分離小鼠血清,通過間接elisa分析抗muc1抗體的效價。簡而言之,采用0.5μg/wellmuc1多肽包被96孔板,4℃過夜,次日,通過3%bsa封閉液封閉1h,采用0.5‰tween-20的pbs(pbs-t)液洗滌后,加入小鼠不同稀釋度的血清,均設雙復孔,37℃孵育0.5-1.5h,棄去孔內液體,pbs-t洗液5-7次后,加入hrp標記山羊抗小鼠igg或igg2c或igg1(按說明書稀釋),37℃孵育0.5-1.5h,棄去孔內液體,pbs-t洗液5-7次后加入底物opd顯色5-10min,加2mol/l硫酸溶液終止反應,采用酶標儀檢測a490吸光光度值。
3.結果
為研究muc1-mbp疫苗誘導小鼠產生特異性體液免疫應答情況,在小鼠末次免疫后眼球采血,分離血清,采用間接elisa檢測muc1特異性抗體及亞類。如表1結果所示,生理鹽水對照組、cpg-odn2006以及cpg-odn2006+mf59各組均未見muc1特異性抗體產生;muc1-mbp單獨免疫組小鼠產生較微量的抗muc1igg,igg2c以及igg1抗體;cpg-odn2006聯合muc1-mbp組,muc1特異性抗體igg,igg2c以及igg1均明顯較單獨muc1-mbp組增高;mf59聯合muc1-mbp組,muc1特異性抗體igg和igg1效價較muc1-mbp單獨用略有增加,但igg2c未見明顯增加。當cpg-odn2006、mf59以及muc1-mbp聯合后,三者聯用比muc1-mbp與cpg-odn2006二者聯用更加顯著提高了muc1特異性抗體igg,igg2c以及igg1的效價,而且以igg2c增加的幅度最高;當muc1-mbp聯合cpg-odn2006與al(oh)3或bcg三者聯用,與二者聯用比較均未見muc1特異性抗體igg,igg2c以及igg1有明顯提高。上述結果提示cpg-odn2006與muc1-mbp二者聯用能協同促進muc1特異性抗體應答的產生,cpg-odn2006和mf-59與muc1-mbp三者聯用更加顯著協同誘導muc1特異性體液免疫應答,誘導產生較高水平的igg2c,間接提示cpg-odn2006或cpg-odn2006聯合mf59不僅促進muc1-mbp疫苗產生th2應答,同時也產生th1應答。而muc1-mbp與mf-59二者聯用只能產生較低水平的抗體應答;cpg-odn2006與muc1-mbp聯合后再加入al(oh)3或bcg,muc1特異性抗體應答并未見明顯提升。
表1cpg-odn2006、mf59以及muc-mbp三者協同促進產生muc1特異性抗體igg、igg2c和igg1
4.結論
cpg-odn2006、mf-59與muc1-mbp三者聯合比cpg-odn2006與muc1-mbp二者聯合更加顯著協同誘導muc1特異性體液免疫應答,誘導產生較高水平的igg2c,可作為優良的腫瘤疫苗開發利用。
實驗例3
1.材料
小鼠淋巴細胞分層液購自索萊寶公司,il-2購自protech30個氨基酸muc1多肽(純度95%)由上海紫域生物,胎牛血清購自biobio、imdm購自gibco,wst試劑購自promega,il-4以及ifn-γelesa試劑盒均購自于ebioscience公司。
2.方法
2.1muc1特異性淋巴細胞分泌細胞因子分析
如上所述,在第4次免疫后4-7天殺鼠,無菌取脾、研磨、細胞記數,制備脾細胞懸液,采用小鼠淋巴細胞分層液分離小鼠脾臟單個核細胞,用imdm調整細胞濃度至1×107/ml,以100μl/well加入96孔板中。實驗設3組,每組設3復孔,分別為陰性對照組、il-2單獨刺激組(終濃度100u/ml)、muc1多肽刺激組(muc1多肽10μg/ml+il-2100u/ml)。37℃的co2培養箱3天,半量換液,繼續培養5天后,吸取每孔細胞培養上清100μl用于細胞因子的檢測。通過夾心elisa檢測ifn-γ和il-4的分泌水平。按照ebioscience公司的elisa檢測試劑盒說明書進行操作。簡而言之,首先將包被抗體(抗ifn-γ和il-4的抗體)包被96孔酶標板,每個樣本設雙復孔,4℃過夜。采用pbs-0.05%tween-20洗板5次,加入封閉液封閉1h后,洗滌2次,加入標準品(ifn-γ:2000、1000、500、250、125、62.5、32.5、15.625pg/ml;il-4標準品配制:500、250、125、62.5、32.5、15.6、7.8、3.9pg/ml)和樣品,100μl/孔,4℃過夜。洗滌5次后,加入檢測抗體室溫孵育1h,洗滌5次,加入酶標抗體avindin-hrp,室溫孵育30min。洗7次,加tmb,室溫15min。加硫酸終止后,采用酶標儀450nm波長測定吸光度值波長450nm。
3.結果
3.1cpg-odn與mf59以及muc1-mbp協同促進muc1特異性淋巴細胞分泌ifn-γ水平
為研究muc1-mbp疫苗誘導小鼠產生特異性細胞免疫應答情況,在小鼠第4次免疫后取脾,分離淋巴細胞,采用il-2加muc1多肽特異性刺激淋巴細胞5天后,取細胞培養上清,通過雙抗體夾心elisa檢測ifn-γ和il-4分泌水平。將體外muc1多肽聯合il-2刺激所得的數值減去il-2單獨刺激的數值即得到muc1特異性th1釋放的細胞因子。如表2結果所示,cpg-odn2006組和cpg-2006+mf59組,均能產生較低水平的ifn-γ,cpg-odn2006聯合muc1-mbp組,muc1特異性t細胞釋放ifn-γ水平明顯增高,在muc1-mbp聯合cpg-odn2006聯合基礎上,加入mf59后,ifn-γ水平增高更加明顯;加入al(oh)3后,ifn-γ水平略有下調,加入bcg后,ifn-γ水平也明顯上升,但各鼠之間差異較大。同時,各組il-4的水平也不同程度增加。結果提示cpg-odn2006與muc1-mbp二者聯合協同促進muc1特異性th1應答和th2應答,cpg-odn2006與mf59以及muc1-mbp三者聯合協同刺激產生更高水平的muc1特異性th1應答。
表2各組小鼠免疫后muc1特異性淋巴細胞分泌細胞因子(n=10,
其中,a,b:p<0.05,與對照組比較;c,p<0.01,與cpg-2006組比較;d:p<0.01,與muc1-mbp組比較;e,f:p<0.01,與muc1-mbp+cpg-2006
4.結論
cpg-odn2006與mf59以及muc1-mbp三者具有顯著的協同誘導產生產生muc1特異th1應答的作用,提示三者可作為良好的癌癥疫苗開發利用。
實驗例4
1.材料
g418,胎牛血清購自biobio、imdm購自gibco。
動物c57bl/6小鼠,18-20克購自北京華阜康生物公司
細胞b16-muc1細胞系是穩定轉染人全長muc1的小鼠b16黑色素瘤細胞。用含g418(終濃度為600μg/ml),青、鏈霉素(100u/ml)及10%新生牛血清的imdm培養液培養b16-muc1細胞,用流式細胞儀鑒定muc1蛋白的表達,結果顯示b16-muc1細胞muc1的表達率在97.8%以上可用于腫瘤模型的構建。
2.方法
2.1小鼠分組及免疫
c57bl/6小鼠,18-20克50只,隨機分5組,分別為生理鹽水組(ns)cpg-odn2006+mf59+muc1-mbp組,cpgodn2006+muc1-mbp組,mf59+muc1-mbp組,cpg-odn2006+mf59組。每組10只鼠,雌雄各半。首先,給小鼠背部右脅皮下接種b16-muc1細胞,1×106個/只。然后,在腫瘤接種后的7天可觸及小米粒大小腫瘤后,頸背部皮下多點注射免疫,每7天免疫一次,共免疫三次。觀察小鼠的一般狀態,小鼠成瘤情況,記錄小鼠的死亡時間,繪制生存曲線。
3.結果
3.1重組muc1-mbp融合蛋白的抗腫瘤作用
如圖2所示:不同佐劑聯合對muc1-mbp誘導的荷瘤小鼠生存期的影響曲線圖(m-m:muc1-mbp;2006:cpg-odn-2006;ns:生理鹽水),小鼠注射腫瘤細胞后一周,可觸及小米粒大小的腫塊。此后,經cpg-2006與mf59以及muc1-mbp三者聯合組免疫組小鼠腫瘤生長最慢,其次是cpg-2006與muc1-mbp二者聯合組,mf59與muc1-mbp二者聯合組.在腫瘤注射后60天,上述三組小鼠生存率分別為80%,60%和40%;而生理鹽水組與cpg-2006與mf59聯合組小鼠腫瘤生長迅速,在腫瘤注射后60天生存率分別為10%和20%。上述結果提示,cpg-2006與mf59以及muc1-mbp三者聯合組,cpg-odn2006與muc1-mbp二者聯合組,mf59與muc1-mbp二者聯合組均能延長荷瘤小鼠的生存期,尤其以muc1-mbp與cpg-2006以及mf59三者聯合效果最佳。
4.結論
muc1-mbp與cpg-2006二者聯合,muc1-mbp與cpg-2006和mf59三者聯合均明顯延長荷瘤小鼠生存期,尤其以三者聯合最為顯著。因此,muc1-mbp與cpg-2006和mf59三者聯合可作為良好的疫苗開發利用。
- 還沒有人留言評論。精彩留言會獲得點贊!