鐵素體合金的制作方法
本公開涉及根據權利要求1的前序部分的鐵素體合金(fecral合金)。本公開還涉及根據權利要求16的鐵素體合金的用途,其在300-800℃的溫度范圍內使用。
背景技術:
在所謂的鉛冷快堆(lfr)系統中,使用液態鉛作為冷卻劑。液態鉛和鉛鉍低共熔物(lbe)提供被動冷卻的可能性,并因此有助于使核能安全。然而,液態鉛具有高度腐蝕性,并對在lfr系統中使用的建造材料的耐腐蝕性提出高要求。
最近已提出將fecral合金作為候選材料用于鉛冷快堆中,這是由于這些合金的良好的氧化性質,這是在合金表面上形成氧化鋁(al2o3)層的結果。fecral合金基于鋁、鉻和鐵,并且由于它們的抗氧化性和良好的抗蠕變性,這些合金常用于溫度在1000℃左右和超過1000℃的加熱元件和加熱線中。然而,鉛冷快堆在400-600℃的溫度區間中運轉,并且在這個溫度范圍內,通常含有15-20wt%左右的cr的商購fecral合金,由于所述fe-cr系統中存在的混溶間隙而遭受α-α’相分離困擾。所述α-α’相分離引起所述fecral合金脆化,這使所述商購fecral合金不適合在lfr系統中使用的溫度范圍內作為建造材料。
已在液態鉛或液態鉛-鉍-低共熔溶液中測試了fecral組合物。在weisenburger等人的研究中顯示,含有≥12.5wt%cr和≥6wt%al的模型fecral合金能夠在400-600℃的溫度區間內形成薄的保護性氧化鋁垢[weisenburger,jianu,doyle,bruns,fetzer,heinzel,delgiacco,an,müller,“在暴露于含有氧的熔融鉛的基于fe-cr-al的模型合金上形成的氧化物垢”(oxidescalesformedonfe-cr-al-basedmodelalloysexposedtooxygencontainingmoltenlead),journalofnuclearmaterials437(2013)282-292]。由lim等人進行的另一項工作顯示,fe-13cr-4al合金能夠從500℃起形成保護性氧化鋁[lim,hwang,kim,“用于鉛或鉛-鉍冷卻的快速反應堆的形成氧化鋁的fecral鋼的設計”(designofaluminaformingfecralsteelsforleadorlead-bismuthcooledfastreactors),journalofnuclearmaterials441(2013)650-660]。
韓國專利kr10-1210531示出了一種旨在用于核能應用的fecral合金。
fecral合金也可以包含反應性元素(re),其是對氧和碳具有高親和性的元素。在約1000℃的高溫下,反應性元素例如y、zr和hf的添加通過平衡金屬離子的向外擴散和氧的向內擴散來改進所述合金的氧化性質,這導致平衡的氧化物生長以及因此氧化物垢中機械應力和/或孔隙度的降低。關于zr和ti的添加對fe-10cr-6al合金在550℃的液態鉛中的長期(10,000h)耐腐蝕性的影響,已進行了研究[ejenstam等,“在550℃下暴露于pb10,000h的fe10cral-re合金的氧化研究”(oxidationstudiesoffe10cral-realloysexposedtopbat550℃for10,000h),journalofnuclearmaterials443(2013)161-170]。
然而,盡管上面公開的研究有助于改進fecral合金的性能,但仍需要進一步提高這些合金的耐腐蝕性。
因此,本公開的一個方面是提供一種具有改進的耐腐蝕性的fecral合金。具體來說,本發明的一個方面是提供一種在300-800℃范圍內的溫度下,在高腐蝕性環境中具有非常好的耐腐蝕性的fecral合金。此外,本發明的另一個方面是提供一種在300-800℃范圍內的溫度下,對液態鉛中的腐蝕具有抗性的fecral合金。本公開的另一方面是提供一種適合在諸如鍋爐、熔爐和產熱和產能設備和工藝的應用中作為建造材料的fecral合金。其他適合的應用包括用于堆焊、噴涂或復合管的材料。具體來說,本發明的一個方面是提供一種適合在300-800℃的溫度范圍下的鉛冷快堆系統中作為建造材料的fecral合金。
發明詳述
因此,本公開涉及一種鐵素體(fecral)合金,其以重量%計包含:
c:0.01–0.1;
n:0.001-0.1;
o:≤0.2;
b:≤0.01;
cr:9–13;
al:2.5–8;
si:≤0.5;
mn:≤0.4;
y:≤2.2;
sc+ce+la:≤0.2;
mo+w:≤4.0;
ti:≤1.7;
zr:≤3.3;
nb:≤3.3;
v:≤1.8;
hf+ta+th:≤6.5;
余量為fe和不可避免的雜質,
其中,使ti+zr+nb+hf+v+ta+th以及c、n和o的量平衡,使得:
其中x是0.5,除非y的含量大于或等于0.01wt%,此時x是0.67。
本公開還涉及一種鐵素體合金,其以重量%計包含:
c:0.01–0.1;
n:0.001-0.1;
o:≤0.2;
b:≤0.01;
cr:9–11.5;
al:2.5–8;
si:≤0.5;
mn:≤0.4;
y:≤2.2;
sc+ce+la:≤0.2;
mo+w:≤4.0;
ti:≤1.7;
zr:≤3.3;
nb:≤3.3;
v:≤1.8;
hf+ta+th:≤6.5;
余量為fe和不可避免的雜質,
其中,使ti+zr+nb+hf+v+ta+th以及c、n和o的量平衡,使得:
其中x是0.5,除非y的含量大于或等于0.01wt%,此時x是0.67。
本公開還涉及一種鐵素體合金,其以重量%計包含:
c:0.01–0.1;
n:0.001-0.1;
o:≤0.2;
b:≤0.01;
cr:9–11;
al:2.5–8;
si:≤0.5;
mn:≤0.4;
y:≤2.2;
sc+ce+la:≤0.2;
mo+w:≤4.0;
ti:≤1.7;
zr:≤3.3;
nb:≤3.3;
v:≤1.8;
hf+ta+th:≤6.5;
余量為fe和不可避免的雜質,
其中,使ti+zr+nb+hf+v+ta+th以及c、n和o的量平衡,使得:
其中x是0.5,除非y的含量大于或等于0.01wt%,此時x是0.67。
本公開還涉及一種鐵素體合金,其以重量%計包含:
c:0.01–0.1;
n:0.001-0.1;
o:≤0.2;
b:≤0.01;
cr:9–13;
al:2.5–8;
si:≤0.5;
mn:≤0.4;
y:≤2.2;
mo+w:≤4.0;
sc:≤0.2;
ti:≤1.7;
zr:≤3.3;
nb:≤3.3;
v:≤1.8;
hf+ta+th:≤6.5;
余量為fe和不可避免的雜質,
其中,使ti+zr+nb+hf+v+ta+th以及c、n和o的量平衡,使得:
其中x是0.5,除非y的含量大于或等于0.01wt%,此時x是0.67。
本公開還涉及一種鐵素體合金,其以重量%計包含:
c:0.01–0.1;
n:0.001-0.1;
o:≤0.2;
b:≤0.01;
cr:9–13;
al:2.5–8;
si:≤0.5;
mn:≤0.4;
y:≤2.2;
mo+w:≤4.0;
ti:≤1.7;
zr:≤3.3;
nb:≤3.3;
v:≤1.8;
hf+ta+th:≤6.5;
余量為fe和不可避免的雜質,
其中,使ti+zr+nb+hf+v+ta+th以及c、n和o的量平衡,使得:
其中x是0.5,除非y的含量大于或等于0.01wt%,此時x是0.67。
本公開的合金還包含鉻和反應性元素例如ti、zr、nb、hf、v、ta和th。所述反應性元素可以單獨地或以任何組合存在于所述合金中。正如將在下面更詳細解釋的,將這些元素添加到所述合金以改善保護性al2o3層的形成或其性質。fecral合金通常含有碳。碳可能是故意添加的,以例如提高強度,或者可能作為例如由生產過程產生的偶然雜質存在于所述合金中。這些反應性元素例如ti、zr、nb、hf、v、ta和th,也是強的碳化物形成劑,即它們對碳的親和性高,因此所述合金中存在的碳將被吸引到鉻或所述反應性元素并形成碳化物。
通過實驗,本發明人令人吃驚地發現,當所述反應性元素的以原子百分數計的量與所述合金中碳的以原子百分數計的量平衡,使得反應性元素與碳之間的商等于或大于1時,fecral合金的抗氧化性得到極大改進。
當在相對于碳來說缺乏反應性元素的合金中進行腐蝕研究時,更容易理解本公開背后的機制。
圖1示意性示出了其中反應性元素與碳的商接近或小于1的fecral合金。
在所述合金鑄造后的固化期間,反應性元素(re)首先在所述合金的本體中形成碳化物和氮化物。
根據本公開,所述反應性元素的以原子百分數計的量與所述合金中碳的以原子百分數計的量平衡,使得可用于形成碳化物的反應性元素與可用的碳之間的商等于或大于1。這導致在上文中或下文中所定義的合金中存在至少等量的可用反應性元素原子和可用碳原子。由于所述反應性元素是所述合金中最強的碳化物形成劑,比鉻和其他合金組成成分更強,因此所有游離碳將被吸引到所述可用的反應性元素并與其形成碳化物。因此,只要可用的反應性元素的含量足夠,合金中將沒有游離的碳留下以形成富鉻碳化物。
其他的積極效應是所述反應性元素的形成的碳化物均勻分布在上文中或下文中所定義的fecral合金的整個本體中,因此通過彌散硬化對所述合金的機械強度有貢獻。
根據上文中或下文中所定義的fecral合金的一個實施方式,可用的反應性元素與碳之間的商大于或等于1,即在所述合金中存在過剩的反應性元素。因此,原因在于一些反應性元素將在保護性al2o3層的形成過程中消耗并有助于提高所述al2o3層與所述合金表面之間的粘附性。通過平衡反應性元素的量使得在它與碳和氮反應后存在過剩的反應性元素,避免了即使是少量的富鉻碳化物的形成。
根據另一個實施方式,對于上文中或下文中所定義的fecral合金來說,最低的商為至少或等于1.1。這個商意味著在形成al2o3層以消耗掉所有游離的碳之后,所述合金中存在至少足夠的反應性元素。
所述反應性元素與碳之間的可能的最高的商由所述反應性元素在所述合金中可能形成的金屬間化合物的穩定性決定。根據本發明的fecral合金的實施方式,最高的商可能為2.3或更低。
反應性元素與碳之間的商也可以為1.1–2.2,例如1.2–2.0。
上文中或下文中所定義的鐵素體合金可以通過常規的鋼鐵制造方法、即所謂的熔體冶金來制造,其包括:在感應爐中熔化,通過在模具中澆鑄對所述熔體進行鋼包精煉,隨后進行熱軋。上文中或下文中所定義的鐵素體合金也可以通過粉末冶金來制造,在這種情況下包括通過粉化生產金屬粉末,將所述粉末壓實,并且隨后進行燒結或熱等靜壓的步驟。
下面將詳細描述上文中或下文中所定義的合金的組成成分。
上文中或下文中所定義的fecral合金中的余量是fe和不可避免的雜質。不可避免的雜質的實例是沒有故意添加,但由于通常作為雜質出現在例如用于制造所述fecral合金的材料中而不能完全避免的元素和化合物。
當在下面的背景、即“元素≤數字”中使用術語“≤”時,本領域技術人員知道所述范圍的下限是0wt%,除非具體陳述了另一個數字。
碳(c)
碳被包含在上文中或下文中所定義的fecral合金中,以通過沉淀硬化提高強度。碳也可能作為由生產過程帶來的不可避免的雜質而存在。為了在所述合金中實現足夠的強度,碳應該以至少0.01wt%的量存在。在過高含量下,碳可能造成材料形成困難和對耐腐蝕性的不利影響。因此,在上文中或下文中所定義的合金中碳的最大量為0.1wt%。例如,碳為0.02–0.09wt%,例如0.02–0.08wt%,例如0.02–0.07wt%,例如0.02–0.06wt%,例如0.02–0.05wt%,例如0.01–0.04wt%。
氮(n)
氮可以被包含在上文中或下文中所定義的fecral合金中,以通過沉淀硬化提高強度。氮也可能作為由生產過程帶來的不可避免的雜質而存在。在過高含量下,氮可能造成材料形成困難并可能對耐腐蝕性有不利影響。因此,在上文中或下文中所定義的fecral合金中氮的最大量為0.1wt%。為了在熔體冶金中實現充分的沉淀硬化,氮應該為至少0.001wt%,氮的適合范圍的實例是例如0.001–0.08wt%,例如0.001–0.05wt%,例如0.001–0.04wt%,例如0.001–0.03wt%,例如0.001–0.02wt%,例如0.001–0.01wt%。在粉末冶金中,氮含量可以為至少0.01wt%。例如,在粉末冶金中,氮為0.01–0.1wt%,例如0.01–0.08wt%。
氧(o)
氧可能作為由生產過程帶來的雜質,以最高0.02wt%、例如最高0.005wt%的量存在于上文中或下文中所定義的鐵素體合金中。
在熔體冶金中,氧可以為0.001–0.08wt%,例如0.001–0.05wt%,例如0.001–0.02wt%。在粉末冶金中,可以故意添加氧以實現沉淀硬化效果。此時上文中或下文中所定義的合金包含最多0.2wt%的氧,例如0.01–0.2wt%的氧,例如0.01–0.1wt%,例如0.01–0.08wt%。
鉻(cr)
鉻通過所謂的第三元素效應,即通過在瞬態氧化階段中氧化鉻的形成,促進在上文中或下文中所定義的合金上形成al2o3層。鉻應該以至少9wt%的量存在于上文中或下文中所定義的合金中。然而,由于上文中或下文中所定義的合金旨在用于300–800℃的溫度范圍內,鉻應該不超過13wt%以便避免fe-cr系統中的混溶間隙,其中在混溶間隙中α-α’相分離引起所述fecral合金的脆化。例如,鉻可以為9–13wt%,例如9–12wt%,例如9–11wt%,例如9-10wt%。根據一個特定實施方式,cr在9-11wt%、例如9至10wt%的范圍內。根據又一個特定實施方式,cr在9至11.5wt%的范圍內。
鋁(al)
鋁是上文中或下文中所定義的合金中的重要元素,因為鋁在高溫下暴露于氧時將形成致密且薄的氧化物al2o3,其將保護下方的合金表面免于進一步氧化。鋁的量應該為至少2.5wt%,以確保形成所述al2o3層并且存在足夠的鋁以在損壞時使所述al2o3層恢復。然而,鋁對合金的成形性具有不利影響,并且在上文中或下文中所定義的合金中鋁的量應該不超過8wt%。例如,鋁可以為3–7wt%,例如3–5wt%,例如3.5–6wt%,例如4至6wt%。
硅(si)
硅可能作為雜質以最多0.5wt%、例如0至0.4wt%的量存在于上文中或下文中所定義的合金中。
錳(mn)
錳可能作為雜質以最多0.4wt%、例如0至0.3wt%的量存在于上文中或下文中所定義的合金中。
釔(y)
釔可以以最高0.8wt%的量添加以提高al2o3層的粘附性,例如最高0.3wt%,例如最高0.1wt%。然而,如果以大于或等于0.01wt%的量向上文中或下文中所定義的鐵素體合金添加釔,則釔氧化物的形成將影響商,且x將為0.67。此外,當使用粉末冶金時,如果添加釔,則釔含量以至少0.01wt%的量存在,以便通過氧化物和/或氮化物實現所需的彌散硬化效果。在彌散硬化的合金中釔的最大量可以高達2.2wt%,例如高達1.2wt%,例如高達1wt%。適合的范圍的實例是:0.01至1.2wt%,0.01至1wt%和0.04至1wt%。
鈧(sc)、鈰(ce)和鑭(la)
鈧、鈰和鑭是可互換的元素,并且可以單獨地或組合地以最多0.2wt%的總量添加,以改善氧化性質、al2o3層的自我恢復或合金與al2o3層之間的粘附性。根據一個特定實施方式,上文中或下文中所定義的鐵素體合金不包含任何添加的sc、ce和la,即故意添加的sc、ce和/或la為0wt%。根據又一個特定實施方式,上文中或下文中所定義的鐵素體合金不包含任何添加的ce和/或la。
鉬(mo)和鎢(w)
鉬和鎢兩者對上文中或下文中所定義的合金的熱強度具有積極效應,并且可以單獨地或組合地以最高4.0wt%、例如0至2.0wt%的量添加。
反應性元素(re)
根據定義,反應性元素與碳、氮和氧具有高反應性。在對碳具有高親和性的意義上,鈦(ti)、鋯(zr)、鈮(nb)、釩(v)、鉿(hf)、鉭(ta)和釷(th)是反應性元素,因此是強的碳化物形成劑。添加這些元素是為了通過平衡金屬離子和氧的擴散來改善上文中或下文中所定義的合金的氧化性質,所述擴散將控制氧化物生長過程的動力學。各反應性元素的最大量主要取決于所述元素形成不利的金屬間相的傾向性。釔通常被認為是反應性元素,但是在單獨的段落中討論的本公開中不是反應性元素,并且也不是商的一部分(除了它將影響數字x應該具有的值之外),因為它不像上面提到的其他反應性元素那樣形成為強的碳化物。
因此,在上文中或下文中所定義的合金中,鈦的最大量為1.7wt%,例如0.02-1.7wt%。在熔體冶金中,鈦的適合的量為0.02–1.3wt%,例如0.02–0.98wt%,例如0.02–0.85wt%,例如0.04–0.75wt%。在粉末冶金中,鈦的適合的量為0.02–1.3wt%,例如0.04–0.75wt%,例如0.05–0.75wt%。
在上文中或下文中所定義的合金中,鋯和鈮的最大量分別為3.3wt%。鋯和鈮的量可以分別為0.04–3.3wt%。在熔體冶金中,鋯可以為0.04–2.4wt%,例如0.04–1.9wt%,例如0.04–1.6wt%,例如0.08–1.4wt%,例如0.1至0.9wt%,例如0.1至0.6wt%。在粉末冶金中,鋯可以為0.04–2.4wt%,例如0.08–1.4wt%,例如0.3–1.4wt%,例如0.1至0.9wt%,例如0.1至0.6。在熔體冶金中,鈮可以為0.04–2.4wt%,例如0.04–1.9wt%,例如0.04–1.6wt%,例如0.08–1.4wt%。在粉末冶金中,鈮可以為0.04-2.4wt%,例如0.08–1.4wt%,例如0.08–1.2wt%。
作為實例,合金可以包含量為0.04–3.1wt%的ti+zr。適合于熔體冶金的合金可以包含量為0.06–2.0wt%、例如0.12–1.7wt%的ti+zr。適用于粉末冶金的合金可以包含量為0.04–2.3wt%、例如0.06-2.0wt%的ti+zr。
其他實例是:
合金可以包含量為0.04–3.1wt%的ti+nb。適合于熔體冶金的合金可以包含量為0.06–2.0wt%、例如0.12–1.7wt%的ti+nb。適合于粉末冶金的合金可以包含量為0.04–2.3wt%、例如0.06–2.0wt%的ti+nb。
合金可以包含量為0.04–4.6wt%的zr+nb。適合于熔體冶金的合金可以包含量為0.08–2.8wt%、例如0.16–2.5wt%的zr+nb。適合于粉末冶金的合金可以包含量為0.04–3.3wt%、例如0.08–2.8wt%的zr+nb。
釩的最大量為1.8wt%。
鉿、鉭和釷是可互換的元素,并且可以單獨地或組合地以最多6.5wt%的總量添加到上文中或下文中所定義的合金。
鐵(fe)和不可避免的雜質構成上文中或下文中所定義的合金中的其余物質。
可用的反應性元素和氧、氮與碳之間的商:
在上文中或下文中所定義的合金中,考慮到在合金制造期間占優勢的條件下熱力學穩定的碳化物類型,將每種反應性元素的量調到與碳的量平衡。
在合金制造期間占優勢的熱力學條件下,所述反應性元素形成下述碳化物:
在某些情況下,反應性元素nb和v也可能形成較低價碳化物:
然而,在制造過程中合金中占優勢的熱力學條件下,這些碳化物具有低的穩定性,因此在所述商中可以被忽略。
此外,除了碳含量之外,所述fecral合金還可能含有氮和/或氧,因此在所述商中也必須考慮這兩種元素。如上所述,氮和氧可能作為雜質存在于所述合金中,或者可能被故意添加以便改善所述fecral合金的性能。例如,當所述fecral合金被用于粉末冶金應用中時,fecral合金中氮和氧的含量可能是大量的。當氮和氧存在時,一些反應性元素以氮化物和氧化物的形式被消耗。這將導致留下更少的反應性元素與游離的碳反應以形成穩定的碳化物,這進而對保護性氧化物形成具有影響。
所述合金中反應性元素的熱力學穩定的氮化物的實例是:tin,zrn,hfn,vn,tan和thn,并且所述合金中反應性元素的熱力學穩定的氧化物的實例是:tio2,zro2,hfo2,y2o3和tho2。
因此,為了補償由形成穩定的氮化物和氧化物所消耗的反應性元素,從所述商中反應性元素的量中扣除合金中氮和氧的量。
所述商中氧的量必須乘以權重因數“x”,其選自0.5或0.67。權重因數的值取決于形成的氧化物的類型,即它取決于合金中包含哪些元素并且也取決于在制造期間占優勢的條件下哪種氧化物在熱力學上最穩定。由于最通常形成的氧化物是二氧化物,因此可以將權重因數選擇為約0.5。然而,如果在所述合金中存在元素釔(大于或等于0.01wt%),則形成的最穩定的氧化物是三氧化物例如y2o3或alyo3,此時x為0.67。
在所述商中,反應性元素、碳和如果適用的話氮和氧,在各元素的原子百分率的基礎上平衡,因為重要的是確保對于每種反應性元素,添加足夠的量以匹配合金中的游離碳的數量,以便形成所需碳化物。
在操作中,上文中或下文中所定義的鐵素體合金將會形成,并因此構成表面氧化物層。所述表面氧化物層將包含(al2fe)o4-氧化物的外層、cr2o3氧化物的中間層和al2o3的內層。
上文中或下文中所定義的鐵素體合金也可以包含zrc和/或nbc和/或nb2c和/或hfc和/或vc和/或thc和/或tac的分散膠體。所述分散膠體可以采取包含tic分散膠體核并被zrc和/或nbc和/或nb2c和/或hfc和/或vc和/或thc和/或tac的分散膠體包圍的簇的形式。
附圖簡述
圖1:示出了平衡re和碳的目的的示意圖。
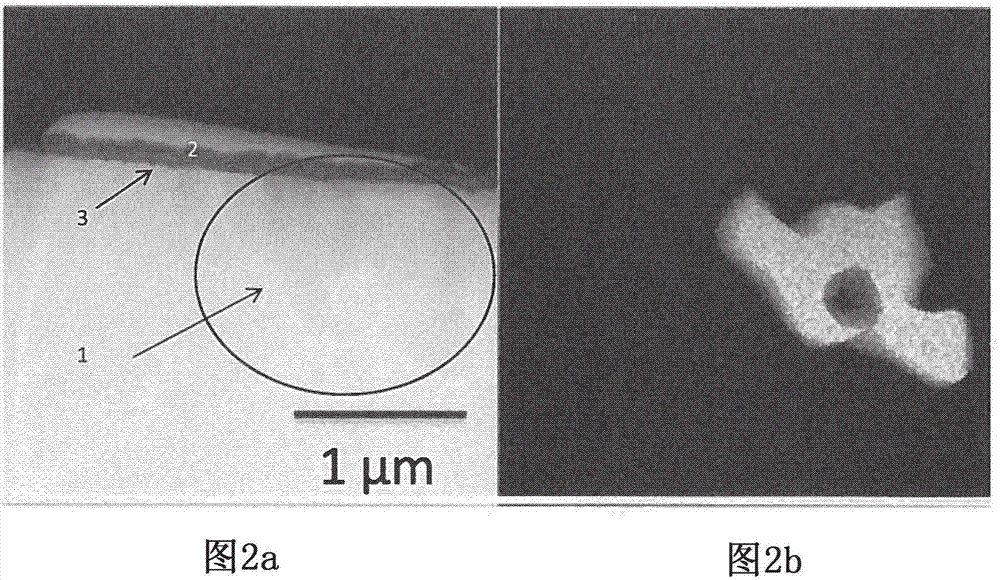
圖2a和2b:示出了在比較性合金中形成的富鉻碳化物的顯微照片。
圖3a和3b:示出了比較性合金中的氧化行為的顯微照片。
圖4a和4b:示出了根據本公開的第一可選方式的合金中的氧化行為的顯微照片。
圖5a和5b:示出了根據本公開的第二可選方式的合金中的氧化行為的顯微照片。
實施例的詳細描述
本公開將通過下面的非限制性實施例進行描述:
所述實施例旨在調查fe-10cr-4al合金,具體來說是調查不同反應性元素(re)對在550℃下的液態鉛的長期(8,760h)耐腐蝕性的影響。此外,出于比較的原因,進行了450℃下的短期(1,000h)試驗。
添加反應性元素(re)的影響:選擇zr、nb和y用于本實施例。在真空感應爐中生產了具有不同re含量的9種實驗性合金。將樣品熱軋成8×1mm帶材,并在每一步后在1050℃下均化5分鐘。所有研究的合金的分析的化學組成展示在表1中。
表1:研究的合金的化學組成(wt%)
*盡管根據本文中的定義的商不包含y,但對于最后三種合金來說將y
包含在商中用于比較。然而,正如將會顯示的并且也在本公開中討論的,與re相比釔的作用不同。
在所述9種樣品中re和碳的含量不同,使得某些樣品具有與碳的量相比缺乏的re(樣品zr-0.1、y-0.02、y-0.1),某些樣品中re和碳的量處于平衡(樣品zr-0.2、nb-0.8c、y-0.2),并且某些樣品中re與碳相比過量(樣品zr-0.4、nb-0.4、nb-0.8)。
為了進行氧化研究,制備每合金的試片,尺寸為30×8×1mm。使用sic砂紙將表面拋光至#800磨砂光潔度,然后將試片在乙醇中超聲處理,隨后置于裝有2mm99.9%(以金屬計)鉛粒的氧化鋁坩堝中。在管式爐中進行氧化試驗,其中將所述坩堝置于密封的石英管內。利用流動的ar-h2-h2o氣體混合物控制液態鉛中的溶解氧含量。使用1.3和0.2的h2/h2o比率分別在550℃和450℃的液態鉛中實現10-7wt%的溶解氧濃度。在完成450℃下1000h和550℃下8760h的氧化試驗后,將樣品空氣冷卻,并在乙酸和過氧化氫的(1:1)溶液中清潔以除去殘留的鉛。使用feiquanta3d場發射掃描電子顯微鏡(feg-sem),通過標準的提升法(lift-out)制備透射電子顯微術(tem)樣品。使用jeoljem-2100ffegtem進行tem評估。使用oxfordinstruments80mm2x-maxn硅漂移探測器(sdd)進行能量色散譜(eds)元素分析。通過將氧化的樣品模制在導電樹脂中,然后精細拋光至最終0.25μm菱形階梯(diamondstep),來制備sem樣品。使用zeissleo1530feg-sem和oxford50mm2x-maxsddeds進行總體表征。熱力學建模使用運行tcfe7和ssol4數據庫的thermocalc來進行。
研究結果
來自于550℃下的8,760h氧化試驗的結果顯示出對于各種不同的re添加來說,氧化性質存在明顯差異。
與碳相比缺乏re的三種合金(zr-0.1、y-0.02和y-0.1)形成顯著量的富cr碳化物,圖2a示出了cr-碳化物(1),其靠近形成在樣品表面(3)上的富含al的氧化物垢(2)。在圖2a中,所述富cr碳化物可能被檢測為圓圈區域內的白色形狀。圖2b是圖2a中圓圈圍住的富鉻區域(1)的temcreds圖。在這里可以清楚地看到所述富鉻區域的形狀。
所述實施例顯示,幾乎所有形成的cr碳化物都與樣品表面處的富含al的氧化物相接觸。這可以被解釋為是因為鋁抑制碳化物形成,即使石墨穩定。因此,似乎可能在貧al的金屬氧化物相邊界處所述cr碳化物的成核受到促進。因此,保護性的al氧化物沒有恰當形成。
此外,三種合金zr-0.1、y-0.02和y-0.1在氧化試驗中都顯示出不良的氧化性質。這種不良的結果在550℃和450℃下是一致的,這顯示選擇上文中或下文中所定義的正確的商是重要的。
圖3a示出了在550℃的溫度下氧化后從zr-0.1合金獲取的樣品的橫截面的sem圖像。在所述圖像中可以清楚地看到形狀不規則的混合氧化物,其已生長到合金本體中。zr-0.1樣品的金屬氧化物界面中大量的富鉻表面碳化物,似乎引起點蝕類型的加速氧化,展現出尺寸高達約5μm的向內生長的混合金屬氧化物。
在較低溫度下,當需要低的cr含量以避免α-α’相分離時,富鉻表面碳化物的存在導致形成非保護性氧化物垢。這通過在450℃下的較短(1000h)氧化試驗得以驗證。同樣的三種合金含有接近表面的碳化物(zr-0.1、y-0.02、y-0.1)并且與碳相比缺乏re,它們完全被三層氧化物結構覆蓋,所述結構由向外生長的fe3o4垢和向內生長的fecral混合氧化物構成,其下可以看到內部氧化區。圖3b示出了具有上述氧化物層結構的y-0.02樣品的sem顯微照片。所述y-0.02樣品上腐蝕侵蝕的總深度經測量為3-4μm。
平衡的合金
因此,通過平衡c和re的含量來改善fecral合金的腐蝕性能。這項研究中的三種合金zr-0.2、y-0.2和nb-0.8c含有相對于c含量接近平衡的re,在550℃下表現出顯著不同的氧化行為。
zr-0.2
zr-0.2合金沒有顯示出氧化侵蝕的跡象。進行了tem評估以研究zr-0.2樣品的表面,它顯示出存在薄的約100nm厚的氧化物,其在液態鉛中8,760h的暴露期間形成,參見圖4b。所述氧化物分為三層,向內生長的al2o3層,向外生長的feal混合氧化物,以及隔開它們的薄的富cr氧化物層。圖4b是temeds線性掃描,示出了圖3a中的層的化學組成隨所述層距表面的距離的變化。
在450℃下,zr-0.2合金表現出有利的氧化性質,即形成保護性氧化物層,參見圖4a。利用tem來研究在其表面上形成的薄的氧化物,經測量約為40nm。與550℃下的tem結果相似,在450℃下形成的氧化物被分為三個區,只富含al的內層,富含fe的外部部分,以及富含cr的中間層(圖4b)。圖5b是temeds線性掃描,示出了圖5a中的層的化學組成隨所述層距表面的距離的變化。
nb-0.8c
nb-0.8c合金在550℃下沒有顯示出氧化侵蝕。
y-0.2
盡管y相對于c略微過量,但在550℃下處理后,在y-0.2合金上發現了局部氧化點蝕。這可以通過釔碳化物與zr和nb的碳化物相比相對弱的穩定性來解釋。微觀結構表征發現了富含y的沉淀物,其富含c、o、s,特別是fe。
大過量比率的合金
與c相比具有大過量re的樣品(即樣品zr-0.4、nb-0.4、nb-0.8)在550℃和450℃下都顯示出不良的氧化性質。zr-0.4合金在550℃下顯示出點蝕類型的氧化侵蝕,并且在整個基質中發現尺寸高達2μm的富含fe和zr的相。此外,同一合金上的氧化物點蝕富含zr。
合金zr-0.4和y-0.2在450℃下的表現相似。與550℃下的情況相同,在450℃下過量y和zr的影響不引起氧化性質的顯著降低。然而,與550℃相比在450℃下較慢的反應動力學和較短的暴露時間可能掩蓋了結果。
在550℃下處理后,nb-0.8合金幾乎完全被尺寸高達5μm的氧化點蝕覆蓋。優選地,發現這些沉淀物與萊夫斯相的行為類似,修飾合金晶界,但也存在于nb-0.8合金的晶粒內部。
結論
已顯示,當re添加與合金的碳含量處于平衡,即re略微過量時,獲得最佳的抗氧化性。相對于碳來說缺乏re將導致接近合金表面的富鉻碳化物的形成,其進而引起不良的氧化性質并降低耐點蝕性。此外,re的過量摻入將導致金屬間化合物或萊夫斯相的形成,其也降低合金的抗氧化性。
- 還沒有人留言評論。精彩留言會獲得點贊!