一種高強度雙網絡抗菌生物水凝膠的制備方法與流程
本發明涉及生物醫用水凝膠的合成領域,具體涉及一種高強度雙網絡抗菌生物水凝膠的制備方法。
背景技術:
水凝膠是一種能夠吸收與存儲大量水分的三維高分子材料,這種優異的性能歸功于水凝膠具有親水基團和交聯的三維網絡骨架結構。由于水凝膠具備良好的親水性、滲透性和生物相容性,以及低摩擦系數性能(Jason W. Nichol , Sandeep T. Koshy, et, al. Cell-laden micro-engineered gelatin methacrylate hydrogels. Bio-materials 31,2010,5536-5544),使得水凝膠廣泛的應用在藥物緩釋、角膜接觸鏡、組織工程支架、生物免疫調節、體外診斷等領域。但是,良好的生物相容性導致易被細菌侵染,類生物組織的構造使得力學性能較差,限制了水凝膠的應用。所以,提高水凝膠的力學性能與抗菌性能,使水凝膠的功能多樣化,具有重要的科研和應用價值。
金屬離子與雜環化合物的螯合作用啟發于對生物仿生學的應用(Stephan S,Antje R ,et al. Metal-Mediated Molecular Self-Healing in Histidine Rich Mussel Peptides. Bio-macromolecules 2014, 15, 1644?1652),貝類生物利用絲足能夠將自身牢固的結合在形貌復雜的海岸巖石上,并且抵御高強度與高頻率的浪擊。由于絲足中存在離子螯合作用,在被破壞后具有高度的自修復能力,能夠使貝類在惡劣的海岸環境中生存下來,具有離子螯合作用構建物理交聯網絡的水凝膠力學性能良好。
在水凝膠中構筑不同結合性質的網絡結構,是為了達到改善水凝膠力學性能的目的(Matthew S., Craig J. ,et al. Versatile tuning of supra-molecular hydrogels through metal complexation of oxidation-resistant catecholinspired ligands. Soft Matter, 2013, 9, 10314–10323)。目前在一級共價鍵化學網絡的基礎上構建二級物理網絡結合作用的包括氫鍵、雙硫鍵、π-π交互作用、離子交互作用和金屬螯合交互作用等 (Marcel E, Stefan B, Jürgen V, et, al. Self-healing response in supra-molecular polymers based on reversible zinc histidine interactions. Polymer 69 ,2015, 274-282)。選用金屬螯合交互作用,可以在水凝膠中引入特征基團與金屬離子的同時,考慮引入基團與離子的功能性。使水凝膠在構建二級網絡改善了力學性能的同時,通過引入的特定基團與離子,獲取一些新的特征功能。鋅離子與咪唑基是公認的具有抗菌功能的無機與有機材料(Dominic E, Li H ,et al. Mussel Inspired Histidine Based Transient Network Metal Coordination Hydrogels. Macromolecule 2013, 46, 1167?1174)。在明膠水凝膠的兩步改性過程中引入了咪唑基與鋅離子,制備出的雙網絡水凝膠力學性良好,生物性能優異,同時也具有了抗菌功能。能很好的解決現有技術面臨的接枝組氨酸過程容易氧化的問題,現階段的技術采用其他類型的離子僅僅使雙網絡水凝膠的力學性能得到增強,而引入鋅離子改善雙網絡水凝膠力學性能的同時引入了抗菌功能。
制備物理螯合力與化學共價鍵共存的雙網絡生物水凝膠的方法,其核心思想在于,通過在明膠上引入咪唑基團,(Clemens N. Z. Schmitt, Yael Politi, et al. Role of Sacrificial Protein?Metal Bond Exchange in Mussel Byssal Thread Self-Healing. Bio-macromolecules 2015, 16, 2852?2861)使明膠水凝膠具備螯合金屬離子構筑二級螯合力物理網絡能力的基礎。制備出的雙網絡水凝膠力學性良好,剛度、韌性得到了極大提高,對大腸桿菌(革蘭氏陰性菌)與金黃色葡萄球菌(革蘭氏陽性菌)的殺菌率均達到99.9%,同時又保留了基材水凝膠良好的生物相容性,在生物醫用材料、組織工程等領域具有很好的應用前景。
技術實現要素:
為達到上述目的,本發明提供了一種高強度雙網絡抗菌生物水凝膠的制備方法。制備的高強度雙網絡抗菌生物水凝膠,提高了基材水凝膠的力學性能,賦予了基材水凝膠的高效抗菌性能,保留了基材水凝膠的生物活性。
本發明通過如下技術方案實現。
一種高強度雙網絡抗菌生物水凝膠的制備方法,包括如下步驟:
(1)將改性的明膠與改性的組氨酸混合后,溶解在磷酸鹽緩沖溶液(PBS)中,得到預聚液,加入光引發劑,在紫外點光源下引發聚合,構建一級共價鍵化學網絡,并引入活性位點,得到引入了咪唑基團的明膠水凝膠;
(2)采用二價金屬離子鹽溶液浸泡引入了咪唑基團的明膠水凝膠,浸泡過程中,二價金屬離子螯合咪唑活性位點,構建二級物理網絡;浸泡結束后,用無菌水洗滌,得到所述高強度雙網絡抗菌生物水凝膠。
進一步地,步驟(1)中,所述改性的明膠是采用甲基丙烯酸酐進行改性得到的甲基丙烯酸酐明膠,改性反應過程中,明膠和甲基丙烯酸酐的質量之比為5:2~4,反應的時間為2~4h,反應的溫度為40~60℃;改性結束后,通過透析分離產物,透析的時間為6~10天,透析的溫度為40~60℃。
進一步地,步驟(1)中,所述改性的組氨酸是采用丙烯酰氯進行改性得到的組氨酸,改性反應的全過程在氮氣氛圍中避光進行,反應溶劑為氫氧化鈉堿性溶液;改性反應過程中,組氨酸與丙烯酰氯物質的量之比為5:4~6,反應的時間為30~60min,反應的溫度為0~5℃;改性反應結束后,產物采用丙酮離心洗滌后收集,再低溫負壓干燥。
進一步地,步驟(1)中,所述改性的明膠與改性的組氨酸的質量比為1:0.5~1。
進一步地,步驟(1)中,所述光引發劑為Irgacure2959,用量為預聚液的0.3~0. 5w/v %。
進一步地,步驟(1)中,所述紫外點光源的參數設置為:光的強度6~8mW/cm2,光的波長360~480nm。
進一步地,步驟(1)中,所述紫外點光源與預聚液的垂直距離為8~12cm。
進一步地,步驟(1)中,所述聚合的時間為30~50s。
進一步地,步驟(2)中,所述二價金屬離子鹽包括二價金屬離子的硫酸鹽、氯鹽或硝酸鹽。
進一步地,步驟(2)中,所述二價金屬離子包括鋅離子。
進一步地,步驟(2)中,所述二價金屬離子鹽溶液中,二價金屬離子的濃度為12~24mM。
進一步地,步驟(2)中,所述浸泡的時間為2~4h。
與現有技術相比,本發明具有以下優點和有益效果:
(1)本發明得到的高強度雙網絡抗菌生物水凝膠的力學性良好,剛度、韌性得到了極大提高,達到甲基丙烯酸酐明膠水凝膠的4倍;
(2)本發明得到的高強度雙網絡抗菌生物水凝膠具有廣譜抗菌功能,對以大腸桿菌為代表的革蘭氏陰性菌與以金黃色葡萄球菌為代表的革蘭氏陽性菌的殺菌率均達到99.9%;
(3)本發明得到的高強度雙網絡抗菌生物水凝膠保留了甲基丙烯酸酐明膠水凝膠良好的生物相容性,在生物醫用材料、組織工程等領域具有很好的應用前景;
(4)本發明制備方法具有反應條件溫和、可操作性強、技術流程可控等優點。
附圖說明
圖1是實施例1中制備的高強度雙網絡抗菌生物水凝膠的微觀形貌的掃描電鏡圖;
圖2是實施例2中制備的高強度雙網絡抗菌生物水凝膠與對照樣的力學性能曲線圖;
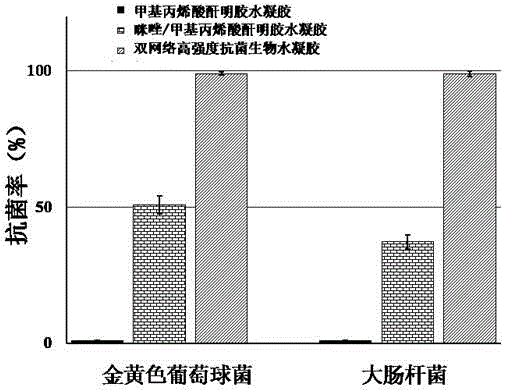
圖3是實施例2中合成的高強度雙網絡抗菌生物水凝膠的抗菌性能測試結果柱狀圖;
圖4是實施例3中制備的高強度雙網絡抗菌生物水凝膠對MC-3T3細胞的死活細胞熒光染色圖。
具體實施方式
下面結合實施例,對本發明作進一步的詳細說明,實施方法并不僅限于此。
實施例1
(1)稱取5g明膠到50ml磷酸鹽緩沖溶液中,在40℃下攪拌溶解;取2ml甲基丙烯酸酐,緩慢滴加到上述溶液中,攪拌反應2h;將反應后的混合液倒入40℃的磷酸鹽緩沖溶液中,攪拌2min,終止反應;用透析袋分裝上述液體,在40℃的去離子水中透析6天;將透析過的溶液用離心管分裝后離心,收集上清液,在超低溫冰箱凍存24h,再在冷凍干燥機中凍干,得到高純度甲基丙烯酸酐明膠樣品。
(2)稱取3g 組氨酸溶解到7ml氫氧化鈉溶液中,通入氮氣并冰浴溶解;取1.5ml的丙烯酰氯,在氮氣氛圍與避光條件下,逐滴緩慢加入到上述溶液中;保持0℃反應30min后,將反應混合液避光加入到丙酮中,攪拌3min,得到沉積物;沉積物用丙酮離心洗滌4次,收集最后一次離心沉淀,在超低溫冰箱凍存24h,再在冷凍干燥機中凍干,得到高純度丙烯酰氯改性組氨酸樣品。
(3)按質量比2:1稱取凍干的甲基丙烯酸酐明膠樣品與丙烯酰氯改性組氨酸樣品,在恒溫箱中溶解在含光引發劑的磷酸鹽緩沖溶液中,得到預聚液,光引發劑用量為預聚液的0.3w/v%;用移液槍移取預聚液到48孔板內,在紫外點光源下進行聚合;紫外點光源的光強度為6mW/cm2,波長360nm;紫外點光源與預聚液的垂直距離為8cm,聚合時間30s,得到引入了咪唑活性位點的明膠水凝膠。
(4)制備鋅離子濃度為12mM的氯化鋅無菌溶液,用于浸泡48孔板內的光聚合產物,浸泡時間為2h,結束后用無菌水反復洗滌2次,得到所述高強度雙網絡抗菌生物水凝膠。
得到的高強度雙網絡抗菌生物水凝膠的微觀形貌的掃描電鏡圖如圖1所示,由圖1可知,凍干后的雙網絡水凝膠孔洞均勻連續且沒有析出物,鋅離子良好的分散到水凝膠內部。
得到的高強度雙網絡抗菌生物水凝膠的力學性能明顯改善,具有高效的殺菌性能,且具有優異的生物相容性。
實施例2
(1)稱取5g明膠到50ml 磷酸鹽緩沖溶液中,在50℃下攪拌溶解;取3ml甲基丙烯酸酐,緩慢滴加到上述溶液中,攪拌反應3h;將反應后的混合液倒入50℃的磷酸鹽緩沖溶液中,攪拌2min,終止反應;用透析袋分裝上述液體,在50℃的去離子水中透析8天;將透析過的溶液用離心管分裝后離心,收集上清液,在超低溫冰箱凍存24h,再在冷凍干燥機中凍干,得到高純度甲基丙烯酸酐明膠樣品。
(2)稱取3g組氨酸溶解到7ml氫氧化鈉溶液中,通入氮氣并冰浴溶解;取1.7ml的丙烯酰氯,在氮氣氛圍與避光條件下,逐滴緩慢加入到上述溶液中;保持2℃反應40min后,將反應混合液避光加入到丙酮中,攪拌3min,得到沉積物;沉積物用丙酮離心洗滌4次,收集最后一次離心沉淀,在超低溫冰箱凍存24h,再在冷凍干燥機中凍干,得到高純度丙烯酰氯改性組氨酸樣品。
(3)按質量比1:1稱取凍干的甲基丙烯酸酐明膠樣品與丙烯酰氯改性組氨酸樣品,在恒溫箱中溶解在含光引發劑的磷酸緩沖液中,得到預聚液,光引發劑用量為預聚液的0.4w/v%;用移液槍移取預聚液到48孔板內,在紫外點光源下進行聚合;紫外點光源的光強度為7mW/cm2,波長400nm;紫外點光源與預聚液的垂直距離為9cm,聚合時間40s,得到引入了咪唑活性位點的明膠水凝膠。
(4)制備鋅離子濃度為18mM的氯化鋅無菌溶液,用于浸泡48孔板內的光聚合產物,浸泡時間為3h,結束后用無菌水反復洗滌2次,得到所述高強度雙網絡抗菌生物水凝膠。
得到的高強度雙網絡抗菌生物水凝膠的微觀形貌掃描電鏡圖參見圖1,雙網絡水凝膠孔洞均勻連續,鋅離子在水凝膠內部的分散良好;且得到的高強度雙網絡抗菌生物水凝膠具有優異的生物相容性。
得到的高強度雙網絡抗菌生物水凝膠的力學性能測試結果如圖2所示,由圖2可知,形成雙網絡后的水凝膠最大形變量處斷裂應力達到59KPa,比甲基丙烯酸酐明膠水凝膠的最大形變量處斷裂應力14KPa高出4倍,體現出明顯的力學性能改善。
將得到的高強度雙網絡抗菌生物水凝膠、咪唑/甲基丙烯酸酐明膠水凝膠、甲基丙烯酸酐明膠水凝膠與大腸桿菌(革蘭氏陰性細菌)、金黃色葡萄球菌(革蘭氏陽性細菌)分別共同培養24h,得到的抗菌性能測試結果如圖3所示,由圖3可知,高強度雙網絡抗菌生物水凝膠對大腸桿菌(革蘭氏陰性細菌)與金黃色葡萄球菌(革蘭氏陽性細菌)的抗菌率均達到99.9%,相比沒有抗菌作用的明膠水凝膠,體現出高效的抗菌性能。
實施例3
(1)稱取5g明膠到50ml 磷酸鹽緩沖溶液中,在60℃下攪拌溶解;取4ml甲基丙烯酸酐,緩慢滴加到上述溶液中,攪拌反應4h;將反應后的混合液倒入60℃的磷酸鹽緩沖溶液,攪拌2min,終止反應;用透析袋分裝上述液體,在60℃的去離子水中透析10天;將透析過的溶液用離心管分裝后離心,收集上清液,在超低溫冰箱凍存24h,再在冷凍干燥機中凍干,得到高純度甲基丙烯酸酐明膠樣品。
(2)稱取3g 組氨酸溶解到7ml氫氧化鈉溶液中,通入氮氣并冰浴溶解;取1.8ml的丙烯酰氯,在氮氣氛圍與避光條件下,逐滴緩慢加入到上述溶液中;保持0℃反應60min后,將混合液避光加入到丙酮中,攪拌3min,得到沉積物;沉積物用丙酮離心洗滌4次,收集最后一次離心沉淀,在超低溫冰箱凍存24h,再在冷凍干燥機中凍干,得到高純度丙烯酰氯改性組氨酸樣品。
(3)按質量比1:0.8稱取凍干的甲基丙烯酸酐明膠樣品與丙烯酰氯改性組氨酸樣品,在恒溫箱中溶解在含光引發劑的磷酸緩沖液中,得到預聚液,光引發劑的用量為預聚體的0.5w/v%;用移液槍移取預聚液到48孔板內,在紫外點光源下進行聚合;紫外點光源的強度為8mW/cm2,波長480nm;紫外點光源與預聚物垂直距離為12cm,聚合時間50s,得到引入了咪唑活性位點的明膠水凝膠。
(4)制備鋅離子濃度為24mM的硝酸鋅無菌溶液,用于浸泡48孔板內的光聚合產物,浸泡時間為4h,結束后用無菌水反復洗滌2次,得到所述高強度雙網絡抗菌生物水凝膠。
得到的高強度雙網絡抗菌生物水凝膠的微觀形貌掃描電鏡圖參見圖1,雙網絡水凝膠孔洞均勻連續,鋅離子在水凝膠內部的分散良好;且得到的高強度雙網絡抗菌生物水凝膠的力學性能明顯改善,具有高效的殺菌性能。
分析得到的高強度雙網絡抗菌生物水凝膠的生物相容性,得到的高強度雙網絡抗菌生物水凝膠對MC-3T3細胞的死活細胞熒光染色圖如圖4所示,由圖4可知,細胞在合成的雙網絡水凝膠表面生長狀態良好,雙網絡水凝膠保留了原有的優異生物相容性。
- 還沒有人留言評論。精彩留言會獲得點贊!