一種少Pb鈣鈦礦材料及其制備方法、和鈣鈦礦太陽能電池與流程
本發明屬于鈣鈦礦太陽能電池技術領域,具體涉及一種少pb鈣鈦礦材料及其制備方法、和鈣鈦礦太陽能電池。
背景技術:
面對目前能源危機及環境污染,太陽能作為一種可再生能源,是滿足全球范圍內日益增長的能源需求的重要方法之一。將太陽能轉換為電能的一種有效的方法是制備基于光生伏特效應的太陽電池。有機—無機雜化鈣鈦礦材料(ch3nh3pbx3)制備的太陽電池能量轉換效率自2009年從3.8%增長到現在已被認證的22.1%,因其良好的電子和空穴傳輸性能、較高的光吸收系數、較低的生產成本及易于制備等諸多優勢獲得了廣泛關注。
傳統的鈣鈦礦太陽電池包括介孔鈣鈦礦太陽電池和平面鈣鈦礦太陽電池,然而平面電池相對介孔而言,具有結構簡單、容易制備等優點,一般的平面鈣鈦礦太陽電池結構為:透明導電薄膜/電子傳輸層/鈣鈦礦吸收層/空穴傳輸層/金屬電極。但作為核心材料的鈣鈦礦吸收材料中含有可溶解的重金屬pb,有毒且對環境會造成污染,這嚴重阻礙了鈣鈦礦太陽電池的商業化,因此,為推動鈣鈦礦太陽電池的商業化步伐,制備少pb甚至無pb的高效環保鈣鈦礦太陽電池勢在必行。
技術實現要素:
本發明的目的在于提供一種少pb鈣鈦礦材料及其制備方法,采用過渡金屬fe(或co)和cl元素對鈣鈦礦中的pb和i元素進行部分摻雜替代,從而制備出高效環保的鈣鈦礦材料,為鈣鈦礦太陽電池的商業化提供一個新的思路及途徑。
本發明采用如下技術方案:
一種少pb鈣鈦礦材料,其分子式為ch3nh3pb1-xfexi3(cl)或ch3nh3pb1-xcoxi3(cl),其中0<x<0.6。
上述少pb鈣鈦礦材料的制備方法,將以下前驅體材料按摩爾比pbi2:fecl2·4h2o或cocl2·6h2o:ch3nh3i=(1-x):x:1溶于二甲基亞砜或含二甲基亞砜的溶劑中,其中0<x<0.6,得到前驅體溶液,取30-50μl所述前驅體溶液滴加到導電玻璃上,先600~800rpm旋涂10~20s,后2000~4000rpm旋涂20~30s并于旋涂結束前的5~10s滴加氯苯,最后退火處理,所得薄膜即為所述鈣鈦礦材料。
上述少pb鈣鈦礦材料的制備方法,將以下前驅體材料按摩爾比pbi2:fecl2·4h2o或cocl2·6h2o=(1-x):x溶于二甲基亞砜或含二甲基亞砜的溶劑中,其中0<x<0.6,得到前驅體溶液,取30-50μl所述前驅體溶液滴加到導電玻璃上,2000~4000rpm旋涂20~40s,然后60~80℃退火處理10~20min,冷卻到室溫后,于ch3nh3i的異丙醇溶液(ch3nh3i濃度為8~12mg/ml)中浸泡數分鐘,最后100~120℃退火處理15~30min,所得薄膜即為所述鈣鈦礦材料。
上述少pb鈣鈦礦材料的制備方法,所述含二甲基亞砜的溶劑選自二甲基亞砜、二甲基亞砜和n,n-二甲基甲酰胺的混合溶劑或二甲基亞砜和γ-丁內酯的混合溶劑。
利用上述少pb鈣鈦礦材料制備得到的鈣鈦礦太陽能電池。
本發明的有益效果如下:
本發明用過渡金屬fe(或co)和cl對鈣鈦礦吸收層中的pb和i進行了同步摻雜替代,由此制備的鈣鈦礦太陽電池的光電轉換效率高達17.31%,fe(或co)和cl的摻雜為以后制備少pb甚至無pb的高效環保鈣鈦礦太陽電池提供了一個新的思路及途徑。
附圖說明
此處以fecl2摻雜為例來說明本發明的相關測試表征:
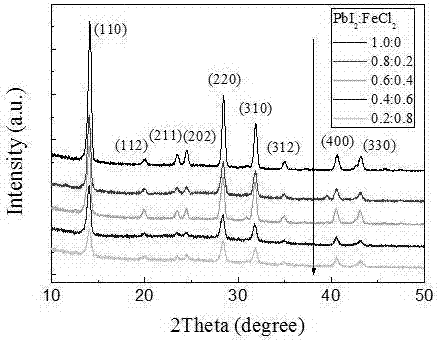
圖1為采用兩步法制備的摻雜不同量的fe和cl得到的鈣鈦礦材料的xrd圖:可以發現,隨著前驅體溶液中fecl2含量的增加,鈣鈦礦材料的衍射峰強度逐步減弱,但仍保持四方相鈣鈦礦結構;
圖2采用兩步法制備的摻雜不同量的fe和cl得到的鈣鈦礦材料的sem圖(對應地,前驅體溶液中pbi2:fecl2的含量比:(a)0.2:0.8;(b)0.4:0.6;(c)0.6:0.4;(d)0.8:0.2;(e)1.0:0):隨著溶液中pbi2含量的降低,立方體晶粒生長特征增強,晶粒密度減小,晶粒尺寸增加,有利于提高電池的開路電壓;
圖3采用兩步法制備的摻雜不同量的fe和cl得到的鈣鈦礦材料的的熒光光譜:隨著溶液中fecl2含量的增加,發光強度有所降低,發光峰出現藍移,說明該薄膜材料的帶隙隨著fe和cl的摻入,逐步增加;當pbi2:fecl2含量比為0.8:0.2,發光強度較低,當pbi2:fecl2含量比為0.2:0.8時,發光消失,說明存在最佳范圍的摻雜濃度;
圖4采用兩步法制備的摻雜不同量的fe和cl得到的鈣鈦礦材料的eds和xps能譜圖:可以看出,得到的鈣鈦礦材料中含有fe和cl;
圖5采用一步法制備的摻雜不同量的fe和cl得到的鈣鈦礦材料的吸收光譜:可以看出,適量的摻雜有助于提高薄膜的吸收系數;
圖6采用一步法制備的摻雜fe和cl得到的鈣鈦礦材料制備得到的鈣鈦礦電池的j-v特性曲線:采用適量的fe和cl摻雜后,電池的性能得到了提高。
具體實施方式
為了使本發明的技術目的、技術方案和有益效果更加清楚,下面結合附圖和具體實施例對本發明的技術方案作出進一步的說明。
實施例一:
(1)將以下前驅體材料按摩爾比為pbi2:fecl2·4h2o:ch3nh3i=0.8:0.2:1溶于二甲基亞砜溶劑中,經過加熱攪拌得到前驅體溶液;
(2)將透明導電玻璃用洗潔精清洗后,再分別經過去離子水、丙酮、酒精、異丙醇各超聲清洗10min,自然晾干,最后經過紫外燈處理10min,備用;
(3)將30-50μl步驟(1)所配制的前驅體溶液滴加到上述(2)中清潔干凈的導電玻璃上,先600rpm下旋涂20s,后2000rpm旋涂25s并于旋涂結束前的10s滴加反溶劑氯苯(即先2000rpm旋涂15s,滴加氯苯,再2000rpm旋涂10s,旋涂過程不間斷,本發明相關描述均表此意),對于常規實驗室規格的電池,氯苯用量約300~400ul,最后120℃退火處理15min,即得所述鈣鈦礦材料。
實施例二:
(1)將以下前驅體材料按摩爾比為pbi2:cocl2·6h2o:ch3nh3i=0.6:0.4:1溶于二甲基亞砜和γ-丁內酯的混合溶劑中,經過加熱攪拌得到前驅體溶液;
(2)將透明導電玻璃用洗潔精清洗后,再分別經過去離子水、丙酮、酒精、異丙醇各超聲清洗10min,自然晾干,最后經過紫外燈處理10min,備用;
(3)將30-50μl步驟(1)所配制的前驅體溶液滴加到上述(2)中清潔干凈的導電玻璃上,先700rpm下旋涂15s,后3000rpm旋涂30s并于旋涂結束前的6s滴加反溶劑氯苯,最后100℃退火處理15min,即得所述鈣鈦礦材料。
實施例三:
(1)將前驅體材料按摩爾比為pbi2:fecl2·4h2o=0.9:0.1的量溶于二甲基亞砜和γ-丁內酯的混合溶劑中,經過加熱攪拌得到前驅體溶液;
(2)將透明導電玻璃用洗潔精清洗,再分別經過去離子水、丙酮、酒精、異丙醇各超聲清洗10min,自然晾干,最后經過紫外燈處理10min,備用;
(3)將30-50μl步驟(1)中的所配制的前驅體溶液滴加到步驟(2)清潔干凈的導電玻璃上,在2000rpm旋涂40s,然后80℃退火處理10min,自然冷卻到室溫后,于ch3nh3i濃度為10mg/ml的異丙醇溶液中浸泡12min,最后120℃退火處理15min,即得鈣鈦礦材料。
實施例四:
(1)將前驅體材料按摩爾比為pbi2:cocl2·6h2o=0.5:0.5的量溶于二甲基亞砜和n,n-二甲基甲酰胺的混合溶劑中,經過加熱攪拌得到前驅體溶液;
(2)將透明導電玻璃用洗潔精清洗,再分別經過去離子水、丙酮、酒精、異丙醇各超聲清洗10min,自然晾干,最后經過紫外燈處理10min,備用;
(3)將30-50μl步驟(1)中的所配制的前驅體溶液滴加到步驟(2)清潔干凈的導電玻璃上,在3000rpm旋涂30s,然后70℃退火處理10min,自然冷卻到室溫后,于ch3nh3i濃度為10mg/ml的異丙醇溶液中浸泡12min,最后100℃退火處理30min,即得鈣鈦礦材料。
電池制作流程:
(1)將透明導電玻璃首先用洗潔精清洗,再分別用去離子水、丙酮、酒精、異丙醇各超聲清洗10min,自然晾干,最后經過紫外燈處理10min,備用;
(2)于步驟(1)清洗干凈的導電玻璃上用化學水浴法沉積電子傳輸層tio2,具體操作為:首先將冷藏的ticl4(質量分數為99.9%)溶液用冰水混合物稀釋至濃度為200mm,需要注意的是,為確保獲得澄清且混合均勻的溶液,在滴加冰水混合物時,速度一定要緩慢,同時于500~1000rpm的轉速下攪拌;將導電玻璃浸在稀釋后的ticl4溶液中,為保證獲得高質量的tio2薄膜,將導電玻璃以30°的傾角斜放,然后放入恒溫水浴鍋中,70℃保溫1h,隨后將導電玻璃從ticl4溶液中取出,依次用去離子水和無水乙醇清洗,最后放入馬弗爐中500℃退火處理30min,從而得到厚度約80nm的tio2層;
(3)將經步驟(2)處理后的導電玻璃從馬弗爐取出,自然冷卻到室溫,取30-50μl實施例二所配制的前驅體溶液滴加到tio2層上,先700rpm旋涂15s,后3000rpm旋涂20s,滴加反溶劑氯苯后,再3000rpm旋涂6s,最后100℃退火處理15min,得到鈣鈦礦材料層;
(4)在步驟(3)得到的鈣鈦礦材料上旋涂50μl的spiro-ometad,轉速為3000rpm,時間為30s,從而得到空穴傳輸層;
(5)于空穴傳輸層上蒸鍍金電極,從而制得鈣鈦礦太陽電池,經測試,其光電轉換效率高達17.31%。
最后所應說明的是:上述實施例僅用于說明而非限制本發明的技術方案,任何對本發明進行的等同替換及不脫離本發明精神和范圍的修改或局部替換,其均應涵蓋在本發明權利要求保護的范圍之內。
- 還沒有人留言評論。精彩留言會獲得點贊!