二苯乙烯苷在制備肥胖性高血壓的治療藥物及保健品中的應用的制作方法
本發明涉及肥胖癥相關的心血管疾病的候選藥物,具體涉及二苯乙烯苷在治療肥胖性高血壓中的應用。
背景技術:
世界衛生組織將超重定義為體重指數(body mass index,BMI)大于25kg/m2,超過30kg/m2即為肥胖;而基于人種差異,國內指標分別為24kg/m2和28kg/m2。隨著當代社會科學技術日益進步,人們的運動量減少,而飲食習慣和飲食結構卻趨向愉悅口舌而有損健康,高糖、高脂、高熱量食品逐漸占據飲食金字塔底層,導致超重和肥胖人數急劇增多。一項2014年5月發表在Lancet上,時間超過30年、有188個國家參與的最新流行病學研究的調查數據表明,全球肥胖或超重人群已經達到21億人,幾乎相當于30%的全球總人數。在中國,僅從1991年到2002年,超重人口增加了40%,而肥胖比例更是翻了1倍。超重和肥胖人群的健康狀況已經并日益受到更多關注。本質上說,肥胖是由于能量代謝紊亂導致的脂肪堆積。超額的體重不但增加了心、腎、肺、血管系統等的負擔,更易造成全身各系統功能紊亂,其中病死率最高的并發癥是心腦血管病。肥胖被視為動脈粥樣硬化相關心腦血管病發生的獨立危險因素,例如,冠心病、高血壓及腦卒中等。因此,肥胖所引起的上述疾病已成為世界衛生健康的主要威脅之一。由于心血管事件一旦發生即難于逆轉,病死率高,所以早期發現心血管危險因素、早期實施干預一直是控制肥胖相關心血管疾病的重要策略。
肥胖與高脂血癥、高胰島素血癥等密切相關,嚴重者可導致動脈粥樣硬化、高血壓等心腦血管疾病。研究表明,血管內皮功能障礙是上述病變的始動環節,是引起成人動脈粥樣硬化的獨立高危因素。鑒于其在臨床上冠心病、腦血管病及外周血管病變發展中的核心作用,血管內皮功能障礙被認為是減少心血管疾病發病率和死亡率風險的重要的治療靶標。研究表明,內皮功能障礙是由一系列復雜的遺傳、環境和其它因素相互作用所引起,這些因素包括吸煙、活性氧自由基、脂質氧化、高血糖、高甘油三酯血癥和切力應激等。這些因素單獨或者相互協同作用可導致血管內皮細胞損傷、分泌功能異常、以及對舒張/收縮因子反應異常等,后者即構成血管內皮功能障礙。然而,盡管肥胖相關的血管內皮功能障礙一直是重點關注和研究的領域,但迄今為止,其誘發機制,尤其是分子病因學機制,尚未完全闡明。
自噬是指從粗面內質網的無核糖體附著區脫落的雙層膜包裹部分胞質和細胞內需降解的細胞器、蛋白質等成分形成自噬體(autophagosome),并與溶酶體融合形成自噬溶酶體(autolysosome),降解其所包裹的內容物,以實現細胞本身的代謝需要和細胞器的更新。自噬在機體的生理和病理過程中都能見到,其所起的作用是正面還是負面,根據其所處微環境而各有不同,尚未完全闡明,值得關注。新近的研究已證實血管內皮細胞存在自噬現象。前期的研究結果表明,在幼年自發性高血壓大鼠(SHR)中,過度自噬可能是誘發其微血管內皮功能障礙的重要原因之一(Am J Chin Med,2016)。此外,長期攝入必需脂肪酸α-亞麻酸(ALA)可通過抑制氧化應激而改善糖尿病性的內皮功能障礙(PLoS ONE,2013;Vasa,2013)。
中藥何首烏在我國沿用已有上千年的歷史,有補益精血、烏須發、補肝腎、強筋骨之效。2002年被衛生部列入“可用于保健食品的物品”名單。二苯乙烯苷(2,3,5,4’-Tetrahydroxystilbene-2-O-β-D-glucoside,TSG)是蓼科植物何首烏PolygonummultiflorumThunb中提取的主要有效成分(水溶性有效成分),現代藥理研究表明其具有較好的保護內皮、抗氧化、抗衰老、抗動脈粥樣硬化作用。前期研究發現,TSG治療能通過上調Akt/mTOR通路、抑制過度自噬部分恢復SHR的阻力血管內皮功能,但未能顯著地降低其血壓。
目前尚未見到TSG在治療肥胖性高血壓中的作用及機制的研究報道。TSG對肥胖狀態下的血壓升高和血管內皮功能障礙有何影響、其機制為何?這些問題尚不清楚。如能徹底闡明,將為應用TSG防治肥胖相關的心血管病提供理論依據,具有較為重要的公共衛生意義。
技術實現要素:
本發明的目的在于提供二苯乙烯苷在制備肥胖性高血壓的治療藥物及保健品中的應用。
為達到上述目的,本發明采用了以下技術方案:
與正常對照組大鼠(Lean ZDF)相比,肥胖大鼠(ZDF)的收縮壓升高,長期攝食或膳食補充二苯乙烯苷(TSG)則可降低ZDF大鼠的動脈血壓,其作用機制包括:
1)TSG可改善ZDF大鼠的內皮依賴性血管舒張效應。
2)TSG可顯著上調ZDF大鼠的阻力血管Akt/mTOR通路。
3)TSG可降低ZDF大鼠血管LC3II/I、Beclin1表達。
TSG具有降低肥胖性高血壓個體的動脈血壓的作用,可保護肥胖性高血壓個體的血管內皮功能,能夠用于制備肥胖性高血壓的治療藥物或保健品。
本發明的有益效果體現在:
本發明經過對血壓明顯升高的肥胖大鼠膳食性補充二苯乙烯苷實驗測試,發現二苯乙烯苷具有降低肥胖大鼠收縮壓和平均動脈壓的作用,能夠用于制備肥胖性高血壓的治療藥物或保健品,具有良好的研究與應用前景,為肥胖患者進行早期有效的血壓干預,從而預防肥胖癥心腦血管并發癥的發生發展提供新的防治策略和實驗證據。
本發明通過實驗研究,發現二苯乙烯苷可下調血管LC3II/I、Beclin1表達,并改善血管內皮功能、降低其收縮壓和平均動脈壓,表明二苯乙烯苷可通過抑制過度自噬來改善阻力血管功能,從而改善肥胖性高血壓。
附圖說明
圖1為二苯乙烯苷(TSG)分子結構圖示。
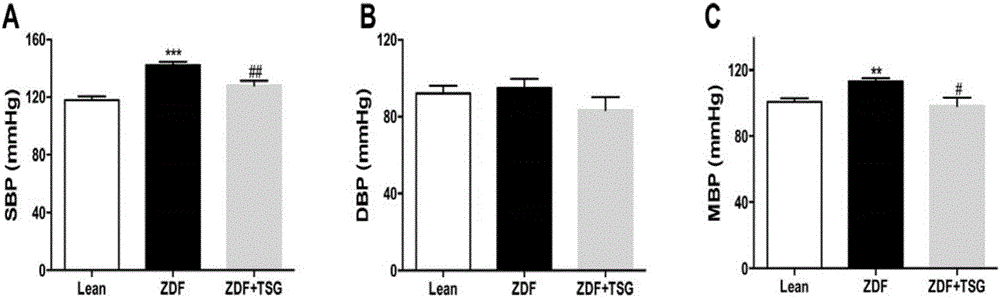
圖2為肥胖大鼠長期攝食二苯乙烯苷降低動脈血壓升高的結果;(A)二苯乙烯苷對大鼠收縮壓的影響;(B)二苯乙烯苷對大鼠舒張壓的影響;(C)二苯乙烯苷對大鼠平均動脈壓的影響。其中,**P<0.01,***P<0.001vs Lean組;#P<0.05,##P<0.01vs ZDF組。
圖3為二苯乙烯苷改善肥胖大鼠的內皮依賴性血管舒張效應的結果;(A)ACh誘導的血管舒張效應;(B)SNP誘導的血管舒張效應。其中,*P<0.05,**P<0.01,***P<0.001vs Lean組;#P<0.05,###P<0.001vs ZDF組,n=6。
圖4為二苯乙烯苷抑制肥胖大鼠腸系膜微血管組織LC3II/I、Beclin1表達并增強Akt、mTOR磷酸化水平的結果;(A)各組大鼠腸系膜微動脈的Western blot結果,p-Akt、p-mTOR分別表示Akt總蛋白、mTOR總蛋白中相應磷酸化蛋白,β-Actin為內參;(B)二苯乙烯苷提高肥胖大鼠血管組織Akt、mTOR的磷酸化水平的結果,其中,*P<0.05,**P<0.01vs Lean組;#P<0.05,##P<0.01vs ZDF組;(C)二苯乙烯苷降低肥胖大鼠血管組織LC3II/I、Beclin1的表達的結果,其中,**P<0.01vs Lean組;#P<0.05vs ZDF組。
具體實施方式
下面結合附圖和實施例對本發明做進一步詳細說明。
超重/肥胖是心腦血管疾病的獨立危險因素,且發生率日益增高,已成為重大的社會健康問題。通過圍繞肥胖狀態下內皮功能障礙與高血壓的發生機制及防治策略進行的研究,前期發現Akt/mTOR信號受損誘導過度自噬可能是促發幼年自發性高血壓大鼠微血管內皮功能障礙的原因,提示自噬與血管功能障礙及高血壓的可能關系(Am J Chin Med,2016)。最新的實驗結果證實,與正常對照組大鼠(Lean ZDF)相比,肥胖大鼠(ZDF)腸系膜微動脈的自噬啟動和調節關鍵蛋白beclin1、自噬標記蛋白微管相關蛋白1輕鏈3-Ⅱ(LC3-Ⅱ)的水平均增高,結果提示,肥胖狀態下的血管內皮細胞發生自噬,從而可能在促發血管內皮功能障礙中起到作用。
本發明中,通過研究證實,在肥胖動物模型膳食補充TSG,可通過上調Akt/mTOR通路、抑制過度自噬部分恢復微血管內皮功能。進一步研究證實,且可顯著降低肥胖狀態下的收縮壓和平均動脈壓,提示TSG確可通過抑制血管過度自噬而治療肥胖型高血壓,具體研究及結果如下:
1、攝食TSG對ZDF大鼠血壓的影響實驗:
采用雄性ZDF大鼠及年齡性別匹配的正常血壓Lean ZDF大鼠。實驗動物共分為3組(n=6):①正常對照組(Lean組):雄性Lean ZDF大鼠,普通飼料喂養,每日灌胃生理鹽水。②雄性肥胖大鼠組(ZDF組):雄性ZDF大鼠,高脂飼料喂養,每日灌胃生理鹽水。③雄性肥胖大鼠二苯乙烯苷灌胃組(ZDF+TSG組):雄性ZDF大鼠,高脂飼料喂養,灌胃TSG(100mg/kg/day,TSG參見圖1)。2周后,大鼠禁食12h,清醒、安靜狀態下,用Softron BP-98A大小鼠無創血壓儀測量大鼠尾動脈收縮壓(SBP)和舒張壓(DBP),測量前大鼠在39℃加熱套中適應10min左右,連續測量3次,計算平均值;根據收縮壓(SBP)和舒張壓(DBP)計算平均動脈壓(MBP)。結果顯示,TSG可顯著降低ZDF大鼠的收縮壓,提示肥胖狀態下膳食補充TSG可延緩ZDF大鼠動脈血壓升高,參見圖2。
2、腸系膜微動脈分離及功能檢測實驗:
灌胃TSG處理結束后,稱重,30mg/kg戊巴比妥鈉腹腔麻醉,動物深度麻醉后仰臥位固定于手術操作臺上,剪開腹腔,迅速取出腸系膜微動脈,置于0℃預冷的PSS緩沖液中,在體式顯微鏡下分離血管周圍脂肪及結締組織,并小心避免損傷血管內皮,然后截取長約1mm的血管環(3-4個血管環/動物)。生理鹽溶液[physiologic salt solution,PSS(mM):NaCl 119.0,KCl 4.7,NaHCO3 25.0,MgSO4 1.2,KH2PO4 1.2,CaCl2 2.5,Glucose5.5,EDTA 0.026,pH 7.4]預先置于37℃恒溫水浴加熱;在微血管灌流儀的灌流槽中加入預熱的PSS液5mL,持續通入含95%O2和5%CO2混合氣體,保持37℃恒溫。在血管環中穿入兩根直徑40μm的不銹鋼絲,移入微血管灌流儀的灌流槽中,一根鋼絲連接張力換能器,另一根連張力調節器(調節負荷張力),通過硬件PowerLab 8通道橋式放大器和軟件LabChart8.0顯示血管負荷張力于計算機屏幕。調節血管環靜息負荷2mN,平衡60min,平衡時每20min換液。高鉀(60mM)溶液使血管預收縮2次,棄用活性差的血管,血管收縮反應平臺后,用37℃PSS液清洗灌流槽3次,每次10min。加入10-6mol/L苯腎上腺素(PE)引起血管收縮,平臺后濃度累加法加入ACh(乙酰膽堿,一種內皮依賴性血管舒張因子,累積濃度為10-11-10-6mol/L),以觀察內皮依賴性舒張反應,或SNP(S-亞硝基-N-乙酰基-青霉胺,一種內皮非依賴性血管舒張因子,累積濃度為10-10-10-5mol/L)以觀察非內皮依賴性舒張反應,或TSG(累積濃度為10-9-10-3mol/L),各次給藥結束后用預熱的PSS液沖洗3次,每次10min;PE的預收縮幅度為100%,舒張率(%)=藥物引發的舒張張力/PE的預收縮張力×100%,從而評定血管內皮的功能。實驗結果顯示,與Lean ZDF大鼠相比,ZDF大鼠對ACh誘導的內皮依賴性血管舒張效應明顯下降,表明其血管內皮功能受損;給予TSG兩周可改善ACh誘導的血管舒張效應,而SNP誘導的內皮非依賴性血管舒張效應在Lean ZDF大鼠和ZDF大鼠中并沒有顯著差異。這一現象說明在ZDF大鼠中,影響血管功能并進一步升高動脈血壓的重要因素之一可能是受損的血管內皮,而給予TSG治療后可部分逆轉這一過程,恢復內皮依賴性血管舒張功能,并發揮降血壓功效,參見圖3。
3、Western Blotting檢測大鼠血管組織LC3II/I、Beclin1、Akt/mTOR信號通路表達水平實驗:
大鼠血管組織用0℃PBS(pH 7.4)清洗,稱重后移入預冷的RIPA裂解液中剪碎。于冰上組織勻漿30s,12000×g 4℃離心10min,取上清。BCA蛋白定量試劑盒進行蛋白定量。加入5×SDS上樣緩沖液煮沸10min,冷卻后離心分裝,-80℃保存。蛋白樣品行SDS-PGEA電泳,6%濃縮膠,12%分離膠,每孔上樣30μg蛋白,第一階段恒壓90V 30min,第二階段恒壓150V至溴酚藍跑至分離膠最前端,停止電泳。用濕轉法恒流300mA 90min將凝膠轉移到PVDF膜上。轉移后的PVDF膜放入5%脫脂奶粉室溫封閉1h。用anti-beclin1(1:1000)、anti-LC3Ⅱ/Ⅰ(1:1000)、anti-pAkt(1:1000)、anti-Akt(1:1000)、anti-pmTOR(1:1000)、anti-mTOR(1:1000)及anti-βactin(1:1000)孵育PVDF膜,4℃過夜;孵育結束后PBST緩沖液清洗,用HRP標記的羊抗兔二抗(1:5000)室溫孵育60min,PBST緩沖液清洗,1:1混合ECL發光檢測A液和B液,凝膠成像系統進行化學發光檢測。結果顯示,膳食補充TSG后,ZDF大鼠腸系膜微動脈中表達的自噬啟動和調節關鍵蛋白LC3II/I、Beclin1水平均降低,Akt和mTOR磷酸化水平增加。以往的研究發現,Akt/mTOR信號通路、AMPK信號通路、MAPK/ERK1/2信號通路都能調節自噬,其中Akt/mTOR信號通路起到關鍵的調節作用。Akt/mTOR是蛋白質合成的主要信號調節通路,參與細胞增殖、分化等調節,該通路的活化可抑制細胞凋亡及細胞自噬,促進細胞周期進展。本研究的結果表明Akt/mTOR信號增強介導的自噬蛋白LC3II/I、Beclin1下調可能參與了TSG改善血管內皮功能、進而降低動脈血壓的作用,參見圖4。
本發明通過實驗研究發現肥胖大鼠進行TSG膳食補充可改善血管內皮功能,降低動脈血壓;且可部分激活其阻力血管Akt/mTOR通路、降低自噬相關蛋白LC3II/I、Beclin1表達。以上結果提示肥胖患者攝入TSG具有治療肥胖性高血壓的作用,其機制可能與TSG抑制過度自噬并改善阻力血管功能有關。
- 還沒有人留言評論。精彩留言會獲得點贊!