一種芽孢表面穩定展示海藻糖合酶的工程菌及其構建方法與流程
本發明涉及一種芽孢表面穩定展示海藻糖合酶的工程菌及其構建方法,特別涉及一種芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌工程菌及其構建方法,屬于生物工程技術領域。
背景技術:
枯草芽孢桿菌(Bacillus subtilis)是一類好氧型、內生抗逆孢子的桿狀細菌,是革蘭氏陽性細菌的典型代表,具有無治病性,表達系統穩定的特點;其細胞壁的組成簡單,在細胞壁合成過程中沒有內毒素的生成,已經被美國、日本、歐盟和中國認定為安全無毒的菌株,廣泛應用于食品、飼料等行業。芽孢(內生孢子或稱孢子)是芽孢桿菌營養細胞受到營養缺乏,代謝產物積累,或溫度變化等外部環境因子的觸發而形成的休眠體,芽孢的形成需要經過一系列復雜的生理生化反應。
近年來以芽孢衣殼蛋白為分子載體,通過芽孢表面展示技術將外源目的蛋白展示于重組枯草芽孢桿菌芽孢表面,制備具有生物活性的重組芽孢抗體和酶制劑已成為人們研究和關注的熱點。構建重組枯草芽孢桿菌的芽孢表面展示體系時,利用芽孢衣殼蛋白融合展示海藻糖合酶,將底物麥芽糖轉化為海藻糖,不僅能夠避免因誘導劑的使用而造成限制,而且融合酶不需要穿過細胞膜,將海藻糖合酶直接應用于高端海藻糖的生產制備中,避免因細胞破碎,雜質分離造成的成本增加及熱源物質對海藻糖的污染,該法是海藻糖生產的有效技術手段。但是由于芽孢易受萌發劑刺激而萌發,使展示芽孢在轉化麥芽糖制備海藻糖體系中穩定性較差,海藻糖合酶異源表達后,只能利用一次,不能充分回收利用。
技術實現要素:
本發明主要針對現有技術的不足,提供一種芽孢表面穩定展示海藻糖合酶的工程菌及其構建方法。
本發明技術方案如下:
一種芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌工程菌,使枯草芽孢桿菌中編碼芽孢萌發的皮層溶解酶基因sleB和cwlJ失活后獲得;
所述sleB基因核苷酸序列如SEQ ID NO.1所示;cwlJ基因核苷酸序列如SEQ ID NO.2所示。
根據本發明優選的,所述編碼芽孢萌發的皮層溶解酶基因sleB和cwlJ失活為通過基因敲除、基因增補、基因替換或基因突變引起編碼內切纖維素酶基因celB的啟動子、終止子或編碼區的變化導致編碼芽孢萌發的皮層溶解酶基因sleB和cwlJ無法表達。
上述芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌工程菌的構建方法,步驟如下:
(i)以枯草芽孢桿菌為模板,進行PCR擴增,分別得到sleB1,cwlJ1片段;
sleB1片段擴增的PCR引物序列如下:
sleB-up:5’-CGGGATCCCGGGGGATGATGTGGTCGAG-3’; SEQ ID NO.3
sleB-down:5’-ACTGACTCACTCAAAAATAACCCCCGCTACT-3’; SEQ ID NO.4
cwlJ1片段擴增的PCR引物序列如下:
cwlJ-up:5’-CGGGATCCCGTTCTGAAGTAATGAAATATGATG-3’; SEQ ID NO.5
cwlJ-down:5’-CTATGGTGTGTGGGAAAAGCAGTGGACTTAAATCT-3’; SEQ ID NO.6
(ii)以質粒pPIC9k為模板,進行PCR擴增,得到kmr片段;
所述的kmr片段PCR擴增引物序列如下:
kmr-up:5’-CGGGGGTTATTTTTGAGTGAGTCAGTCATAGGGAG-3’; SEQ ID NO.7
kmr-down:5’-CGGGATCCCGGGTTGAGGCCGTTGAGCA-3’; SEQ ID NO.8
(iii)以pPICZαA質粒為模板,進行PCR擴增,得到zeor片段;
所述的zeor片段PCR擴增引物序列如下:
zeor-up:5’-TAAGTCACACTGCTTTTCCCACACACCATAGCTTCA-3’; SEQ ID NO.9
zeor-down:5’-CGGGATCCCGGTTGGTCTCCAGCTTGCAAA-3’; SEQ ID NO.10
(iv)利用重疊PCR技術連接sleB1和kmr片段,制得sleB1-kmr片段,步驟如下:
初次PCR擴增,擴增體系如下:
2×Taq PCR MasterMix 12.5μl,模板sleB1 1μl,模板kmr 1μl,用ddH2O補足25μl;
初次PCR擴增,擴增程序如下:
95℃預變性5min;94℃變性30sec,57℃退火30sec,72℃延伸3.5min,5個循環;
補充PCR擴增,擴增體系如下:
向初次擴增后的體系中加入2×Taq PCR MasterMix 12.5μl,10μmol/L引物sleB-up 1μl,10μmol/L引物kmr-down 1μl,用ddH2O補足50μl;
補充PCR擴增,擴增程序如下:
95℃預變性5min;94℃變性30sec,56℃退火30sec,72℃延伸4.5min,30個循環;72℃延伸10min,-20℃保存;
(v)利用重疊PCR技術連接cwlJ1和zeor片段,制得cwlJ1-zeor片段,步驟如下:
初次PCR擴增,擴增體系如下:
2×Taq PCR MasterMix 12.5μl,模板cwlJ1 1μl,模板zeor 1μl,用ddH2O補足25μl;
初次PCR擴增,擴增程序如下:
95℃預變性5min;94℃變性30sec,57℃退火30sec,72℃延伸3min,5個循環;
補充PCR擴增,擴增體系如下:
向初次擴增后的體系中加入2×Taq PCR MasterMix 12.5μl,10μmol/L引物cwlJ-up 1μl,10μmol/L引物zeor-down 1μl,用ddH2O補足50μl;
補充PCR擴增,擴增程序如下:
95℃預變性5min;94℃變性30sec,56℃退火30sec,72℃延伸4min,30個循環;72℃延伸10min,-20℃保存;
(vi)將步驟(iv)制得的sleB1-kmr片段轉化枯草芽孢桿菌獲得sleB基因缺失菌后,再將步驟(v)制得的cwlJ1-zeor基因轉化sleB基因缺失菌中獲得sleB,cwlJ基因雙缺失菌株,經篩選,制得芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌。
根據本發明優選的,所述步驟(i)中,sleB1片段擴增的PCR擴增體系為50μl:
2×Taq PCR MasterMix 25μl,10μmol/L引物sleB-up 2.5μl,10μmol/L引物sleB-down 2.5μl,模板2.5μl,用ddH2O補足50μl;
sleB1片段擴增的PCR擴增程序如下:
95℃預變性5min;95℃變性30sec,56℃退火30sec,72℃延伸1.5min,30個循環;72℃延伸10min,-20℃保存。
根據本發明優選的,所述步驟(i)中,cwlJ1片段擴增的PCR擴增體系為50μl:
2×Taq PCR MasterMix 25μl,10μmol/L引物cwlJ-up 2.5μl,10μmol/L引物cwlJ-down 2.5μl,模板2.5μl,用ddH2O補足50μl;
cwlJ1片段擴增的PCR擴增程序如下:
95℃預變性5min;95℃變性30sec,56℃退火30sec,72℃延伸1.5min,30個循環;72℃延伸10min,-20℃保存。
根據本發明優選的,所述步驟(ii)中,所述的kmr片段PCR擴增體系為50μl:
2×Taq PCR MasterMix 25μl,10μmol/L引物kmr-up 2.5μl,10μmol/L引物kmr-down 2.5μl,模板2.5μl,用ddH2O補足50μl;
所述的kmr片段PCR擴增程序如下:
95℃預變性5min;95℃變性30sec,56℃退火30sec,72℃延伸3.5min,30個循環;72℃延伸10min,-20℃保存。
根據本發明優選的,所述步驟(iii)中,所述的zeor片段PCR擴增體系為50μl:
2×Taq PCR MasterMix 25μl,10μmol/L引物zeor-up 2.5μl,10μmol/L引物zeor-down 2.5μl,模板2.5μl,用ddH2O補足50μl;
所述的zeor片段PCR擴增程序如下:
95℃預變性5min;95℃變性30sec,56℃退火30sec,72℃延伸3min,30個循環;72℃延伸10min,-20℃保存。
根據本發明優選的,所述步驟(vi)中的枯草芽孢桿菌為枯草芽孢桿菌168。枯草芽孢桿菌168來源于杭州寶賽生物有限公司。
根據本發明優選的,所述步驟(vi)中的轉化為:將枯草芽孢桿菌感受態細胞在2500V、25uF的條件下電擊一次,時間常數=4.5~5.0ms。
根據本發明優選的,所述步驟(vi)中的篩選,包括卡那青霉素篩選和博來霉素篩選。
根據本發明進一步優選的,所述卡那青霉素篩選步驟如下:
在含有卡那青霉素抗生素的平板上進行白斑篩選,挑取白色單一斑點,接種到含有卡那青霉素的液體LB培養基,培養至對數末期,對能在含有卡那青霉素抗生素的LB培養基上生長的菌液進行PCR驗證,將能夠擴增出目的條帶的轉化子進行提取質粒,對提取的質粒進行酶切驗證,含有目的條帶的,即得;
含有卡那青霉素的液體LB培養基,每升組分如下:
10g蛋白胨、10g NaCl、5g酵母浸粉、5mg卡那青霉素,定容至1L。
根據本發明進一步優選的,所述博來霉素篩選步驟如下:
在含有博來霉素抗生素的平板上進行白斑篩選,挑取白色單一斑點,接種到含有博來霉素的液體LB培養基,培養至對數末期,對能在含有博來霉素抗生素的LB培養基上生長的菌液進行PCR驗證,將能夠擴增出目的條帶的轉化子進行提取質粒,對提取的質粒進行酶切驗證,含有目的條帶的,即得;
含有博來霉素的液體LB培養基,每升組分如下:
10g蛋白胨、10g NaCl、5g酵母浸粉、5mg博來霉素,定容至1L。
有益效果
1、本發明首次通過失活芽孢萌發的皮層溶解酶基因sleB和cwlJ弱化芽孢萌發的方式提高芽孢表面展示海藻糖合酶的穩定性,經實際驗證,可有效提高海藻糖合酶的酶活,12h內海藻糖合酶酶活可保持95%以上;
2、本發明所述的枯草芽孢桿菌工程菌表達體系具有安全、無內毒素的特點,在食品與醫藥產業化領域倍受認可;
3、本發明構建的芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌工程菌,既不影響菌株本身形成芽孢,同時還弱化了芽孢在麥芽糖轉化生成海藻糖體系中的萌發。
附圖說明
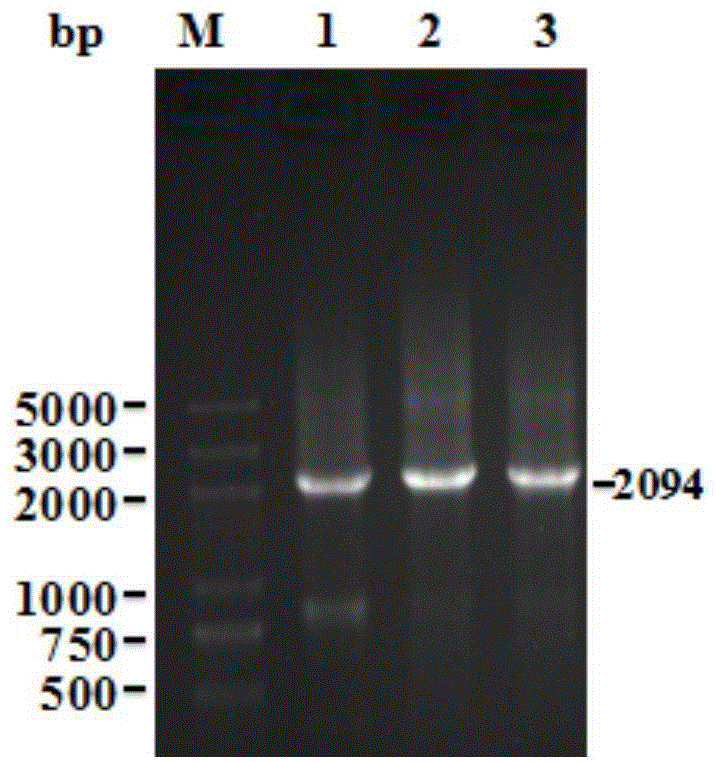
圖1為本發明的sleB基因敲除轉化子的瓊脂糖凝膠電泳圖;
圖中:泳道M為DNA分子量標記(DNA marker),泳道1-3為轉化子條帶,大小為2094bp;
圖2為本發明的cwlJ基因敲除轉化子的瓊脂糖凝膠電泳圖;
圖中:泳道M為DNA分子量標記(DNA marker),泳道1-3為轉化子條帶,大小為1656bp;
圖3為本發明的麥芽糖轉化生成海藻糖的高效液相色譜;
圖中:M為麥芽糖,T為海藻糖糖,A為Bacillus Subtilis 168轉化麥芽糖生成海藻糖色譜,B為Bacillus Subtilis 168ΔsleBΔcwlJ工程菌轉化麥芽糖生成海藻糖色譜;
圖4為本發明的芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌海藻糖酶相對酶活;
圖中:芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌的海藻糖合酶的相對酶活在12h內可保持95%以上,較枯草芽孢桿菌原始菌有顯著提高。
具體實施方式
下面結合實施例對本發明的技術方案做進一步闡述,但本發明所保護范圍不限于此。
生物材料來源:
枯草芽孢桿菌168、穿梭質粒pPIC9k和pPICZαA均購自杭州寶賽生物有限公司;
實施例1:基因敲除片段構建
(i)提取Bacillus Subtilis 168DNA,以DNA為模板,進行PCR擴增,得到同源臂sleB1;
所述的PCR引物序列如下:
sleB-up:5’-CGGGATCCCGGGGGATGATGTGGTCGAG-3’;
sleB-down:5’-ACTGACTCACTCAAAAATAACCCCCGCTACT-3’;
所述的PCR擴增體系為:
所述的PCR擴增程序如下:
95℃預變性5min;94℃變性30sec,56℃退火30sec,72℃延伸1.5min,30個循環;72℃終延伸10min,4℃保存;
瓊脂糖凝膠電泳檢驗PCR產物,長度為592bp,使用SanPrep柱式DNA膠回收試劑盒(上海生工)進行膠回收,回收產物-20℃保存,備用;
(ii)提取Bacillus Subtilis 168 DNA,以DNA為模板,進行PCR擴增,得到同源臂cwlJ1;
所述的PCR引物序列如下:
cwlJ-up:5’-CGGGATCCCGTTCTGAAGTAATGAAATATGATG-3’;
cwlJ-down:5’-CTATGGTGTGTGGGAAAAGCAGTGGACTTAAATCT-3’;
所述的PCR擴增體系為:
所述的PCR擴增程序如下:
95℃預變性5min;94℃變性30sec,56℃退火30sec,72℃延伸1min,30個循環;72℃終延伸10min,4℃保存;
瓊脂糖凝膠電泳檢驗PCR產物,長度為451bp,使用SanPrep柱式DNA膠回收試劑盒(上海生工)進行膠回收,回收產物-20℃保存,備用;
(iii)提取穿梭質粒pPIC9k的DNA,以DNA為模板,進行PCR擴增,得到kmr片段;
所述的PCR引物序列如下:
kmr-up:5’-CGGGGGTTATTTTTGAGTGAGTCAGTCATAGGGAG-3’;
kmr-down:5’-CGGGATCCCGGGTTGAGGCCGTTGAGCA-3’;
所述的PCR擴增體系為:
所述的PCR擴增程序如下:
95℃預變性5min;94℃變性30sec,56℃退火30sec,72℃延伸3.5min,30個循環;72℃終延伸10min,4℃保存;
瓊脂糖凝膠電泳檢驗PCR產物,長度為1502bp,使用SanPrep柱式DNA膠回收試劑盒(上海生工)進行膠回收,回收產物-20℃保存,備用;
(iv)提取穿梭質粒pPICZαA的DNA,以DNA為模板,進行PCR擴增,得到zeor片段;
所述的PCR引物序列如下:
zeor-up:5’-TAAGTCACACTGCTTTTCCCACACACCATAGCTTCA-3’;
zeor-down:5’-CGGGATCCCGGTTGGTCTCCAGCTTGCAAA-3’;
所述的PCR擴增體系為:
所述的PCR擴增程序如下:
95℃預變性5min;94℃變性30sec,57℃退火30sec,72℃延伸3min,30個循環;72℃終延伸10min,4℃保存;
瓊脂糖凝膠電泳檢驗PCR產物,長度為1205bp,使用SanPrep柱式DNA膠回收試劑盒(上海生工)進行膠回收,回收產物-20℃保存,備用;
(v)將步驟(i)制得的sleB1片段與步驟(iii)制得的kmr片段進行重疊PCR,制得sleB1-kmr片段;
所述的重疊PCR的擴增體系為:
所述的重疊PCR的初次擴增程序如下:
95℃預變性5min;94℃變性30sec,57℃退火30sec,72℃延伸3.5min,5個循環;72℃終延伸10min;
所述的重疊PCR的補充擴增程序如下:
95℃預變性5min;94℃變性30sec,56℃退火30sec,72℃延伸4.5min,30個循環;72℃終延伸10min,4℃保存;
瓊脂糖凝膠電泳檢驗PCR產物,長度為2094bp,使用SanPrep柱式DNA膠回收試劑盒(上海生工)進行膠回收,回收產物-20℃保存,備用;
(vi)將步驟(ii)制得的cwlJ1片段與步驟(iv)制得的zeor片段進行重疊PCR,制得cwlJ1-zeor片段;
所述的重疊PCR的擴增體系為:
所述的重疊PCR的初次擴增程序如下:
95℃預變性5min;94℃變性30sec,57℃退火30sec,72℃延伸3min,5個循環;72℃終延伸10min;
所述的重疊PCR的補充擴增程序如下:
95℃預變性5min;94℃變性30sec,56℃退火30sec,72℃延伸4min,30個循環;72℃終延伸10min,4℃保存;
瓊脂糖凝膠電泳檢驗PCR產物,長度為1656bp,使用SanPrep柱式DNA膠回收試劑盒(上海生工)進行膠回收,回收產物-20℃保存,備用;
實施例2:制備Bacillus Subtilis 168感受態
(i)挑取新鮮LB固體培養基表面的Bacillus Subtilis 168單菌落,接種于10mL GM培養基中,37℃、220r/min,過夜培養;
(ii)取1mL上述菌液轉接到100mLGM培養基,37℃、220r/min培養至OD600=1.0;
(iii)將菌液轉移至100mL離心管,冰浴10min,使菌體停止生長;
(iv)冰浴后4℃、7000r/min、5min離心,收集菌體;
(v)離心后的菌體用預冷的電轉緩沖液(ETM)洗滌2-3次;
(vi)洗滌結束后,使用1000μL電轉緩沖液重懸菌體;
(vii)將制備好的感受態細胞分裝100μL每管,-80℃保存,備用。
其中,GM培養基:LB培養基+0.5M山梨醇;
ETM:0.5M山梨醇+0.5M甘露醇+10%甘油,余量水;
RM培養基:LB培養基+0.5M山梨醇+0.38M甘露醇;
實施例3:sleB1-kmr片段電轉化Bacillus Subtilis 168及陽性重組子的鑒定
(i)將sleB1-kmr片段用限制性內切酶BamH I酶切;
酶切體系(40μL)如下:
(ii)濃縮純化酶切產物
(1)加入1/10體積3M醋酸鈉和2.5倍體積無水乙醇,置于-20℃冰箱20min;
(2)12000r/min,離心5min得沉淀;
(3)300μL體積百分比濃度為75%的乙醇溶液重懸沉淀;
(4)12000r/min,離心5min,除去乙醇,37℃風干30min;
(5)加入15~18μL ddH2O重懸DNA,并置于-20℃保存。
(iii)電轉化
首先利用核酸超微量分光光度計測定sleB1-kmr片段濃度,達到100~400ng/uL濃度后進行電轉化,電轉化條件為電壓2000V,電擊時間5ms,將得到的細胞經液體復蘇培養基在37℃復蘇培養4h,取200μL涂布在含濃度25μmol/mL卡那霉素的LB固體培養基上,在37℃培養1~2天,篩選具有卡那霉素抗性的轉化子;
所述液體復蘇培養基每升組分如下:
蛋白胨10g,酵母浸粉5g,氯化鈉10g,山梨醇91g,甘露醇69g,蒸餾水1000mL。
(iv)挑取上述陽性重組菌落,接種到含卡那霉素抗性的液體LB培養基中37℃培養過夜,培養完成后,使用上海生物工程有限公司提供的試劑盒提取重組菌DNA,并以獲得的基因組為模板,sleBF和kmR為引物進行PCR擴增,擴增產物利用瓊脂糖凝膠電泳進行驗證;
所述的PCR引物序列如下:
sleB-up:5’-CGGGATCCCGGGGGATGATGTGGTCGAG-3’
kmr-down:5’-CGGGATCCCGGGTTGAGGCCGTTGAGCA-3’
其中,下劃線標識的為酶切位點
所述的PCR擴增體系為20μl:
所述的PCR擴增程序如下:
95℃預變性5min;94℃變性30sec,56℃退火30sec,72℃延伸3.5min,30個循環;72℃延伸10min,4℃保存,瓊脂糖凝膠電泳檢驗PCR產物。
實施例4cwlJ1-zeor片段電轉化Bacillus Subtilis 168ΔsleB及陽性重組子的鑒定
(i)按照實施例2中的步驟制備Bacillus Subtilis 168ΔsleB感受態
(ii)將cwlJ1-zeor片段用限制性內切酶BamH I酶切;酶切體系(40μL)如下:
(iii)按照實施例3(ii)中的步驟濃縮純化酶切產物
(iv)電轉化
首先利用核酸超微量分光光度計測定cwlJ1-zeor片段濃度,達到100~400ng/uL濃度后進行電轉化,電轉化條件為電壓2000V,電擊時間5ms,將得到的細胞經液體復蘇培養基在37℃復蘇培養4h,取200μL涂布在含濃度25μmol/mL卡那霉素和50μmol/mL博來霉素的LB固體培養基上,在37℃培養1~2天,篩選具有卡那霉素和博來霉素抗性的轉化子;
所述液體復蘇培養基每升組分如下:
蛋白胨10g,酵母浸粉5g,氯化鈉10g,山梨醇91g,甘露醇69g,蒸餾水1000mL。
(v)挑取上述陽性重組菌落,分別依次接種到含卡那霉素和博來霉素抗性的液體LB培養基中37℃培養過夜,培養完成后,使用上海生物工程有限公司提供的試劑盒提取重組菌DNA,并以獲得的基因組為模板,cwlJF和zeoR為引物進行PCR擴增,擴增產物利用瓊脂糖凝膠電泳進行驗證;
所述的PCR引物序列如下:
cwlJ-up:5’-CGGGATCCCGTTCTGAAGTAATGAAATATGATG-3’
zeor-down:5’-CGGGATCCCGGTTGGTCTCCAGCTTGCAAA-3’
其中,下劃線標識的為酶切位點
所述的PCR擴增體系為20μl:
所述的PCR擴增程序如下:
95℃預變性5min;94℃變性30sec,56℃退火30sec,72℃延伸3min,30個循環;72℃終延伸10min,4℃保存,瓊脂糖凝膠電泳檢驗PCR產物。
最終制得芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌。
實施例5:芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌在麥芽糖轉化生成海藻糖體系中的應用:
(1)將芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌接種于活化培養基中于37℃下活化培養3~4h,然后按體積百分比為1%的比例接種于裝液量為30~50mL三角瓶,其中抗生素濃度為25mg/mL,培養條件為35~37℃、200~220rpm、10~14h,得到Bacillus Subtilis 168ΔsleBΔcwlJ的菌液;
活化培養基配方如下,單位g/L:
蛋白胨9~11、酵母浸粉5~7、氯化鈉9~11,蒸餾水定容,pH7.0~7.4;121℃滅菌20~30min;
(2)將步驟(1)中得到Bacillus Subtilis 168ΔsleBΔcwlJ的菌液按體積百分比2~4%的接種量接種于80~100mL發酵培養基中,在35~37℃、180~220rpm的條件下搖瓶發酵48h,得到發酵液;
搖瓶發酵培養基組分如下,單位g/L:
葡萄糖5~10、玉米漿10~15、磷酸二氫鉀2~3、硫酸錳0.3~0.5、結晶硫酸鎂2~3、氯化鈉4~6,蒸餾水定容;115℃滅菌20~30min;
(3)芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌在麥芽糖轉化生成海藻糖體系中海藻糖合酶酶活檢測
將發酵液8000r/min離心20min,棄上清,用去離子水洗滌沉淀2次,并用去離子水懸浮,加入溶菌酶使其終濃度為2mg/mL,37℃處理30min破壞營養細胞,8000r/min離心10min,烘干,稱量干菌體重量,最后用去離子水懸浮得到芽孢懸浮液。取5ml發酵48h后的重組菌芽孢懸浮液與10ml pH 7.5的磷酸鹽緩沖液配制的終濃度30%的麥芽糖漿混勻后制備成海藻糖合酶的反應體系。將此反應體系置于50℃恒溫水浴震蕩搖床中反應12h,每隔4h取樣,測定海藻糖合酶的酶活。
酶活力單位定義:在酶的最佳酶反應條件下(25℃,pH 8.0),將300g/L麥芽糖轉化為海藻糖,每小時產生1μmol海藻糖所需的酶量定義一為個酶活單位(U)。
經實驗證明原始菌的相對酶活在4h后酶活就下降到65%,10h后穩定在50%,而本專利中構建的芽孢表面穩定展示海藻糖合酶的枯草芽孢桿菌海藻糖合酶的相對酶活在12h內可穩定在95%以上,與原始菌相比海藻糖合酶酶活有顯著提高。
SEQUENCE LISTING
<110> 齊魯工業大學
<120> 一種芽孢表面穩定展示海藻糖合酶的工程菌及其構建方法
<160> 10
<170> PatentIn version 3.5
<210> 1
<211> 874
<212> DNA
<213> Bacillus Subtilis
<400> 1
atgaagtcca aaggatcgat tatggcatgt ctcatccttt tttctactga aacgatccat 60
tcaaagaggg gcaacagggg atgatgtggt cgagcttcag gcgcgtcttc aatacaacgg 120
atattataac ggaaaaattg acggggttta tggatggggg acgtactggg cagttcgaaa 180
ttttcaggat caattcgggt taaaagaggt tgacggcctt gtaggagcta aaacaaagca 240
aaccttaata tgtaaatcaa aatactatcg tgaatatgtc atggaacagc tcaataaagg 300
gaatacattc acgcattacg gaaaaattcc gctaaagtat cagacgaaac catcaaaagc 360
agcaacacaa aaggcaagac aacaagcaga agcacggcag aaacagcctg cggaaaaaac 420
aacgcagaag cctaaagcga atgcgaataa acagcaaaac aatacaccag caaaagcaag 480
aaaacaggat gcggtagcag cgaacatgcc tggtggattt tccaacaacg atatcaggct 540
gcttgctcaa gcggtttatg gcgaagcccg gggcgagccg tacgaggggc aggttgctat 600
tgcagcagtc attttaaacc gtttgaacag cccgttattt ccaaattcag tagcgggggt 660
tatttttgag ccgcttgcct tcacagcagt agccgacgga caaatttaca tgcagccgaa 720
tgaaacggca cgagaagcag tgctggatgc catcaatggc tgggacccat cagaggaagc 780
actttactac tttaatccgg atacggctac aagtccgtgg atttgggggc gtccgcagat 840
taaaagaatc ggtaaacaca ttttctgtga gtag 874
<210> 2
<211> 429
<212> DNA
<213> Bacillus Subtilis
<400> 2
atggcggtcg tgagagcaac gagtgcggat gtcgatttga tggcaaggct gctcagagcg 60
gaagcggaag gcgaaggcaa gcaggggatg ctgcttgtcg gcaacgttgg aattaatcgg 120
ctgcgggcga attgctcaga ttttaaaggc ctccgcacca tcaggcagat gatttatcag 180
ccacacgcgt ttgaggctgt gactcatgga tatttttatc aaagggcgcg agatagcgag 240
cgtgcccttg cacgccggtc gattaatggt gaaaggcgct ggcctgcaaa atttagttta 300
tggtacttca ggccgcaggg ggactgtcca gcccagtggt ataaccagcc gtttgtggcc 360
agatttaagt cacactgctt ttatcagccg acggcggaga cgtgtgaaaa tgtatataac 420
acattttag 429
<210> 3
<211> 28
<212> DNA
<213> 人工合成
<400> 3
cgggatcccg ggggatgatg tggtcgag 28
<210> 4
<211> 31
<212> DNA
<213> 人工合成
<400> 4
actgactcac tcaaaaataa cccccgctac t 31
<210> 5
<211> 33
<212> DNA
<213> 人工合成
<400> 5
cgggatcccg ttctgaagta atgaaatatg atg 33
<210> 6
<211> 35
<212> DNA
<213> 人工合成
<400> 6
ctatggtgtg tgggaaaagc agtggactta aatct 35
<210> 7
<211> 35
<212> DNA
<213> 人工合成
<400> 7
cgggggttat ttttgagtga gtcagtcata gggag 35
<210> 8
<211> 28
<212> DNA
<213> 人工合成
<400> 8
cgggatcccg ggttgaggcc gttgagca 28
<210> 9
<211> 36
<212> DNA
<213> 人工合成
<400> 9
taagtcacac tgcttttccc acacaccata gcttca 36
<210> 10
<211> 30
<212> DNA
<213> 人工合成
<400> 10
cgggatcccg gttggtctcc agcttgcaaa 30
- 還沒有人留言評論。精彩留言會獲得點贊!