電解方法、電解槽、電解系統(tǒng)、用途和設(shè)備與流程
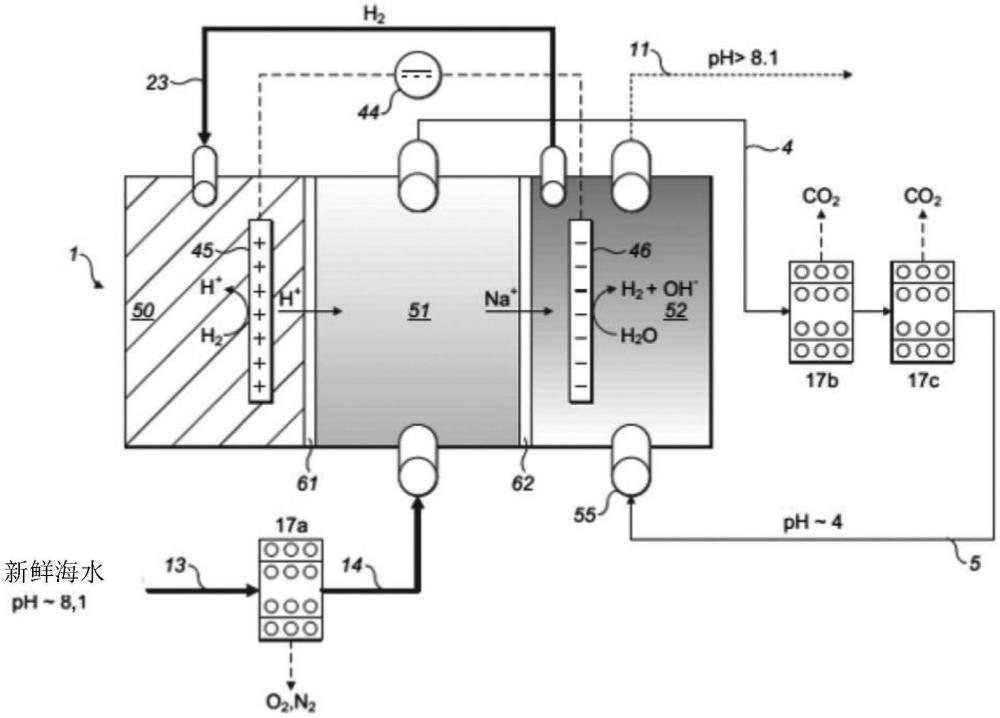
本發(fā)明涉及一種用于尤其從海水或含有二氧化碳的氣體、尤其是空氣或點(diǎn)源中提取二氧化碳的方法、一種用于二氧化碳提取的電解槽、一種包括這樣的電解槽的電解系統(tǒng)、這樣的電解槽在用于從海水或含有二氧化碳的氣體、尤其是空氣或點(diǎn)源中電解提取二氧化碳的設(shè)備中的用途,以及一種用于從海水中電解提取二氧化碳的設(shè)備。
背景技術(shù):
1、隨著大氣中二氧化碳的濃度增加以及由此引起的全球平均溫度的升高,用于從大氣中提取二氧化碳的系統(tǒng)變得越來越重要。除了從環(huán)境空氣中直接捕獲空氣(dac)之外,還存在從含碳酸鹽的水溶液、特別是海水中提取或回收二氧化碳的技術(shù)可能性。
2、電化學(xué)方法可以將水分解成堿性組分和酸性組分。在酸性環(huán)境中,化學(xué)平衡從經(jīng)向co2和h2o移動(參見下面的方程式(1))。
3、
4、用于將水分解成酸性流和堿性流的常見電化學(xué)方法通常使用一個(gè)或多個(gè)離子交換膜。這些膜選擇性地允許陽離子(cem)或陰離子(aem)穿過。另外,可以采用雙極性膜(bpm)來將含水體系分離成酸性(h+)流和堿性(oh-)流。
5、所謂的e-cem(電催化陽離子交換模塊)系統(tǒng)在電極之間設(shè)有兩個(gè)陽離子交換膜。在此,水流過所有三個(gè)分離的隔室。通過施加電壓,中間隔室中的質(zhì)子濃度由于h+離子的遷移而增加。因此,ph值降低,使得從溶液中提取co2成為可能。這樣的系統(tǒng)的能源消耗為約20,000kwh/t-co2。
6、與e-cem系統(tǒng)相比,雙極膜電滲析系統(tǒng)(bpmed)更節(jié)能,需要約920kwh/t-co2或1,400kwh/t-co2來從水溶液中提取co2。使用直接在陰極或陽極處循環(huán)的氧化還原活性電解質(zhì)流可以抑制氧化還原反應(yīng),諸如由h2o形成h2(her)和o2(oer)。優(yōu)選的電解質(zhì)包括含fe(ii)和fe(iii)離子的體系,諸如六氰合鐵(ii)酸鉀和六氰合鐵(iii)酸鉀,但是也可以使用其它化合物。在雙極性膜處,水分子被分解成酸性(h+)流和堿性(oh-)流。酸性流可被用于回收co2,而堿性流被用于堿化工藝用水。
7、迄今為止,根據(jù)現(xiàn)有技術(shù)水平從含水體系中回收co2的最高能源效率是使用電化學(xué)氫循環(huán)(ehl)來實(shí)現(xiàn)的。這種設(shè)置涉及三個(gè)隔室。陰極隔室充滿海水,在陰極處產(chǎn)生h2和oh-。所得氫氣被引導(dǎo)到陽極隔室中。在那里,h2被氧化成h+,并被轉(zhuǎn)移到中間隔室以酸化進(jìn)入的海水。
8、對于從海水中除去或回收二氧化碳的電化學(xué)方法,納米過濾通常是必需的。如果系統(tǒng)的某些部分諸如陰極隔室中存在高ph條件,則這可能導(dǎo)致二價(jià)鎂離子或鈣離子的礦物沉淀。這些離子是維持高海水堿度、從而維持再吸收大氣二氧化碳的能力所必需的。此外,被沉淀的礦物可能污染系統(tǒng),引起諸如電極結(jié)垢等問題,隨著時(shí)間的推移,這將增加能源成本。
9、納米過濾是一種高度復(fù)雜且昂貴的工藝,每處理一立方米水的運(yùn)營成本估計(jì)為0.20歐元。為了從溶解二氧化碳濃度為2.2mm的海水中以90%的效率提取一噸二氧化碳,將需要11477m3的水。該計(jì)算得出,對于提取一噸co2,僅納米過濾成本就為約2000歐元。
10、因此,本發(fā)明旨在減少或消除這些缺點(diǎn)。
技術(shù)實(shí)現(xiàn)思路
1、上述目的通過如獨(dú)立權(quán)利要求中所限定的發(fā)明來實(shí)現(xiàn)。
2、根據(jù)第一方面,本發(fā)明涉及一種用于二氧化碳提取的電解方法、特別是連續(xù)操作的電解方法,其包括以下步驟:
3、a)對氫氣進(jìn)行陽極氧化,以獲得酸性氧化產(chǎn)物;
4、b)用含堿性碳酸鹽的水溶液轉(zhuǎn)化酸性氧化產(chǎn)物,該含堿性碳酸鹽的水溶液特別地具有>7至9的ph,以獲得酸性水溶液;
5、c)從酸性水溶液中取出二氧化碳,以獲得二氧化碳?xì)怏w和經(jīng)脫氣的酸性水溶液;
6、d)對經(jīng)脫氣的酸性水溶液的酸性組分進(jìn)行陰極還原,以獲得陰極生成的氫氣和ph為10至≥7.1的堿性水溶液。
7、根據(jù)第二方面,本發(fā)明提供了一種用于二氧化碳提取的電解槽,其包括:
8、·陽極隔室,
9、·中間隔室,以及
10、·陰極隔室,其中
11、中間隔室布置在陽極隔室與陰極隔室之間;陽極隔室經(jīng)由第一輸送膜連接到中間隔室;
12、陰極隔室經(jīng)由第二輸送膜連接到中間隔室;
13、陽極隔室和陰極隔室經(jīng)由氫氣管線流體連接;
14、中間隔室具有入口和出口,出口流體連接到二氧化碳提取裝置,并且二氧化碳提取裝置經(jīng)由液體管線直接流體連接到陰極隔室的入口。
15、根據(jù)第三方面,本發(fā)明涉及一種電解系統(tǒng),其包括至少一個(gè)根據(jù)本發(fā)明的第二方面的電解槽。
16、根據(jù)第四方面,本發(fā)明涉及根據(jù)本發(fā)明的第二方面的電解槽在用于從海水中電解提取二氧化碳的設(shè)備中的用途。
17、根據(jù)第五方面,本發(fā)明涉及一種用于從海水中電解提取二氧化碳的設(shè)備,其包括根據(jù)本發(fā)明的第二方面的電解槽或根據(jù)本發(fā)明的第三方面的電解系統(tǒng)。
18、根據(jù)第六方面,本發(fā)明涉及根據(jù)本發(fā)明的第二方面的電解槽在用于從含有二氧化碳的氣體、特別是從空氣或點(diǎn)源中電解提取二氧化碳的設(shè)備中的用途。
19、根據(jù)第七方面,本發(fā)明涉及一種用于從含有二氧化碳的氣體、特別是從空氣或點(diǎn)源中電解提取二氧化碳的設(shè)備,其包括根據(jù)本發(fā)明的第二方面的電解槽或根據(jù)本發(fā)明的第三方面的電解系統(tǒng)。
20、本發(fā)明的技術(shù)效果
21、本發(fā)明的這些方面能夠?qū)崿F(xiàn)比先前用于二氧化碳電解提取的方法顯著更節(jié)能的工藝操作。另外,即使在二價(jià)陽離子的存在下,這些方面也減少了含碳酸鹽的溶液的礦物沉淀,特別是在陰極隔室中。這導(dǎo)致工藝操作更溫和,因?yàn)檠娱L了陰極維護(hù)間隔。這尤其是由于通過減少鈣和/或鎂的氫氧化物沉淀而減少了陰極材料的結(jié)垢。同時(shí),二價(jià)陽離子諸如mg2+和ca2+可以返回到海中,消除了對納米過濾器的需要。這通過允許經(jīng)由碳酸鹽進(jìn)一步吸收co2而具有生態(tài)學(xué)優(yōu)點(diǎn),并且通過消除對昂貴且維護(hù)密集的納米過濾器的需求而具有經(jīng)濟(jì)益處。此外,本發(fā)明允許不顯著偏離海水的ph值,例如約8.1。這避免了將來自電解的流出物排放到ph低于海水的海中。因此,本方法在ph方面對于海洋生態(tài)系統(tǒng)是有利的,因?yàn)樗苊饬撕Q笏峄?/p>
22、此外,利用本發(fā)明的這些方面可以改善從空氣中提取二氧化碳的能源效率,因?yàn)榭梢詫?shí)現(xiàn)更低的電壓。
23、通過本發(fā)明實(shí)現(xiàn)的技術(shù)效果的更多細(xì)節(jié)可以在詳細(xì)說明中找到。
24、定義
25、除非另有說明,否則本文所用的所有技術(shù)術(shù)語均對應(yīng)于普通專業(yè)人員的理解。
26、術(shù)語“二氧化碳提取”被廣義地理解為意指從含碳酸鹽的水溶液中除去氣態(tài)形式的二氧化碳,使用h+陽離子將碳酸鹽/碳酸氫鹽形式上轉(zhuǎn)化為碳酸二氫鹽,其分解成水和二氧化碳?xì)怏w,如以上方程式(1)所示。
27、術(shù)語“酸性”被廣義地理解為是指ph值<7的“酸性水溶液”。因此,“ph中性”是指ph值為7。
28、術(shù)語“堿性(alkaline/basic)”也被廣義地理解為是指ph值>7的“堿性水溶液”。
29、術(shù)語“ph值”對應(yīng)于普通技術(shù)人員的理解,并且可以用ph計(jì)測量。本文所公開的ph值可以例如使用voltcraft?pht-200ph值和氧化還原電位(orp)組合測量儀來測量。下面提供了該測量裝置的以下技術(shù)規(guī)范:
30、·測量范圍(mv):-1999至1999mv
31、·準(zhǔn)確度(mv):±0.5%
32、準(zhǔn)確度(ph):
33、±(0.02ph+2d)
34、自動溫度補(bǔ)償
35、是
36、操作溫度0至50℃
37、分辨率0.01
38、電源(細(xì)節(jié))
39、9v
40、尺寸(l?x?w?x?h)68x?30x?195mm重量
41、250g
42、高度:
43、195mm
44、長度:
45、68mm
46、寬度:
47、30mm
48、測定范圍(ph)
49、0-14ph
50、校準(zhǔn)
51、工廠標(biāo)準(zhǔn)(無證書)
52、顯示器
53、數(shù)字
54、接口
55、rs-232
56、測量功能
57、ph值
58、氧化還原(orp)
59、最大ph測量范圍
60、14ph
61、最小ph測量范圍
62、0ph
63、產(chǎn)品類型
64、組合測量裝置
65、指定的測量裝置按標(biāo)準(zhǔn)進(jìn)行出廠校準(zhǔn),并且可以另外用遞送中包括的ph緩沖溶液(ph=4和ph=7)進(jìn)行校準(zhǔn)。
66、術(shù)語“酸性氧化產(chǎn)物”被廣義地理解,并且不受特定理論的束縛,是指雙原子氫、特別是氫氣的氧化的形式質(zhì)子產(chǎn)物。該形式質(zhì)子產(chǎn)物可以作為h3o+(aq)溶劑化存在于水溶液中,cl-(aq)可能作為抗衡陰離子存在,和/或作為固體電極材料和/或固體膜材料的一部分存在,使得能夠經(jīng)由已知機(jī)制輸送形式質(zhì)子產(chǎn)物。除了氯化物之外,來源于酸諸如h2so4、hco3-、h2co3、h3bo3和hbr的其它抗衡陰離子在所有上述情況下也可以形式上存在。
67、術(shù)語“含碳酸鹽的水溶液”被廣義地理解,并且包括任何化學(xué)形式的碳酸鹽。“含碳酸鹽的水溶液”通常是堿性的,ph>7至9、>7至9.4,或>7至10。這意味著水溶液含有溶解的碳酸鹽(co32-)和/或碳酸氫鹽。“含碳酸鹽的水溶液”的實(shí)例是海水。含碳酸鹽的水溶液特別地含有二價(jià)陽離子,諸如鎂、鈣和/或鍶。此外,含碳酸鹽的水溶液還可以包含一價(jià)陽離子,諸如鈉。
68、術(shù)語“海水”與“鹽水”和“含鹽水”可互換且等同地使用,廣義上是指源自含鹽水體、特別是含鹽海諸如海洋的水溶液。當(dāng)然,精確的化學(xué)組成可以根據(jù)海水收集的位置而變化。例如,由kester,d.r.、duedall,i.w.、connors,d.n.和pytkowicz,r.m.(1967),preparation?of?artificial?seawater?archived?2008-12-17.limnology&oceanography,12,176–179)提供的組成,其通過引用并入,用作近似實(shí)例。根據(jù)該出版物,表1和表2作為海水組成的近似實(shí)例提供。
69、表1:海水中關(guān)于重量鹽的近似組成的信息。
70、重量鹽
71、 鹽 分子量 <![cdata[g?kg<sup>-1</sup>溶液]]> 氯化鈉(nacl) 58.44 23.926 <![cdata[硫酸鈉(na<sub>2</sub>so<sub>4</sub>)]]> 142.04 4.008 硫酸鉀(kcl) 74.56 0.677 <![cdata[碳酸氫鈉(nahco<sub>3</sub>)]]> 84.00 0.196 溴化鉀(kbr) 119.01 0.098 <![cdata[硼酸(h<sub>3</sub>bo<sub>3</sub>)]]> 61.83 0.026 氟化鈉(naf) 41.99 0.003
72、表2:海水中關(guān)于體積鹽的近似組成的信息。
73、體積鹽
74、 鹽 分子量 <![cdata[mol?kg<sup>-1</sup>溶液]]> <![cdata[氯化鎂(mgcl<sub>2</sub>.6h<sub>2</sub>o)]]> 203.33 0.05327 <![cdata[氯化鈣(cacl<sub>2</sub>.2h<sub>2</sub>o)]]> 147.03 0.01033 <![cdata[氯化鍶(srcl<sub>2</sub>.6h<sub>2</sub>o)]]> 266.64 0.00009
75、術(shù)語“經(jīng)脫氣的酸性水溶液”廣義上是指ph<7的水溶液,二氧化碳?xì)怏w已經(jīng)基本上完全從該水溶液中除去。這樣的經(jīng)脫氣的酸性溶液可以通過例如經(jīng)由膜接觸器從酸性水溶液中提取二氧化碳?xì)怏w來獲得。這種經(jīng)脫氣的酸性水溶液特別地保留了二價(jià)陽離子,諸如鎂和/或鈣。具體地,經(jīng)脫氣的酸性水溶液含有≤10wt%,優(yōu)選≤5wt%的二氧化碳,其中質(zhì)量百分比是基于在含堿性碳酸鹽的水溶液中作為碳酸鹽和/或碳酸氫鹽存在的二氧化碳的初始質(zhì)量。換句話說,分離效率為至少90%,優(yōu)選至少95%。
76、術(shù)語“酸性組分”一般是指含水形式的質(zhì)子,即h3o+(aq)。
77、術(shù)語“流體連接”被廣義地理解,特別是指兩個(gè)電解單元之間的連接,諸如管道,其被設(shè)計(jì)為將流體,諸如液體或氣體如氫氣,從一個(gè)電解單元輸送到另一個(gè)電解單元。這樣的電解單元可以包括陰極隔室、陽極隔室,或位于陽極隔室與陰極隔室之間的中間隔室。
78、術(shù)語“含有二氧化碳的氣體”被廣義地理解。特別地,這樣的氣體可以包括空氣。本領(lǐng)域技術(shù)人員熟悉給定位置處的空氣組成或了解測量該組成的方法。另外,“含有二氧化碳的氣體”也可以來源于點(diǎn)源。點(diǎn)源通常是co2的工業(yè)來源,其中工藝生成的二氧化碳?xì)怏w比正常存在于空氣中的更多。實(shí)例包括來自工業(yè)過程諸如水泥生產(chǎn)和/或煤燃燒的煙道氣。基于濕氣體的總體積,點(diǎn)源可以含有二氧化碳含量為約10mol%至25mol%、特別是14mol%至21mol%的氣體。這樣的氣體還可以具有約10vol%至20vol%的二氧化碳含量。總體而言,含有二氧化碳的氣體中的二氧化碳的質(zhì)量/體積/摩爾分?jǐn)?shù)對于本發(fā)明及其各方面的功能基本上是非關(guān)鍵的。
79、在圖4中舉例說明了從含有二氧化碳的氣體中捕獲二氧化碳的樣品工藝。對于co2吸收,可以考慮各種技術(shù)配置。例如,對于諸如在空氣中的低co2濃度,使用具有冷卻塔狀結(jié)構(gòu)的交叉流方法將氣體暴露于堿性溶劑可能是有利的。對于較高的co2濃度,諸如在來自工業(yè)過程的煙道氣中,使用逆流原理使氣體和堿性水溶液接觸的塔在技術(shù)上和經(jīng)濟(jì)上可能更合適。此外,含碳酸鹽的水溶液還可以包含一價(jià)陽離子,諸如鈉。含碳酸鹽的水溶液可以特別地或排他地含有一價(jià)陽離子,諸如鈉或鉀。這些一價(jià)陽離子可以例如與選自硫酸根、高氯酸根、硝酸根、碘離子或其組合的抗衡陰離子配對。具體地,溶解的鹽可以選自na2so4、k2so4、naclo4、kclo4、nano3、kno3、nai、ki。術(shù)語“含堿性碳酸鹽的水溶液”與“含碳酸鹽的水溶液”等同地使用。
- 還沒有人留言評論。精彩留言會獲得點(diǎn)贊!