白頭翁皂苷B4在制備治療疼痛的藥物中的應用的制作方法
本發明屬于藥物用途技術,具體涉及白頭翁皂苷b4在制備治療疼痛的藥物中的應用。
背景技術:
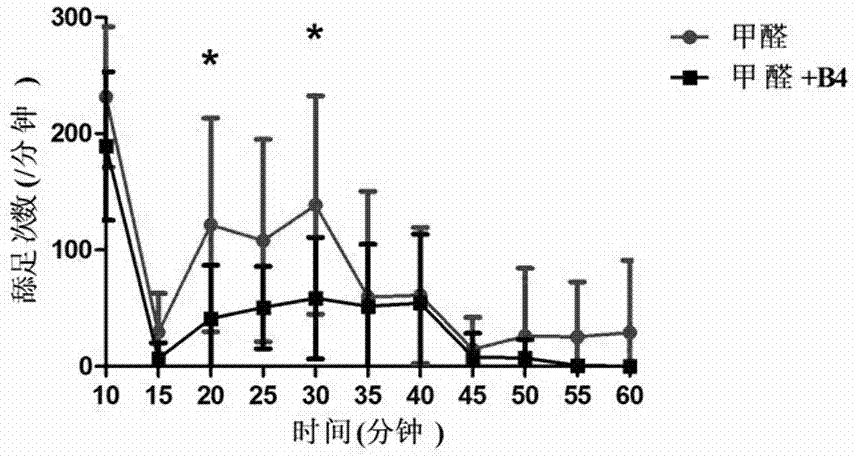
:疼痛是一種不愉快的感覺,是伴有實際或潛在組織損傷的情緒體驗,是臨床上最常見的癥狀,會給患者造成多方面的損害,嚴重影響人們的生活質量,目前疼痛仍是困擾病人的一個常見問題。疼痛可分為多種。按疼痛的部位,可分為淺表痛、深部痛和牽涉痛,例如由機械性、化學性、物理性的不良刺激引起皮膚和黏膜部位的疼痛。深部痛是指內臟、胸膜、關節、腹膜等部位受刺激而產生的疼痛。常表現為灼痛,不呈局限性。牽涉痛是指深部痛表現為遠離病灶的淺表痛,如膽囊炎表現為右肩痛。此外,按疼痛起因分為炎癥性痛、神經病理性痛、癌痛、創傷性疼痛等,按疼痛程度可分為輕度痛、中度痛、重度痛、極度痛等。持續的疼痛嚴重影響人們的生活質量,給患者帶來痛苦,可導致患者的抑郁、情緒低落。據統計,全世界人口1/3以上遭受著持續或反復發作的疼痛折磨。導致疼痛的原因很多,目前疼痛機制研究比較多,但是疼痛的機制還不是很清楚。疼痛根據其神經生理學機制可分為感受性疼痛和神經病理性疼痛兩類,前者直接由傷害性刺激引起,與組織損傷有關;后者由軀體感覺神經系統的損傷或疾病直接造成的慢性疼痛。目前,大家比較關心的還有癌性疼痛,有75%~95%的晚期癌和轉移癌患者都有癌癥疼痛。癌癥誘導的骨疼痛(簡稱骨癌痛)是癌癥疼痛的典型代表,是一種獨特的疼痛狀態,嚴重影響癌癥患者的生活質量,目前尚缺乏有效的治療手段。腫瘤組織壓迫并侵蝕鄰近的感覺神經,腫瘤細胞及相關免疫細胞釋放一系列因子致敏外周傷害性感受器,腫瘤導致的骨質破壞和局部缺血、缺氧的微環境是骨癌痛形成的起始因素,在這些因素的持續刺激下中樞神經系統也被致敏,并對骨癌痛的維持起重要作用。臨床上癌癥疼痛主要表現為:持續的進行性的背景痛(ongoingpain)、突破痛(beakthroughpain)和痛覺異常。骨癌痛的治療藥物包括非類固醇類藥、阿片類藥物、二膦酸鹽類藥物和其他尚在開發中的藥物等。此外,在各種類型的病理性疼痛中,神經性疼痛(neuropathiepain)被視為最難攻克的難題。神經性疼痛是指由神經系統受損或功能失調引起的病理性疼痛。主要表現為:1)自發性疼痛,如外傷、腫瘤、燒傷、病毒感染、糖尿病和化療藥物等多種原因引起神經損傷,從而引起的疼痛;2)痛敏,就是痛反應增強;3)痛超敏,指痛閾顯著下降。外周和中樞機制共同參與神經病理痛的發生。外周神經損傷后,早期的異位放電不僅是早期急性痛的重要原因。并且這些異位放電不斷轟擊脊髓背角等中樞部位.誘發產生脊髓背角長時程增強等中樞敏化現象,中樞敏化和下行易化系統的激活等中樞機制在神經病理痛后期維持中起到重要作用。關節疼痛是一種常見的疼痛疾病,其基本病理改變為多種致病因素引起的進行性關節軟骨變性、破壞及喪失,關節軟骨及軟骨下骨邊緣骨贅形成,由此引起關節疼痛、僵硬、腫大、畸形及功能障礙,其中關節疼痛為最突出的癥狀。隨著病情的進展,疼痛呈輕度至中度間歇性疼痛,最后發展成為持續性疼痛。關節疼痛的機制是復雜的,包括支配關節的a8和c纖維具有小的感受野,可以被關節的傷害性刺激所激活,這些感受器能夠感受關節的機械刺激,也能感受關節的化學刺激。此外,關節內還有一些其他的神經纖維,不能夠被正常的傷害性刺激所激活,稱之為靜止感受器,只有在關節內損傷已經形成,才能被激活并應答、敏化,從而形成痛敏。此外,伴隨外周損傷,導致神經中樞敏化包括活化、調控以及修飾,因此關節疼痛是一個復雜的過程。目前治療疼痛的藥物有兩大類,包括以阿片類藥物(麻醉性緩解疼痛藥)和非甾體類藥為主。阿片類藥物作用于中樞神經系統,有強大的緩解疼痛作用,臨床上主要用于癌性疼痛和其他各種銳痛的治療。然而,因其成癮性而在臨床應用受到很大的限制。非甾體類緩解疼痛藥是具有解熱、緩解疼痛,但是長期大量使用會產生嚴重的不良反應,包括胃腸道反應、肝腎毒性、引發心血管系統疾病和出血傾向。因此,選擇性高、安全性好、副作用小的新型緩解疼痛藥物的研究和開發日益成為醫藥界研究的熱點。目前,上市用于臨床治療和臨床實驗中的緩解疼痛藥物還包括(1)激肽受體抑制劑類,包括緩激肽和胰激肽受體抑制劑以及速激肽受體拮抗劑,這類藥物具有高效、長效緩解疼痛作用,并且在鎮咳、止吐等方面也有良好的開發前景;(2)選擇性環氧化酶抑制劑。代表藥物有替尼達普,一種脂氧合酶-環氧合酶雙效抑制劑;(3)no合酶抑制劑,如7-硝基吲唑,此藥對血壓、血管平滑肌無影響;(4)辣椒素衍生物。目前,臨床已局部應用辣椒素緩解疼痛,如乳房切除后疼痛等,但因其燒灼感而限制了應用。白頭翁為毛莨科植物白頭翁(pulsatillachinensis(bunge)regel)的干燥根,始載于《神農本草經》。是中醫治療熱毒血痢的臨床常用藥,尤善清大腸濕熱及血分熱毒。目前對白頭翁化學成分、藥理作用、含量測定等已有較為廣泛的研究。現代藥理研究發現白頭翁具有增強免疫功能、抗腫瘤、抗病原微生物、抗寄生蟲、保肝、毒性及治療內毒素血癥等作用。白頭翁的化學成分研究始于60年代初,共分得了約19種成分,主要為皂苷和內酯等成分,目前認為白頭翁的有效化學成分主要為三萜皂苷。最近的研究表明白頭翁皂苷元(23-羥基白樺酸)具有最有效的抗黑色素瘤作用,低糖基白頭翁皂苷能促進皮膚膠元蛋白合成及抗自由基氧化,故可將其應用于皮膚抗老化化妝品行業及保健食品行業。白頭翁主要有效成分為皂苷類成分,其中白頭翁皂苷b4為其主要代表。近年來對于b4的化學結構及含量測定的研究居多,對于其藥理活性卻知之甚少。近年也已有關于白頭翁皂苷b4抗肝癌的研究,但對白頭翁皂苷b4的疼痛作用尚未有文獻報道。技術實現要素:本發明公開了白頭翁皂苷b4在治療疼痛中的應用。為達到上述發明目的,本發明采用如下技術方案:白頭翁皂苷b4在制備治療疼痛的藥物中的應用。本發明還公開了一種治療疼痛的藥物,其活性成份為白頭翁皂苷b4。上述技術方案中,所述治療疼痛的藥物還包括藥物輔料。本發明還公開了一種治療疼痛的藥物的制備方法,將白頭翁皂苷b4與藥物輔料混合,制備治療疼痛的藥物。白頭翁皂苷b4在制備治療足腫脹的藥物中的應用。白頭翁皂苷b4在制備提高痛閾值的藥物中的應用。白頭翁皂苷b4在制備減輕踝關節變形和滑膜組織異常增生的藥物中的應用。本發明還公開了一種治療疼痛的試劑,包括白頭翁皂苷b4、藥物輔料以及包裝瓶。本發明的藥物為片劑、丸劑、滴丸劑、膠囊劑、顆粒劑、散劑、涂劑、巴布劑、噴霧劑或注射劑。本發明藥物的劑量為0~60mg/kg,且不含0,優選5~60mg/kg。本發明采用小鼠醋酸扭體法,觀察給藥后不同劑量組的小鼠扭體次數,采用福爾馬林誘導的小鼠疼痛模型,觀察舔足時間和次數,采用大鼠完全弗氏佐劑誘導模型,通過熱板實驗,足趾容積,機械性痛閾測定,病理學檢查等測定進行觀察。結果表明在小鼠醋酸扭體實驗中,與造模組比較,白頭翁皂苷b4各劑量組的小鼠扭體次數明顯減少,b4低劑量組(12.5mg/kg)的數據具有統計學意(p<0.05),b4中劑量組(25mg/kg)的扭體次數減少有顯著性差異(p<0.01),b4高劑量(50mg/kg)的扭體次數減少具有非常顯著性差異(p<0.001),并且與陽性對照組(aspirin)相比,扭體次數也明顯減少,具有顯著性差異(p<0.01);在福爾馬林誘導的疼痛模型中,白頭翁皂苷b4(50mg/kg)減少小鼠的舔足時間和次數(p<0.05);白頭翁皂苷b4(6.25mg/kg)抑制大鼠的關節腫脹,降低足體積腫脹度(p<0.05)和痛閾值(p<0.05),病理切片顯示白頭翁皂苷b4減輕踝關節的變形和滑膜組織的異常增生,并減少細胞浸潤。在小鼠熱板實驗中,b白頭翁皂苷4(12.5mg/kg)能提高小鼠的痛閾。總之,白頭翁皂苷b4對醋酸所致小鼠扭體模型,熱輻射痛模型,福爾馬林誘導的小鼠疼痛模型和大鼠疼痛模型具有良好的緩解疼痛作用。附圖說明圖1白頭翁皂苷b4對醋酸所致小鼠扭體反應的影響;圖2為小鼠甲醛模型的舔足次數的變化圖;圖3為小鼠甲醛模型的兩相中舔足次數的變化圖;圖4為小鼠甲醛模型的兩相中舔足時間的變化圖;圖5為15d各組大鼠足腫脹情況比較圖;圖6為白頭翁皂苷b4對弗氏佐劑模型大鼠足體積的影響圖;圖7為白頭翁皂苷b4對熱板實驗的小鼠痛閾提高率的影響圖;圖8為各組大鼠機械痛閾的變化圖;圖9為大鼠踝關節與膝關節滑膜組織病理切片情況圖;圖10為小鼠熱輻射甩尾實驗痛閾提高百分率圖。具體實施方式白頭翁皂苷b4(純度為99.8%),由蘇州大學天然藥物化學課題組分離純化而得;完全弗氏佐劑cfa(其含有在液體石蠟中的10mg/ml熱滅活的結核分枝桿菌),每支10ml,sigma公司產品;冰乙酸:純度99.5%,江蘇強盛功能化學股份有限公司,批號20160601;甲醛:國藥集團化學試劑有限公司,含量37-40%,批號20161011。el204電子天平,梅特勒-托利多儀器(上海)有限公司生產;pv-200足趾容積測量儀,成都泰盟科技有限公司生產;rb-200智能熱板儀,成都泰盟科技有限公司生產;vonfreyfilaments纖毛機械刺激絲。觀察指標足體積測量造模成功后,每天腹腔注射b4給藥,在第6h,1天,2天,3天,11天,13天,15天,17天和19天給藥后1h測量大鼠足腫脹,根據容積排水法原理在足容積測量儀上測定足體積,求出腫脹度(δml=腫脹后關節體積-腫脹前關節體積)。熱板實驗(20±2)℃室溫條件下,置大鼠于(55±0.5)℃的熱板測痛儀上,以大鼠舔后足作為痛反應的指標,大鼠接觸熱板至舔后足所經歷的時間為痛閾值;造模前兩天每天測量痛閾值,取平均值作為給藥前(基礎)痛閾值。在第6h,1天,2天,3天,11天,13天,15天,17天和19天測量給藥后1h各大鼠的痛閾值,并計算各大鼠給藥前后痛閾值的差值(基礎痛閾值-給藥后痛閾值),痛閾提高率=[(基礎痛閾值-給藥后痛閾值)/基礎痛閾值]×%。機械性痛閾測定纖毛機械刺激絲法檢測痛閾是較常用的慢性疼痛模型檢測方法。檢測時,將大鼠置于塑料板隔開的單獨空間內,底部是鐵制網格結構。在安靜環境下,將大鼠置于疼痛檢測架上,用透明鼠籠約束大鼠,適應10min后,使用vonfreyfilaments纖毛機械刺激絲,刺激大鼠的后足,每次測評均從輕到重(1.2,1.4,2.0,4.0,6.0,8.0,10,12,15,26和50g)觸壓后足的足底表面,當vonfreyfilaments纖毛機械刺激絲彎曲90°,大鼠仍然不抬足,視為無反應,以刺激開始6s內出現躲避或抬足記為陽性反應。每次刺激持續3s,間隔15s,連續5次。若3次不抬足,換用更高克數的纖毛;若5次中有3次抬足,則返回下一克數的纖毛,直到每5次測試中有3次抬足。能夠引起3/5次抬足的最低vonfrey纖毛克數被定義為機械痛閾值(mwt)。先提前1天測量基礎值,然后在第6,24,48,72h,11天,13天,15天,17天和19天測量機械痛閾值(mwt),并計算痛閾差值。組織病理檢查第21天脫頸處死大鼠,解剖對照組、弗氏佐劑誘導模型組、b4給藥組大鼠,取右后足的膝關節滑膜組織和踝關節,并保持關節完整。置于多聚甲醛固定液中固定至少24h,然后脫鈣2-3天。脫鈣完全后,將整個踝關節縱向切為4μm切片,膝關節滑膜橫切。石蠟包埋切片,he染色,在光鏡下觀察細胞浸潤,滑膜增生及關節破壞情況。熱輻射甩尾實驗(20±2)℃室溫條件下,輕輕將小鼠置于熱輻射甩尾儀上,以小鼠甩尾作為痛反應的指標,小鼠接觸熱輻射甩尾儀的輻射熱刺激至甩尾所經歷的時間為痛閾值;計算各大鼠給藥前后痛閾值的差值(基礎痛閾值-給藥后痛閾值),痛閾提高率=[(基礎痛閾值-給藥后痛閾值)/基礎痛閾值]×%。統計學處理所有數據表示為平均值±標準差,統計分析使用spss13.0統計軟件分析結果。單因素方差分析用于確定各實驗組值之間的統計學顯著性差異。p<0.05為有統計學意義。實施例一18-22g的icr小鼠50只,合格證號:scyk(蘇)2013-0003,隨機分為4組,即醋酸扭體模型組,b4低劑量組(12.5mg/kg),中劑量組(25mg/kg)和高劑量組(50mg/kg),陽性對照組。給藥組的給藥劑量分別為12.5mg/kg,25mg/kg,50mg/kg。陽性對照藥物為阿司匹林。小鼠提前適應實驗室環境1天,給藥組小鼠提前1h腹腔注射白頭翁皂苷b4,造模組給予等量生理鹽水,腹腔注射0.6%-1%醋酸溶液,觀察并記錄各鼠在20min內扭體次數。小鼠扭體表現為伸展后肢、腹部內凹和臀部抬高。圖1白頭翁皂苷b4對醋酸所致小鼠扭體反應的影響(***與造模組相比,p<0.001;**與造模組相比,p<0.01;*與造模組相比,p<0.05),與造模組相比,白頭翁皂苷b4各劑量組的小鼠扭體次數明顯減少,尤其是本發明的技術方案與現有成熟臨床藥物陽性對照組(aspirin)的扭體次數相當甚至減少;結果顯示白頭翁皂苷b4有較強的緩解疼痛作用。實施例二19-21g清潔級的icr雄性小鼠32只,合格證號:scyk(蘇)2013-0003,隨機分為甲醛造模組和b4給藥組(50mg/kg)。所有實驗動物均由昭衍(蘇州)新藥研究中心有限公司提供。19-21g的icr雄性小鼠適應實驗室環境3天。分為造模組和b4給藥組(50mg/kg),實驗前把小鼠放入觀察籠(10×20×15cm)內適應環境1h,從觀察籠內取出。用25μl微量注射器在小鼠右后足趾皮下注射20μl的2%甲醛溶液,立即放入觀察籠內觀察舔足時間和次數。產生一種明顯的自發性痛行為反應,即右后足表現出縮腿、舔爪及顫抖等反應,觀察1h,分為12個時間段,每5min為一個時間段,記錄小鼠舔足時間,作為疼痛指標。把觀察得到的小鼠實驗數據分為2個時間段處理:0-10min時間段為第一相,這個時間段實驗小鼠感受急性疼痛的時間段,15-55min時間段為第二相。在小鼠右后足趾皮下注射20μl的2%甲醛溶液后,小鼠產生舔足反應在第1相(0-10min)中立即發生雙相傷害感染行為,結果見圖2-4,圖2為小鼠甲醛模型的舔足次數的變化,圖3為小鼠甲醛模型的兩相中舔足次數的變化,圖4為小鼠甲醛模型的兩相中舔足時間的變化。與造模組比較,b4給藥組(50mg/kg)舔足次數和時間逐漸減少;在第2相(15-55min)中b4給藥組(50mg/kg)的舔足次數明顯減少(p<0.05)(見圖3),舔足時間有一定程度減少(見圖4)。實施例三年齡4-6周的清潔級雌性sd大鼠20只,合格證號:scyk(蘇)2013-0003,體重180-210g,隨機分為3組,即空白對照組8只,完全弗氏佐劑誘導的模型組,白頭翁皂苷b4給藥組(6.25mg/kg),每組6只。給藥組提前2天腹腔注射白頭翁皂苷b4,每天1次。第0天給藥后1h開始造模,除對照組足趾皮下注射0.1ml生理鹽水外,其他組通過在右后足跖皮下單次注射0.1mlcfa(其含有在液體石蠟中的10mg/ml熱滅活的結核分枝桿菌);足爪腫脹,表現為對側后肢和雙前肢足爪腫脹,進行性加重,耳和尾部出現結節和紅斑,提示弗氏佐劑誘導模型誘導成功。對照組和弗氏佐劑誘導模型組給生理鹽水,給藥組大鼠腹腔注射白頭翁皂苷b4,均每天1次,連續腹腔注射21天。白頭翁皂苷b4給藥組的劑量為6.25mg/kg。在第6h,1天,2天,3天,11天,13天,15天,17天和19天給藥后1h觀察足腫脹,熱板實驗和機械絲痛閾三項指標。完全弗氏佐劑模型大鼠的足腫脹一般變化情況為:足腫脹程度在第3天時達到峰值,屬于急性期;之后開始消退,而后在第14天足腫脹度又開始增大達到另一個峰值,然后慢慢消腫。除正常對照組外,其余2組大鼠在第0天注射0.1mlcfa之后,在第1天時右后足明顯腫脹,造模后的足體積測量實驗顯示造模成功;第3天后可見b4給藥組(6.25mg/kg)中大鼠足腫脹逐漸消退,該組大鼠在第15天后足腫脹更是明顯消腫,具有緩解疼痛的效果。第15天各組大鼠足腫脹情況見圖5,a:正常組;b:造模組;c:b4給藥組(6.25mg/kg)。在第6h,1天,2天,3天,11天,13天,15天,17天和19天,正常對照組、完全弗氏佐劑誘導模型組、白頭翁皂苷b4給藥組(6.25mg/kg)的大鼠足體積的比較見圖6;b4給藥組(6.25mg/kg)的大鼠足體積與模型組相比明顯減小,說明b4給藥組(6.25mg/kg)抑制大鼠足腫脹。從第11天開始到19天b4給藥組(6.25mg/kg)大鼠右后足體積與造模組相比有顯著性差異(p<0.01),而且在第11天的數據有非常顯著性差異(p<0.001)。從表1中可看出,第19天造模組大鼠的足體積大于正常大鼠,說明完全弗氏佐劑誘導模型在實驗期間造模成功,且從造模第2天起發現白頭翁皂苷b4給藥組(6.25mg/kg)抑制足腫脹,腫脹度減小。表1造模后19d各組大鼠右后足關節腫脹度的變化(`x±s)組別劑量(mg/kg)足腫脹體積(△ml)正常-0.18±0.19弗氏佐劑誘導模型-0.92±0.19###b46.250.43±0.18**注:###與正常對照組相比,p<0.001,**與造模組相比,p<0.01。第6h,1天,2天,3天,11天,13天,15天,17天和19天的熱板實驗結果見表2和圖7。與造模組比較,白頭翁皂苷b4給藥組(6.25mg/kg)大鼠給藥后從第13天開始明顯抑制熱板所致大鼠疼痛反應,延長動物痛閾值。痛閾提高率變化情況見圖7,b4給藥組(6.25mg/kg)的大鼠在第15、17天的痛閾提高率相對完全弗氏佐劑誘導模型組具有統計學意義(p<0.05),而第13、19天的痛閾提高率有顯著性差異(p<0.01)。表2造模后19d白頭翁皂苷b4對熱板刺激的影響(`x±s)組別劑量(mg/kg)痛閾差值(s)痛閾提高率(%)正常_0.05±2.700.05±0.30弗氏佐劑誘導模型_-4.87±3.73#-0.44±0.14#b46.25-1.13±4.000.08±0.19*注:#與正常對照組相比,p<0.05;*與造模組相比,p<0.05。第6h,1天,2天,3天,11天,13天,15天,17天和19天的機械絲痛閾值結果見圖8。由圖8可知,弗氏佐劑誘導模型組大鼠機械痛閾值逐漸降低,與對照組相比差異有統計學意義(p<0.05);在第2、11、19天b4給藥組(6.25mg/kg)與模型組比較,明顯延長痛閾值,其差異有統計學意義(p<0.05)。結果表明白頭翁皂苷b4給藥組(6.25mg/kg)具有緩解疼痛作用。各組動物的踝關節病理學檢查結果顯示,正常對照組中滑膜襯里層是由1~2層滑膜細胞及滑膜下層組成,無明顯細胞浸潤;弗氏佐劑誘導模型組踝關節病理切片可見關節軟骨變薄不明顯;但是白頭翁皂苷b4給藥組(6.25mg/kg)的踝關節結構保持完整,無明顯軟骨破壞,滑膜無明顯增生。弗氏佐劑誘導模型組膝關節的滑膜組織細胞明顯浸潤,滑膜異常增生,血管擴張;白頭翁皂苷b4給藥組(6.25mg/kg)滑膜病理改變較模型組明顯減輕,滑膜細胞層增生程度減弱,細胞浸潤明顯減少。說明白頭翁皂苷b4減輕踝關節的變形和滑膜組織的異常增生,并減少細胞的浸潤(見圖9,踝關節比較:①正常對照組;②弗氏佐劑誘導模型組;③b4給藥組(6.25mg/kg)。滑膜組織比較:④正常對照組;⑤弗氏佐劑誘導模型組;⑥b4給藥組(6.25mg/kg)。圖10所示為小鼠熱輻射甩尾實驗結果,生理鹽水對照組給生理鹽水后,痛閾沒有改變。b4給藥組(6.25mg/kg)腹腔注射2小時后,與生理鹽水組相比,痛閾明顯提高,陽性對照抗炎藥地塞米松不能提高小鼠的痛閾,無法起到鎮痛作用。當前第1頁12
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1