DLL3抗原結合構建體的制作方法
本文中的實施方式涉及抗原結合構建體、微抗體(minibodies)和cys-雙抗體(cys-diabodies)。具體地,dll3特異性抗原結合構建體、微抗體和cys-雙抗體。
背景技術:
1、delta樣蛋白3(δ樣蛋白3,dll3)是notch信號轉導通路的抑制蛋白。dll3在小細胞肺癌(sclc)和其他高級別內分泌腫瘤的細胞表面上表達。
技術實現思路
1、本文中的實施方式涉及抗原結合構建體、微抗體和cys-雙抗體。一些實施方式是dll3特異性抗原結合構建體、微抗體和cys-雙抗體。本文中的一些實施方式涉及包含dll3特異性抗原結合構建體、微抗體和cys-雙抗體的治療劑、制劑和組合物。本文中的一些實施方式涉及使用本文所公開的抗原結合構建體、微抗體和cys-雙抗體治療dll3相關疾病或病癥的方法。
2、本文提供了抗原結合構建體,所述抗原結合構建體包含:包含下列的輕鏈可變(vl)結構域:作為seq?id?no:15的lcdr1;作為seq?id?no:19、21或23中任一項的lcdr2;作為seq?id?no:25的lcdr3;和/或包含下列的重鏈可變(vh)結構域:作為seq?id?no:27的hcdr1;作為seq?id?no:29的hcdr2;和作為seq?id?no:31的hcdr3。
3、本文提供了結合至dll3的微抗體,所述微抗體包含:結合至dll3的單鏈可變片段(scfv);包含鉸鏈區的鉸鏈-延伸結構域;和igg?ch3序列,所述scfv包含與重鏈可變(vh)結構域連接的輕鏈可變(vl)結構域,所述vl結構域包含:作為seq?id?no:15的lcdr1;作為seqid?no:19、21或23中任一項的lcdr2;作為seq?id?no:25的lcdr3;且所述vh結構域包含:作為seq?id?no:27的hcdr1;作為seq?id?no:29的hcdr2;作為seq?id?no:31的hcdr3。
4、本文提供了結合至dll3的cys-雙抗體,所述cys-雙抗體包含多肽,所述多肽包含:單鏈可變片段(scfv),所述單鏈可變片段包含與重鏈可變(vh)結構域連接的輕鏈可變(vl)結構域;并且所述vl結構域包含:作為seq?id?no:15的lcdr1;作為seq?id?no:19、21或23中任一項的lcdr2;作為seq?id?no:25的lcdr3;且所述vh結構域包含:作為seq?id?no:27的hcdr1;作為seq?id?no:29的hcdr2;和作為seq?id?no:31的hcdr3。
5、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述vl結構域還包含seq?id?no:35或37所示的lfr2。
6、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體;其中所述vl結構域包含與seq?id?no:48中的vl結構域具有至少90%同一性的氨基酸序列;并且其中所述抗原結合構建體、微抗體或cys-雙抗體包含y50d和/或y55n突變(kabat)。
7、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體;其中所述vl結構域包含與seq?id?no:48中的vl結構域具有至少90%同一性的氨基酸序列;并且其中所述抗原結合構建體、微抗體或cys-雙抗體包含a43s和/或q45r突變(kabat)。
8、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體;其中所述vl結構域包含與seq?id?no:49中的vl結構域具有至少90%同一性的氨基酸序列,并且其中所述抗原結合構建體、微抗體或cys-雙抗體包含y50d和/或y55n突變(kabat)。
9、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體;其中所述vl結構域包含與seq?id?no:49中的vl結構域具有至少90%同一性的氨基酸序列;并且其中所述抗原結合構建體、微抗體或cys-雙抗體包含a43s和/或q45r突變(kabat)。
10、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體;其中所述抗原結合構建體、微抗體或cys-雙抗體還包含作為seq?id?no:45的信號肽。
11、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體;其中所述抗原結合構建體、微抗體或cys-雙抗體包含作為seq?id?no:39-44中任一項的接頭。
12、根據以上實施方式中任一項所述的抗原結合構建體或微抗體;其中所述ch3結構域是igg?ch3結構域。
13、根據以上實施方式中任一項所述的抗原結合構建體或微抗體;其中所述igg?ch3結構域是igg1、igg2、igg3或igg4?ch3結構域。
14、根據以上實施方式中任一項所述的抗原結合構建體或微抗體;其中所述igg?ch3結構域包含作為seq?id?no:65-68中任一項的igg1?ch3結構域。
15、根據以上實施方式中任一項所述的抗原結合構建體或微抗體;其中所述igg?ch3結構域包含作為seq?id?no:69-71中任一項的igg1?ch3結構域。
16、根據以上實施方式中任一項所述的抗原結合構建體或微抗體;其中所述igg?ch3結構域包含作為seq?id?no:72-82中任一項的igg1?ch3結構域。
17、根據以上實施方式中任一項所述的抗原結合構建體或微抗體;其中所述igg?ch3結構域包含作為seq?id?no:83-85中任一項的igg1?ch3結構域。
18、根據以上實施方式中任一項所述的抗原結合構建體,其中所述抗原結合構建體是抗體。
19、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體特異性結合至dll3。
20、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,還包含可檢測標志物。
21、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物是熒光可檢測標志物。
22、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物包含光療相容性染料(phototherapy?compatibledye)。
23、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物與采用硼中子俘獲療法(boron?neutron?capture?therapy,bnct)的用途相容。
24、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物是放射性標記。
25、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物是α發射體放射性標記。
26、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物是β發射體放射性標記。
27、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物是正電子發射體放射性標記(positron-emitter?radiolabel)。
28、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物是γ發射體放射性標記。
29、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物包含镥-177。
30、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物適合用于俄歇電子能譜法(auger?electron?spectroscopy)。
31、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物包含同位素。
32、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物包含生物發光化合物。
33、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物包含化學發光化合物。
34、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物包含酶。
35、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物包含金屬螯合劑。
36、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體還包含治療劑。
37、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述治療劑包含治療性同位素或離子。
38、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述治療劑是放射性標記。
39、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述治療劑是α發射體放射性標記。
40、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述治療劑是β發射體放射性標記。
41、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述治療劑是正電子發射體放射性標記。
42、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述治療劑是γ發射體放射性標記。
43、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述治療劑包含镥-177。
44、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述治療劑包含光療相容性染料。
45、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述治療劑包含硼。
46、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述治療劑與采用硼中子俘獲療法(bnct)的用途相容。
47、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可檢測標志物和/或治療劑包含毒性有效載荷(payload)。
48、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體是雙重特異性的。
49、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體包含一價scfv。
50、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,從所述多肽的n末端至c末端為vl,vh。
51、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述可變結構域的順序,從所述多肽的n末端至c末端為vh,vl。
52、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述微抗體是人源化抗原結合構建體、微抗體或cys-雙抗體。
53、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述人源化抗原結合構建體、微抗體或cys-雙抗體包含:作為seq?id?no:15的lcdr1;作為seq?id?no:19、21或23中任一項的lcdr2;作為seq?id?no:25的lcdr3;作為seq?id?no:27的hcdr1;作為seq?id?no:29的hcdr2;和作為seq?id?no:31的hcdr3。
54、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述vl結構域還包含seq?id?no:35或37所示lfr2的lfr2。
55、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中與包含seq?id?no:1的抗原結合構建體、微抗體或cys-雙抗體相比,所述抗原結合構建體、微抗體或cys-雙抗體在哺乳動物細胞中具有提高的表達得率(表達產率,expressionyield)。
56、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中與包含seq?id?no:1的抗原結合構建體、微抗體或cys-雙抗體相比,所述抗原結合構建體、微抗體或cys-雙抗體具有約75%至300%、75%至200%、75%至150%或者75%至100%之間的表達得率。
57、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中與包含seq?id?no:1的抗原結合構建體、微抗體或cys-雙抗體相比,所述抗原結合構建體、微抗體或cys-雙抗體具有約75%、80%、85%、90%、95%、100%、105%、110%、115%、120%、125%、150%、175%、200%、250%或300%的表達得率,或者在以上值中任意兩個所限定的范圍內的百分比(例如,約75-300%、約80-250%、約100%-300%、約110%-250%、約120%-200%等)。
58、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體在受試者的血液、肝臟、腎臟、脾臟、肺臟、肌肉、骨骼、心臟、胃、小腸、大腸、胰臟、腫瘤或其中任意組合中積累至可檢測的水平。
59、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述受試者是哺乳動物。
60、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體在、在約或者在至多約0.1%、0.5%、1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、15%、20%、25%、30%或35%?id/g,或者在以上值中任意兩個所限定的范圍內的百分比是可檢測的。
61、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體在約0.1%至35%、0.1%至30%、1%至35%、1%至30%、5%至35%或5%至30%?id/g之間是可檢測的。
62、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體包含seq?id?no:35或37所示lfr2的lfr2;并且其中與包含作為seq?id?no:33所示lfr2的lfr2的抗原結合構建體、微抗體或cys-雙抗體相比,所述抗原結合構建體、微抗體或cys-雙抗體具有改善的生物分布。
63、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體的kd小于約1×10-10m。
64、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體的kd小于約1×10-12m。
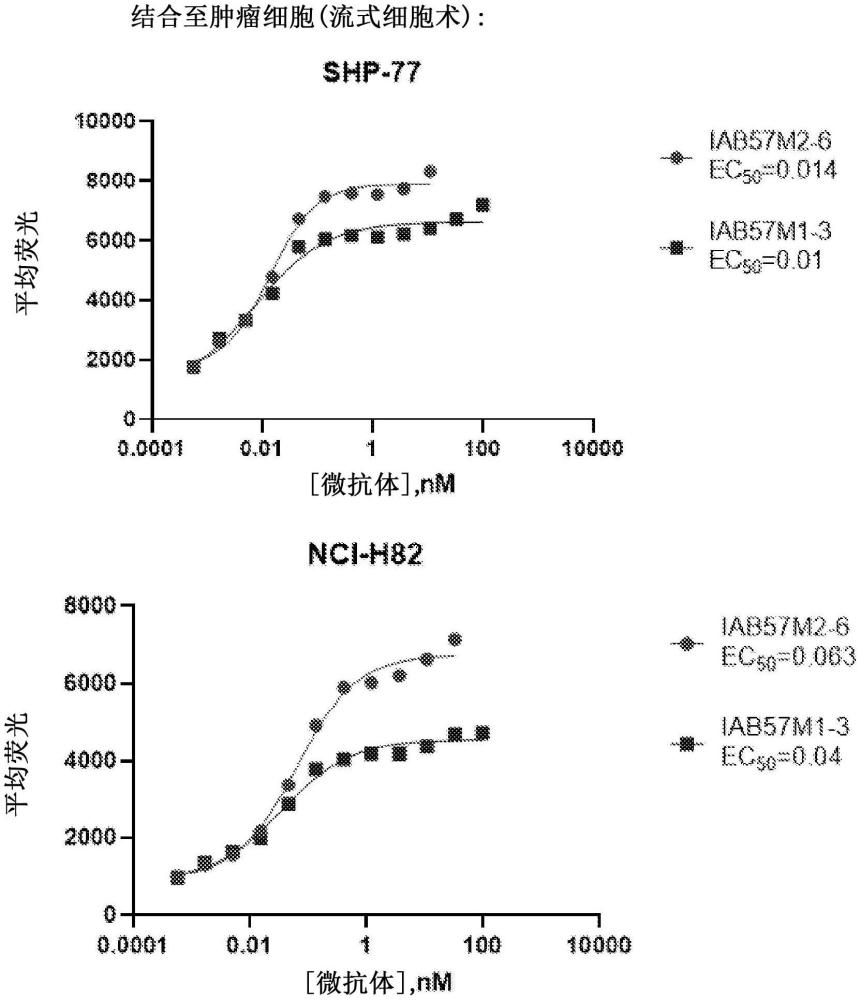
65、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體的ec50為、為約或者至多為0.001、0.005、0.01、0.02、0.03、0.04、0.05、0.06、0.07、0.08、0.09、0.10、0.11、0.12、0.13、0.14、0.15、0.16、0.17、0.18、0.19或0.20nm,或者ec50在以上值中任意兩個所限定的范圍內。
66、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體的ec50在約0.001至0.20nm、0.001至0.17nm、0.001至0.12nm、0.01至0.20nm、0.01至0.17nm、0.01至0.12nm、0.05至0.20nm、0.05至0.17nm、0.05至0.15nm、0.05至0.12nm、0.08至0.20nm、0.08至0.17nm或0.08至0.12nm之間。
67、根據以上實施方式中任一項所述的抗原結合構建體、微抗體或cys-雙抗體,其中所述抗原結合構建體、微抗體或cys-雙抗體的ec50至高達約10nm。
68、本文提供了核酸,其編碼根據任何上述實施方式的抗原結合構建體、微抗體或cys-雙抗體。
69、根據以上實施方式中任一項所述的核酸,其中所述核酸是seq?id?no:51-65中任一項。
70、本文提供了細胞系,所述細胞系產生根據以上實施方式中任一項的抗原結合構建體、微抗體或cys-雙抗體。
71、本文提供了試劑盒,所述試劑盒包含:根據以上實施方式中任一項的抗原結合構建體、微抗體或cys-雙抗體;和螯合劑,其中所述螯合劑允許可檢測標志物的摻入(并入、引入,incorporation)。
72、本文提供了試劑盒,所述試劑盒包含:根據以上實施方式中任一項的抗原結合構建體、微抗體或cys-雙抗體;和螯合劑,其中所述螯合劑允許治療性同位素或試劑的摻入。
73、本文提供了試劑盒,所述試劑盒包含:根據以上實施方式中任一項的抗原結合構建體、微抗體或cys-雙抗體;和接頭,其中所述接頭允許可檢測標志物的摻入。
74、本文提供了試劑盒,所述試劑盒包含:根據以上實施方式中任一項的抗原結合構建體、微抗體或cys-雙抗體;和接頭,其中所述接頭允許治療性同位素或試劑的摻入。
75、本文提供了試劑盒,所述試劑盒包含:根據以上實施方式中任一項的抗原結合構建體、微抗體或cys-雙抗體;和可檢測標志物。
76、本文提供了檢測dll3的存在或不存在的方法,所述方法包括:將根據以上實施方式中任一項的所述抗原結合構建體、微抗體或cys-雙抗體應用(施加,apply)于樣品;和檢測所述抗原結合構建體的存在或不存在,借此檢測dll3的存在或不存在。
77、根據以上實施方式中任一項所述的方法,其中將所述抗原結合構建體、微抗體或cys-雙抗體綴合(結合,conjugate)至可檢測標志物。
78、根據以上實施方式中任一項所述的方法,其中應用所述抗原結合構建體、微抗體或cys-雙抗體包括將所述抗原結合構建體施用至受試者。
79、根據以上實施方式中任一項所述的方法,其中檢測所述抗原結合構建體、微抗體或cys-雙抗體與dll3的結合或不存在結合包括正電子發射斷層掃描(positron?emissiontomography)、單光子發射計算機斷層掃描(single-photon?emission?computedtomography)或者熒光斷層掃描(fluorescent?tomography)中的至少一種。
80、根據以上實施方式中任一項所述的方法,所述方法還包括將第二抗原結合構建體應用于樣品,其中所述第二抗原結合構建體特異性結合至所述抗原結合構建體。
81、根據以上實施方式中任一項所述的方法,其中將所述抗原結合構建體、微抗體或cys-雙抗體與樣品培育(孵育)不超過20小時。
82、根據以上實施方式中任一項所述的方法,其中將所述抗原結合構建體、微抗體或cys-雙抗體與樣品培育不超過6小時。
83、根據以上實施方式中任一項所述的方法,其中將所述抗原結合構建體、微抗體或cys-雙抗體施用于宿主,并且其中其第一量的抗原結合構建體、微抗體或cys-雙抗體從dll3脫除結合(unbound),并且第二量的抗原結合構建體、微抗體或cys-雙抗體結合至dll3,其中至少約80%的第一量的抗原結合構建體、微抗體或cys-雙抗體在不超過12小時內被消除。
84、本文提供了將治療劑靶向dll3的方法,所述方法包括向受試者施用根據前述權利要求中任一項的抗原結合構建體、微抗體或cys-雙抗體,其中將所述抗原結合構建體綴合至治療劑。
85、本文提供了靶向dll3的治療性組合物,其中所述治療性組合物包含:抗原結合構建體,所述抗原結合構建體包含:包含下列的輕鏈可變(vl)結構域:作為seq?id?no:15的lcdr1;作為seq?id?no:19、21或23中任一項的lcdr2;作為seq?id?no:25的lcdr3;和包含下列的重鏈可變(vh)結構域:作為seq?id?no:27的hcdr1的hcdr1;作為seq?id?no:29的hcdr2的hcdr2;作為seq?id?no:31的hcdr3的hcdr3;和治療劑、毒性有效載荷和/或可檢測標志物。
86、本文提供了靶向dll3的治療性組合物,其中所述治療性組合物包含:結合至dll3的微抗體,所述微抗體包含:結合至dll3的單鏈可變片段(scfv);包含igg1鉸鏈區的鉸鏈-延伸結構域;igg?ch3序列;和治療劑、毒性有效載荷和/或可檢測標志物,所述scfv包含與重鏈可變(vh)結構域連接的輕鏈可變(vl)結構域,所述vl結構域包含:作為seq?id?no:15的lcdr1;作為seq?id?no:19、21或23中任一項的lcdr2;作為seq?id?no:25的lcdr3,且所述vh結構域包含:作為seq?id?no:27的hcdr1;作為seq?id?no:29的hcdr2;作為seq?id?no:31的hcdr3。
87、本文提供了靶向dll3的治療性組合物,其中所述治療性組合物包含:結合至dll3的cys-雙抗體;和治療劑、毒性有效載荷和/或可檢測標志物,所述cys-雙抗體包含多肽,所述多肽包含:單鏈可變片段(scfv),所述單鏈可變片段包含與重鏈可變(vy)結構域連接的輕鏈可變(vy)結構域;所述vy結構域包含:作為seq?id?no:15的lcdr1;作為seq?id?no:19、21或23的lcdr2;作為seq?id?no:25的lcdr3;所述vy結構域包含:作為seq?id?no:27的hcdr1;作為seq?id?no:29的hcdr2;作為seq?id?no:31的hcdr3。
88、根據以上實施方式中任一項所述的治療組合物,其中所述可檢測標志物是放射性標記。
89、根據以上實施方式中任一項所述的治療組合物,其中所述可檢測標志物是α發射體放射性標記。
90、根據以上實施方式中任一項所述的治療組合物,其中所述可檢測標志物是β發射體放射性標記。
91、根據以上實施方式中任一項所述的治療組合物,其中所述可檢測標志物是正電子發射體放射性標記。
92、根據以上實施方式中任一項所述的治療組合物,其中所述可檢測標志物包含镥-177。
- 還沒有人留言評論。精彩留言會獲得點贊!