一種鑒定高毒力型肺炎克雷伯菌的熒光定量PCR的引物組、應(yīng)用和檢測方法與流程
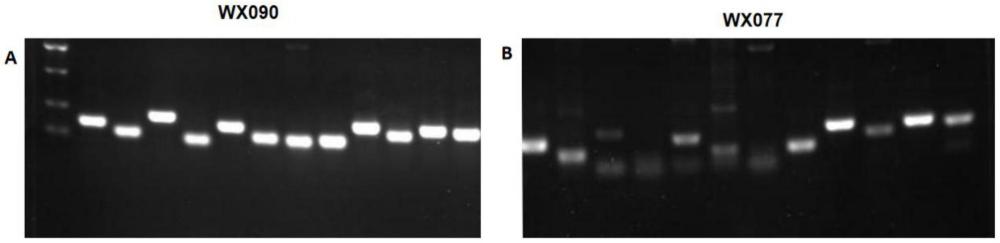
本申請涉及生物檢測,更具體地,涉及一種鑒定高毒力型肺炎克雷伯菌的熒光定量pcr的引物組、應(yīng)用和檢測方法。
背景技術(shù):
1、肺炎克雷伯菌是一種日益重要的細(xì)菌病原體,可導(dǎo)致嚴(yán)重的器官損傷和危及生命的疾病,其顯著特征之一是獲取新基因的能力。目前,該病原體主要分為兩種病理類型:經(jīng)典型(classic?klebsiella?pneumoniae,ckp)和高毒力型(hypervirulentklebsiellapneumoniae,hvkp)。高毒力型肺炎克雷伯菌具高黏液性和強(qiáng)毒力,易導(dǎo)致肺炎、肝膿腫、血流感染等危重癥,且治療難度大、病死率高。現(xiàn)有毒力檢測方法存在不足,臨床上通常需結(jié)合多種方法以提高準(zhǔn)確性,這給醫(yī)生和患者都帶來了很大的困惑。
2、hvkp的特性及其與ckp的差異尚未得到充分研究。盡管hvkp被描述為一種高毒力的病原體,但社區(qū)中由hvkp引起的感染報道日益增多。臨床流行病學(xué)研究表明,hvkp感染可發(fā)生于任何年齡段,且感染者通常會表現(xiàn)出多個感染部位,隨后可能會發(fā)生轉(zhuǎn)移性傳播,這使得肺炎克雷伯菌成為一種非同尋常的腸桿菌科成員。hvkp幾乎可以感染人體的任何部位。這些感染性綜合征包括肝膿腫、肺炎、壞死性筋膜炎、眼內(nèi)炎和腦膜炎。最初認(rèn)為對hvkp菌株敏感和特異的高粘表型現(xiàn)已被證實(shí)并非唯一標(biāo)志,因?yàn)椴⒎撬械膆vkp菌株都是高粘的,一些ckp菌株也具有這種特征。因此,單獨(dú)使用高粘表型來定義hvkp菌株是不準(zhǔn)確的。同樣,染色體編碼的需氧菌素(iuta)受體或iroe基因在許多ckp菌株中也存在,無法單獨(dú)用于定義hvkp。k1或k2莢膜型的存在也不能單獨(dú)作為鑒別hvkp的標(biāo)準(zhǔn)。然而,hvkp已獲得了在大毒力質(zhì)粒(如pk2044和plvpk)上存在的毒力基因,以及賦予其高毒力表型的整合染色體元件(ice),這些元素被稱為毒力質(zhì)粒上的生物標(biāo)記。
3、傳統(tǒng)的肺炎克雷伯菌毒力基因檢測方法主要依賴于pcr技術(shù)來檢測一系列已知的毒力基因,如rmpa、rmpa2、maga等。這些基因被認(rèn)為與細(xì)菌的毒力特性相關(guān),理論上其存在與否可以作為評估菌株毒力的指標(biāo)。然而,近期研究表明,這些傳統(tǒng)毒力基因檢測方法在實(shí)際臨床應(yīng)用中存在若干局限性:毒力基因的普遍存在,即使在經(jīng)典型菌株中,這些傳統(tǒng)毒力基因也經(jīng)常被檢測到。例如,基因rmpa和maga等在一些毒力較低的肺炎克雷伯菌菌株中也能被檢測到。這一發(fā)現(xiàn)提示我們,僅僅檢測這些基因的存在并不足以準(zhǔn)確評估菌株的毒力水平。
4、肺炎克雷伯菌的毒力基因包括莢膜基因、脂多糖、菌毛、外膜蛋白、氮源物質(zhì)利用系統(tǒng)和鐵載體系統(tǒng)等。然而,實(shí)驗(yàn)結(jié)果發(fā)現(xiàn),無論是通過檢測菌毛還是毒力基因來鑒定hvkp,相對于金標(biāo)準(zhǔn)—大蠟螟模型的準(zhǔn)確性都不夠高。
技術(shù)實(shí)現(xiàn)思路
1、提供了本申請以解決現(xiàn)有技術(shù)中存在的上述缺陷。需要一種鑒定高毒力型肺炎克雷伯菌的熒光定量pcr的引物組、應(yīng)用和檢測方法,能夠提高高毒力型肺炎克雷伯菌的鑒定準(zhǔn)確性。
2、本申請的第一方面,提供了一種鑒定高毒力型肺炎克雷伯菌的熒光定量pcr的引物組,所述引物組包括如下任一種或多種的引物對:
3、針對aco54002.1表達(dá)基因的seq?id?no:1和seq?id?no:2所示的引物對;
4、針對aop87411.1表達(dá)基因的seq?id?no:3和seq?id?no:4所示的引物對;
5、針對avx34350.1表達(dá)基因的seq?id?no:5和seq?id?no:6所示的引物對;
6、針對awf76568.1表達(dá)基因的seq?id?no:7和seq?id?no:8所示的引物對;
7、針對ctq24123.1表達(dá)基因的seq?id?no:9和seq?id?no:10所示的引物對;
8、針對epa91234.1表達(dá)基因的seq?id?no:11和seq?id?no:12所示的引物對;
9、針對wp_000872613.1表達(dá)基因的seq?id?no:13和seq?id?no:14所示的引物對;
10、針對wp_000888080.1表達(dá)基因的seq?id?no:15和seq?id?no:16所示的引物對;
11、針對wp_008502228.1表達(dá)基因的seq?id?no:17和seq?id?no:18所示的引物對;
12、針對wp_008502230.1表達(dá)基因的seq?id?no:19和seq?id?no:20所示的引物對;
13、針對wp_009310051.1表達(dá)基因的seq?id?no:21和seq?id?no:22所示的引物對;
14、針對wp_020324597.1表達(dá)基因的seq?id?no:23和seq?id?no:24所示的引物對;
15、針對wp_001091224.1表達(dá)基因的seq?id?no:25和seq?id?no:26所示的引物對。
16、本申請的第二方面,提供了一種鑒定高毒力型肺炎克雷伯菌的熒光定量pcr的試劑盒,所述試劑盒包含本申請任一實(shí)施例所述的引物組。
17、本申請的第三方面,提供了一種本申請任一實(shí)施例所述的引物組或本申請任一實(shí)施例所述的試劑盒在鑒定高毒力型肺炎克雷伯菌中的應(yīng)用。
18、本申請的第四方面,提供了一種本申請任一實(shí)施例所述的引物組或本申請任一實(shí)施例所述的試劑盒在制備鑒定高毒力型肺炎克雷伯菌的產(chǎn)品中的應(yīng)用。
19、本申請的第五方面,提供了一種高毒力型肺炎克雷伯菌的鑒定方法,所述鑒定方法包括如下步驟:1)提取待測菌的rna;2)對提取的rna進(jìn)行逆轉(zhuǎn)錄;3)以cdna為模版,采用權(quán)利要求1所述的引物組進(jìn)行pcr擴(kuò)增,得到pcr產(chǎn)物;根據(jù)pcr產(chǎn)物的序列確定待測菌的類型。
20、本申請各個實(shí)施例提供的鑒定高毒力型肺炎克雷伯菌的熒光定量pcr的引物組、應(yīng)用和檢測方法,提出了熒光定量pcr的引物組,實(shí)驗(yàn)結(jié)果表明通過本申請的引物組能夠更準(zhǔn)確地鑒定肺炎克雷伯菌為高毒力型肺炎克雷伯菌,能夠更精確地區(qū)分于經(jīng)典型肺炎克雷伯菌。解決了傳統(tǒng)的基因存在檢測方法可能無法準(zhǔn)確評估細(xì)菌的毒力水平的問題。
技術(shù)特征:
1.一種鑒定肺炎克雷伯菌的熒光定量pcr的引物組,其特征在于,所述引物組包括如下任一種或多種的引物對:
2.根據(jù)權(quán)利要求1所述的引物組,其特征在于,所述引物組包括如下任一種或多種的引物對:
3.一種鑒定高毒力型肺炎克雷伯菌的熒光定量pcr的試劑盒,其特征在于,所述試劑盒包含權(quán)利要求1或2所述的引物組。
4.權(quán)利要求1-2任一項(xiàng)所述的引物組或權(quán)利要求3所述的試劑盒在鑒定高毒力型肺炎克雷伯菌中的應(yīng)用。
5.權(quán)利要求1-2任一項(xiàng)所述的引物組或權(quán)利要求3所述的試劑盒在制備鑒定高毒力型肺炎克雷伯菌的產(chǎn)品中的應(yīng)用。
6.一種高毒力型肺炎克雷伯菌的鑒定方法,其特征在于,所述鑒定方法包括如下步驟:
7.根據(jù)權(quán)利要求6所述的鑒定方法,其特征在于,根據(jù)pcr產(chǎn)物的序列確定待測菌的類型包括:在pcr產(chǎn)物包含aco54002.1表達(dá)基因、aop87411.1表達(dá)基因、avx34350.1表達(dá)基因、awf76568.1表達(dá)基因、ctq24123.1表達(dá)基因、epa91234.1表達(dá)基因、wp_000872613.1表達(dá)基因、wp_000888080.1表達(dá)基因、wp_008502228.1表達(dá)基因、wp_008502230.1表達(dá)基因、wp_009310051.1表達(dá)基因、wp_020324597.1、wp_001091224.1中的一種或多種的情況下,確定所述待測菌為高毒力型肺炎克雷伯菌。
8.根據(jù)權(quán)利要求6所述的鑒定方法,其特征在于,根據(jù)pcr產(chǎn)物的序列確定待測菌的類型包括:在pcr產(chǎn)物包含wp_008502230.1表達(dá)基因、epa91234.1表達(dá)基因、wp_009310051.1表達(dá)基因、ctq24123.1表達(dá)基因和awf76568.1表達(dá)基因中任一種或多種的情況下,確定所述待測菌為高毒力型肺炎克雷伯菌。
9.根據(jù)權(quán)利要求6所述的鑒定方法,其特征在于,所述提取待測菌的rna包括:將菌液離心除去上清液,得到細(xì)胞固體物;將細(xì)胞固體物和緩沖液混合后經(jīng)過裂解、吸附柱吸附后,將吸附后的吸附柱經(jīng)過去蛋白、漂洗和離心處理后得到待測菌的rna。
10.根據(jù)權(quán)利要求6所述的鑒定方法,其特征在于,cdna的合成方法包括:rna或mrna與寡核苷酸、反轉(zhuǎn)錄試劑盒、逆轉(zhuǎn)錄試劑盒和水混合孵育后得到cdna。
技術(shù)總結(jié)
本申請實(shí)施例涉及一種鑒定高毒力型肺炎克雷伯菌的熒光定量PCR的引物組、應(yīng)用和檢測方法,引物組包括SEQ?ID?NO:1至SEQ?ID?NO:26中的一種或多種的引物對,能夠提高高毒力型肺炎克雷伯菌的鑒定準(zhǔn)確性。
技術(shù)研發(fā)人員:王明勇,劉君
受保護(hù)的技術(shù)使用者:蘇州木芮生物科技有限公司
技術(shù)研發(fā)日:
技術(shù)公布日:2025/4/24
- 還沒有人留言評論。精彩留言會獲得點(diǎn)贊!