一種代代花萼多酚在制備減肥藥物中的應用的制作方法
本發(fā)明屬于中藥領域,具體涉及一種代代花萼多酚在制備減肥藥物中的應用。
背景技術:
代謝綜合征是多種代謝異常癥候群的總稱,包括肥胖、胰島素抵抗,血脂異常,高胰島素血癥、高血壓等。在這些代謝異常中,肥胖首當其沖,成為其他代謝異常的首要體現(xiàn),已經(jīng)在全球范圍內危害著人類的健康。Ⅱ型糖尿病、高血壓、心腦血管疾病、腫瘤等多種疾病的發(fā)生、發(fā)展都與肥胖有著密切的關系。目前肥胖已成為危害人類健康的全球性健康問題,它與Ⅱ型糖尿病、高血壓、心腦血管疾病、腫瘤等多種疾病的發(fā)生、發(fā)展密切相關。
3T3-L1前脂肪細胞分離自小鼠胚胎(17~19d)的Swiss 3T3細胞,能特異性地被誘導分化成成熟的脂肪細胞。由于小鼠前體脂肪細胞的取材較為方便,并且關于小鼠前體脂肪細胞的培養(yǎng)研究技術較成熟,使得3T3-L1前脂肪細胞已成為國際上公認的研究脂肪代謝的細胞模型。越來越多的研究發(fā)現(xiàn)中藥可通過抑制3T3-L1前脂肪細胞的增殖發(fā)揮預防或減肥的功效。比如于華強等利用MTT法以及油紅O染色法研究不同濃度的芹菜素對前脂肪細胞增殖以及分化的影響,實驗結果表明,芹菜素能夠顯著地抑制3T3-L1前脂肪細胞的增殖以及分化,并呈劑量依賴性,提示芹菜素可能具有預防或治療肥胖的作用。
代代(Citrus aurantium L.var.amara Engl)是蕓香科柑橘屬植物酸橙的一個變種,代代花是其花蕾的干品,具有良好的藥理作用,常用于治療氣郁不舒、脘腹脹痛、積食不化、惡心嘔吐等。目前國內外對代代花的研究主要以其揮發(fā)油類化合物為主,而對代代花其它有效成分的研究報道幾乎沒有。代代花作為藥食兩用價值的天然保健品,其有效成分的提取純化和藥理活性等方面的研究還有待進一步深入探討,全面加強代代花的生物利用,對于開發(fā)新藥、指導臨床用藥具有重要的意義。
技術實現(xiàn)要素:
為了克服現(xiàn)有技術的不足和缺點,本發(fā)明的首要目的在于提供一種代代花萼多酚在制備減肥藥物中的應用。
本發(fā)明的目的通過下述方案實現(xiàn):
一種代代花萼多酚在制備減肥藥物中的應用。
所述代代花萼多酚的制備方法,包含如下步驟:
將代代花萼粗粉加入溶劑中,加熱提取,離心取上清液,濃縮,干燥,得代代花萼多酚;所述溶劑為水、甲醇溶液或乙醇溶液。
以蒸餾水做為溶劑提取到的代代花萼多酚記為CAV-W,以乙醇做為溶劑提取到的代代花萼多酚記為CAV-E,以甲醇做為溶劑提取到的代代花萼多酚記為CAV-M。
所述溶劑與代代花萼粗粉的體積質量比(水料比)為(10~30)mL:1g;
所述加熱提取的溫度為80~100℃;所述加熱提取的時間為1~3h。
所述離心的轉速為3000~5000r/min;所述離心的時間為8~12min。
所述濃縮為減壓濃縮;所述減壓濃縮的溫度為40~60℃。
所述乙醇水溶液的體積分數(shù)40~60%、所述甲醇水溶液的體積分數(shù)為40~60%。
所述代代花萼粗粉是將代代花萼(Citrus aurantium L.var.amara Engl)進行干燥,粉碎過篩得到。
所述干燥溫度為40~60℃;所述干燥時間為12~24h;所述的粉碎過篩為40~60目篩。
一種代代花萼多酚(CAV-W、CAV-E、CAV-M),通過上述制備方法制備得到;
所述的代代花萼多酚(CAV-W、CAV-E、CAV-M)在制備減肥藥物中的應用;
所述的代代花萼多酚(CAV-W、CAV-E、CAV-M)可作為新型的減肥藥物,應用于肥胖癥的治療。
一種減肥藥物,含有上述代代花萼多酚(CAV-W、CAV-E、CAV-M)中的至少一種;
本發(fā)明的原理:天然植物來源的有效成分能通過抑制前脂肪細胞的增殖發(fā)揮減肥的功效。本發(fā)明發(fā)現(xiàn)和確證天然植物有效成分具有顯著的減肥活性,且使用劑量低,在同樣劑量下的毒副作用也較低。
本發(fā)明相對于現(xiàn)有技術具有如下的優(yōu)點及效果:
(1)本發(fā)明首次發(fā)現(xiàn)代代花萼多酚(CAV-W、CAV-E、CAV-M)在體外能顯著抑制3T3-L1前脂肪細胞的增殖。
(2)本發(fā)明使用劑量低,在同樣劑量下的毒副作用也較低。
附圖說明
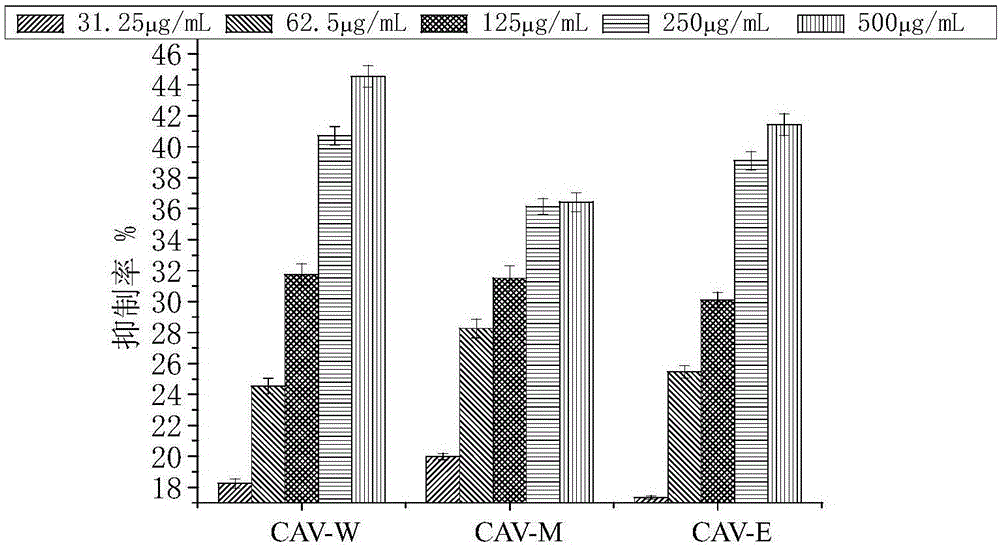
圖1為實施例1制備得到的代代花萼多酚CAV-W、CAV-E和CAV-M對3T3-L1前脂肪細胞增殖抑制作用圖;
圖2為采用Folin-Ciocalteu比色法測得的沒食子酸標準曲線,以此曲線計算實施例1制備的代代花萼多酚的得率。
具體實施方式
下面結合實施例及附圖對本發(fā)明作進一步詳細的描述,但本發(fā)明的實施方式不限于此。
實施例中,小鼠3T3-L1前脂肪細胞購自中科院上海生命科學研究院細胞資源中心;代代花萼購自廣州清平藥材市場。
實施例1從代代花萼中制備得到代代花萼多酚CAV-W、CAV-E和CAV-M
(1)將代代花萼(Citrus aurantium L.var.amara Engl)置于電熱鼓風干燥箱中50℃干燥24h,用粉碎機粉碎后,過60目篩,得代代花萼粗粉備用;
(2)稱量代代花萼粗粉5.0g三份于錐形瓶中,分別加入100mL的蒸餾水、100mL的50%乙醇溶液和100mL的50%甲醇溶液,充分震蕩搖勻,水浴鍋90℃加熱1h;加熱結束后,離心機4000r/min下離心10min,取上層澄清液,將上清液用旋轉蒸發(fā)儀在50℃下減壓濃縮,50℃下真空干燥箱干燥至恒重,即得代代花萼多酚(其中用蒸餾水做為溶劑的命名為CAV-W,用50%乙醇溶液做為溶劑的命名為CAV-E,用50%甲醇溶液做為溶劑的命名為CAV-M)。
實施例2從代代花萼中制備得到代代花萼多酚CAV-W、CAV-E和CAV-M
(1)將代代花萼(Citrus aurantium L.var.amara Engl)置于電熱鼓風干燥箱中45℃干燥18h,用粉碎機粉碎后,過50目篩,得代代花萼粗粉備用;
(2)稱量代代花萼粗粉5.0g三份于錐形瓶中,分別加入150mL的蒸餾水、150mL的60%乙醇溶液和150mL的60%甲醇溶液,充分震蕩搖勻,水浴鍋100℃加熱2h;加熱結束后,離心機3000r/min下離心12min,取上層澄清液,將上清液用旋轉蒸發(fā)儀在55℃下減壓濃縮,55℃真空干燥箱干燥至恒重,即得代代花萼多酚(其中用蒸餾水做為溶劑的命名為CAV-W,用60%乙醇溶液做為溶劑的命名為CAV-E,用60%甲醇溶液做為溶劑的命名為CAV-M)。
實施例3從代代花萼中制備得到代代花萼多酚CAV-W、CAV-E和CAV-M
(1)將代代花萼(Citrus aurantium L.var.amara Engl)置于電熱鼓風干燥箱中50℃干燥24h,用粉碎機粉碎后,過60目篩,得代代花萼粗粉備用;
(2)稱量代代花萼粗粉5.0g三份于錐形瓶中,分別加入50mL的蒸餾水、50mL的40%乙醇溶液和50mL的40%甲醇溶液,充分震蕩搖勻,水浴鍋80℃加熱3h;加熱結束后,離心機5000r/min下離心8min,取上層澄清液,將上清液用旋轉蒸發(fā)儀在60℃下減壓濃縮,60℃真空干燥箱干燥至恒重,即得代代花萼多酚(其中用蒸餾水做為溶劑的命名為CAV-W,用40%乙醇溶液做為溶劑的命名為CAV-E,用40%甲醇溶液做為溶劑的命名為CAV-M)。
實施例4Folin-Ciocalteu比色法測定代代花萼多酚CAV-W、CAV-E和CAV-M中多酚含量
(1)沒食子酸標準曲線的測定:精確稱量5.0mg沒食子酸粉末,加蒸餾水完全溶解并定容至25mL,得到0.2mg/mL的沒食子酸母液。取10個25mL的容量瓶,各加入0.2mg/mL的沒食子酸母液0.1mL,0.2mL,0.3mL,0.4mL,0.5mL,0.6mL,0.7mL,0.8mL,0.9mL,1.0mL,再分別加入蒸餾水0.9mL,0.8mL,0.7mL,0.6mL,0.5mL,0.4mL,0.3mL,0.2mL,0.1mL,0mL,則分別得0.02mg/mL,0.04mg/mL,0.06mg/mL,0.08mg/mL,0.1mg/mL,0.12mg/mL,0.14mg/mL,0.16mg/mL,0.18mg/mL,0.2mg/mL的沒食子酸溶液各1mL。然后在每個容量瓶中加入3.0ml的福林酚試劑,充分搖勻后再室溫下靜置反應5min,再加入4.5ml的飽和Na2CO3溶液,加水定容至25ml,搖勻,避光靜置反應2h,用紫外分光光度計檢測在747nm處的吸光值。以沒食子酸濃度為橫坐標,747nm處的吸光值為縱坐標繪制沒食子酸標準曲線。
(2)樣品多酚含量的測定:將由實施例1制得的CAV-W、CAV-E和CAV-M用蒸餾水完全溶解,并定容至100mL,混勻,用移液槍移取200μL CAV-W、CAV-E和CAV-M樣品溶液于25mL容量瓶中,加入3mL福林酚試劑,混勻靜置5min后,再加入4.5mL飽和的Na2CO3溶液,加蒸餾水定容,混勻,室溫下避光反應2h,然后用紫外分光光度計測定在747nm下的吸光值。
圖2為沒食子酸標準曲線,利用此曲線經(jīng)測定和計算得到代代花萼多酚CAV-W、CAV-E和CAV-M的多酚得率分別為3.7%、2.1%和3.3%,表明以蒸餾水做為提取溶劑得到的代代花萼多酚的得率更高。
實施例5MTT法檢測代代花萼多酚CAV-W、CAV-E、CAV-M對3T3-L1前脂肪細胞增殖的影響
分別取生長對數(shù)期的小鼠3T3-L1前脂肪細胞,1000rpm離心5min,棄去上清液,用含質量分數(shù)為10%胎牛血清的DMEM培養(yǎng)基調整細胞數(shù)為5×104/mL,100μL接種于96孔培養(yǎng)板中,置于5%CO2培養(yǎng)箱中,37℃培養(yǎng)24h后,棄去上清液,各組分別加入含有CAV-W(實施例1制得)、CAV-E(實施例1制得)、CAV-M(實施例1制得)的DMEM培養(yǎng)基(CAV-W、CAV-E、CAV-M的終濃度分別為31.25、62.5、125、250和500μg/mL)。在37℃、5%CO2培養(yǎng)箱中培養(yǎng)24h,棄去上清液,PBS清洗兩次,每孔加入200μL不含血清的DMEM基礎培養(yǎng)基和20μL噻唑藍(MTT),放入培養(yǎng)箱中繼續(xù)孵育4h,棄上清液,每孔加入150μL二甲基亞砜(DMSO),避光放置于微量振蕩器均勻震蕩10min,用酶標儀測量在490nm波長下的OD值,計算細胞增殖抑制率;
而CAV-W(圖1)、CAV-E(圖1)、CAV-M(圖1)在31.25~500μg/mL范圍內對小鼠3T3-L1前脂肪細胞均表現(xiàn)出顯著的增殖抑制作用。
上述實施例為本發(fā)明較佳的實施方式,但本發(fā)明的實施方式并不受上述實施例的限制,其他的任何未背離本發(fā)明的精神實質與原理下所作的改變、修飾、替代、組合、簡化,均應為等效的置換方式,都包含在本發(fā)明的保護范圍之內。
- 還沒有人留言評論。精彩留言會獲得點贊!