一種復合水凝膠軟骨修復材料及其制備方法與流程
本發明涉及一種復合水凝膠軟骨修復材料及其制備方法,特別涉及制備具有降解速率可調控,且降解行為熒光可視化功能的軟骨修復材料的方法。
背景技術:
軟骨是一種透明的軟組織,在關節潤滑、減震和承重中起重要作用。當人體內的軟骨發生損傷時,由于缺乏血液供應,其再生能力很弱,要想治療只有采取體外移植軟骨替代材料進行修復。因此研發力學性能優良、在體降解程度可控及可視的軟骨修復材料具有迫切的必要性。
聚合物水凝膠因具有良好的力學性能、生物兼容性等性質,引起了生物醫學界的廣泛關注。采用水凝膠制備生物體內軟骨損傷修復材料具有諸多優勢。聚乙烯醇(PVA)是一種無毒、無腐蝕性并且擁有良好的生物相容性的聚合物,其力學性能良好,且可生物降解,目前已被廣泛應用于組織工程的支架材料、軟骨組織替代、修復等領域(J. P. Gong, Advanced Materials, 2003, 15,1155-1158)。目前已有許多研究者在PVA中摻雜與成骨細胞具有高度親和能力的納米羥基磷灰石(HA),從而達到提高軟骨修復材料的生物親和性并改善其力學性能的目的。
碳點是一種具有良好的上轉換熒光性能及生物兼容性的納米材料(Y. Y. Zhang, M. Wu, Y. Q. Wang, Talanta, 2013, 117, 196-202),其較高的熒光量子產率為它在生物醫藥領域的廣泛應用奠定了基礎。目前,碳點在與聚合物材料的結合方面取得許多進展(P. Zhang, W. C. Li, X. Y. Zhai, Chemical Communications, 2012, 48, 10431-10433;P. P. Li, Nanotechnology, 2014, 25, 055603-055609)。在臨床醫學應用中,外科醫生發現,傳統的軟骨修復材料雖然力學性能良好,但是在實時、可視化跟蹤研究方面并不方便。要想跟蹤研究復合水凝膠軟骨修復材料移植入體內后隨著生理代謝及機體正常的生命活動,其轉移、變形及老化情況、受力后的變形情況及在體內的降解程度等相對來說較為困難。
技術實現要素:
本發明旨在提供一種具有優良力學性能、熒光自示蹤性能及降解速率可控功能的復合水凝膠軟骨修復材料及其制備方法,拓寬了人工關節軟骨的應用范疇。該制備方法過程簡單,制備所得的復合水凝膠材料具有熒光示蹤性能,降解可控性能及良好的力學性能。
本發明提供了一種復合水凝膠軟骨修復材料,包括以下重量配比的原料:
碳點(CDs) 0-1.5%
納米羥基磷灰石(HA) 2%~6%
聚乙烯醇(PVA) 65%~85%
纖維蛋白凝膠 7.5%~33%
本發明提供了一種上述復合水凝膠軟骨修復材料的制備方法,首先采用碳點作為優良的熒光信號源,采用聚乙烯醇作為高分子網絡結構,采用納米羥基磷灰石作為共摻雜試劑,賦予了該水凝膠材料良好的骨組織親和性,制備得到碳點/納米羥基磷灰石/聚乙烯醇(CDs/HA/PVA)復合水凝膠軟骨修復材料,然后在其孔穴內進一步填充纖維蛋白凝膠。
上述復合水凝膠軟骨修復材料的制備方法,具體包括以下步驟:
①碳點的合成:將反應容器用王水、乙醇、二次水依次洗滌后,先加入乳糖,再加入三羥甲基氨基甲烷,最后加入二次水,并攪拌均勻,在90℃-100℃下加熱回流,反應進行20-30h后即得到黃色的CDs溶液,所得產物透析24-48h;
②CDs/HA/PVA復合水凝膠的合成:稱取聚乙烯醇與納米羥基磷灰石并溶于去離子水中,90-100℃下加熱回流1-2h,然后將上述步驟①制備所得碳點溶液加入其中,于80-90℃下磁力攪拌1-4h,最后將該混合溶液冷卻至室溫并澆注于模具中,放入-15--20℃冰箱冷凍15-25h,然后取出并在室溫下放置10-15h解凍,如此冷凍-解凍循環3-10次,即可制備得到CDs/HA/PVA復合水凝膠,隨后采用冷凍干燥的方式將該水凝膠制成固體支架材料,冷凍干燥處理時間為36-48h;
③導入纖維蛋白原溶液:將纖維蛋白原溶液在負壓的條件導入到CDs/HA/PVA多孔支架中,然后在負壓的作用下把凝血酶的氯化鈣溶液導入,用無菌紗布吸去支架表面液體,將該材料置于恒溫培養箱中,充分孵育0.5-1h,待纖維蛋白原完全凝膠,最終得到孔穴內填充有纖維蛋白凝膠的CDs/HA/PVA復合水凝膠軟骨修復材料。
上述制備方法中,所述碳點(CDs)的合成中,乳糖溶液的濃度為1.0-6.0g/L,三羥甲基氨基甲烷溶液的濃度為20.0-100.0g/L,采用逐滴加入NaOH稀溶液的方式調節該混合溶液的pH為9.5-11.5,隨后于100℃下加熱回流24-48小時。
上述制備方法中,所述CDs/HA/PVA復合水凝膠的合成中,所用碳點的濃度為0.5-4.0 mg/mL,所用各試劑比例為:水、碳點溶液的體積比為10:1-20:1,水、聚乙烯醇的質量比為10:1-40:1。
上述制備方法中,所述步驟③中,CDs/HA/PVA復合水凝膠置于負壓中,采用注射器導入10-25mg/mL的纖維蛋白原溶液,隨后導入凝血酶(2-10U/mL)的氯化鈣溶液,氯化鈣溶液的濃度為0.01-0.05mol/mL,用無菌紗布吸去支架表面液體,最后將該材料置于35℃-40℃的恒溫培養箱中,充分孵育0.5-1h。
本發明在PVA水凝膠材料中摻雜碳點,由于碳點表面富含大量的羥基,可與聚乙烯醇上的羥基間形成良好的氫鍵相互作用,從而使碳點摻雜于HA/PVA的高分子網狀結構中。通過觀察熒光信號的強度及范圍,便可實時掌握該軟骨替代材料在機體內的降解程度。纖維蛋白原是人體血液蛋白的重要組成部分,含量極其豐富,其具有優異的生物相容性和生物降解性能。纖維蛋白凝膠可誘使軟骨細胞再生并與周圍組織自然融合。通過調節PVA水凝膠中纖維蛋白原的比例,即可調節該軟骨支架材料的生物降解過程,從而實現軟骨修復材料的降解速率可控性。
本發明的有益效果:
1)碳點通過氫鍵作用力結合于聚丙烯酰胺的網絡結構中,不僅可賦予該軟骨修復材料熒光自示蹤能力,而且可提高其力學性能。
2)將纖維蛋白凝膠填充于水凝膠網絡結構內,可賦予該軟骨修復材料誘導成骨細胞生長與分化的能力,并且通過調節纖維蛋白凝膠的比例,可以實現對該軟骨修復材料降解速率的調控。
附圖說明
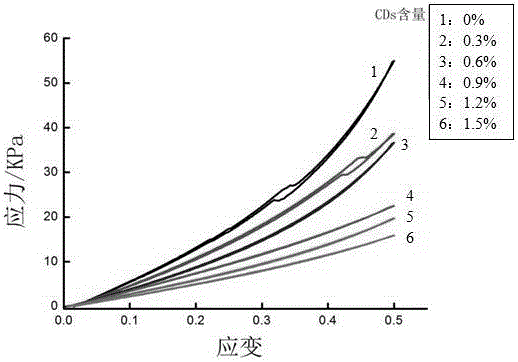
圖1是不同碳點含量的CDs/HA/PVA復合水凝膠在受到初始長度50%的拉伸變形情況下,循環加載-卸載時的應力-應變曲線圖。該復合水凝膠材料中碳點所占的質量比分別為0%,0.3%,0.6%,0.9%,1.2%,1.5%。
圖2是不同碳點含量的CDs/HA/PVA復合水凝膠的熒光發射光譜圖。該復合水凝膠材料中碳點所占的質量比分別為0%,0.6%,1.2%,1.5%。
圖3是不同碳點含量的CDs/HA/PVA復合水凝膠的溶脹率曲線圖。該復合水凝膠材料中碳點所占的質量比重分別為0%,0.9%,1.5%。
具體實施方式
下面通過實施例來進一步說明本發明,但不局限于以下實施例。
實施例1:一種復合水凝膠軟骨修復材料的制備方法
具體制備過程包括如下步驟:
①碳點(CDs)的合成:將反應容器用王水、乙醇、二次水依次洗滌后,先加入0.2g乳糖,再加入4.0g三羥甲基氨基甲烷(Tris),最后加入100mL的二次水,并攪拌均勻,在100℃下加熱回流,采用稀NaOH溶液逐滴加入的方式調節溶液pH至10.5,反應進行24h后即得到黃色的CDs溶液,所得產物透析48h;
②稱取3g聚乙烯醇(PVA)與0.1g納米羥基磷灰石(HA)并溶于20mL去離子水中,90℃下加熱回流1h,然后將4.5mL的上述步驟①制備所得碳點溶液加入其中,于85℃下磁力攪拌2h,最后將該混合溶液冷卻至室溫并澆注于模具中,放入-20℃冰箱冷凍20h,然后取出并在室溫下放置10h解凍,如此冷凍-解凍循環,5次,即可制備得到CDs/HA/PVA復合水凝膠;
③采用冷凍干燥的方式將該水凝膠制成固體支架材料,冷凍干燥時間為48h,隨后將20mg/mL的纖維蛋白原溶液在負壓的條件導入到CDs/HA/PVA多孔支架中,并在負壓的作用下把3.0U/mL凝血酶的氯化鈣溶液導入,用無菌紗布吸去支架表面液體,將該材料置于37℃恒溫培養箱中,充分孵育30min,待纖維蛋白原完全凝膠,最終得到孔穴內填充有纖維蛋白凝膠的CDs/HA/PVA水凝膠軟骨修復材料,如圖1中曲線2所對應即為按照實施例1的步驟制備所得樣品,該樣品中所對應碳點的重量比為0.3%。
實施例2:一種復合水凝膠軟骨修復材料的制備方法
實驗條件和操作步驟與實施例1部分相同,改變的條件如下:
將0mL的碳點溶液加入該混合溶液,制備得到HA/PVA復合水凝膠。如圖1中曲線1所對應即為按照本實施例制備所得樣品,該樣品中所對應碳點的重量比為0%。
實施例3:一種復合水凝膠軟骨修復材料的制備方法
實驗條件和操作步驟與實施例1部分相同,改變的條件如下:
將9mL的碳點溶液加入該混合溶液,制備得到HA/PVA復合水凝膠。如圖1中曲線3所對應即為按照本實施例制備所得樣品,該樣品中所對應碳點的重量比為0.6%。
實施例4:一種復合水凝膠軟骨修復材料的制備方法
實驗條件和操作步驟與實施例1其他相同,改變的條件如下:
將13.5mL的碳點溶液加入該混合溶液,制備得到HA/PVA復合水凝膠。如圖1中曲線4所對應即為按照本實施例制備所得樣品,該樣品中所對應碳點的重量比為0.9%。
實施例5:一種復合水凝膠軟骨修復材料的制備方法
實驗條件和操作步驟與實施例1其他相同,改變的條件如下:
將18mL的碳點溶液加入該混合溶液,制備得到HA/PVA復合水凝膠。如圖1中曲線5所對應即為按照本實施例制備所得樣品,該樣品中所對應碳點的重量比為1.2%。
實施例6:一種復合水凝膠軟骨修復材料的制備方法
實驗條件和操作步驟與實施例1其他相同,改變的條件如下:
將22.5mL的碳點溶液加入該混合溶液,制備得到HA/PVA復合水凝膠。如圖1中曲線6所對應即為按照本實施例制備所得樣品,該樣品中所對應碳點的重量比為1.5%。
用熒光分光光度計測定制備所得的CDs/HA/PVA水凝膠(熒光分光光度計:Horiba,日本,FluoroMax-4;激發狹縫10nm,發射狹縫10nm,激發波長設定在400nm,在450-750nm范圍內記錄熒光發射光譜的實驗數據,光電培增管的電壓為950V)。
圖1是不同碳點含量的CDs/HA/PVA復合水凝膠在受到初始長度50%的拉伸變形情況下,循環加載-卸載時的應力-應變曲線圖。該復合水凝膠材料中碳點所占的質量比重分別為0%,0.3%,0.6%,0.9%,1.2%,1.5%。圖中顯示,隨著復合水凝膠中碳點所占的質量百分比的增加,復合材料的抗拉剛度逐漸減小,但是總體影響不大,復合材料的機械強度仍在軟骨修復材料的可應用范圍。
圖2是不同碳點含量的CDs/HA/PVA復合水凝膠的熒光發射光譜圖。該復合水凝膠材料中碳點所占的質量比重分別為0%,0.6%,1.2%,1.5%。圖中顯示,隨著碳點所占質量百分比的增加,復合水凝膠的熒光強度也在逐漸增強。
圖3是不同碳點含量的CDs/HA/PVA復合水凝膠的溶脹率曲線圖。該復合水凝膠材料中碳點所占的質量比重分別為0%,0.9%,1.5%。圖中顯示,隨著碳點所占質量百分比的增加,復合水凝膠達到溶脹平衡所需的時間越短。
- 還沒有人留言評論。精彩留言會獲得點贊!