靶向配體修飾的還原響應型磁性納米載體及其制備方法與流程
本發明屬于生物醫用高分子材料與納米生物技術領域,具體涉及靶向配體修飾的還原響應型磁性納米載體及其制備方法。
背景技術:
惡性腫瘤在世界范圍內已經成為人類面臨的主要殺手之一,每年導致全球大約13%的死亡率。據世界衛生組織(World Health Organization,WHO)統計,在世界范圍內,每年有近100萬人被診斷出癌癥,在近十年有超過8000萬人死于癌癥。雖然化療在近些年的抗癌治療中取得了良好的效果,但是由于它治療的過程中不具有腫瘤靶向性,導致嚴重的副反應,給患者帶來極大地痛苦。此外,由于許多化療藥物還存在溶解度低,穩定性差,生物利用度低,容易引發多藥耐性等問題,嚴重限制了抗腫瘤藥物在臨床上的應用。所以,研究抗癌藥物合適的給藥載體是十分必要的。
隨著近年材料化學的進步與發展,越來越多的人聚焦于納米遞藥系統,包括納米載體,納米粒,脂質體,聚合物-藥物共聚體,碳納米管,介孔硅載藥體系等。在這其中,聚合物載體作為一種具有廣闊應用前景的新型納米給藥系統,引起了人們的廣泛關注。
殼寡糖(CSO),一種低分子量的殼聚糖,在保留了殼聚糖的諸多理化性質的條件下水溶性獲得了極大的提高,它是自然界中存在的唯一一種帶有氨基的堿性多糖,具有良好的生物相容性,生物可降解性和低毒性,因此可對其進行疏水改性,來負載疏水性的藥物。
許多研究表明透明質酸(HA)在腫瘤發生、發展過程中起著重要作用,其特異性受體CD44在許多腫瘤細胞中過表達,而正常細胞表面的CD44受體則處于一種非活躍的沉默狀態,而透明質酸與CD44之間的相互作用可介導藥物進入細胞,可作為透明質酸作為靶向配體治療惡性腫瘤的基礎。目前針對透明質酸對藥物的靶向遞送多集中于利用透明質酸中的羧基對載體進行化學修飾或直接對透明質酸進行兩親性修飾,但有文獻報道,過多利用透明質酸中的羧基對其進行改性可能會影響透明質酸對CD44受體的靶向結合能力,并且通過化學方法進行透明質酸修飾制備靶向載體,存在工藝復雜,過程繁瑣,批次重現差等問題。因此,采用靜電吸附作用結合透明質酸作為靶向配體,可有效減少對透明質酸結構的影響,增加載體對CD44受體的靶向性,同時無需化學合成,節省時間和成本。
傳統腫瘤治療方法中常常會存在短時間內頻繁用藥,出現血藥濃度高,毒副作用大,治療效果不明顯等問題,刺激響應型納米載體由于可提高藥物的生物利用度,選擇性的將藥物濃集于腫瘤組織,經腫瘤部位刺激(如溫度、PH、光、磁場、超聲強度、電子脈沖等)而迅速釋藥,因此智能型藥物遞釋系統的設計已逐漸成為藥劑學領域的研究熱點之一。基于腫瘤細胞與正常細胞之間還原型谷胱甘肽(GSH)濃度的顯著性差異設計的還原敏感性遞藥系統可以實現藥物高效安全遞送。
兩親性聚合物除了可以裝載藥物,還可以裝載磁性或者熒光納米粒子作為造影劑用做磁共振成像(MIR)或熒光成像,對藥物在腫瘤組織或者細胞中的分布進行監測。磁性納米粒子是一種智能型的納米磁性材料,它既具有納米材料所特有的性質如粒徑小,比表面積大,又具有磁響應性及超順磁性,可以在恒定磁場下聚集和定位。Fe3O4具有優異的超順磁性能,可以用于體內磁共振成像和實現藥物的磁靶向遞送,已經被美國FDA批準應用于臨床。
目前利用兩親性聚合物形成膠束遞送藥物已有眾多報道,通過將超順磁性納米粒摻雜于兩親性聚合物中構建磁性納米載體用于磁靶向或磁共振成像的案例也有相關報道,但是尚未發現將還原響應特性、磁靶向、配體靶向多重特性集一身的靶向配體修飾的還原響應型磁性納米載體的相關報道。本發明首次基于殼寡糖設計合成還原響應型兩親性聚合物包裹超順磁性Fe3O4,同時利用靜電吸附作用附著透明質酸作靶向配體,構建靶向配體修飾的還原響應型磁性納米載體,該載體具良好的生物相容性,是疏水性抗腫瘤藥物的理想載體。
技術實現要素:
本發明的目的在于提供靶向配體修飾的還原響應型磁性納米載體及其制備方法。
本發明所述的是靶向配體修飾的還原響應型磁性納米載體,它具典型的核殼結構。以超順磁性Fe3O4納米粒為內核,包裹在具還原響應性的兩親性聚合物內部;所述的具還原響應性的兩親性聚合物是由疏水基團與親水性聚合物通過含還原敏感鍵的Linker連接而成;所述兩親性聚合物構成所述納米載體的殼結構,殼表面通過靜電吸附作用附著靶向配體。
所述的具還原響應性的兩親性聚合物是由疏水基團與親水性聚合物通過含還原敏感鍵的Linker連接而成;進一步地,所述的親水性聚合物為殼寡糖,其分子量為1000~10000Da;進一步地,所述殼寡糖分子量為5000Da。
所述的具還原響應性的兩親性聚合物是由疏水基團與殼寡糖通過含還原敏感鍵的Linker連接而成;進一步地,所述含還原敏感鍵的Linker為二硫代二丙酸,Linker中所含還原敏感鍵為二硫鍵;所述疏水基團選自膽固醇、維生素E、C8~C16脂肪醇;
所述的具還原響應性的兩親性聚合物合成過程中,鍵合有含還原敏感鍵Linker的疏水基團與殼寡糖中氨基摩爾投料比為5%~100%。
所述靶向配體修飾的還原響應型磁性納米載體,靶向配體為透明質酸,并且通過靜電吸附作用與聚合物殼結構相連,透明質酸分子量為3500~250000Da;進一步地,透明質酸分子量為14600Da;
所述的靶向配體修飾的還原響應型磁性納米載體具超順磁性,為球形結構,粒徑大小為50~250nm,磁性納米粒子具有超順磁性,粒徑為5~18nm。
當殼寡糖分子量取5000Da,鍵合有含還原敏感鍵Linker的疏水基團為十六醇時,隨著投料比的改變,納米粒的平均粒徑(dn)和臨界膠束濃度(CMC),多分散系數(PDI)也發生改變。結果見表1。
表1
從表中可以看出,鍵合有含還原敏感鍵Linker的十六醇投料比越大,載體臨界膠束濃度越小,粒徑越小,當投料比為30%時載體粒徑分布相對比較均一,PDI較小,透射電鏡下外觀呈球形,如圖7,因此本發明中鍵合有含還原敏感鍵Linker的十六醇投料比優選為30%。
透明質酸的投量會嚴重影響載藥體系的粒徑和穩定性,參照Int.J.Biol.Macromol.2015,72:1391-1401,通過考察HA加入量對載體溶液在450nm處的吸光度的影響,可以反映所形成的納米粒的多少與粒徑的大小。如圖1可以看出當HA與還原響應性兩親性聚合物投料比在1/20~8/20時,所形成的納米粒在48h內比較穩定,并且隨著HA投量的增加,溶液在450nm處的吸光度逐漸增大,這表明所形成的納米粒數目逐漸增多,載體粒徑逐漸變大,當將所得納米粒溶液過0.22μm微孔濾膜后,投料比為4/20~8/20的納米粒溶液,納米粒大部分被截留,因此在本發明中HA的投料比優選為3/20。
該納米載體具有超順磁性和腫瘤細胞多重靶向性,可同時用于體內的磁共振成像和靶向遞送疏水性抗腫瘤藥物。
本發明所構建的靶向配體修飾的還原響應性磁性納米載體,具有以下優點:
1)具多重腫瘤靶向能力,提高抗腫瘤效率,降低對正常組織器官的毒副作用。
2)通過靜電吸附附著靶向配體,無需化學反應,節約時間和成本,增強載體腫瘤靶向性。
3)能快速響應腫瘤高GSH微環境,使藥物在腫瘤細胞內快速釋放,增強腫瘤抑制作用。
本發明的另一目的旨在提供一種制備前述納米載體的方法,包括以下步驟:
1.疏水性超順磁性Fe3O4納米粒子的合成:參照文獻J.Am.Chem.Soc.2004,126:273-279所述的高溫熱解法合成5~18nm、高度單分散、粒徑均一、具超順磁性的Fe3O4納米粒子,其形貌如圖2,磁滯回線如圖3。
2.鍵合有含還原敏感鍵Linker的疏水基團的合成:將3,3’-二硫代二丙酸(1.50g,7.13mmol)和二環己基碳二亞胺(DCC,1.618g,7.84mmol)溶于20ml無水有機溶劑中,氬氣保護下冰浴攪拌30min,將疏水基團(7.13mmol)和4-二甲氨基吡啶(DMAP,87mg,0.713mmol)加入其中,繼續在冰浴下攪拌反應1h,之后將其轉移到室溫條件下繼續攪拌反應,反應完全后加入等體積的乙酸乙酯終止反應,過濾除去二環己脲,濾液加入少量水后用乙酸乙酯萃取,合并乙酸乙酯層,減壓濃縮,于混合溶劑中重結晶,即得鍵合有含還原敏感鍵Linker的疏水基團。
合成路線詳解如下:
3.鍵合有含還原敏感鍵Linker的疏水基團改性殼寡糖:取殼寡糖1g溶于2ml超純水中后,加入20ml二甲基亞砜對其進行稀釋,65℃下預熱30min,按照殼寡糖氨基含量的0.05~1倍摩爾當量稱取2)中合成的鍵合有還原敏感鍵Linker的疏水基團,加入相當于鍵合有還原敏感鍵Linker的疏水基團1.5倍摩爾當量的1-乙基-(3-二甲基氨基丙基) 碳酰二亞胺鹽酸鹽(EDCI)和N-羥基琥珀酰亞胺(NHS),溶于適量的二甲基亞砜中,65℃下活化30min,將其逐滴加入已預熱好的殼寡糖溶液中,65℃下反應24h,反應結束后將溶液逐滴加入到10倍體積的丙酮中,11000r/min離心3min,收集沉淀,用少量水復溶后,逐滴加入丙酮中,離心收集沉淀,重復上述操作三次,最后將所得紅棕色沉淀溶于適量水中,裝入透析袋中(MWCO 1000Da)透析24h,冷凍干燥,得具還原響應性的兩親性聚合物。該兩親性材料具良好的水溶性,在水溶液中可自組裝形成納米載體。
合成路線詳解如下:
4.還原響應性兩親性聚合物對Fe3O4納米粒子的裝載:將Fe3O4納米粒溶解于氯仿或二氯甲烷或正己烷中,20mg兩親性聚合物溶解于10ml超純水中,通過超聲乳化-溶劑揮發法將Fe3O4納米粒包封于載體內部;Fe3O4納米粒與兩親性聚合物的重量比為5%~50%,在有機溶劑揮發的過程中,Fe3O4納米粒子自發被負載于兩親性聚合物內部。
5.靶向配體修飾還原響應型磁性載藥納米載體:將0.1~2mg/ml的透明質酸溶液逐滴緩慢滴加于還原響應型磁性載藥納米載體中(其中含兩親性材料的濃度為0.5~2mg/ml),室溫攪拌10min,將載體溶液依次通過0.45μm,0.22μm濾膜,通過冷凍干燥即得靶向配體修飾的還原響應型磁性納米載體。
本發明所發明納米載體可用于疏水性抗腫瘤藥物的運載,故本發明還提供一種負載疏水性抗腫瘤藥物的方法,其制備過程包括以下步驟:
1.還原響應性兩親性聚合物對Fe3O4納米粒子和藥物的裝載:該過程通過一步法將Fe3O4納米粒子和藥物同時裝載或分兩步將二者中一種先裝載后再將另外一種裝載。采用一步法時裝載方法選用超聲乳化-溶劑揮發法或透析法,溶劑選自四氫呋喃、二氯甲烷、氯仿、正己烷、二甲亞砜、乙醇、N,N-二甲基甲酰胺、水;采用兩步法時,裝載Fe3O4選用超聲乳化-溶劑揮發法,裝載藥物選擇透析法或超聲乳化-溶劑揮發法,溶劑選自四氫呋喃、二氯甲烷、氯仿、正己烷、二甲亞砜、乙醇、N,N-二甲基甲酰胺、水。
2.靶向配體修飾還原響應性磁性載藥納米復合物:將0.1~2mg/ml的透明質酸溶液逐滴緩慢滴加于1所得溶液(其中含兩親性材料的濃度為0.5~2mg/ml),室溫攪拌10min,將載體溶液依次通過0.45μm,0.22μm濾膜,通過冷凍干燥即得靶向配體修飾的還原響應型磁性納米載藥復合物。
與現有技術相比,本發明所述的技術方案具以下優點:
1)可同時負載Fe3O4納米粒子和疏水性抗腫瘤藥物,結合靶向配體主動靶向作用,超順磁性磁納米的磁靶向作用和載體腫瘤微環境還原響應特性,使該載體更具腫瘤細胞靶向性,到達腫瘤細胞內部后,能快速響應腫瘤細胞高GSH,迅速將抗腫瘤藥物釋放,具較強的抗腫瘤效率,能有效降低毒副作用。
2)該納米載體具超順磁性,可同時用于體內磁共振成像和藥物的靶向遞送。
3)靶向配體通過靜電吸附作用附著于載體表面,制備方法簡單,操作簡便。
4)所用材料具有良好的生物相容性。
附圖說明
圖1:透明質酸的加入量對納米載體在450nm處的吸光度的影響;
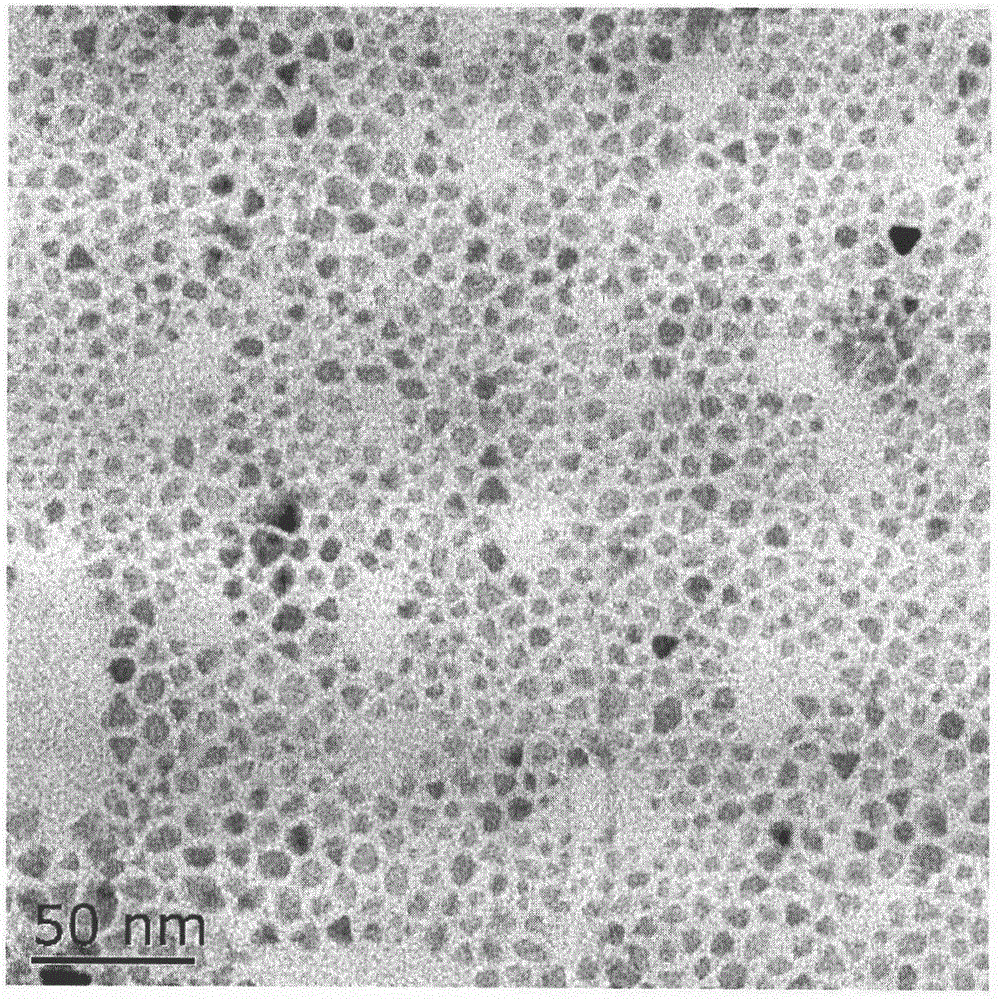
圖2:實施例1中通過高溫熱解法合成的高度單分散、粒徑較均一約為8nm的Fe3O4的TEM圖;
圖3:實施例1中通過高溫熱解法合成的Fe3O4在300K下的磁滯回線;
圖4:實施例2中Hex-SS-COOH的1H-NMR圖譜;
圖5:實施例2中殼寡糖(CSO)的1H-NMR圖譜;
圖6:實施例2中CSO-SS-Hex的1H-NMR圖譜;
圖7:實施例2中還原響應性兩親性材料的TEM圖;
圖8:實施例2中還原響應性兩親性材料的粒徑分布圖;
圖9:實施例2中還原響應性兩親性材料在10mM GSH條件下粒徑的動態變化圖;
圖10:實施例5中透明質酸修飾的還原響應型磁性納米載體(HA/CSO-SS-Hex/Fe3O4)的TEM圖;
圖11:實施例5中透明質酸修飾的還原響應型磁性納米載體(HA/CSO-SS-Hex/Fe3O4)的動態光散射柱狀分布圖;
圖12:實施例5中透明質酸修飾的還原響應型磁性納米載體(HA/CSO-SS-Hex/Fe3O4)在300K下的磁滯回線;
圖13:實施例5中透明質酸修飾的還原響應型磁性納米載體磁響應性,a為加磁鐵吸附前載體溶液的狀態,b為加磁鐵吸附1h后載體溶液的狀態,c為將b輕搖后載體溶液的狀態;
圖14:實施例5中透明質酸修飾的還原響應型磁性納米載體(HA/CSO-SS-Hex/Fe3O4)的細胞毒性;
圖15:實施例5中A549細胞對透明質酸修飾的還原響應型磁性納米載體(HA/CSO-SS-Hex/Fe3O4)攝取的定量分析;
圖16:實施例5中A549細胞對未經透明質酸修飾的還原響應型磁性納米載體(CSO-SS-Hex/Fe3O4)攝取的定量分析;
圖17:實施例8中透明質酸修飾的還原響應型磁性納米載藥復合物(HA/CSO-SS-Hex/Fe3O4/PTX)在不同環境下的藥物釋放曲線圖。
具體實施方式
以下具體實施例是對本發明的進一步說明,但下述僅用于說明本發明而非用于限定本發明的范圍。
1.疏水性超順磁性Fe3O4納米粒的合成
實施例1:
參照文獻J.Am.Chem.Soc.2004,126,273-279,稱取乙酰丙酮鐵(0.7063g,2mmol),1,2-十二烷二醇(2.0234g,10mmol),油酸(l.6948g,6mmol),油胺(1.605g,6mmol),二苯醚(20mL)在氬氣流110℃下攪拌1h以除去水和氧氣,將溫度上升至200℃(每分鐘升高8℃),在此溫度下反應2h,停止通氮氣,溫度加熱到265℃,回流反應30min,等反應液冷卻至室溫后,將反應液倒入40ml乙醇中沉淀,11000r/min*30min,用無水乙醇洗滌三次之后,將其分散到25ml的氯仿中保存。
通過透射電鏡(TEM)對其進行形貌觀察,結果如圖2,粒子形態近球形,粒徑在10nm以下。
通過振動樣品磁強計(VSM)對它的磁性能進行表征,結果如圖3,磁滯回線表明,合成的磁納米粒飽和磁化強度為39.58emu/g,幾乎沒有剩磁和矯頑力,驗證了合成的Fe3O4納米粒具有很好的超順磁性行為。
2.還原響應性兩親性聚合物的制備
實施例2:鍵合有含還原敏感鍵Linker的十六醇改性殼寡糖的制備(CSO-SS-Hex)
1)鍵合有含還原敏感鍵Linker的疏水基團的合成:
將3,3’-二硫代二丙酸(1.50g,7.13mmol)和DCC(1.618g,7.84mmol)溶于20ml無水DMF中,氬氣保護下冰浴攪拌30min,將十六醇(1.729g,7.13mmol)和DMAP(87mg,0.713mmol)加入其中,繼續在冰浴下攪拌反應1h,之后將其轉移到室溫條件下攪拌反應2h,加入等體積的乙酸乙酯終止反應,過濾除去二環己脲,濾液加入少量水后乙酸乙酯萃取,合并乙酸乙酯層,減壓濃縮,于20ml甲醇/乙酸乙酯=1/1的混合溶劑中重結晶即得產物Hex-SS-COOH。其1H-NMR譜圖如圖4。
2)疏水改性殼寡糖的合成:
取分子量為5000Da的殼寡糖1g溶于2ml超純水中后,加入20ml DMSO對其進行稀釋,65℃下預熱半小時,按照殼寡糖氨基含量的0.3倍當量稱取上述合成的含還原敏感連接臂的疏水基團,加入1.5倍當量的EDCI,NHS,溶于適量的DMSO中,65℃下活化30min,將其逐滴加入已預熱好的殼寡糖溶液中,65℃下反應24h,反應結束后將溶液逐滴加入到10倍體積的丙酮中,11000r/min離心3min,收集沉淀,用少量水復溶后,逐滴加入丙酮中,離心收集沉淀,重復上述操作三次,最后將所得紅棕色沉淀溶于適量水中,裝入透析袋中(MWCO 1000Da)透析24h,冷凍干燥,得CSO-SS-Hex。
Hex-SS-COOH 1H-NMR圖譜如圖4,圖譜中δ=1.25的峰歸屬22個亞甲基H信號,δ=0.874的峰歸屬為端甲基H信號,殼寡糖(CSO)1H-NMR圖譜如圖5,圖譜中δ=1.99的峰歸屬為-NHCOCH3的H的特征峰,CSO-SS-Hex 1H-NMR譜圖如圖6,圖譜中同時出現了上述兩種物質的特征峰,說明Hex-SS-COOH成功鍵合到了殼寡糖的骨架上。
通過透射電鏡對其形貌進行考察,結果如圖7,載體外觀呈球形,形態完整,具核殼結構。
通過馬爾文粒度儀對其粒徑分布進行考察,結果如圖8,粒徑比透射電鏡所測稍大,可能與透射電鏡測定是在粒子干燥情況下測定有關。
本發明采用將一定量的CSO-SS-Hex加入到10mM還原性谷胱甘肽溶液中,模擬載體在腫瘤組織中還原響應特點,間隔一段時間對其粒徑分布進行考察,結果如圖9,隨時間推移,載體粒徑分布逐漸變大,出現大于1000nm的粒子,表明該載體能快速響應高谷胱甘肽環境。
實施例3:鍵合有含還原敏感鍵Linker的膽固醇改性殼寡糖的制備(CSO-SS-Chol)
1)鍵合有含還原敏感鍵Linker的疏水基團的合成:
將3,3’-二硫代二丙酸(1.50g,7.13mmol)和DCC(1.618g,7.84mmol)溶于20ml無水THF中,氬氣保護下冰浴攪拌30min,將膽固醇(2.756g,7.13mmol)和DMAP(87mg,0.713mmol)加入其中,繼續在冰浴下攪拌反應1h,之后將其轉移到室溫條件下攪拌反應12h,過濾除去二環己脲,減壓濃縮,于20ml乙酸乙酯/正己烷=1/1的混合溶劑中重結晶即得產物Chol-SS-COOH。
2)疏水改性殼寡糖的合成:
取分子量為5000Da的殼寡糖1g溶于2ml超純水中后,加入20ml DMSO對其進行稀釋,65℃下預熱半小時,按照殼寡糖氨基含量的0.3倍當量稱取上述合成的含還原敏感連接臂的疏水基團,加入1.5倍當量的EDCI,NHS,溶于適量的DMSO中,65℃下活化30min,將其逐滴加入已預熱好的殼寡糖溶液中,65℃下反應24h,反應結束后將溶液逐滴加入到10倍體積的丙酮中,11000r/min離心3min,收集沉淀,用少量水復溶后,逐滴加入丙酮中,離心收集沉淀,重復上述操作三次,最后將所得紅棕色沉淀溶于適量水中,裝入透析袋中(MWCO 1000Da)透析24h,冷凍干燥,得CSO-SS-Chol。
實施例4:鍵合有含還原敏感鍵Linker的維生素E改性殼寡糖的制備(CSO-SS-VE)
1)鍵合有含還原敏感鍵Linker的疏水基團的合成:
將3,3’-二硫代二丙酸(1.50g,7.13mmol)和DCC(1.618g,7.84mmol)溶于20ml無水CH2Cl2中,氬氣保護下冰浴攪拌30min,將維生素E(3.071g,7.13mmol)和DMAP(87mg,0.713mmol)加入其中,繼續在冰浴下攪拌反應1h,之后將其轉移到室溫條件下攪拌反應12h,過濾除去二環己脲,減壓濃縮,于20ml乙酸乙酯/正己烷=1/1的混合溶劑中重結晶即得產物VE-SS-COOH。
2)疏水改性殼寡糖的合成:
取分子量為5000Da的殼寡糖1g溶于2ml超純水中后,加入20ml DMSO對其進行稀釋,65℃下預熱半小時,按照殼寡糖氨基含量的0.3倍當量稱取上述合成的含還原敏感連接臂的疏水基團,加入1.5倍當量的EDCI,NHS,溶于適量的DMSO中,65℃下活化30min,將其逐滴加入已預熱好的殼寡糖溶液中,65℃下反應24h,反應結束后將溶液逐滴加入到10倍體積的丙酮中,11000r/min離心3min,收集沉淀,用少量水復溶后,逐滴加入丙酮中,離心收集沉淀,重復上述操作三次,最后將所得紅棕色沉淀溶于適量水中,裝入透析袋中(MWCO:1000Da)透析24h,冷凍干燥,得CSO-SS-VE。
3.配體修飾的的還原響應兩親性聚合物對Fe3O4納米粒子裝載
實施例5:
稱取具還原響應性的兩親性聚合物(CSO-SS-Hex)20mg溶于10ml超純水中,吸取1ml Fe3O4溶液(約10mg),在劇烈攪拌條件下將其注入兩親性聚合物溶液中,細胞破碎儀(振幅30%,工作2s,停3s)超聲乳化3min,室溫下敞口攪拌使氯仿自然揮發,待氯仿揮盡后,在劇烈攪拌下,以極緩慢的速度逐滴將3ml 1mg/ml的透明質酸(分子量為14600Da)溶液加入其中,攪拌30min后,將溶液以4000r/min離心10min,棄去沉淀,收集上清液,上清液過0.45μm微孔濾膜,收集濾液,凍干即為配體修飾的還原響應型磁性納米載體。
為了更好的說明本方法制備的透明質酸修飾的還原響應型磁性納米載藥載體的性能,根據以下測試方法進行性能測定,包括形貌表征、粒徑分布測定、磁性能考察。
本發明通過透射電鏡(TEM)對制備的透明質酸修飾的還原響應型磁性納米載藥載體形貌進行表征,制備的載藥載體外觀呈球形,形貌均一,結果如圖10。
通過馬爾文粒度儀對其粒徑分布進行考察,所測粒徑大小與透射電鏡結果相一致,結果如圖11。
利用振動樣品磁強計(VSM)對其磁性能進行考察,所得磁滯回線如圖12,飽和磁強度為8.53emu/g,幾乎觀測不到矯頑力和剩磁,故表現出超順磁性行為,可滿足生物醫學的應用。
本發明利用永磁鐵對所制備的靶向配體修飾的還原響應型磁性納米載體的磁響應行為進行更加直觀的考察。準確配制1mg/ml的靶向配體修飾的還原響應型磁性納米載體水溶液,將其置于10ml的西林瓶中,在西林瓶一側放一磁鐵,觀測載體的磁響應行為,結果如圖13,所制備的靶向配體修飾的還原響應型磁性納米載體具良好的磁響應性,放置磁鐵前載體溶液呈均一的溶液狀態(圖13a),在溶液一側放置磁鐵后可快速在磁體附近富集(圖13b),輕搖后立即重新分散為均一狀態,無沉淀析出(圖13c)。
本發明制備的靶向配體修飾的還原響應型磁性納米載體通過MTT實驗對其生物相容性進行考察。精密稱取一定量的靶向配體修飾的還原響應型磁性納米載體,加入適量的PBS緩沖液(PH=7.4),超聲配制成2mg/ml的載體懸液,實驗前,在無菌的條件下,用新鮮的DMEM不完全培養基將載體懸液分別稀釋為400μg/ml,200μg/ml,100μg/ml,50μg/ml,25μg/ml,10μg/ml,5μg/ml,1μg/ml。取對數生長期的的A549或SMMC-7721細胞,胰酶消化收集細胞后,以5*10^3個/孔的密度接種到96孔板中,每孔加入100μl含10%胎牛血清的的DMEM培養基,每組設置三個平行孔。孵育24h待細胞貼壁80%后,用移液槍吸棄上清液,更換為100μl DMEM培養基或者含不同濃度樣品的DMEM培養基,繼續孵育48h,取出96孔板,避光條件下加入10μl 5mg/ml的MTT溶液,繼續避光孵育2h,使用酶標儀在570nm波長下測定各孔的吸光度值,記錄結果,按照下述公式計算細胞的存活率:
其結果如圖14,本發明制備的靶向配體修飾的還原響應型磁性納米載體即使在400μg/ml的高濃度下,對人非小細胞性肺癌細胞(A549)和人肝癌細胞(SMMC-7721)共孵育48h,仍保持有70%以上田胞存活率,表明本發明制備的靶向配體修飾的還原響應型磁性納米載體具有較低的細胞毒性,具有較好的生物相容性。
為說明本發明制備的靶向配體修飾的還原響應型磁性納米載體中靶向配體的修飾有助于腫瘤細胞對該載體的攝取,本發明以未經靶向配體修飾的載體為對照組,通過FITC對載體進行熒光標記,以A549為模型細胞,采用流式細胞儀對細胞內熒光強度進行定量分析,HA/CSO-SS-Hex/Fe3O4和CSO-SS-Hex/Fe3O4細胞內熒光強度結果分別如圖15和圖16,結果表明,經共孵育后,胞內載體的熒光強度呈時間依賴性,同一時間點時,靶向配體修飾的載體組胞內熒光強度更強,說明靶向配體的加入能有效促進腫瘤細胞對載體的攝入。
實施例6:
稱取具還原響應性的的兩親性聚合物(CSO-SS-Chol)20mg溶于10ml超純水中,吸取1ml Fe3O4溶液(約10mg),在劇烈攪拌條件下將其注入兩親性聚合物溶液中,細胞破碎儀(振幅30%,工作2s,停3s)超聲乳化3min,室溫下敞口攪拌使氯仿自然揮發,待氯仿揮盡后,在劇烈攪拌下,以極緩慢的速度逐滴將3ml 1mg/ml的透明質酸(分子量為14600Da)溶液加入其中,攪拌30min后,將溶液以4000r/min離心10min,棄去沉淀,收集上清液,上清液過0.45μm微孔濾膜,收集濾液,凍干即為配體修飾的還原響應型磁性納米載體。
實施例7:
稱取具還原響應性的的兩親性聚合物(CSO-SS-VE)20mg溶于10ml超純水中,吸取1ml Fe3O4溶液(約10mg),在劇烈攪拌條件下將其注入兩親性聚合物溶液中,細胞破碎儀(振幅30%,工作2s,停3s)超聲乳化3min,室溫下敞口攪拌使氯仿自然揮發,待氯仿揮盡后,在劇烈攪拌下,以極緩慢的速度逐滴將3ml 1mg/ml的透明質酸(分子量為14600Da)溶液加入其中,攪拌30min后,將溶液以4000r/min離心10min,棄去沉淀,收集上清液,上清液過0.45μm微孔濾膜,收集濾液,凍干即為配體修飾的還原響應型磁性納米載體。
4.配體修飾的還原響應型磁性納米載體對疏水性抗腫瘤藥物的裝載
實施例8:
稱取具還原響應性的的兩親性聚合物(CSO-SS-Hex)20mg溶于10ml超純水中,吸取1ml Fe3O4溶液(約10mg),在劇烈攪拌條件下將其注入兩親性聚合物溶液中,細胞破碎儀(振幅30%,工作2s,停3s)超聲乳化3min,室溫下敞口攪拌使氯仿自然揮發,待氯仿揮盡后,精密稱取10.0mg紫杉醇,溶于1ml無水乙醇中,配制成10mg/ml的紫杉醇乙醇溶液,將其以極緩慢的速度逐漸滴加到上述磁性納米載體溶液中,攪拌30min后,冰浴超聲(振幅30%,工作2s,停3s,15min),超聲完畢,在劇烈攪拌下,以極緩慢的速度逐滴將3ml 1mg/ml的透明質酸(分子量為14600Da)溶液加入其中,攪拌30min后,將其轉移到透析袋(MWCO:1000Da)中透析過夜,待透析結束,將透析袋中溶液全部轉移至燒杯中,以4000r/min離心10min,棄去沉淀,收集上清液,上清液過0.45μm微孔濾膜,收集濾液,凍干即為配體修飾的還原響應型磁性納米載藥復合物。
本發明采用將一定量的透明質酸修飾的還原響應型磁性納米載藥復合物置于3500Da透析袋中,并將其放入含有不同濃度還原性谷胱甘肽(GSH)的緩沖液中,模擬載體在不同生理環境下的藥物釋放行為,間隔一定時間取出一定量的透析液,利用高效液相色譜計算不同時間藥物的累計釋放量,結果如圖17所示,該載體具明顯的還原響應性,在高濃度的還原條件下可使藥物短時間內大量釋放,而在非還原條件下,藥物可以被很好地保護,不會使其過早的釋放和泄露。
實施例9:
稱取具還原響應性的的兩親性聚合物(CSO-SS-Chol)20mg溶于10ml超純水中,吸取1ml Fe3O4溶液(約10mg),在劇烈攪拌條件下將其注入兩親性聚合物溶液中,細胞破碎儀(振幅30%,工作2s,停3s)超聲乳化3min,室溫下敞口攪拌使氯仿自然揮發,待氯仿揮盡后,精密稱取10.0mg紫杉醇,溶于1ml無水乙醇中,配制成10mg/ml的紫杉醇乙醇溶液,將其以極緩慢的速度逐漸滴加到上述磁性納米載體溶液中,攪拌30min后,冰浴超聲(振幅30%,工作2s,停3s,15min),超聲完畢,在劇烈攪拌下,以極緩慢的速度逐滴將3ml 1mg/ml的透明質酸(分子量為14600Da)溶液加入其中,攪拌30min后,將其轉移到透析袋(MWCO:1000)中透析過夜,待透析結束,將透析袋中溶液全部轉移至燒杯中,以4000r/min離心10min,棄去沉淀,收集上清液,上清液過0.45μm微孔濾膜,收集濾液,凍干即為配體修飾的還原響應型磁性納米載藥復合物。
實施例10:
稱取具還原響應性的兩親性聚合物(CSO-SS-VE)20mg溶于10ml超純水中,吸取1mlFe3O4溶液(約10mg),在劇烈攪拌條件下將其注入兩親性聚合物溶液中,細胞破碎儀(振幅30%,工作2s,停3s)超聲乳化3min,室溫下敞口攪拌使氯仿自然揮發,待氯仿揮盡后,精密稱取10.0mg紫杉醇,溶于1ml無水乙醇中,配制成10mg/ml的紫杉醇乙醇溶液,將其以極緩慢的速度逐漸滴加到上述磁性納米載體溶液中,攪拌30min后,冰浴超聲(振幅30%,工作2s,停3s,15min),超聲完畢,在劇烈攪拌下,以極緩慢的速度逐滴將3ml 1mg/ml的透明質酸(分子量為14600Da)溶液加入其中,攪拌30min后,將其轉移到透析袋(MWCO:1000)中透析過夜,待透析結束,將透析袋中溶液全部轉移至燒杯中,以4000r/min離心10min,棄去沉淀,收集上清液,上清液過0.45μm微孔濾膜,收集濾液,凍干即為配體修飾的還原響應型磁性納米載藥復合物。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 靶向PD-1的多肽及其應用的制造方法與工藝
- 靶向同位素生產系統的制造方法與工藝
- 在制備68GA?螯合物官能化的靶向劑中用作金屬抑制劑的單糖、二糖或多糖的制造方法與工藝
- 用于引導和靶向按需物質遞送的納米結構的載體的制造方法與工藝
- 通過PROSTRATIN靶向K?RAS介導的信號轉導通路和惡性腫瘤的制造方法與工藝
- 腫瘤靶向核磁共振/熒光雙模態成像造影劑及其制備和應用的制造方法與工藝
- pH氧化還原雙敏感的PAMAM靶向納米給藥載體及其制備方法與制造工藝
- 具有卵巢腫瘤靶向D構型多肽及其基因遞釋系統的制造方法與工藝
- 靶向survivin納米抗體及其制備方法和應用與制造工藝
- 用于PSMA靶向的成像和放射療法的金屬/放射性金屬標記的PSMA抑制物的制造方法與工藝
- 阻斷UBE2M介導Neddylation修飾在腎細胞癌治療中的應用的制造方法與工藝
- 無載體共組裝腫瘤靶向抗癌納米藥物及其制備方法與應用與流程
- 一種用于判斷靶向單克隆抗體治療腫瘤療效的預測分子的制造方法與工藝
- 一種靶向CD47的免疫檢查點抑制劑藥物組合物及其制備方法與流程
- 具有淋巴靶向功能的生物自組裝納米晶注射劑及制備方法與流程
- 用于檢測肝癌的基因標志物及其用途的制造方法與工藝
- 特異性shRNA篩選及其靶向Ang?2基因抑制肺癌細胞的驗證方法與流程
- 一種多功能自動化生物細胞提取分離控制系統及采用該系統實現的細胞提取分離方法與流程
- 一種融合蛋白及光敏劑復合物及其制備方法和應用與流程
- 具有可視化和顯示光斑邊界功能的光動力治療系統的制造方法與工藝
- 腫瘤靶向核磁共振/熒光雙模態成像造影劑及其制備和應用的制造方法與工藝
- pH氧化還原雙敏感的PAMAM靶向納米給藥載體及其制備方法與制造工藝
- 具有卵巢腫瘤靶向D構型多肽及其基因遞釋系統的制造方法與工藝
- 靶向survivin納米抗體及其制備方法和應用與制造工藝
- 用于PSMA靶向的成像和放射療法的金屬/放射性金屬標記的PSMA抑制物的制造方法與工藝
- 一種線粒體靶向的粘度熒光探針及其制備方法和應用與制造工藝
- 一種兼具熒光可視、磁靶向和pH敏多功能的復合空心微球藥物載體及其制備方法與制造工藝
- 一種用于修飾微泡的多肽以及靶向GBM的藥物制劑的制造方法與工藝
- 白果內酯作為腦靶向增效劑在制備防治腦腫瘤藥物的應用的制造方法與工藝
- 機器人輔助精確靶向穿刺軟組織目標柔性針夾緊固定裝置的制造方法