含亞氨基二乙酸的99mTc標記的RGD多肽腫瘤診斷藥物及其制備方法與流程
本發明涉及用于腫瘤診斷的放射性藥物,特別涉及含新雙功能連接劑的用于intergrinαvβ3受體陽性腫瘤診斷的RGD多肽放射性藥物及其制備方法。
背景技術:
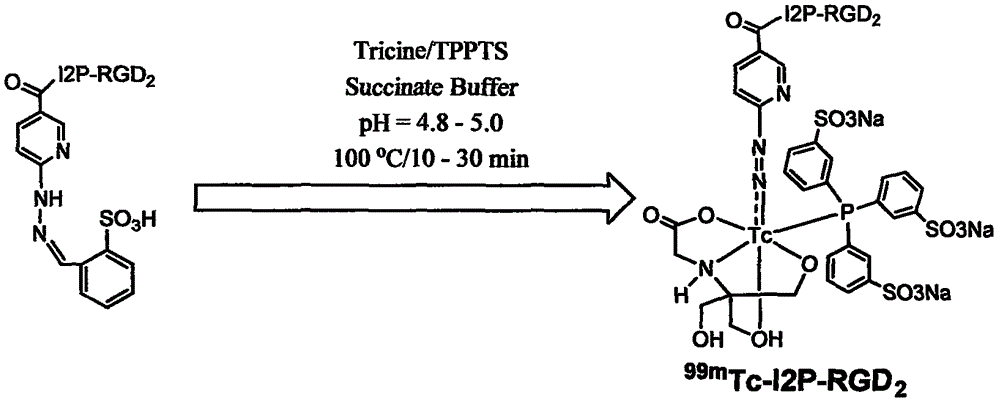
:據世界衛生組織(WHO)統計,全世界惡性腫瘤每年發病1100多萬人,病死800多萬人。惡性腫瘤發病率在我國也呈明顯上升趨勢,據國家衛生資料統計,近兩年來我國城市居民惡性腫瘤占死亡原因的第1位,每年新增患者約220萬人。近年來惡性腫瘤的治療手段在不斷發展,不僅傳統的化療和放療技術更加規范化和科學化,新的治療方法,如:分子靶向治療、免疫治療和基因治療等,正在逐步應用于臨床。與之相適應,要求惡性腫瘤診斷技術不僅要能夠進行準確的診斷,更迫切需要進一步反映惡性腫瘤的生物學行為和病理特點,為治療方案的科學化決策提供確切的依據。惡性腫瘤的轉移潛力直接關系到患者的預后,同時對于臨床醫師選擇治療方案具有至關重要的意義。但目前臨床上還缺乏準確判定惡性腫瘤轉移能力的檢測方法,而主要依靠經驗判斷。新生血管和淋巴管的形成在腫瘤發生、發展和轉移中發揮著重要的作用,腫瘤新生血管形成促進腫瘤生長和轉移,淋巴道形成與腫瘤轉移直接相關。整合素(integrin)是一組跨膜糖蛋白,由一個α亞單位和β亞單位通過非共價鍵組成的異二聚體,也是細胞外基質蛋白的受體,與細胞外基質蛋白(如纖維結合蛋白、玻璃結合蛋白、層粘蛋白和膠原等)的受體識別序列RGD(精氨酸-甘氨酸-天冬氨酸)特異結合。整合素調控新生血管和淋巴道的形成。諸多研究表明,整合素調控金屬基質蛋白酶等蛋白水解酶,直接參與細胞外基質的降解,促使腫瘤轉移;整合素的豐富表達是促使腫瘤細胞和血管內皮細胞遷移和侵襲的重要分子,它直接介導腫瘤細胞與基質蛋白的粘附和結合;參與調控胞內細胞骨架構成,細胞增殖。αvβ3是目前研究最多的整合素分子,在骨肉瘤、成神經細胞瘤、肺癌、乳腺癌、前列腺癌、膀胱癌、膠質母細胞瘤及浸潤性黑色素瘤等多種實體腫瘤細胞表面和腫瘤新生血管均有豐富的表達,在成熟血管內皮細胞和絕大多數正常組織表達缺乏或幾乎不表達。αvβ3受體介導腫瘤細胞粘附和移行,在腫瘤新生血管生成和淋巴道轉移發揮重要作用。αvβ3的表達水平與惡性腫瘤的浸潤轉移能力等惡性表型有關,也可以作為評價某些惡性腫瘤預后的的指標。放射性核素標記的RGD序列配體已經被用于腫瘤的放射性核素顯像研究,用于檢測轉移潛力較高的integrinαvβ3表達陽性的腫瘤。已有的研究結果認為:RGD多肽二聚體顯像劑與惡性腫瘤表面integrinαvβ3的親和力更好,要優于RGD多肽四聚體。目前報道的RGD環肽二聚體E[c(RGDxk)]2(E代表谷氨酸,c代表環化,R代表精氨酸,G代表甘氨酸,D代表天冬氨酸,x為f或y,分別代表苯丙氨酸和酪氨酸),其兩個RGD模序之間的距離為6個鍵,由于距離不夠長,因此E[c(RGDxk)]2的兩個RGD模序很難同時與細胞表面相鄰的兩個integrinαvβ3受體結合。但目前已有的RGD多肽二聚體顯像劑在非靶器官,特別是腸道等器官的攝取較多,腹部本底較高,干擾了腹部腫瘤的成像效果,肝臟和腎臟攝取高。因此,有必要發明新型的RGD多肽二聚體顯像劑,通過改變配體的結構,采用新的雙功能連接劑進一步降低顯像劑在腸等非靶器官的攝取,從而降低放射性本底,提高腫瘤顯像的圖像質量。技術實現要素:為克服已有技術的缺點,本發明的主要目的在于提供一種具有制備簡單、價格低廉、標記率和放射化學純度高、靶與非靶比值高、腫瘤攝取值高且滯留時間長等優點的以亞氨基二乙酸為雙功能連接劑的99mTc標記RGD多肽腫瘤診斷藥物。為達到上述目的,本發明的主要技術方案如下:將HYNIC-OSu與亞氨基二乙酸化的RGD肽二聚體I2P-RGD2相連接,制備得到配體HYNIC-I2P-RGD2。再利用配體中HYNIC的螯合作用,實現99mTc標記,制成RGD多肽二聚體顯像藥物99mTc-I2P-RGD2。在配體結構中引入亞氨基二乙酸以及兩個PEG4連接鏈,減少了藥物在肝臟、腎臟和腸道中的攝取,從而降低了放射性本底,提高了腫瘤顯像的圖像質量。具體技術方案如下:(1).一類含亞氨基二乙酸為雙功能連接劑的99mTc配合物99mTc-I2P-RGD2,其結構式如下式(1)所示:(2).一種用于制備如上述(1)所述的含亞氨基二乙酸的99mTc配合物99mTc-I2P-RGD2的方法,其特征在于,主要步驟為:先將HYNIC-OSu與亞氨基二乙酸化的RGD肽二聚體I2P-RGD2反應,使二者相連接,制備得到配體HYNIC-I2P-RGD2;再向反應瓶中加入20-25μgHYNIC-I2P-RGD2、5mg三苯基膦三間磺酸鈉(TPPTS)、6.5mgN-三(羥甲基)甲基甘氨酸(Tricine)、40mg甘露醇、38.5mg六水合琥珀酸二鈉、12.7mg琥珀酸和1.0-1.5mLNa99mTcO4生理鹽水溶液(1,110-1,850MBq),在沸水浴下反應10-15min得到。(3)如(1)所述的含亞氨基二乙酸為雙功能連接劑的99mTc配合物99mTc-I2P-RGD2在制備腫瘤診斷藥物中的應用。附圖說明[圖1]是表示標記前體化合物HYNIC-I2P-RGD2的合成路線示意圖;[圖2]是表示99mTc標記的診斷藥物99mTc-I2P-RGD2的合成路線示意圖;[圖3]是表示99mTc-I2P-RGD2的放射性HPLC圖譜;[圖4]是表示在過量E[c(RGDfK)]2抑制或未經E[c(RGDfK)]2抑制的條件下,99mTc-I2P-RGD2在荷U87MG人膠質瘤裸鼠中注射后60min的生物分布。[圖5]是表示99mTc-I2P-RGD2在荷U87MG人膠質瘤裸鼠模型中的3D和橫斷面的SPECT-CT圖像。具體實施方式一.99mTc標記的RGD多肽腫瘤診斷藥物的制備方法1.材料和設備化學試劑均購于美國Sigma/Aldrich公司,無需進一步純化。I2P-RGD2環肽二聚體(I2P-RGD2)由美國PeptidesInternational公司(Louisville,KY)按照常規工藝制造。HYNIC-Osu根據以往文獻中方法進行合成,屬于本領域普通技術知識。ESI(電噴射離子化)質譜數據由FinniganLCQ傳統質譜儀上采集獲得。99mTcO4-從原子高科股份有限公司購得。2.HPLC(高效液相色譜)方法HPLC方法1:使用LabAillance色譜系統,包括紫外-可見光檢測儀(波長為254nm)和ZorbaxC18半制備柱(柱寬×柱長為9.4nm×250mm,固定相的孔徑大小為美國AgilentTechnologies公司提供)。流速為2.5mL/min,流動相A相為含0.1%TFA的水;B相為含0.1%TFA的甲醇。流動相梯度:0-5min,90%A->80%A;5.01-20min,80%A->70%A。HPLC方法2:使用LabAillance色譜系統,包括-ramIN/US檢測儀(Tampa,FL)和ZorbaxC18色譜柱(柱寬×柱長為4.6mm×250mm,固定相的孔徑大小為美國AgilentTechnologies公司提供)。流速為1mL/min,流動相A相為25mMNH4OAc;B相為乙腈。流動相梯度為0-5min,90%A;5.01-20min,90%A->60%A;20.01-25min,60%A->40%A。3.標記前體化合物HYNIC-I2P-RGD2的制備方法將HYNIC-Osu(13.5mg,30μmol)和I2P-RGD2(5.9mg,3.2μmol)溶于DMF(2mL)。滴加過量的DIEA(5滴)至上述混合液,室溫攪拌24h至反應結束。將2mL水加至反應液中,用三氟乙酸(TFA)調節pH至3~4。產品經HPLC分離純化(HPLC方法1),收集保留時間12~15min的組分,冷凍干燥后得到5.8mg目標產物HYNIC-I2P-RGD2(合成路線圖參見圖1)。ESI-MS(C95H141N25O30S):實驗值為2145.28([M]+),計算值為2145.00([M]+)。4.99mTc-I2P-RGD2的制備方法將1.0~1.5mL含有1110~1850MBqNa99mTcO4的生理鹽水加至含有20-25μgHYNIC-I2P-RGD、5mgTPPTS、6.5mgtricine、40mg甘露醇、38.5mg六水合琥珀酸二鈉和12.7mg琥珀酸的凍干瓶中。將上述反應液在沸水浴中反應10~15min,然后在室溫中放置5min,采用HPLC對反應產物進行分析(HPLC方法2)(合成路線參見圖2)。將上述反應液配制成約30μCi/mL的生理鹽水溶液用于生物分布研究,配制成約1mCi/mL的生理鹽水溶液用于顯像研究。用于上述兩個實驗的99mTc-I2P-RGD2,其放化純度>90%。在給動物注射前,溶液均經0.20μmMillex-LG濾膜過濾,每只動物注射0.1mL。從99mTc-I2P-RGD2的放射性HPLC圖譜(參見圖3)可見,99mTc-I2P-RGD2具有高的放射化學純度,RCP>95%。二.動物實驗生物分布及顯像研究依據美國國家衛生研究院動物實驗指南進行,并符合動物倫理的要求。U87MG膠質瘤細胞株用含厄爾平衡鹽緩沖液的MEM培養基培育,并培養基中添加了10%胎牛血清和1%青霉素和鏈霉素。腫瘤細胞于37℃,含有5%CO2的培養箱中培養。所有細胞單層生長,待達到90%匯合度時收獲。選擇雌性4-5周齡裸鼠,將腫瘤細胞懸于生理鹽水中,數量調整為5×107個/mL,取0.1mL細胞懸液植于裸鼠肩側。所有步驟均于超凈臺內進行。待腫瘤長至0.1~0.5g時進行實驗。1.99mTc-I2P-RGD2在荷U87MG人膠質瘤的裸鼠中的生物分布實驗隨機選擇5只荷瘤小鼠(20~25g),均于尾靜脈注射約3μCi99mTc-I2P-RGD2。在注射5、30、60和120min后,將動物用過量的戊巴比妥鈉(約200mg/kg)麻醉處死。從心臟取血樣,再取出腫瘤及正常器官(腦、眼、心、脾、肺、肝、腎、肉和腸),用生理鹽水洗滌后擦干稱重,并用PerkinElmerWizard1480γ計數器(Shelton,CT)測計數,從而計算出各組織的單位質量注射劑量百分數(%ID/g)和瘤與正常組織的比值。表1列出了99mTc-I2P-RGD2在荷U87MG人膠質瘤的裸鼠中不同時相的生物分布數據;表2對荷U87MG人膠質瘤裸鼠注射后60min后,99mTc-99mTc-I2P-RGD2和99mTc-3P-RGD2的生物分布數據進行了比較。表199mTc-I2P-RGD2在荷U87MG人膠質瘤的裸鼠中的生物分布數據(%ID/g)器官5min30min60min120min血3.62±0.411.02±0.040.51±0.050.27±0.04腦0.34±0.100.30±0.060.16±0.020.18±0.06眼2.48±0.633.46±0.922.25±1.111.96±0.72心4.30±0.913.21±0.801.82±0.391.51±0.43腸23.99±5.7212.32±2.897.36±1.347.11±0.84腎24.80±3.8316.07±1.4312.17±1.169.73±1.37肝5.55±0.492.45±0.191.76±0.211.67±0.40肺6.44±1.214.55±0.482.28±0.452.27±0.27肌肉2.46±0.502.19±0.281.39±0.341.21±0.36脾5.03±0.653.26±0.622.91±0.702.69±0.53腫瘤7.24±1.186.61±0.885.61±1.385.28±1.31腫瘤/血2.04±0.296.48±0.729.31±0.4422.35±4.51腫瘤/肝1.32±0.282.68±0.592.85±0.333.47±0.75腫瘤/肺1.08±0.121.44±0.202.13±0.302.34±0.41腫瘤/肌肉3.13±0.513.10±0.263.33±0.523.82±0.15表2注射后60min,99mTc-I2P-RGD2與99mTc-3P-RGD2在荷U87MG人膠質瘤裸鼠中的生物分布數據比較(%ID/g)器官99mTc-I2P-RGD299mTc-3P-RGD2血0.51±0.050.70±0.11腦0.16±0.020.16±0.02眼2.25±1.112.00±0.28心1.82±0.392.01±0.19腸7.36±1.344.98±0.21腎12.17±1.1620.39±0.90肝1.76±0.214.68±0.40肺2.28±0.453.41±0.57肌肉1.39±0.341.73±0.25脾2.91±0.703.64±0.34腫瘤5.61±1.384.68±0.61腫瘤/血9.31±0.446.68±1.21腫瘤/肝2.85±0.331.01±0.45腫瘤/肺2.13±0.301.37±0.25腫瘤/肌肉3.33±0.522.70±0.89從表1中可以看出,注射后5、30、60和120min,99mTc-I2P-RGD2的腫瘤攝取依次為7.24±1.18、6.61±0.88、5.61±1.38和5.28±1.31%ID/g,注射后60min的腫瘤攝取值明顯高于99mTc-3P-RGD2。注射后5、30、60和120min,99mTc-I2P-RGD2在肝中的攝取依次為5.55±0.49、2.45±0.19、1.76±0.21和1.67±0.40%ID/g,腫瘤/肝攝取比值依次為1.32±0.28、2.68±0.59、2.85±0.33和3.47±0.75。注射后60min內,99mTc-I2P-RGD2在肝中的攝取與99mTc-3P-RGD2相比明顯降低。99mTc-I2P-RGD2在腎臟中的攝取值為12.17±1.16%ID/g,也明顯低于99mTc-3P-RGD2的20.39±0.90%ID/g,p<0.01(表2)。因此,認為99mTc-I2P-RGD2在非靶組織中的攝取更低,性能優于99mTc-3P-RGD2。2.99mTc-I2P-RGD2在荷U87MG人膠質瘤的裸鼠中的抑制實驗隨機選擇4只荷瘤小鼠(20-25g),均于尾靜脈共注射約3μCi99mTc-I2P-RGD2和約350μg(約14mg/kg)的經典整合素αvβ3拮抗劑E[c(RGDfK)]2(RGD2)。在注射60min后,將動物用過量的戊巴比妥鈉(約200mg/kg)麻醉處死。從心臟取血樣,再取出腫瘤及正常器官(腦、眼、心、脾、肺、肝、腎、肉和腸),用生理鹽水洗滌后擦干稱重,并用PerkinElmerWizard1480γ計數器(Shelton,CT)測計數,從而計算出各組織的單位質量注射劑量百分數(%ID/g)。抑制實驗的結果見圖4。由圖可知,未注射過量RGD2時99mTc-I2P-RGD2的腫瘤攝取為5.61±1.38%ID/g,而共注射過量RGD2后腫瘤攝取降至0.59±0.28%ID/g,可見過量的RGD2顯著抑制了99mTc-I2P-RGD2在腫瘤中的攝取。同樣地,RGD2也抑制了99mTc-I2P-RGD2在正常組織中的攝取。未經抑制時99mTc-I2P-RGD2在腸、肺和脾的攝取為7.36±1.34,2.28±0.45,2.91±0.71%ID/g,而抑制后它們相應的攝取依次降至0.88±0.26、0.85±0.39和0.51±0.03%ID/g。上述實驗清楚地證明,99mTc-I2P-RGD2在腫瘤中的定位是具有integrinαvβ3特異性的。3.99mTc-I2P-RGD2在荷U87MG人膠質瘤的裸鼠中的SPECT-CT顯像研究SPECT/CT顯像采用配有0.6mm多針孔準直器的u-SPECT-II/CT掃描儀(Milabs,Utrecht,TheNetherlands)。荷膠質瘤的小鼠經尾靜脈注射劑量為37.0MBq的99mTc-I2P-RGD2,體積為0.1mL。注射后60min后將其置于連有異氟醚麻醉裝置的屏蔽室內(Univentor,Zejtun,Malta),通過流速為350mL/min含有3.0%異氟醚的氣流進行麻醉。麻醉完畢后,立即將動物仰臥在掃描床上進行SPECT-CT掃描,并將氣流調整為流速250mL/min,含有2.0%異氟醚。顯像結束后,SPECT圖像采用迭代法(6次迭代,16個子集)進行重建,并進行SPECT圖像與CT圖像的融合。顯像結果見圖5,可見腫瘤部位放射性濃聚,顯影清晰,肺、腸道等器官放射性本底較低。由上述數據可見,99mTc-I2P-RGD2相比99mTc-3P-RGD2在多個方面均具備明顯的優勢,可適用于臨床中。當前第1頁1 2 3
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1