用于修復尿道損傷的生物修復材料及其制備方法與應用與流程
本發明涉及生物醫學領域中用于修復尿道損傷的生物修復材料及其制備方法與應用。
背景技術:
尿道損傷是一種常見的泌尿系統疾病,通常分為尿道內損傷和外損傷。尿道內損傷絕大多數是在應用經尿道器械操作或排出異物(如結石)時發生,少數由于異物插入尿道而引起;尿道誤注某些化學藥物如硝酸銀、硫酸銅、石炭酸等可引起化學灼傷。經尿道行電切除術時可致尿道電灼傷。尿道外暴力損傷較多見,可為貫通傷或閉合傷。前者主要見于戰場,尿道被火器或利器所穿破。受傷部位大多在球、膜部。海綿體部和前列腺部則少見。閉合性尿道損傷,在戰時和平時均可見到。會陰部騎跨傷或踢傷時受損部位多見于球部尿道,而伴骨盆骨折,時常伴膜部尿道損傷。
嚴重的尿道損傷往往需要重建手術來恢復其結構和功能。由于缺乏適當的重建材料,目前在臨床上進行尿道重建始終非常困難,尤其是大面積損傷尿道的重建在臨床治療上仍面臨挑戰,目前陰莖皮膚和粘膜是最常用的尿道重建替代物,不僅造成病人二次損傷,而且自體組織替代物隨著時間推移常常會萎縮,造成尿道再狹窄及其他一些并發癥。據統計,治療五年內的并發癥發生率超過21%,包括尿道再狹窄、尿道瘺、感染、勃起功能障礙等。而且如果尿道損傷長度超過4厘米,自體組織移植的尿道成形術往往不能成功。
技術實現要素:
本發明所要解決的技術問題是如何修復損傷尿道。
為解決上述技術問題,本發明首先提供了能修復尿道損傷的生物修復材料。
本發明所提供的生物修復材料,為用膠原結合血管內皮生長因子(CBD-VEGF)修飾膠原支架材料得到的生物材料;
所述膠原結合血管內皮生長因子為下述A1)或A2)或A3)的蛋白質:
A1)氨基酸序列為SEQ ID No.1的第1-184位氨基酸所示的蛋白質;
A2)在SEQ ID No.1的第1-184位氨基酸序列中經過取代和/或缺失和/或添加一個或幾個氨基酸殘基得到的具有相同功能的由A1)衍生的蛋白質;
A3)在A1)或A2)的N端或/和C端連接標簽得到的融合蛋白質。
其中,SEQ ID No.1由192個氨基酸組成,SEQ ID No.1的第1-166位氨基酸為血管內皮生長因子的序列;SEQ ID No.1的第178-184位氨基酸為膠原結合域的序列;SEQ ID No.1的第187-192位氨基酸為His標簽的序列。
上述A2)中的蛋白質可人工合成,也可先合成其編碼基因,再進行生物表達得到。上述A2)中的蛋白質的編碼基因可通過將序列表中SEQ ID No.2的第1-184位核苷酸所示的DNA序列中缺失一個或幾個氨基酸殘基的密碼子,和/或進行一個或幾個堿基對的錯義突變得到。上述A3)中的蛋白質可在SEQ ID No.2的第1-184位核苷酸所示的DNA序列的5′端和/或3′端連上標簽的編碼序列得到。所述標簽可為His標簽。
其中,SEQ ID No.2由576個核苷酸組成。SEQ ID No.2的第1-498位核苷酸編碼SEQ ID No.1的第1-166位氨基酸所示的血管內皮生長因子。
上述生物修復材料中,所述膠原支架材料可由如下方法制備:
1)用氫氧化鈉水溶液處理離體的動物皮膚,得到氫氧化鈉處理的材料;
2)用去污劑處理所述氫氧化鈉處理的材料,得到去污劑處理的材料;
3)除去所述去污劑處理的材料中的雜質,得到所述膠原支架材料。
上述生物修復材料中,所述生物修復材料可為用于修復尿道損傷的生物修復材料。所述標簽可為His標簽。
所述膠原支架材料可通過鈷源照射滅菌。
所述1)可重復1-4次。所述氫氧化鈉水溶液中氫氧化鈉的濃度可為2-5mol/L。
所述膠原結合血管內皮生長因子可通過表達含有所述膠原結合血管內皮生長因子的編碼基因的重組細胞得到;
所述膠原結合血管內皮生長因子的編碼基因可為如下a1)或a2)或a3)所示的基因:
a1)核苷酸序列是序列表中SEQ ID No.2的第1-552位或SEQ ID No.2的cDNA分子或DNA分子;
a2)與a1)限定的核苷酸序列具有75%或75%以上同一性,且編碼所述膠原結合血管內皮生長因子的cDNA分子或基因組DNA分子;
a3)在嚴格條件下與a1)限定的核苷酸序列雜交,且編碼所述膠原結合血管內皮生長因子的cDNA分子或基因組DNA分子。
其中,所述核酸分子可以是DNA,如cDNA、基因組DNA或重組DNA;所述核酸分子也可以是RNA,如mRNA或hnRNA等。SEQ ID No.2由576個核苷酸組成。SEQ ID No.2的第1-498位核苷酸編碼SEQ ID No.1的第1-166位氨基酸所示的血管內皮生長因子;SEQ ID No.2的第532-552位核苷酸編碼SEQ ID No.1的第178-184位氨基酸所示的膠原結合域;SEQ ID No.2的第559-576位核苷酸編碼SEQ ID No.1的第187-192位氨基酸所示的His標簽。
本領域普通技術人員可以很容易地采用已知的方法,例如定向進化和點突變的方法,對本發明的編碼所述膠原結合血管內皮生長因子的核苷酸序列進行突變。那些經 過人工修飾的,具有與本發明分離得到的所述膠原結合血管內皮生長因子的核苷酸序列75%或者更高同一性的核苷酸,只要編碼所述膠原結合血管內皮生長因子且具有相同功能,均是衍生于本發明的核苷酸序列并且等同于本發明的序列。
這里使用的術語“同一性”指與天然核酸序列的序列相似性。“同一性”包括與本發明的編碼SEQ ID No.1的第1-184位或SEQ ID No.1所示的氨基酸序列組成的蛋白質的核苷酸序列具有75%或更高,或85%或更高,或90%或更高,或95%或更高同一性的核苷酸序列。同一性可以用肉眼或計算機軟件進行評價。使用計算機軟件,兩個或多個序列之間的同一性可以用百分比(%)表示,其可以用來評價相關序列之間的同一性。
上述生物修復材料中,所述嚴格條件是在2×SSC,0.1%SDS的溶液中,在68℃下雜交并洗膜2次,每次5min,又于0.5×SSC,0.1%SDS的溶液中,在68℃下雜交并洗膜2次,每次15min;或,0.1×SSPE(或0.1×SSC)、0.1%SDS的溶液中,65℃條件下雜交并洗膜。
上述75%或75%以上同一性,可為80%、85%、90%或95%以上的同一性。
上述生物修復材料中,所述動物可為哺乳動物;所述去污劑為吐溫-80或其水溶液、或吐溫-20或其水溶液、或Triton X-100或其水溶液。
上述生物修復材料中,所述哺乳動物可為豬、牛、羊、馬或兔。
上述生物修復材料中,所述吐溫-80水溶液中吐溫-80的質量百分濃度可為1-5%;
所述吐溫-20水溶液中吐溫-20的質量百分濃度可為1-5%;
所述Triton X-100水溶液中Triton X-100的質量百分濃度可為1-5%。
上述生物修復材料中,所述膠原支架材料的制備方法還可包括在用所述氫氧化鈉水溶液處理所述離體的動物皮膚前去除所述動物皮膚粘附的肌肉組織和/或脂肪。
上述生物修復材料中,所述用氫氧化鈉水溶液處理所述離體的動物皮膚的時間可為10-60分鐘;
和/或,
所述用去污劑處理所述氫氧化鈉處理的材料的時間可為1-5小時。
上述生物修復材料中,所述除去所述去污劑處理的材料中的雜質可為用去熱原水清洗去污劑處理的材料,得到所述膠原支架材料。
上述生物修復材料中,所述生物修復材料可按照如下方法制備:將所述膠原支架材料浸泡在含有所述膠原結合血管內皮生長因子的溶液中得到所述生物修復材料。
上述生物修復材料中,所述膠原支架材料與所述溶液中所述膠原結合血管內皮生長因子的比例關系可為1cm2:(5-15)μg,如1cm2:10μg。
上述生物修復材料中,所述浸泡的時間可為20-40分鐘,如30分鐘。
為解決上述技術問題,本發明還提供了所述生物修復材料的制備方法。
本發明所提供的所述生物修復材料的制備方法,包括用所述膠原結合血管內皮生長因子修飾所述膠原支架材料得到所述生物修復材料。
上述方法中,所述用所述膠原結合血管內皮生長因子修飾所述膠原支架材料得到的生物材料的方法可包括將所述膠原支架材料浸泡在含有所述膠原結合血管內皮生長因子的溶液中得到所述生物修復材料。
上述方法中,所述膠原支架材料與所述溶液中所述膠原結合血管內皮生長因子的比例關系可為1cm2:(5-15)μg,如1cm2:10μg。
上述方法中,所述浸泡的時間可為20-40分鐘,如30分鐘。
上述方法中,所述方法還可包括利用所述膠原支架材料的制備方法制備所述膠原支架材料。
上述處理的溫度均可為2-8℃,優選是4℃。
為解決上述技術問題,本發明還提供了用于制備所述生物修復材料的成套試劑。
本發明所提供的用于制備所述生物修復材料的成套試劑,為下述M或N:
M、用于制備所述生物修復材料的成套試劑,由所述膠原結合血管內皮生長因子和所述膠原支架材料組成;
N、用于制備所述生物修復材料的成套試劑,由與所述膠原結合血管內皮生長因子相關的生物材料和所述膠原支架材料組成;
所述與所述膠原結合血管內皮生長因子相關的生物材料,為B1)至B16)中的任一種:
B1)編碼所述膠原結合血管內皮生長因子的核酸分子;
B2)含有B1)所述核酸分子的表達盒;
B3)含有B1)所述核酸分子的重組載體;
B4)含有B2)所述表達盒的重組載體;
B5)含有B1)所述核酸分子的重組微生物;
B6)含有B2)所述表達盒的重組微生物;
B7)含有B3)所述重組載體的重組微生物;
B8)含有B4)所述重組載體的重組微生物;
B9)含有B1)所述核酸分子的轉基因動物細胞系;
B10)含有B2)所述表達盒的轉基因動物細胞系;
B11)含有B3)所述重組載體的轉基因動物細胞系;
B12)含有B4)所述重組載體的轉基因動物細胞系;
B13)含有B1)所述核酸分子的轉基因植物細胞系;
B14)含有B2)所述表達盒的轉基因植物細胞系;
B15)含有B3)所述重組載體的轉基因植物細胞系;
B16)含有B4)所述重組載體的轉基因植物細胞系。
上述成套試劑中,B1)所述核酸分子可為所述膠原結合血管內皮生長因子的編碼基因。
上述成套試劑中,B2)所述的含有編碼所述膠原結合血管內皮生長因子的核酸分子的表達盒,是指能夠在宿主細胞中表達所述膠原結合血管內皮生長因子的DNA,該DNA不但可包括啟動所述膠原結合血管內皮生長因子基因轉錄的啟動子,還可包括終止所述膠原結合血管內皮生長因子基因轉錄的終止子。進一步,所述表達盒還可包括增強子序列。
可用現有的表達載體構建含有所述膠原結合血管內皮生長因子基因表達盒的重組載體。
上述成套試劑中,所述載體可為質粒、黏粒、噬菌體或病毒載體。
上述成套試劑中,所述微生物可為酵母、細菌、藻或真菌,如大腸桿菌。所述大腸桿菌具體可為BL21(DE3)。
上述成套試劑中,所述轉基因植物細胞系和轉基因動物細胞系均不包括繁殖材料。
為解決上述技術問題,本發明還提供了下述任一應用:
X1、所述生物修復材料在制備促進尿道損傷修復的材料中的應用;
X2、所述生物修復材料在制備促進尿道血管再生的材料中的應用;
X3、所述生物修復材料在制備促進尿道上皮再生的材料中的應用;
X4、所述生物修復材料在制備促進尿道平滑肌再生的材料中的應用;
X5、所述成套試劑在制備生物修復材料中的應用;
X6、所述成套試劑在制備促進尿道損傷修復的材料中的應用;
X7、所述成套試劑在制備促進尿道血管再生的材料中的應用;
X8、所述成套試劑在制備促進尿道上皮再生的材料中的應用;
X9、所述成套試劑在制備促進尿道平滑肌再生的材料中的應用;
X10、所述方法在制備生物修復材料中的應用;
X11、所述方法在制備促進尿道損傷修復的材料中的應用;
X12、所述方法在制備促進尿道血管再生的材料中的應用;
X13、所述方法在制備促進尿道上皮再生的材料中的應用;
X14、所述方法在制備促進尿道平滑肌再生的材料中的應用。
上述應用中,所述尿道可為哺乳動物尿道。所述哺乳動物可為大鼠。
實驗證明,本發明的生物修復材料可以修復尿道的損傷,并促進尿道上皮、尿道 血管及尿道平滑肌的再生與尿道功能的恢復:
(1)植入生物修復材料的術后實驗組比格犬中出現排尿困難,植入膠原支架材料的術后對照組比格犬全部出現了排尿困難癥狀。
(2)術后對照組比格犬和植入生物修復材料的術后實驗組比格犬的平均再造尿道直徑分別為0.92±0.13mm和1.86±0.19mm,術后實驗組比格犬的平均再造尿道直徑顯著大于術后對照組比格犬的平均再造尿道直徑(p<0.05);術后對照組比格犬出現尿道瘺,術后實驗組比格犬均沒有尿道瘺的出現。
(3)術前實驗組比格犬尿道的最大尿道壓在陰莖骨包繞的尿道部位;術后實驗組比格犬再造尿道的尿道壓普遍顯著升高,甚至高于術前實驗組比格犬尿道的陰莖骨包繞的尿道部位,而新的最大尿道壓通常位于再造尿道和原尿道連接部位。
(4)植入生物修復材料的術后實驗組比格犬的沒有后尿道擴張出現,而術后對照組比格犬出現后尿道擴張。術后實驗組比格犬再造尿道的平均長度是4.6±0.3cm,顯著高于術后對照組比格犬的再造尿道的平均長度3.4±0.8cm(p<0.05);實驗組比格犬的再造尿道軟而光滑,而對照組比格犬則硬而粗糙,且對照組比格犬的再造尿道周圍出現更多的瘢痕組織。術后對照組有80%的比格犬出現尿道閉塞,術后實驗組比格犬均沒有出現尿道閉塞。
(5)植入生物修復材料的術后實驗組比格犬的尿道上皮細胞覆蓋了整個再造尿道,而對照組比格犬的尿道上皮細胞層在再造尿道中間部分常是不完整的,且對照組比格犬的尿道上皮細胞層比實驗組薄。
(6)植入生物修復材料的術后實驗組比格犬再造尿道的上皮由8-10層上皮細胞組成,覆蓋整個再造尿道,細胞排列整齊,具有正常尿道組織上皮細胞的形態特征;而對照組比格犬再造尿道的上皮由3-5層上皮細胞組成,細胞排列松散,未能完整覆蓋再造尿道,且有尿道瘺出現。實驗組比格犬再造尿道的上皮層的厚度為99.60±11.37μm,與健康雄性比格犬尿道上皮層厚度(95.32±22.41μm)無顯著差異(P>0.05),但與比格犬尿道損傷處的上皮層厚度(42.66±3.77μm)有顯著性差異(P<0.01)。
(7)術后對照組比格犬尿道重建處的血管平均熒光強度為0.026±0.003,術后實驗組比格犬尿道重建處的血管平均熒光強度為0.038±0.008,健康雄性比格犬尿道的血管平均熒光強度為0.041±0.008。術后實驗組比格犬尿道重建處的血管平均熒光強度高于術后對照組比格犬尿道重建處的血管平均熒光強度,并且二者具有顯著性差異(P<0.01)。
(8)術后對照組比格犬尿道重建處的平滑肌組織平均熒光強度2.58±1.50,術后實驗組比格犬尿道重建處的平滑肌組織平均熒光強度為65.04±4.85,術后實驗組 比格犬尿道重建處的平滑肌組織平均熒光強度高于術后對照組比格犬尿道重建處的平滑肌組織平均熒光強度,并且二者具有顯著性差異(P<0.01)。
實驗證明,本發明的生物修復材料可以用來修復尿道損傷。
附圖說明
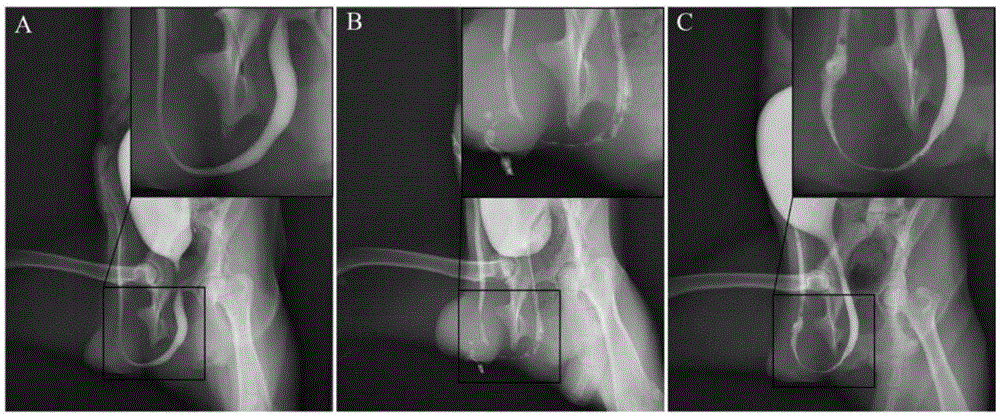
圖1為術后6個月對照組比格犬和術后6個月實驗組比格犬的逆行尿道造影。其中,A為未經行任何手術的健康雄性比格犬;B為術后6個月對照組比格犬;C為術后6個月實驗組比格犬。
圖2為術前和術后6個月的實驗組比格犬的尿動力學測定。其中,A為術前實驗組比格犬,B為術后6個月的實驗組比格犬。
圖3為術后6個月實驗組比格犬和術后6個月對照組比格犬泌尿系統的形態觀察。其中A為術后6個月對照組比格犬的完整泌尿系統;B為術后6個月對照組比格犬的尿道;C為術后6個月對照組縱形剖開后的比格犬的再造尿道;D為術后6個月實驗組比格犬的完整泌尿系統;E為術后6個月實驗組比格犬的尿道;F為術后6個月實驗組縱形剖開后的比格犬的再造尿道。
圖4為術后6個月實驗組比格犬和術后6個月對照組比格犬尿道重建處的HE染色結果。其中,A為未經行任何手術的健康雄性比格犬的尿道的橫向切片,B為術后6個月實驗組比格犬尿道重建處的橫向切片,C為術后6個月對照組比格犬尿道重建處的橫向切片,D為未經行任何手術的健康雄性比格犬的尿道的縱向切片,E為術后6個月實驗組比格犬尿道重建處的縱向切片,F為術后6個月對照組比格犬尿道重建處的縱向切片。
圖5為術后6個月實驗組比格犬和術后6個月對照組比格犬尿道重建處的免疫熒光染色結果。其中,A為未經行任何手術的健康雄性比格犬的尿道的橫向切片,B為術后6個月實驗組比格犬尿道重建處的橫向切片,C為術后6個月對照組比格犬尿道重建處的橫向切片,D為未經行任何手術的健康雄性比格犬的尿道的縱向切片,E為術后6個月實驗組比格犬尿道損重建的縱向切片,F為術后6個月對照組比格犬尿道重建處的縱向切片。
圖6為術后6個月實驗組比格犬和術后6個月對照組比格犬尿道重建處的上皮層的厚度。
圖7為術后6個月實驗組比格犬和術后6個月對照組比格犬尿道重建處的血管再生情況。其中,A為未經行任何手術的健康雄性比格犬的尿道的橫向切片,B為術后6個月實驗組比格犬尿道重建處的橫向切片,C為術后6個月對照組比格犬尿道重建處的橫向切片,D為未經行任何手術的健康雄性比格犬的尿道的縱向切片,E為術后6個月實驗組比格犬尿道重建處的縱向切片,F為術后6個月對照組比格犬尿道重建處 的縱向切片。
圖8為術后6個月實驗組比格犬和術后6個月對照組比格犬尿道重建處的血管組織平均熒光強度。
圖9為術后6個月實驗組比格犬和術后6個月對照組比格犬尿道重建處的平滑肌再生情況。其中,A為未經行任何手術的健康雄性比格犬的尿道的橫向切片,B為術后6個月實驗組比格犬尿道重建處的橫向切片,C為術后6個月對照組比格犬尿道重建處的橫向切片,D為未經行任何手術的健康雄性比格犬的尿道的縱向切片,E為術后6個月實驗組比格犬尿道重建處的縱向切片,F為術后6個月對照組比格犬尿道重建處的縱向切片。
圖10為術后6個月實驗組比格犬和術后6個月對照組比格犬尿道損重建的平滑肌組織平均熒光強度。
具體實施方式
下面結合具體實施方式對本發明進行進一步的詳細描述,給出的實施例僅為了闡明本發明,而不是為了限制本發明的范圍。
下述實施例中的實驗方法,如無特殊說明,均為常規方法。
下述實施例中所用的材料、試劑等,如無特殊說明,均可從商業途徑得到。
下述實施例中的比格犬為四川養麝研究所產品。
實施例1、生物修復材料的制備
本發明所提供的生物修復材料為用膠原結合血管內皮生長因子(CBD-VEGF)修飾膠原支架材料得到的生物材料;膠原結合血管內皮生長因子為氨基酸序列是序列表中SEQ ID No.1的蛋白質,其編碼序列為序列表中SEQ ID No.2。
其中,SEQ ID No.1的第1-166位氨基酸為血管內皮生長因子的序列,其編碼序列為SEQ ID No.2的第1-498位核苷酸;SEQ ID No.1的第178-184位氨基酸為膠原結合域的序列,其編碼序列為SEQ ID No.2的第532-552位核苷酸;SEQ ID No.1的第187-192位氨基酸為His標簽的序列,其編碼序列為SEQ ID No.2的第559-576位核苷酸。
一、膠原結合血管內皮生長因子(CBD-VEGF)的制備
將中國專利CN 101671396B的重組表達載體pET28a-VEGF-CBD-6His導入大腸桿菌BL21(DE3)(Novagen產品,貨號為VDN0199)中,得到重組菌,將該重組菌命名為BL21-T-CBD-VEGF,BL21-T-CBD-VEGF能表達SEQ ID No.1所示的CBD-VEGF。
將BL21-T-CBD-VEGF接種至LB培養基中進行培養,得到BL21-T-CBD-VEGF培養液;按2%的接種量將BL21-T-CBD-VEGF培養液轉接至LB培養基中擴大培養后加入IPTG,得到誘導前液,誘導前液中IPTG的濃度為1mM;將誘導前液在37℃下培養5小時,得 到BL21-T-CBD-VEGF誘導液。將BL21-T-CBD-VEGF誘導液在8000rpm、4℃下進行離心,棄上清液,得到BL21-T-CBD-VEGF菌體。將BL21-T-CBD-VEGF菌體進行超聲并進行離心,得到含有CBD-VEGF的上清液,超聲條件為(超聲5s,工作5s,共15min,功率100w)。
將CBD-VEGF的上清液進行鎳柱親和層析純化目的蛋白CBD-VEGF,最后將目的蛋白CBD-VEGF收集在PBS中,得到CBD-VEGF溶液,CBD-VEGF溶液中CBD-VEGF的濃度為300μg/ml,-80℃下保存。
聚丙烯酰胺凝膠電泳檢測CBD-VEGF溶液中的目的蛋白CBD-VEGF,結果顯示,CBD-VEGF溶液中含有預期蛋白大小相符的目的蛋白CBD-VEGF。
二、膠原支架材料的制備
膠原支架材料按照如下的膠原支架材料的制備方法制備:
1)用2-5mol/L氫氧化鈉水溶液處理動物體表皮膚,得到氫氧化鈉處理的材料;
2)用去污劑處理氫氧化鈉處理的材料,得到去污劑處理的材料;
3)除去去污劑處理的材料中的雜質,得到膠原支架材料。
具體制備方法如下:
a1)剝取豬體表皮膚;機械去掉豬體表皮膚表皮下附帶成分(如肌肉、脂肪等)得到豬上皮組織;去離子水清洗豬上皮組織,得到清洗后的豬上皮組織;
a2)將步驟a1)得到的清洗后的豬上皮組織完全浸泡在2-5mol/L氫氧化鈉水溶液中,處理30分鐘,棄液體,重復3次,得到氫氧化鈉處理的材料;
a3)將步驟a2)得到的氫氧化鈉處理的材料完全浸泡在吐溫-80水溶液(吐溫-80水溶液吐溫-80的質量百分濃度為3%)中,處理3小時,棄液體,得到去污劑處理的材料;
a4)用去熱原水充分清洗步驟a3)得到的去污劑處理的材料,去掉化學成分殘留,得到膠原支架材料,將其保存于生理鹽水中;
a5)用生理鹽水漂洗步驟a4)得到的膠原支架材料2小時,然后于凍干機中冷凍干燥,最后用鈷源照射后進行密封保存。
三、生物修復材料的制備
利用步驟一得到的CBD-VEGF和步驟二得到的膠原支架材料制備生物修復材料,具體方法如下:
選取步驟二得到的膠原支架材料,將其浸泡在步驟一得到的CBD-VEGF溶液中,膠原支架材料與CBD-VEGF溶液中CBD-VEGF的比例關系為1cm2:10μg,室溫孵育30分鐘,使CBD-VEGF溶液中的CBD-VEGF被膠原支架材料吸收,得到生物修復材料。
實施例2、生物修復材料對尿道損傷的修復
實驗重復三次,每次重復實驗的具體步驟如下:
1、動物分組
將10只12-14個月的健康雄性比格犬(平均體重11±1.2kg)隨機分為兩組,即對照組和實驗組,每組5只。
2、手術過程:
對實驗組的每只比格犬用腹腔注射戊巴比妥鈉(30mg戊巴比妥鈉/kg體重)進行麻醉,仰臥位固定于手術臺上。縱行切開會陰部暴露尿道海綿體,將陰莖骨和尿道球部之間的尿道海綿體從陰莖海綿體部切除。通過將整個前尿道切除5cm來制作大面積尿道缺陷模型。實施例1的生物修復材料用可吸收線通過間斷縫合術與自體尿道兩端吻合。在縫合之前用12F的導管通過新建的尿道插入膀胱中,用滅菌絲線將該導管與尿道口固定。術后兩周將12F的導管去除,得到術后實驗組比格犬。觀察比格犬有無任何排尿困難、膀胱膨脹、胃腸癥狀或其他不良狀態。
按照上述方法,將實驗組替換為對照組,并將實施例1的生物修復材料替換為實施例1的膠原支架材料,其他步驟均不變,得到術后對照組比格犬。
3、術后排尿狀況
觀察步驟2的術后實驗組和對照組比格犬的排尿情況,結果顯示,5只術后對照組比格犬都出現了排尿困難癥狀。5只術后實驗組比格犬中,有兩只沒有出現排尿困難,一只出現輕微排尿困難,兩只出現排尿困難。
4、逆行尿道造影術
將步驟2的術后實驗組與對照組比格犬,在正常相同條件下喂養6個月,得到術后6個月對照組比格犬和術后6個月實驗組比格犬。對術后6個月對照組比格犬和術后6個月實驗組比格犬行逆行尿道造影術,將未經行任何手術的健康雄性比格犬作為對照。結果顯示(圖1),健康雄性比格犬尿道光滑通暢(圖1中A),平均尿道直徑為5.94±0.65mm;術后6個月對照組比格犬(圖1中B)和術后6個月實驗組比格犬(圖1中C)都出現不同程度的尿道狹窄,術后6個月對照組比格犬尿道狹窄更嚴重,術后6個月對照組比格犬和術后6個月實驗組比格犬的平均再造尿道直徑分別為0.92±0.13mm和1.86±0.19mm,術后6個月實驗組比格犬的平均再造尿道直徑顯著大于術后6個月對照組比格犬的平均再造尿道直徑(p<0.05)。術后6個月對照組比格犬出現尿道瘺,出現尿道瘺的比格犬占術后6個月對照組比格犬的60%;術后6個月實驗組比格犬均沒有尿道瘺的出現。說明本發明的生物修復材料可以修復尿道的損傷,并促進尿道的再生。
5、尿動力學
由于嚴重尿道狹窄會致使尿動力測量導管無法通過再造尿道插入膀胱,所以無法 測量術后6個月對照組比格犬的尿動力學。對步驟4的術前和術后6個月的實驗組比格犬進行尿動力學測試,結果如圖2所示。結果顯示,術前實驗組比格犬尿道的最大尿道壓在陰莖骨包繞的尿道部位(圖2中A);術后實驗組比格犬再造尿道的尿道壓普遍顯著升高,甚至高于術前實驗組比格犬尿道的陰莖骨包繞的尿道部位,而新的最大尿道壓通常位于再造尿道和原尿道連接部位(圖2中B)。充盈性旁觀測壓表明最大膀胱容量和膀胱順應性在術后6個月實驗組比格犬和未經行任何手術的健康雄性比格犬間沒有顯著性差異,表明用實施例1的生物修復材料修復尿道損傷后盡管有尿道狹窄出現,但對膀胱功能幾乎沒有影響。說明,本發明的生物修復材料可以修復尿道的損傷,并促進損傷尿道功能的恢復。
6、再造尿道的形態觀察
對步驟4的術后6個月對照組比格犬和術后6個月實驗組比格犬的泌尿系統進行形態觀察,結果如圖3所示。術后6個月對照組比格犬和術后6個月實驗組比格犬的上泌尿道都沒有出現擴張和腎盂積水,而術后6個月對照組比格犬出現后尿道擴張。術后6個月實驗組比格犬再造尿道的平均長度是4.6±0.3cm,顯著高于術后6個月對照組比格犬的再造尿道的平均長度3.4±0.8cm(p<0.05),表明對照組比格犬的尿道出現了嚴重的萎縮。從形態上來看,實驗組比格犬的再造尿道軟而光滑,而對照組比格犬則硬而粗糙,且對照組比格犬的再造尿道周圍出現瘢痕組織。術后6個月對照組比格犬出現尿道瘺,出現尿道瘺的比格犬占術后6個月對照組比格犬的60%;術后6個月實驗組比格犬均沒有尿道瘺的出現。術后6個月對照組有80%的比格犬出現尿道閉塞,術后6個月實驗組比格犬均沒有出現尿道閉塞。
表明,本發明的生物修復材料可以修復尿道的損傷,并促進尿道的再生。
7、組織學觀察
對步驟4的術后6個月對照組比格犬和術后6個月實驗組比格犬的再造尿道進行HE染色和組織切片。具體方法如下:在再造尿道的中心處將其一分為二,再造尿道的一半用于HE染色,另一半用于免疫用光染色。
每只比格犬的尿道HE染色的方法均為:將再造尿道的一半置于4%中性甲醛中固定24h,石蠟包埋,連續切片,片厚2.5μm,脫蠟,蘇木精-伊紅染色(HE染色),鏡下觀察再生尿道的組織結構,將未經行任何手術的健康雄性比格犬作為對照,結果如圖4所示。
HE染色結果顯示,在對照組比格犬尿道重建處植入的實施例1的膠原支架材料和實驗組比格犬尿道重建處植入的實施例1的生物修復材料在術后6個月均完全降解并被再生組織替代。實驗組比格犬的尿道上皮細胞覆蓋了整個再造尿道,而對照組比格犬的尿道上皮細胞層在尿道重建處是不完整的,且對照組比格犬的尿道上皮細胞層比 實驗組薄。實驗組比格犬尿道重建處的上皮細胞層下面的血管多于對照組比格犬尿道重建處的上皮細胞層下面的血管,并且對照組比格犬尿道損傷處出現尿道瘺。說明,本發明的生物修復材料可以修復尿道的損傷。
8、免疫熒光染色觀察上皮組織再生情況
將步驟7得到的每只再造尿道的另一半進行冰凍切片,片厚5μm。用pan cytokeratin AE1/AE3抗體(Abcam產品,貨號為ab86734)檢測尿道重建處上皮細胞的再生情況(圖5),將未經行任何手術的健康雄性比格犬作為對照。結果顯示,實驗組比格犬尿道重建處的上皮由8-10層上皮細胞組成,覆蓋整個再造尿道,細胞排列整齊,具有正常尿道組織上皮細胞的形態特征;而對照組比格犬尿道重建處的上皮由3-5層上皮細胞組成,細胞排列松散,未能完整覆蓋再造尿道,且有尿道瘺出現。實驗組比格犬尿道重建處的上皮層的厚度為99.60±11.37μm,與健康雄性比格犬正常尿道上皮層厚度(95.32±22.41μm)無顯著差異(P>0.05),但與對照組比格犬尿道重建處的上皮層厚度(42.66±3.77μm)有顯著性差異(P<0.01)(圖6)。說明,本發明的生物修復材料可以修復尿道的損傷,并促進尿道上皮的再生。
9、血管再生情況
觀察步驟4的術后6個月對照組比格犬和術后6個月實驗組比格犬的再造尿道的血管再生情況。將比格犬再造尿道進行冰凍切片,用vWF單抗(Abcam產品,貨號為ab6994,該抗體標記有熒光物質)檢測血管組織再生情況(圖7)及血管平均熒光強度(圖8),將未經行任何手術的健康雄性比格犬作為對照。
結果顯示,術后6個月對照組比格犬尿道重建處的血管平均熒光強度為0.026±0.003,術后6個月實驗組比格犬尿道重建處的血管平均熒光強度為0.038±0.008,健康雄性比格犬尿道的血管平均熒光強度為0.041±0.008。術后6個月實驗組比格犬尿道重建處的血管密度高于術后6個月對照組比格犬尿道重建處的血管密度,并且二者具有顯著性差異(P<0.01)。說明,本發明的生物修復材料可以修復尿道的損傷,并促進尿道血管的再生。
10、平滑肌再生情況
觀察步驟4的術后6個月對照組比格犬和術后6個月實驗組比格犬的再造尿道的平滑肌細胞再生情況。將比格犬再造尿道進行冰凍切片,用α-SMA單抗(Abcam產品,貨號為ab119952,該抗體標記有熒光物質)檢測平滑肌再生情況(圖9)及平滑肌組織平均熒光強度(圖10),將未進行任何手術的健康雄性比格犬作為對照。
結果顯示,健康雄性比格犬尿道的平滑肌組織平均熒光強度為76.16±12.47,術后6個月對照組比格犬尿道重建處的平滑肌組織平均熒光強度為2.58±1.50,術后6個月實驗組比格犬尿道重建處的的平滑肌組織平均熒光強度為65.04±4.85,術 后6個月實驗組比格犬尿道重建處的平滑肌組織平均熒光強度高于術后6個月對照組比格犬尿道損傷處的平滑肌組織平均熒光強度,并且二者具有顯著性差異(P<0.01)。說明,本發明的生物修復材料可以修復尿道的損傷,并促進尿道平滑肌的再生。
- 還沒有人留言評論。精彩留言會獲得點贊!